Как развивается острая сердечная недостаточность
В настоящее время принято считать, что деятельность сердца характеризуется частотой сердечных сокращений, сократительной функцией миокарда, преднагрузкой, постнагрузкой и синергичностью сокращений различных частей миокарда.
Под термином «преднагрузка» (preload) подразумевается прежде всего исходное растяжение миокардиального волокна, определяющее силу его сокращения и, согласно известному закону Франка-Стерлинга, отражающее зависимость длина — сила. Для целого сердца под преднагрузкой понимают объем его наполнения в диастолу, или конечное диастолическое давление.
Постнагрузка (afterload) — это сила, развиваемая сокращающейся мышцей, или сопротивление, оказываемое выбросу крови из сердца, которое определяется системным артериальным давлением и общим периферическим сопротивлением. Термин «сократительная функция миокарда», «сократимость», или «инотропизм», недостаточно четко определен. Очевидно, следует придерживаться мнения S. Sarnoff с соавторами (I960), согласно которому к повышению сократимости следует относить только то увеличение силы и скорости сокращений, которое не сопровождается растяжением исходной длины волокна миокарда или повышением конечного диастолического давления (иными словами, без вовлечения в эту реакцию механизма Франка-Стерлинга). Такая ауторегуляция сердца носит название гомеометрической и связана в основном с двумя эффектами. Первый из них, открытый Н. Bowditch в 1871 г. известен как «лестница» Боудича. Сущность этого феномена в том, что при неизменной длине мышечного волокна со ступенчатым возрастанием частоты сокращений повышается их сила, то есть увеличивается сократимость до определенного (стабилизированного) уровня для каждой ступени.
Второй эффект ауторегуляции сердца, описанный C. Anrep, заключается в том, что с увеличением сопротивления на выходе из желудочка сила сердечных сокращений постепенно повышается. С. Anrep считал, что при этом не изменяется длина мышечного волокна в диастоле, хотя последующие исследователи нашли все же при повышении давления в аорте и увеличение диастолических размеров сердца. Соотношение между силой и скоростью сокращений детально исследовал A. Hill. Он показал, что с увеличением нагрузки на мышцу и, таким образом, с увеличением силы сокращений скорость укорочения мышечного волокна уменьшается (при неизменной исходной длине), то есть имеется обратная зависимость между силой и скоростью сокращений. Положительные инотсопние агенты повышают как скорость сокращений мышечного волокна (при стационарной его длине), так и максимальную его изометрическую силу, что определяется уже не особенностями сердечной мышцы, а ее опосредованной реакцией на воздействие таких средств.
Сила сердечных сокращений (при отсутствии воздействия инотропных агентов) зависит от исходной длины мышечного волокна. Эта зависимость известна как закон Франка-Стерлинга и заключается в том, что растяжение мышцы повышает силу сердечных сокращений (зависимость длина — сила или длина — напряжение, выражаемая кривой Франка-Стерлинга). S. Sarnoff (1960) назвал такую ауторегуляцшо сердца гетерометрической, и ей придается первостепенное значение при увеличении преднагрузки (венозного возврата к сердцу), так как сила сокращений определяется степенью растяжения мышцы непосредственно перед началом сокращения.
При развитии сердечной недостаточности в первую очередь снижается сократительная функция миокарда, хотя механизмы снижения ее еще недостаточно ясны. В целом поддержание нагнетательной функции сердца (сердечного выброса) на уровне, адекватно обеспечивающем метаболические потребности организма, осуществляется за счет взаимодействия всех перечисленных факторов. К примеру, увеличение венозного притока к сердцу, помимо включения в регуляцию механизма Франка-Стерлинга, повышает симпатическую активность и таким образом увеличивает частоту сердечного ритма; соответственно возрастает минутный объем сердца. При снижении объема циркулирующей крови и уменьшении минутного объема сердца компенсаторно повышается функция сампатикоадреналовой системы, увеличивается сократительная способность миокарда, возрастает сердечный выброс.
У здоровых людей умеренная физическая нагрузка повышает симпатическую импульсацию к сердцу, возрастает при этом и количество катехоламинов, повышается частота сердечного ритма и сократительная функция миокарда, увеличивается выброс при неизменном или даже сниженном конечном диастолическом объеме и давлении желудочка. При значительной физической активности сердечный выброс возрастает за счет включения в регуляцию механизма Франка-Старлинга, что проявляется повышением конечного диастолического объема и давления желудочка.
При сердечной недостаточности деятельность сердца может поддерживаться в пределах нормы благодаря включению механизма Франка-Старлинга с увеличением конечного диастолнческого объема желудочка. Правда, вследствие повышения диастолического давления в левом желудочке и в легочных капиллярах появляется одышка — один из характерных симптомов сердечной недостаточности. Умеренная и тем более значительная физическая нагрузка вызывает резкое повышение конечного диастолического объема желудочка, диастолического давления в нем без существенного увеличения сердечного выброса. В этих случаях повышенная симпатическая активность не позволяет увеличить производительность сердца, так как нередко при его недостаточности снижается количество норадреналина в миокарде и уменьшается ответная инотропная реакция сердца на такую импульсацию.
Несоответствие между доставкой кислорода к тканям и их потребностью в нем даже в условиях покоя, несмотря на значительное повышение конечного диастолического объема левого желудочка и давления в нем, способствующее развитию отека легких, приводит к фатальной недостаточности левого желудочка.
Процессы сокращения и расслабления сердечной мышцы реализуются с помощью основных структурных элементов — саркомеров, которые образуют фибриллы или миофибриллы, проходящие по всей длине мышечной клетки (волокна). Клетка состоит на 50 % из миофибрилл, содержит центрально расположенное ярдо, митохондрии (до 36 % общего объема), где проходит окислительное фосфорилирование, и саркоплазматический ретикулум (он состоит из сложной системы мембран, охватывающих миофибриллы), играющий ведущую роль в процессах сопряжения возбуждения и сокращения. Каждое мышечное волокно окружено оболочкой (сарколеммой), а волокна объединяются вставочными дисками (видоизмененной сарколеммой), обеспечивающими функциональную непрерывность клеток и передачу электрической импульсации. Саркомер является основной структурной и функциональной единицей миофибрилл и состоит из двух видов нитей (протофибрилл), образованных крупномолекулярными комплексами сократительных белков. Толстые нити образованы из миозина, а тонкие — из актина Они расположены параллельно и заходят друг за друга, не изменяя своей длины при сокращении саркомера; для объяснения сокращения мышц предложена гипотеза «скользящих нитей». Ультраструктурная основа закона Франка-Старлинга на уровне саркомера предполагает увеличение силы сокращения мышечных волокон с увеличением длины саркомера. Степень увеличения последнего определяется числом контактов миозиновых мостиков с протофибриллами актина.
Во время диастолы, когда концентрация ионов кальция в саркоплазме меньше в 10000 раз, чем во внеклеточной среде, молекулы тропомиозина закрывают активные центры нитей актина. При деполяризации сарколеммальной мембраны концентрация ионов Са++ в саркоплазме резко возрастает. Они образуют комплексы с тропонином, вызывая смещение тропомиозинового стержня и открытие активных центров активной протофибриллы. Последние взаимодействуют с «головкой» миозина и образуют актомиозиновые мостики. Этот процесс протекает с помощью гидролиза АТФ при активировании АТФ-азы миозина. Процесс расслабления, то есть отсоединения «головок» миозина от центров актина, требует возмещения ранее гидролизированнои АТФ. Реализация механизма Франка-Старлинга очевидно, осуществляется без увеличения тока ионов Са++ в кардиомиоцит Первостепенное значение при этом имеет увеличение площади контактов «головок» миозина с активными центрами актиновых протофибрилл вследствие растяжения саркомера.
Увеличение нагрузки на сердце приводит к повышению силы сокращений при уменьшении скорости укорочения мышечного волокна (соотношение «сила-скорость» Хилла). Более медленное скольжение актиновых и миозиновых протофибрилл способствует увеличению актомиозиновых мостиков — возрастает сила сокращений.
Учащение сердечного ритма и воздействие катехоламинов повышают сократительную функцию миокарда посредством увеличения концентрации ионов Са++ в саркоплазме и, как следствие этого, возрастает число кальцийтропониновых комплексов с последующим увеличением активных центров актиновых протофибрилл.
В настоящее время многочисленными исследованиями установлено, что электролиты играют ведущую роль в физиологии сокращения сердца. Как везде, клетки и волокна миокарда имеют разность потенциалов по обе стороны основной клеточной мембраны, положительный заряд находится снаружи, а отрицательный — внутри клетки.
Отрицательно заряженные протеины, анионы Сl — не могут; проникнуть через мембрану, а избирательно притягивают внутрь клетки катионы К+ и удерживают снаружи катионы Na+. Внутри клетки ионов К+ в 20-30 раз больше, чем снаружи, ионов Na+ в 5-10 раз, а ионов Са++ в 100-1000 раз больше снаружи, чем внутри.
При распространении потенциала действия на миокард возникает деполяризация сарколеммальной мембраны с поступлением ионов Na+ в клетку. Одновременно с этим наступает деполяризация и мембран саркоплазматического ретикулума, что приводит к выходу ионов Са++ («кальциевый залп») в саркоплазму. Попутно ионы Са++ проникают в саркоплазму из внеклеточной среды. Эти перемещения осуществляются за счет энергии расщепления АТФ с помощью Са + + активируемой-Mg-зависимой АТФ-азы.
Переход ионов Са++ во внеклеточную среду происходит за счет градиента концентрации Na+ и энергии Na-K-насоса посредством деятельности Na-K-АТФ-азы при расщеплении АТФ.
Таким образом, нормальная сократительная функция миокарда зависит от содержания богатых энергией фосфорных соединений, состояния ионных соотношений и достаточного снабжения организма кислородом. При недостаточности сердца эти физиологические условия нарушаются.
В пораженном миокарде снижается содержание АТФ и КФ (креатинфосфата) — основных источников энергии. Нарушения со стороны сердца могут возникнуть без уменьшения фосфорных соединений вследствие недостаточного их использования. Это наблюдается при блокировании ферментов, в частности аденозинтрифосфатаэы. Но более закономерны и постоянны не только изменения содержания богатых энергией фосфатных соединений — АТФ и КФ, а также нарушения электролитного баланса, играющие патогенетическую роль в прогресенровании сердечной недостаточности.
Так, показано, что в мышечной ткани сердца при недостаточности кровообращения увеличивается содержание натрия и уменьшается содержание калия. Уменьшение же количества внутриклеточного калия является постоянным признаком состояния мышцы, не способной к нормальной функции. При этом может возникнуть порочный круг: сердечная недостаточность вызывает задержку воды в организме, проникновение натрия в клетку с уменьшением внутриклеточного калия; это в свою очередь ведет к понижению сократительной функции миокарда и дальнейшему прогрессированию сердечной недостаточности.
К этому следует добавить, что увеличение внутриклеточного содержания натрия и уменьшение калия в сердечной мышце вызывает нарушения в ресинтезе креатинфосфата, являющегося энергетическим донатором для образования АТФ, что также обусловливает понижение сократительной способности миокарда.
Таким образом, в патогенезе сердечной недостаточности вообще и острой в частности решающее значение имеет нарушение биохимических процессов в миокарде, вызывающее понижение его сократительной функции.
В результате происходящих изменений развиваются гемодинамнческие расстройства с глубокими нарушениями обменных процессов в различных органах и тканях.
Ухудшение сократительной функции миокарда ведет к увеличению остаточного (конечного диасголического) объема желудочков; в связи с этим повышается конечное диастолическое давление в полостях сердца, увеличивается растяжение волокон сердечной мышцы. Вначале это является компенсаторной реакцией по механизму Франка-Стерлинга, но в последующем поддерживать адекватный потребностям тканей в кислороде минутный объем сердца становится невозможно. Развивается различной выраженности сердечная недостаточность, характер которой определяется основным заболеванием и осложнениями деятельности основных жизненно важных органов и систем.
Острая сердечная недостаточность чаще всего бывает двух типов — левожелудочковая, или левопредсердная (левого типа) сердечная недостаточность, приводящая к развитию кардиальной астмы и отека легких, и правожелудочковая сердечная недостаточность.
Проф. А.И. Грицюк
«Как развивается острая сердечная недостаточность» – раздел Неотложные состояния
Острая сердечная недостаточность: когда развивается остро сердечная недостаточность?
Сердечная недостаточность – это такое состояние организма, при котором наше сердце не справляется со своими функциями. Это значит, что органы и ткани получают недостаточное количество кислорода, что негативно сказывается на их функциях. Отсюда сделаем вывод: сердечная недостаточность – это не отдельное заболевание сердца, а это комплекс симптомов, которые проявляется при слабости сердечной мышцы. Поэтому чтобы больше знать о том, как проявляется острая сердечная недостаточность, когда развивается остро сердечная недостаточность, давайте об этом подробнее поговорим.
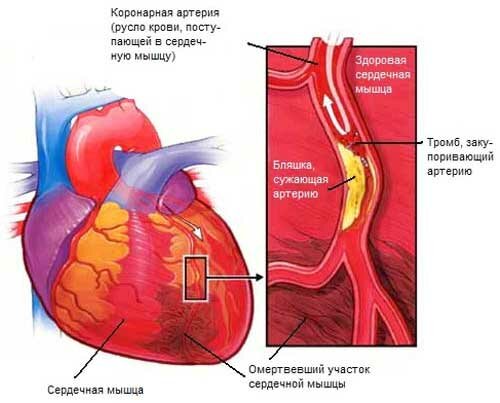
Слабость сердечной мышцы обуславливают различные факторы. В частности, причиной острой сердечной недостаточности являются гипертоническая болезнь, аортальные пороки сердца, острый инфаркт миокарда, тяжелые формы диффузного миокардита, постинфарктный кардиосклероз.
Стоит заметить, что чаще всего остро сердечная недостаточность развивается при поражении левого желудочка, ведь именно на нем лежит основная ответственность за кровоснабжение всего организма.
Острая сердечная недостаточность проявляется в виде сердечной астмы, которая в тяжелых случаях переходит в отек легких. Механизм развития сердечной астмы прост.
Слабая сократительная деятельность левого желудочка приводит к застою крови в малом кругу кровообращения. Кровь скапливается в капиллярах альвеол и не циркулирует. Это провоцирует кислородное голодание тканей всего организма. Чрезмерное кровенаполнение капилляров влечет за собой появление серозного выпота.
Серозный выпот скапливается в плевральной полости и по мере увеличения его количества сдавливает легкое. Резкий скачок количества выпота провоцирует отек легкого и может привести к летальному исходу.
Разобравшись в механизме развития этого патологического состояния, становится сразу понятно, что первые симптомы острой сердечной недостаточности связаны с дыхательной системой. Именно поэтому очень часто употребляют термин острая сердечно-легочная недостаточность.
Клиническая картина сердечной недостаточности очень яркая. Приступ обычно начинается ночью. При этом больной просыпается от острой нехватки воздуха. У него появляется отдышка и затруднен вдох.
При таком состоянии больной занимает вынужденное положение: сидя в кресле, руки лежат на подлокотниках, ноги стоят на полу. Именно такое положение тела способствует оттоку крови в нижнюю часть туловища и ноги, а у легких появляется больше места для расправления.
Со временем отдышка нарастает, появляется кашель. Во время приступа кашля появляется пенистая мокрота, иногда с примесью крови. На лбу появляется холодный липкий пот, синеют губы, появляется цианоз кожных покровов. Больной чувствует усиленное сердцебиение, появляется чувство страха. Именно в этот период необходимо оказать больному необходимую помощь. При отсутствии таковой, возможна кратковременная потеря сознания, а иногда даже коллапс.
При отсутствии специализированной помощи сердечная астма переходит в отек легких. При этом все выше перечисленные симптомы резко ухудшаются. Появляется клокочущее дыхание, увеличивается количество пенистой мокроты. Развиваются признаки удушья.
Как уже было отмечено, остро сердечная недостаточность развивается на фоне какой-либо болезни, поражающей сердце. Поэтому родственника необходимо тщательно следить за состоянием больного и уметь оказать необходимую помощь.
При развитии приступа первое, что необходимо сделать, это обеспечить больному свободный доступ кислорода и сидячее положение(!). У человека, страдающего заболеванием сердца, наверняка в аптечке найдется нитроглицерин. Стоит попробовать принять 1-2 таблетки. Если приступ не купируется, необходимо переходить к более сильным препаратам.
Для снижения возбудимости дыхательного центра необходимо подкожно ввести наркотические анальгетики (Морфин, Омнопон или Промедол) в сочетании с атропином. Это мероприятие позволит купировать сердечную астму. После введения анальгетиков артериальное давление может резко снизиться, в таком случае необходимо ввести сосудистые средства (Мезатон, Кордиамин).
Далее необходимо снизить количество крови в малом круге кровообращения. Этого можно добиться с помощью наложения жгутов на нижние конечности. Таким же эффектом обладает и горячая ванночка для ног с добавлением горчицы.
Ну и третий этап – повышение сократительной функции левого желудочка. Таким эффектом обладают сердечные гликозиды, например, Строфантин.
Эти мероприятия помогут спасти жизнь человеку. Но не стоит без предварительной подготовки заниматься самолечением. Помните, острая сердечная недостаточность очень часто приводит к летальному исходу, поэтому лучше всего доверится врачу.
Юлия Ермоленко, www.rasteniya-lecarstvennie.ru
— Уважаемые наши читатели! Пожалуйста, выделите найденную опечатку и нажмите Ctrl+Enter. Напишите нам, что там не так.
— Оставьте, пожалуйста, свой комментарий ниже! Просим Вас! Нам важно знать Ваше мнение! Спасибо! Благодарим Вас!
Развитие сердечной недостаточности
Несмотря на то что клиническая диагностика синдрома сердечной недостаточности, характеризуемого хорошо известными симптомами, не вызывает больших сложностей, тонкие физиологические и биохимические сдвиги, происходящие в этом случае, значительно труднее поддаются изучению. Тем не менее, с клинической точки зрения, сердечную недостаточность можно рассматривать как состояние, при котором нарушенная функция миокарда служит причиной неспособности сердца нагнетать кровь в сосудистое русло в объеме и со скоростью, соизмеримыми с метаболическими потребностями тканей, или же эти потребности обеспечиваются только благодаря патологически высокому давлению наполнения полостей сердца. При сердечной недостаточности страдать может как систола, так и диастола (рис. 181-7). При так называемой систолической, или классической, сердечной недостаточности нарушение сократимости приводит к ослаблению сокращения миокарда в систолу, а следовательно, к снижению ударного объема и расширению полостей сердца. Идиопатическая дилатационная кардиомиопатия является типичным примером систолической сердечной недостаточности. В случае диастолической сердечной недостаточности происходит неполное расслабление желудочков, приводящих к повышению диастолического давления в желудочке при нормальном его объеме. Невозможность полного расслабления может быть функциональной, как, например, при транзиторной ишемии, или вызванной потерей эластичности и утолщением стенок желудочка. Чаще всего диастолическая недостаточность возникает при вторичных рестриктивных кардиомиопатиях, при таких инфильтративных поражениях, как амилоидоз или гемохроматоз (гл. 192). У многих больных с гипертрофией и дилатацией миокарда систолическая и диастолическая формы сердечной недостаточности сосуществуют. В этом случае нарушается как процесс опорожнения, так и процесс наполнения желудочков. Даже при дилатации полостей сердца сдвиг кривой давление — объем позволяет достичь повышения диастолического давления в желудочке при любом его объеме.
Характерным признаком систолической сердечной недостаточности служит нарушение сократимости миокарда. Однако этот дефект может быть следствием как первичного поражения сердечной мышцы, например при кардиомиопатии, так и вторичного повреждения ее вследствие длительной чрезмерной нагрузки, например при артериальной гипертензии или клапанном пороке сердца, а также при многих вариантах врожденных заболеваний сердца. При ишемической болезни сердца систолическая сердечная недостаточность представляет собой результат уменьшения количества нормально сокращающихся клеток. Очень важно дифференцировать сердечную недостаточность от циркуляторной недостаточности, при которой функция миокарда страдает вторично, например при тампонаде сердца или геморрагическом шоке; от состояний, характеризующихся застоем кровообращения вследствие патологической задержки солей и жидкости в организме (в подобных случаях серьезных расстройств функции сердца не наблюдают); от состояний, при которых нормально сокращающийся миокард внезапно сталкивается с нагрузкой, превосходящей его возможности, например вследствие обострения артериальной гипертензии или разрыва створки клапана при инфекционном эндокардите.
Собственную сократимость миокарда изучали в эксперименте на изолированном сердце, взятом у здоровых животных, у животных с гипертрофией миокарда и у животных с сердечной недостаточностью. Как при гипертрофии миокарда желудочков, так и при сердечной недостаточности было выявлено снижение максимального изометрического напряжения миокарда и скорости укорочения волокон миокарда до субнормальных значений. Эти изменения были более выражены у животных, страдавших сердечной недостаточностью, чем у животных с изолированной гипертрофией миокарда. Однако гипертрофия миокарда желудочков даже при отсутствии сердечной недостаточности также сопровождалась угнетением сократимости единицы массы миокарда, несмотря на то, что абсолютное увеличение общей мышечной массы обеспечивало поддержание функции сердца в целом. Исследование сосочковых мышц, взятых из левого желудочка больных с сердечной недостаточностью, также продемонстрировало невозможность достижения ими максимального активного напряжения. Электронно-микроскопическое исследование сосочковых мышц кошек, страдавших сердечной недостаточностью, в состоянии, соответствовавшем верхней точке кривой длина — активное напряжение, показало, что длина саркомера в среднем составляла 2,2 мкм. Таким образом, нарушение сократимости, видимо, не было связано с изменением взаимоотношений филаментов внутри саркомера.
Рис. 181-7. Нарушение работы сердца при сердечной недостаточности. Взаимоотношения между конечно-диастолическим объемом левого желудочка и 1) конечно-диастолическим давлением (верхняя часть), что отражает податливость левого желудочка, т. е. его диастолические свойства; 2) ударной работой левого желудочка (нижняя часть), что характеризует кривую систолической функции желудочка. Здоровый левый желудочек (слева) создает конечно-диастолическое давление в 30 мм рт. ст. (уровень, выше которого развивается отек легких), когда его конечно-диастолический объем достигает 200 мл. Систолическая функция левого желудочка при его концентрической гипертрофии (в центре) остается в нормальных пределах, поскольку взаимосвязь конечно-диастолического объема левого желудочка и его ударной работы не меняется. Однако при этом имеет место диастолическая недостаточность, характеризующаяся тем, что конечно-диастолическое давление, при котором начинается отек легких ( 30 мм рт. ст.), возникает при меньших значениях конечно-диастолического объема (130 мл). При дилатации желудочка (справа) развивается систолическая недостаточность, характеризующаяся тем, что максимальная ударная работа и ударный объем понижены при любом значении конечно-диастолического объема. При этом у левого желудочка повышается диастолическая податливость, т. е. растяжимость, при значительно более высоких, чем требуется для развития отека легких, величинах конечно-диастолического объема (280 мл). (С разрешения из: R. Gorlin—Prim. Cardiol. 1984, 6, 84.)
При нарушении сократимости миокарда желудочек может продолжать выбрасывать в сосудистое русло нормальное или почти нормальное количество крови, несмотря на существенное угнетение его функции, за счет увеличения конечно-диастолического объема, т. е. благодаря действию механизма Франка — Стерлинга. Как отмечалось выше, увеличение исходного объема желудочка сопровождается растяжением саркомера. В результате этого увеличивается количество точек взаимодействия нитей актина и миозина и/или повышается их чувствительность к ионам кальция. Более того, гипертрофию желудочков можно рассматривать как процесс формирования дополнительных контрактильных единиц, что представляет собой важный механизм компенсации в условиях угнетения собственной сократимости миокарда.