Стресс-индуцированная кардиомиопатия (синдром тако-цубо)
М. Ю. Гиляров М. С. Сафарова А. Л. Сыркин
Cтресс-индуцированная кардиомиопатия (КМП) представляет собой клинический синдром, характеризующийся обратимой остро возникающей апикальной дисфункцией левого желудочка (ЛЖ), сопровождающейся изменениями ЭКГ, которые имитируют инфаркт миокарда, при неизмененных коронарных артериях.
Стресс-индуцированную КМП называют также синдромом тако-цубо (tako-tsubo), ампулоподобной КМП, синдромом транзиторного расширения верхушки ЛЖ или синдромом «разбитого сердца». В настоящее время принято наименование «стресс-индуцированная КМП», которую относят к приобретенным неклассифицированным КМП 48. За последние 16 лет с момента первого описания стресс-индуцированной КМП, опубликованного японским ученым H. Sato и соавт. в 1990 г. 60. интерес к этому патологическому состоянию неуклонно растет. С момента первого описания были опубликованы более 300 статей, причем большая их часть — в последние 5 лет. Широкие массы европейских кардиологов были ознакомлены с проблемой в 2006 г. после доклада S. Kristensen на Европейском конгрессе кардиологов в Барселоне. В России имеются единичные описания данного синдрома, что, вероятнее всего, связано с неосведомленностью врачей, а не с малой распространенностью патологии 1, 2 .
Среди лиц, страдающих стресс-индуцированной КМП, отмечается значительное преобладание женщин в постменопаузе, которые составляют более 90% представленных в литературе случаев. По данным японских авторов, среди больных стресс-индуцированной КМП соотношение женщин и мужчин составляет 7:1. Этот дисбаланс может быть объяснен половыми различиями в характере ответа мозгового вещества надпочечников на чрезмерную активацию симпатической нервной системы (СНС) и разницей в фармакокинетике высвобождаемого адреналина.
Этиологическим фактором стресс-индуцированной КМП является предшествующий физический или эмоциональный стресс. Два сообщения, представленные японскими авторами, демонстрируют увеличение частоты регистрации случаев выявления синдрома после землетрясения, произошедшего в Японии 71, 73. Инвазивные вмешательства 9, 37. травмы, заболевания, вызывающие гиперергическую реакцию организма, например бронхиальная астма, острый живот, микроскопический полиангиит высокой степени активности 5, 8, 49, 59. приводят к развитию данной формы КМП. Имеются описания и таких факторов, как прекращение употребления алкоголя 61. отмена опиатов 57. ограбление и судебное разбирательство 72 .
Базальная концентрация адреналина в плазме крови у женщин ниже, чем у мужчин 17. Это может быть отражением пониженного синтеза, повышенного разрушения или сниженного высвобождения гормона из нервных окончаний с возможностью большего высвобождения при необходимости. Кроме того, определенную роль в патогенезе стресс-индуцированной КМП может играть снижение уровня эстрогенов в постменопаузе 46, 53. Стресс стимулирует преждевременную экспрессию генов как в ЦНС, так и в миокарде желудочков на модели грызунов 65, 66. изменения в миокарде осуществляются за счет активации как α-, так и β-адренорецепторов (АР). Эстрогены уменьшают патологическую экспрессию генов, тем самым уменьшая выраженность дисфункции верхушки желудочков у грызунов с синдромом тако-цубо, индуцированным длительной иммобилизацией 64. Хроническое действие эстрогенов на миокард желудочков у крыс уменьшает экспрессию на поверхность β 1 -АР, возникающую в ответ на воздействие катехоламинов и ишемию 38. Кроме того, отмечено, что после овариэктомии плотность β 1 -АР увеличивается, т.е. наблюдается прямо противоположный эстрогенному воздействию эффект 14. Было также показано, что β 2 -АР гладких мышечных клеток сосудов у женщин характеризуются более высокой чувствительностью, чем у мужчин 42. Следовательно, эстрогены, по-видимому, могут влиять на соотношение β 1 -АР:β 2 -АР, оказывая свое защитное действие за счет увеличения количества комплексов β 2 -АР—Gi-белок и активности, связанных с ними сигнальных систем, в ответ на резкий подъем уровня катехоламинов. При снижении уровня эстрогенов в постменопаузе этот защитный механизм не срабатывает, и токсическое действие надфизиологической концентрации катехоламинов проявляется в области наибольшей плотности β-адренорецепторов — в апикальном отделе миокарда 47 .
Уровень катехоламинов в плазме крови непосредственно после воздействия стрессового фактора у большинства пациентов со стресс-индуцированной КМП в остром периоде значительно повышен. При определении содержания катехоламинов в плазме оказывается, что у пациентов со стресс-индуцированной КМП оно значительно превышает таковое у больных острым инфарктом миокарда или с сердечной недостаточностью, а по сравнению с нормой концентрация катехоламинов повышена более чем в 34 раза 27, 72 .
Однако такие показатели у пациентов со стресс-индуцированной КМП регистрируются не всегда. Период полураспада адреналина составляет приблизительно 3 мин 25. а госпитализация больных осуществляется не менее чем через 30 мин (более 10 периодов полураспада), а в большинстве случаев через несколько часов после появления симптомов заболевания. Таким образом, максимальная концентрация адреналина, которая в действительности воздействует на миокард на высоте стресса, выше, чем при измерении уровня адреналина в сыворотке при госпитализации через определенное время, когда уровень секреции снижается, приближаясь к базальной.
Такой подъем уровня катехоламинов приводит к дисфункции желудочков вследствие «оглушения» миокарда. В англоязычной литературе такое состояние называется «оглушенный миокард при сохранном коронарном кровотоке» («stunning with normal coronary blood flow») 47. Данный феномен — относительно распространенное явление, обнаруживаемое у больных с черепно-мозговыми травмами, особенно с субарахноидальными кровоизлияниями. У таких пациентов наблюдается симпатико-адреналовая гиперреактивность как ответ на повреждение 63. Приблизительно у 10% пациентов с черепно-мозговыми травмами имеются острые изменения ишемического характера на ЭКГ, повышенные уровни кардиоспецифических ферментов и острая обратимая левожелудочковая недостаточность при практически неизмененных коронарных артериях 18, 23, 43. Гистологическая картина миокарда у этих пациентов сходна с таковой у больных стресс-индуцированной КМП (лейкоцитарная инфильтрация и участки некроза) 20. Подобная клиническая картина с повышенным содержанием в крови катехоламинов наблюдается и у пациентов с феохромоцитомой.
В литературе приводятся несколько концепций относительно патогенеза развития стресс-индуцированной КМП. Существует гипотеза о взаимосвязи синдрома и анатомических особенностей левой передней нисходящей коронарной артерии, спазм которой может приводить к дисфункции соответствующих отделов ЛЖ. Результаты нескольких исследований показали, что у таких пациентов артерия длиннее и участвует в кровоснабжении не только передней стенки, но и верхушки с переходом на нижний отдел ЛЖ 4, 34 .
В качестве еще одного патогенетического варианта развития заболевания рассматривается воспалительный процесс в миокарде 51. так как при эндомиокардиальной биопсии определяется гистологическая картина миокардита — фокальный миоцитолиз, участки инфильтрации моноцитами и интерстициальный фиброз 39, 44 .
Имеются данные о связи стресс-индуцированной КМП с S-образным строением межжелудочковой перегородки, обструкцией выходного тракта ЛЖ и меньшим объемом ЛЖ. Эти изменения являются нередкой эхокардиографической находкой у пожилых женщин, особенно на фоне адренергической стимуляции и гиповолемии 69 .
Внутривенное введение адреналина и ацетилхолина пациентам со стресс-индуцированной КМП не позволило выявить у них спазм крупных сосудов. Кроме того, отсутствовали клиническая картина вазоспастической стенокардии и ее электрокардиографические проявления 36 .
В ряде случаев у пациентов со стресс-индуцированной КМП могут выявляться атеросклеротические изменения коронарных артерий. Так, при использовании внутрисосудистого ультразвукового исследования у 16 пациентов со стресс-индуцированной КМП, у 5 была обнаружена «ранимая» эксцентрично расположенная атеросклеротическая бляшка в средней части левой передней нисходящей коронарной артерии, не визуализируемая при коронарографии 35 .
«Оглушение» миокарда может возникать вследствие спазма эпикардиальных сосудов, множественного спазма сосудов 19, 21, 56, 62 и непосредственного воздействия катехоламинов на кардиомиоциты 47 .
Подъем уровня катехоламинов является эволюционно выработанным ответом на внезапный страх, опасность или шок. При физиологических и надфизиологических концентрациях норадреналин, высвобождаемый из симпатических нервных окончаний, действует на кардиомиоциты желудочков в основном через β 1 -АР, оказывая положительное инотропное и хронотропное действие. Возникающий эффект является результатом активации каскада биохимических реакций, запускаемых вследствие изменения конформации белка Gs за счет образования комплекса гормон—рецептор, что приводит к активации аденилатциклазы и как следствие к увеличению концентрации цАМФ. Последний активирует протеинкиназу А посредством вторичных мессенджеров гормонального сигнала, которая фосфорилирует несколько участвующих в этой цепи внутриклеточных мишеней, изменяя их активность и тем самым — скорость регулируемых ими процессов, приводя к увеличению сократительной способности кардиомиоцитов.
Адреналин также способен взаимодействовать с
β 1 -АР, инициируя подобный ответ, однако этот гормон обладает большим сродством к β 2 -АР. В норме соотношение β 1 -АР. β 2 -АР составляет приблизительно 4:1 55. Исследования на трансгенных моделях мышей, у которых структура β 2 -АР сходна с таковой у человека, позволили изучить фармакологию β 2 -АР кардиомиоцитов желудочков человека. В физиологических концентрациях взаимодействие адреналина с β 2 -АР активирует аденилатциклазную систему, оказывая кардиотоническое действие. При повышенных концентрациях медиатора подобное белок-белковое взаимодействие приводит к отрицательному инотропному эффекту. Такой ответ является следствием изменений в центре связывания адренорецептора, который становится комплементарен Gi-ингибирующему белку 31, 32, 76. Хотя зависимость варианта ответа при стимуляции β 2 -АР от концентрации адреналина была показана на трансгенной модели мышей, существуют данные о возможности действия сигнальных систем через β 2 -АР—Gi-белковый комплекс в миокарде как предсердий 41. так и желудочков человека 11. Было показано, что активация сигнальной системы через комплекс β 2 -АР—Gi-белок приводит к снижению силы сокращений кардиомиоцитов желудочков человека 28. хотя полученный эффект был более выражен при исследовании пораженного сердца, в котором плотность ингибирующего белка больше, чем в здоровом миокарде 24. После того как уровень циркулирующего адреналина снижается до физиологического, активный центр β 2 -АР изменяет свою конформацию, связываясь со стимулирующим белком Gs, либо подвергается деградации, вследствие чего кардиомиоциты восстанавливают свою инотропную функцию. Такая последовательность событий позволяет объяснить восстановление функции ЛЖ у пациентов со стресс-индуцированной КМП.
Механизм возникновения отрицательного инотропного эффекта через комплекс β 2 -АР—Gi-белок не до конца понятен. Посредством ингибирующего белка может быть активирована р38-митоген-ассоциированная протеинкиназная сигнальная система, приводящая к снижению силы сокращений сердца 45, 54, 74. Возможно, комплекс β 2 -АР—Gi-белок осуществляет непосредственную регуляцию функции натрийкальциевых каналов 75. или блокирует кальциевые каналы L-типа 30. или действует через другие пока еще неизвестные сигнальные системы. Чрезмерная стимуляция аденилатциклазной системы через комплекс β 1 -АР—Gs-белок индуцирует процессы апоптоза в кардиомиоцитах. При высоком уровне в крови адреналина в клетках происходит переключение на сигнальную систему, связанную с комплексом β 2 -АР—Gi-белок, скорее всего имеющее защитно-приспособительное значение, поскольку комплекс принимает участие в активации инозитолфосфатной системы посредством βγ-субъединиц белка Gi, дающей противоапоптозный эффект 13. Такое действие нейтрализует проапоптозный эффект, возникающий при чрезмерной стимуляции аденилатциклазной системы через комплекс β 1 -АР—Gs-белок 15. Существование подобного баланса предупреждает последствия катехоламиновой токсичности. Однако запуск механизмов апоптоза может возникнуть и несмотря на активацию Gi-зависимых систем, чем объясняется подъем уровня тропонинов у пациентов со стресс-индуцированной КМП.
Отрицательное инотропное действие адреналина, ассоциированное с действием на комплекс β 2 -АР—Gi-белок, позволяет объяснить индуцированную катехоламинами дисфункцию миокарда с преимущественной локализацией в области верхушки ЛЖ. Симпатическая стимуляция адренорецепторов в миокарде желудочков достигается двумя путями: местным высвобождением норадреналина симпатическими нервными окончаниями — непосредственная иннервация миокарда — и диффузией катехоламинов из коронарного русла. При патологоанатомическом исследовании здорового сердца с тирозингидро-ксилазой установлено, что плотность окончаний симпатических нервных волокон приблизительно на 40% больше в базальных отделах, чем в миокарде верхушки 40. У собаки симпатическая иннервация ЛЖ имеет аналогичную картину распределения с тенденцией к снижению плотности нервных окончаний от основания к области верхушки 52. В норме б?ольшая часть норадреналина высвобождается из нервных окончаний; медиатор, поступающий в кровяное русло из мозгового вещества надпочечников, вносит минимальный вклад.
Выраженность действия гормона зависит от плотности распределения адренорецепторов в различных отделах миокарда. Н. Mori и соавт. показали, что плотность β-АР более выражена в апикальной части сердца собаки с уменьшением градиента концентрации от области верхушки к базальному миокарду 52. Указанная особенность распределения АР в миокарде приводит к ответной реакции на воздействие катехоламинов со стороны верхушки, более выраженной, чем базальных отделов. Разница в соотношении нервных окончаний и их рецепторов, возможно, объясняется тем, что повышенная концентрация β-АР в области верхушки необходима для компенсации пониженной непосредственной симпатической иннервации из-за меньшей плотности нервных окончаний в этом отделе миокарда — для адекватного ответа желудочков на воздействие СНС. Эта разница подразумевает, что верхушка чувствительна к циркулирующим катехоламинам в большей степени, чем базальные отделы. При этом необходимо отметить, что в условиях стресса основным медиатором становится адреналин. Н. Mori и соавт. в своем исследовании не разграничивали адренорецепторы на β 1 и β 2. На моделях сердца с недостаточностью, вызванной острой или хронической катехоламиновой токсичностью, продемонстрировано значительное количество участков фиброза в области верхушки, что свидетельствует о повышенной чувствительности миокарда верхушки к циркулирующим катехоламинам 10, 58. Увеличением плотности β 2 -АР от основания к верхушке и наличием выраженного влияния адреналина на функцию верхушки по сравнению с базальными отделами может быть объяснена регионарная разница в ответе сердечной мышцы на высокие уровни катехоламинов 47 .
На фоне этих изменений опосредованный норадреналином спазм коронарных сосудов имеет, вероятно, дополнительное значение 10. хотя в других исследованиях не получено данных, подтверждающих наличие микроциркуляторной или эпикардиальной дисфункции у пациентов со стресс-индуцированной КМП 3. Спазм коронарных сосудов может приводить к вторичной ишемии, накладываясь на первоначальное ассоциированное с адреналином станнирование верхушки 47 .
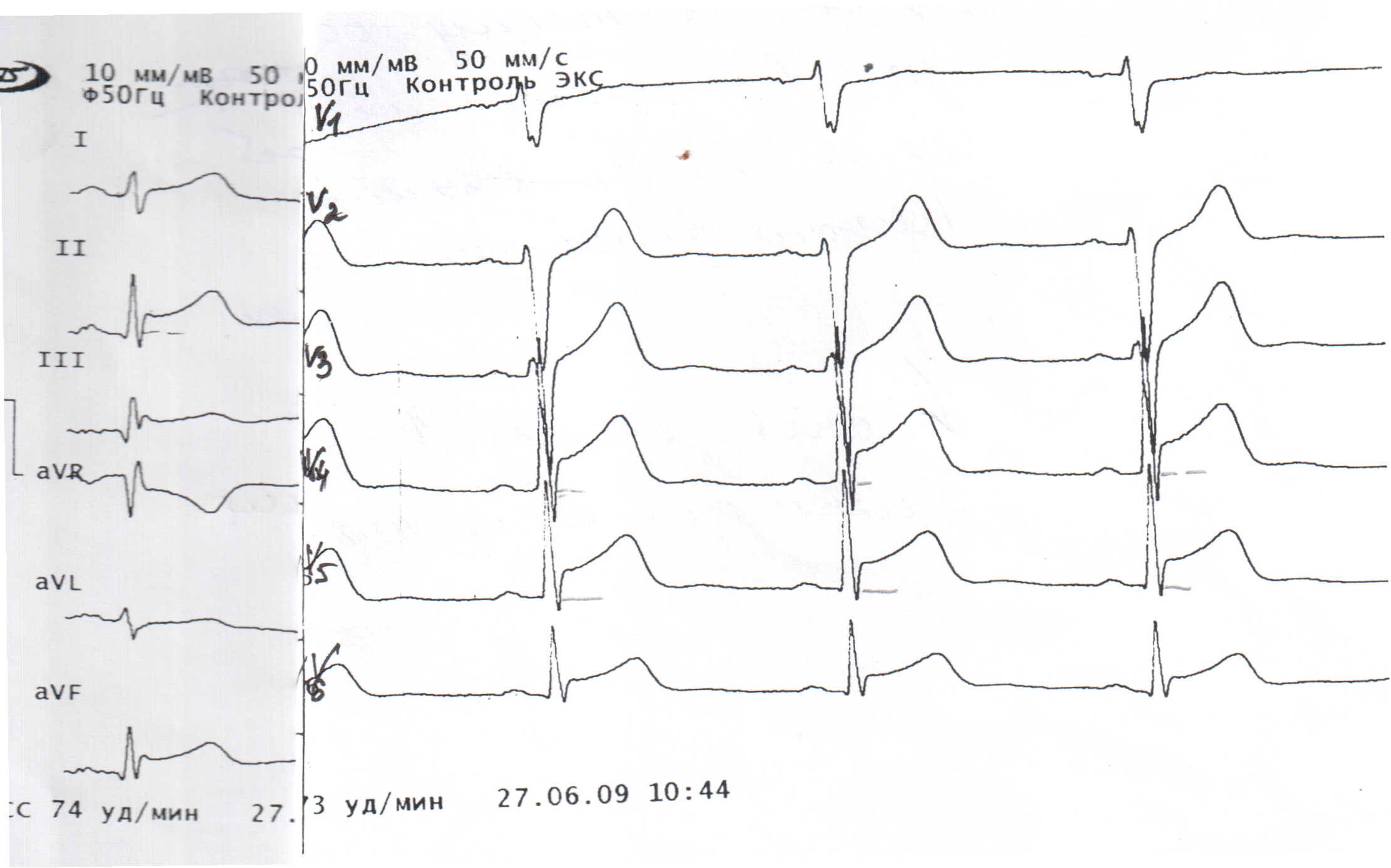
Клинически стресс-индуцированная КМП представляет собой остро возникающую, преходящую дисфункцию ЛЖ, которой обычно предшествует физический или эмоциональный стресс. Пациенты предъявляют жалобы на загрудинные боли, сходные с болями, которые наблюдаются при ишемии миокарда, но длящиеся в течение большего периода времени. Болевой синдром сопровождается острыми ишемическими изменениями на ЭКГ (подъем сегмента ST с последующим удлинением интервала Q—T и инверсией зубца Т; рис. 1). Изменения ЭКГ сопровождаются повышением уровня маркеров некроза миокарда, хотя и не столь значительным, как при инфаркте. Для заболевания характерны дисфункция и дискинезия ЛЖ, затрагивающие верхушку и часто межжелудочковую перегородку, не вовлекая в процесс базальный миокард. В ряде случаев отмечается инвертированный вариант с наличием гипокинезии базальных отделов и гиперкинезией его апикальной части 16, 67. При этом наблюдается несоответствие между выраженностью нарушений локальной и глобальной сократимости и степенью повышения уровня кардиоспецифических ферментов. При вентрикулографии (рис. 2), ЭхоКГ (рис. 3) или магнитно-резонансной томографии (рис. 4) выявляются изменения полости ЛЖ, которые по форме напоминают флягу с узким горлышком и широким округлым дном. Изменения формы ЛЖ могут быть разнообразными (рис.?5), но приобретаемая ЛЖ в конце систолы специфическая конфигурация часто напоминает приспособление, используемое японскими рыболовами для ловли осьминогов — тако-цубо (tako — осьминог, tsubo — горшок), откуда и происходит одно из названий данного синдрома (рис. 6). Возникающая компенсаторно на фоне гипокинезии верхушки и перегородки гиперкинезия базальных отделов в некоторых случаях приводит к обструкции выходного тракта ЛЖ, что может сопровождаться симптомами расстройства мозгового кровообращения в виде потери сознания, головокружения, тошноты и рвоты. Дисфункция миокарда ЛЖ приводит к острой левожелудочковой недостаточности с развитием в ряде случаев отека легких и кардиогенного шока. Кроме того, может возникать дисфункция папиллярных мышц с формированием митральной недостаточности. В ряде случаев развиваются желудочковые нарушения ритма. Дилатация полости ЛЖ может приводить к формированию внутрисердечных тромбов, а истончение миокарда — к разрыву ЛЖ. В тяжелых случаях исходом заболевания может быть смерть.
Рисунок 1. ЭКГ пациентки 71 года со стресс-индуцированной кардиомиопатией 50 .
Заболевания сердечно-сосудистой системы в последние годы стали диагностироваться с заметной частотой. Причиной тому в большинстве случаев служит неправильный образ жизни человека, в котором преобладают алкогольные напитки, жирная пища и продукты быстрого приготовления, минимальная физическая активность (сидячая работа, передвижение только в автомобиле или общественном транспорте).
Несколько лет в таком режиме – и человек может смело отнести себя к группе риска по сердечно-сосудистым заболеваниям. Часто развивается артериальная гипертония, ишемическая болезнь сердца. В данной статье речь пойдет о заболевании под названием кардиомиопатия .
Одной из форм заболевания является стрессовая кардиомиопатия. Она характеризуется дисфункцией левого желудочка, которая проявляется на фоне физического или психического стресса, то есть под воздействием стрессовых ситуаций. Клиническая картина описывается следующим образом:
- специфические признаки — нарушение терморегуляции организма, которое проявляется повышением потливости; одышка; учащенное сердцебиение; внезапная остановка сердца; боль в области грудины, как при стенокардии; в некоторых случаях при серьезных повреждениях левого желудочка происходит расстройство кровообращения мозга, сопровождающееся головокружением и тошнотой, рвотой;
- неспецифические признаки — повышенная тревожность, взволнованность.
К группе факторов риска входят следующие ситуации, которые можно разделить на несколько групп:
- эмоциональные потрясения, примером которых могут стать смерть близкого человека или родственника, материальные потери, участие в дорожно-транспортном происшествии или публичное выступление перед аудиторией, внезапный переезд в другой город или другую квартиру и т.д.;
- физический стресс, который человек испытывает при проведении хирургических операций или при неблагоприятном течении заболеваний неврологического характера, а также при развитии патологий эндокринологической направленности и других состояниях, сопровождающихся сильной болью;
- химический стресс возникает в результате воздействия на организм отравляющих и наркотических веществ, например, кокаина.
Вне зависимости от того, какой вид стресса больной перенес ранее, стремительное развитие кардиомиопатии требует своевременного лечения. Только в этом случае возможен благоприятный прогноз.
Адекватное лечение кардиомиопатии назначается и проводится только высококвалифицированным врачом. Для этого вам необходимо обратиться в центр кардиологии или другое медицинское учреждение, которое располагает кардиологическим отделением. Терапия часто сводится к применению ингибиторов АПФ, которые способствуют восстановлению функции левого желудочка. При выявлении постоянной дисфункции органа требуется терапия мочегонными средствами. Когда лечение носит затяжной характер, показаны бета-адреноблокаторы.
Дополнительные материалы:
Стрессовая кардиомиопатия: «новое» заболевание сердца у женщин
Стресс-индуцированная кардиомиопатия Такотсубо —
новая нозологическая форма приобретенной КМП, характеризующаяся транзиторной дисфункцией левого желудочка в ответ на физический или психический стресс, клинически и электрокардиографически напоминающая острый коронарный синдром, описанная, преимущественно. у женщин постменопаузального периода без признаков ишемической болезни сердца и отличающаяся относительно благоприятным прогнозом