Нейрогенный отек легких. Нейрогенный отек легких после сеанса гемодиализа
Нейрогенный отек легких после сеанса гемодиализа
Neurogenic pulmonary oedema post-haemodialysis. Andrew Davenport (NDT Plus, Volume 1, Number 1, Feb 2008, http://ndtplus.oxfordjournals.org/cgi/content/full/1/1/41)
Введение
Существует множество причин развития отека легких (см. таблицу ниже). У пациентов с почечной недостаточностью отек легких обычно развивается в условиях повышенного давления в легочных артериях в связи с увеличением объема экстрацеллюлярной жидкости, что является следствием междиализного набора веса и невозможностью достижения «сухого веса» или «постдиализного целевого веса», часто в сочетании с нарушением функции сердца. Накопление интерстициальной жидкости в легких также может происходить и при состояниях, характеризующихся нормальным давлением в легочных артериях.
Таблица 1. Причины отека легких
> ГД < ОД > ЭП < ЛД < ИД < С Полиорганная недостаточность +++ +++ +++ ++ — + Печеночная недостаточность ++ +++ +++ — — — Почечная недостаточность ++ + +++ — — — Нейрогенный отек +++ + +++ — — — Перегрузка объемом +++ + — — — — Эмболия легочных сосудов +++ — +++ — — — Сердечная недостаточность +++ + ++ — — — Карциноматоз — ++ ++ +++ — — Высокогорный отек легких +++ + +++ — — — Реэкспансионный отек легких + — +++ — +++ —
ГД — гидростатическое давление, OД — онкотическое давление, ЭП — проницаемость эндотелия, ЛД — лимфодренаж, ИД — интерстициальное давление, С — сурфактант.
Легочные осложнения наблюдаются при острой и хронической печеночной недостаточности. Печеночно-легочный синдром (hepatopulmonary syndrome) связан с чрезмерной дилатацией легочных сосудов и повышением уровня вазопрессина, катехоламинов и усилением активности симпатической нервной системы, что приводит к шунтированию с нарушением соотношения вентиляция/перфузия (увеличение) [1]. Кроме того, накопление циркулирующих эндотоксинов и провоспалительных цитокинов приводит к активации эндотелия и усилению образования интерстициальной жидкости [2]. Усиливает эти эффекты уменьшение онкотического давления коллоидов плазмы.
В случаях нейрогенного отека легких, накопление интерстициальной жидкости происходит в результате увеличения легочного гидростатического давления и активации эндотелия [3]. В статье описан случай острого отека легких (нейрогенного), развившегося после интермиттирующего гемодиализа через 9 дней после приема парацетамола – суицидальной попытки.
Описание случая
Пациентка в возрасте 30 лет поступила в стационар через 2 дня после приема 50 г парацетамола, с нарушением функции печени, и следующими лабораторными показателями: лактат 13 ммоль/л (в норме <2,0), протромбиновое время 91,7 сек (в норме <12), МНО 8,0, АЛТ 9964 мЕд/л (в норме <42), АСТ 9581 мЕд/л (в норме <42), мочевина 13,1 ммоль/л, креатинин 235 мкмоль/л. Наблюдалась гипервентиляция, признаки энцефалопатии отсутствовали. Была начата непрерывная гемодиафильтрация, так как у пациентки развилась олигурия, и проводилась стандартная поддерживающая терапия в связи с острой печеночной недостаточностью. Состояние пациентки стабилизировалась, затем улучшилось, она была переведена в отделение гепатологии, МНО составило 1,7. Сохранялась олигурия, тахикардия, АД 100/60 мм рт. ст. В течение следующих 24 часов уровень креатинина увеличился с 148 до 275 мкмоль/л, и затем до 328 мкмоль/л на следующий день, несмотря на проводимую гемодиафильтрацию. В связи с повышением уровня креатинина и калия (см. таблицу 2), было решено начать гемодиализ (через 9 дней после отравления), с использованием среднепоточного полисульфонового диализатора (Fresenius F80, Bad Homberg, Germany), концентрация натрия в диализирующем растворе 142 ммоль/л, калия – 1,0 ммоль/л, кальция 1,35 ммоль/л, бикарбоната 35 ммоль/л, температура 35°C, скорость подачи диализата 800 мл/мин. Антикоагуляция не проводилась. Скорость кровотока – 220 мл/мин, общая ультрафильтрация 600 мл. До начала диализа артериальное давление составляло 160/94 мм рт. ст. с синусовой тахикардией 126/мин, МНО 1,6, бикарбонат сыворотки 21 ммоль/л, альбумин 28 г/л. Минимальное зафиксированное АД в течение 3-часового сеанса гемодиализа составило 155/95 мм рт. ст. насыщение кислорода поддерживалось на уровне 97–98%.
Таблица 2. Результаты лабораторных обследований
До проведения диализа Непосредственно после диализа Через 6 часов после диализа Натрий (ммоль/л) 132 139 135 Калий (ммоль/л) 6,0 4,1 5,2 Мочевина (ммоль/л) 17,2 9,6 11,2 Креатинин (мкмоль/л) 328 205 234 Глюкоза (ммоль/л) 6,4 4,2 5,4 Осмолярность (мосм/кг) 299,6 300 297
Осмолярность = (натрий + калий) * 2 + глюкоза + мочевина.
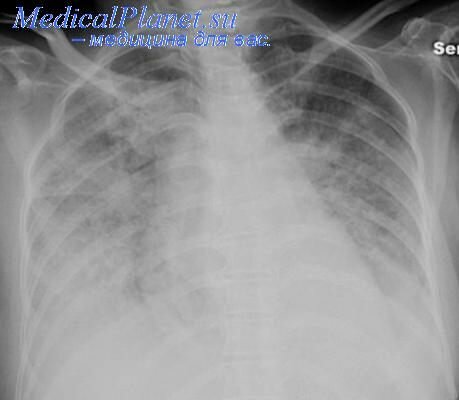
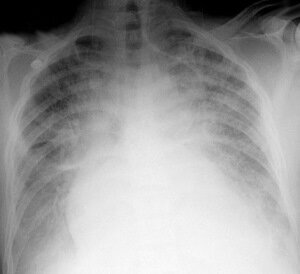
К концу сеанса гемодиализа у пациентки появилось возбуждение и жалобы на усиление одышки, с прогрессирующим ухудшением. При аускультации выслушивался третий тон сердца и распространенные хрипы в легких. При рентгеновском обследовании грудной клетки обнаружен выраженный отек легких, и развилась гипоксия: PaO2 9,3 кПа (в норме 12–14,5) [70 мм рт. ст. в норме 90–109], PaCO2 5,9 кПа (в норме 4,7–6,0) [44 мм рт. ст. в норме 35–45], pH 7,34 (в норме 7,35–7,45), с избытком оснований – 4,6 (в норме ±2), лактат 5,4 ммоль/л (норма <2,0).
Пациентка переведена в отделение интенсивной терапии помощи, проведена интубация с последующей вентиляцией легких, и рекомендована непрерывная гемодиафильтрация. Сердечный выброс составил 11,0 л/мин (показатели неинвазивного мониторинга). Больная была экстубирована через 2 дня и заместительная почечная терапия отменена через 3 дня, в связи с усилением мочеотделения. Однако сохранялось нарушение сознания, с некоординированными движениями глазных яблок, при КТ выявлена энцефалопатия (отек ствола мозга), связанная с повышением проницаемости сосудов. Через несколько дней ее состояние улучшилось, и пациентка была выписана без каких-либо неврологических остаточных явлений.
Обсуждение
В обычной нефрологической практике самой распространенной причиной отека легких у гемодиализных больных является повышение гидростатического давления в легких в связи с перегрузкой внеклеточной жидкости, часто в сочетании с дисфункцией левого желудочка. Также отек легкого может развиваться в результате воспалительного поражения легочного эндотелия, что приводит к повышению его проницаемости, при таких состояниях, как инфекции, васкулиты, действие лекарственных препаратов и компонентов крови, токсинов, лучевого поражения, нарушения функции печени или выраженной уремии [1]. В редких случаях отек легких развивается при обструкции лимфатических сосудов легких, выраженного снижения давления коллоидов плазмы и интерстициального давления альвеолярной ткани (см. таблицу 1). Нейрогенный отек развивается в результате выраженной вазоконстрикции под влиянием симпатической активации – при ишемическом повреждении ядра одиночного пути в продолговатом мозге и/или его связей с гипоталамусом. В результате системной вазоконстрикции происходит перемещение крови из системного кровотока в систему легочного кровообращения, что приводит к выраженной легочной гипертензии, которую осложняет спазм легочных вен, еще более усиливающий капиллярное гидростатическое давление в легких. Развивается гидростатический отек, затем эндотелиальное повреждение и увеличение местной проницаемости [3].
Отек мозга может развиваться при острой печеночной недостаточности, особенно при отравлении парацетамолом [4]. Так, одной из причин смерти при острой печеночной недостаточности является ущемление мозжечка, в данном случае у пациентки имелась дискоординация движений глазных яблок, связанная со сдавлением ствола мозга. Обычно повреждение печени бывает наиболее выраженным через 3-4 дня после передозировке, и затем начинается улучшение (у пациентов, которые выживают без трансплантации печени) [4]. Нарушение функции почек у данной пациентки произошло как в результате влияния острой печеночной недостаточности, так и вследствие токсического действия одного из метаболитов парацетамола – N-ацетил-p-бензохинона, который повреждает почечные канальцы и может приводить к острому повреждению почек на 7-10 день после отравления, если у пациента не развилась тяжелая печеночная недостаточность [6].
Несмотря на то, что данная пациентка приняла потенциально летальную дозу парацетамола, она поступила в стационар через несколько часов после отравления, и быстро была начата терапия n-ацетилцистеином, которая была продолжена и в отделении интенсивной терапии [4]. Ацетилцистеин уменьшает степень печеночного повреждения и увеличивает вероятность спонтанного выздоровления [4].
Известно, что обычный интермиттирующий гемодиализ может вызывать умеренный отек мозга у пациентов с хроническим заболеванием почек, которым назначается гемодиализная терапия. Интермиттирующий гемодиализ/ультрафильтрация может привести к гибели пациентов с уже имеющимся отеком мозга, например, при острой печеночной недостаточности, в связи с усилением отека мозга [7]. Существует несколько теорий, объясняющих этиологию увеличения отека мозга в таких случаях. При интермиттирующем гемодиализе быстро снижается уровень мочевины в плазме в течение первых двух часов [8]. Переход мочевины через клеточные мембраны происходит приблизительно в 20 раз медленнее, чем переход воды [9]. Таким образом, несмотря на быстрое снижение уровня мочевины в плазме, концентрация мочевины в тканях остается высокой, что создает градиент онкотического давления и приводит к диффузии воды в ткани (для выравнивания разницы осмотического давления). Кроме того, поступление бикарбоната из диализата (с высокой концентрацией бикарбоната) повышает рН плазмы [10], однако не приводит к переходу иона бикарбоната через клеточную мембрану. Это вызывает нарушение баланса между концентрациями бикарбоната и диоксида углерода, с парадоксальным развитием внутриклеточного ацидоза, что приводит к угнетению дыхательного центра и нарушению компенсаторных процессов нейтрализации внутриклеточного ацидоза [11], а также к увеличению
Так как объем субтенториального пространства весьма ограничен, клинические проявления возникают даже при небольшой степени отека мозга. Уже давно известно, что пациенты с острой печеночной недостаточностью могут погибнуть в результате ущемления мозжечка, в связи с увеличением давления в субтенориальном пространстве [13]. В описываемом случае повышение внутричерепного давления в этой области привело к сдавлению ствола мозга и последующему нейрогенному отеку легких, при выздоровлении у пациентки отмечались некоординированные движения глазных яблок. При печеночной недостаточности может иметься нарушение кровоснабжения головного мозга, и принудительная ультрафильтрация может еще более нарушать мозговой кровоток, и, как следствие, эффект отдачи в отношении внутричерепного давления, в результате резкого снижения перфузионного давления мозга [14]. Также относительно частым осложнением интермиттирующего гемодиализа является гипотония [14]. Гипотония может приводит к снижению церебрального кровотока у пациентов с острой печеночной недостаточностью.
По данным некоторых авторов, следует принимать ряд мер для поддержания сердечно-сосудистой стабильности у тяжелых пациентов при проведении интермиттирующего гемодиализа [15,16]. Этот подход в описываемом случае был реализован использованием диализата с высокой концентрацией натрия (в сравнении с плазменной), охлажденного, применением синтетических биосовместимых диализаторов и низкой скорости кровотока, ультрафильтрацией 200 мл/час, без антикоагуляции. После сеанса диализа осмолярность плазмы не изменилась. Однако, несмотря на предпринятые меры, быстро наступило ухудшение состояния пациентки, в связи с вазогенным отеком заднего мозга и развитием нейрогенного отека легких.
После приема парацетамола (суицидальная попытка) прошло 9 дней, и не имелось каких-либо признаков печеночной комы, восстановление головного мозга произошло не полностью, и сохранялась повышенная чувствительность к гемодиализ-индуцированному повреждению.
Ранее уже описывались случаи гибели пациентов при отравлении парацетамолом от отека мозга, несмотря на начальное улучшение состояния и хороший прогноз [5]. В меньшей степени на внутричерепное давление оказывает влияние низкообъемная непрерывная заместительная почечная терапия, и этим методам следует отдавать предпочтение у пациентов с высоким риском отека мозга [17].
Какие выводы следует делать из данного случая:
1) Пациенты с острой печеночной недостаточностью имеют повышенный риск развития отека мозга
2) Даже если отсутствуют клинические признаки печеночной энцефалопатии, это не означает, что функции головного мозга находятся в норме
3) Интермиттирующий гемодиализ может приводить к накоплению внутримозговой интерстициальной жидкости
4) Несмотря на то, что был использован диализат с высокой концентрацией натрия, охлажденный, установлена низкая скорость кровотока, интермиттирующий гемодиализ привел к ухудшению состояния пациентки
5) У пациентов с повышенным риском отека мозга предпочтительно применять низкообъемные непрерывные методы проведения заместительной почечной терапии, так как они в меньшей степени приводят к нарушению мозгового кровотока и внутричерепного давления
Литература
1. Varghese J, Ilias-Basha H, Dhanaseliaran R, et al. Hepatopulmonary syndrome—past to present. Ann Hepatol (2007) 6:135–142.
2. Leaver SK, Evans TW. Acute respiratory distress syndrome. Br Med J (2007) 335:389–394.
3. Baumann A, Audibert G, McDonnell J, et al. Neurogenic pulmonary oedema. Acta Anaesthesiol Scand (2007) 51:447–455.
4. Larson AM. Acetaminophen hepatotoxicity. Clin Liver Dis (2007) 11:525–548.
5. Jalan R. Intracranial hypertension in acute liver failure: pathophysiological basis of rational management. Semin Hepatol (2003) 23:271–282.
6. Davenport A, Finn R. Paracetamol (acetaminophen) poisoning resulting in acute renal failure without hepatic coma. Nephron (1988) 50:55–56.
7. Davenport A, Will EJ, Davison AM, et al. Changes in intracranial pressure during haemofiltration in oliguric patients with grade IV hepatic encephalopathy. Nephron (1989) 53:142–146.
8. Arieff AI. Dialysis disequilibrium syndrome: current concepts on pathogenesis and prevention. Kidney Int (1994) 45:629–635.
9. Trinh-Trang-Tan MM, Carton JP, Bankir L. Molecular basis for the dialysis disequilibrium syndrome: altered aquaporin and urea transporter expression in the brain. Nephrol Dial Transplant (2005) 20:1984–1988.
10. Jones JG, Bembridge JL, Sapsford DT, et al. Continuous measurement of oxygenation saturation during haemodialysis. Nephrol Dial Transplant (1992) 7:110–116.
11. Arieff AI, Guisado R, Massry SG, et al. Central nervous system pH in uremia and the effects of hemodialysis. J Clin Invest (1976) 58:306–310.
12. Ware AJ, D’Agostino A, Coombes B. Cerebral oedema: a major complication of massive hepatic necrosis. Gastroenterol (1971) 61:877–884.
13. Davenport A, Will EJ, Losowsky MS. Rebound surges of intracranial pressure as a consequence of forced ultrafiltration used to control intracranial pressure in patients with severe hepatorenal failure. Am J Kidney Dis (1989) 14:516–519.
14. Davenport A. Intradialytic complications during hemodialysis. Hemodial Int (2006) 10:162–167.
15. Schortgen F, Soubrier N, Delclaux C, et al. Haemodynamic tolerance of intermittent haemodialysis in critically ill patients. Am J Respir Crit Care Med (2000) 162:197–202.
16. Vinsonneau C, Camus C, Combes A. Hemodiafe Study Group. Continuous venovenous haemodiafiltration versus intermittent haemodialysis for acute renal failure in patients with multiple-organ dysfunction syndrome: a multicentre randomised trial. Lancet (2006) 368:379–85.
17. Davenport A. Renal replacement therapy in the patient with acute brain injury. Am J Kidney Dis (2001) 37:457–466.
Гемодиализ специалистам
www.medservis.az/dia_doctor.htm
Нейрогенный отек легких
Нейрогенный отек легких описан при заболеваниях ЦНС у лиц без предшествующих нарушений функции левого желудочка. Экспериментально доказано, что в возникновении отека легких важную роль играет повышение симпатического тонуса, однако точные механизмы не выяснены. Известно, что возбуждение симпатических нервов вызывает спазм артериол. повышение АД и централизацию гемодинамики ; кроме того, возможно уменьшение податливости левого желудочка. Все это ведет к повышению давления в левом предсердии и отеку легких, в основе которого лежат нарушения гемодинамики. Имеются экспериментальные данные о том, что стимуляция адренорецепторов непосредственно повышает проницаемость капилляров, но этот эффект имеет меньшее значение, чем нарушение равновесия между гидростатическим и онкотическим давлением.
Нейрогенный отек легких
Гидроэнцефалия
Эпидемиология
Встречаемость: 1-1,5%.