Врожденные пороки сердца
Симптомы врожденных пороков сердца
- Симптомы врожденных пороков (возникших внутриутробно) сердца зависят от вида порока и степени его тяжести.
- Иногда симптомы появляются сразу после рождения или в раннем детском возрасте, реже в подростковом возрасте.
- В некоторых случаях небольшие врожденные пороки могут не проявлять себя на протяжении всей жизни или проявлять себя незначительно, с неспецифическими (характерными для многих заболеваний или состояний) жалобами, и быть случайно обнаруженными при ультразвуковом исследовании (УЗИ) сердца.
- Все симптомы врожденных пороков сердца можно объединить в четыре группы, или синдромы (несколько симптомов, объединенных общим источником происхождения или причинным фактором).
- Симптомы со стороны сердца (кардиальный синдром):
- боли в области сердца;
- сердцебиение;
- ощущение перебоев в работе сердца.
- Симптомы, связанные с развитием сердечной недостаточности (состояния, при котором сердце неспособно полноценно выполнять свою функцию по перекачиванию крови):
- бледность или цианоз (синюшность) кожи;
- акроцианоз (синюшная окраска носа, носогубного треугольника, кончиков пальцев);
- изменение формы грудной клетки (сердечный горб) – выпячивание грудной клетки в области сердца;
- одышечно-цианотические приступы – возникновение одышки, чувства нехватки воздуха, посинения кожных покровов, головокружения, слабости;
- выраженное снижение работоспособности, утомляемость, неспособность выполнять физическую нагрузку, обмороки.
- Симптомы, связанные с хронической системной гипоксией (недостаточным поступлением кислорода во все органы и ткани организма):
- отставание в росте и развитии;
- симптом барабанных палочек (утолщение концевых фаланг пальцев рук и ног);
- симптом часовых стекол (утолщенные синевато-прозрачные ногти);
- постоянная бледность кожи, отсутствие румянца.
- Симптомы дыхательных нарушений (при ухудшении работы легких из-за порока сердца):
- одышка,
- кашель.
Формы
В зависимости от того, у больных какого пола чаще встречается данный порок сердца, выделяют несколько видов пороков.
- « Женские» пороки – порок в полтора и более раза чаще встречается у девочек (женщин), чем у мальчиков (мужчин). Открытый артериальный проток (незаращение сообщения между аортой и легочной артерией, которое функционирует во внутриутробном периоде), дефект межпредсердной перегородки, дефект межжелудочковой перегородки + открытый артериальный проток, триада Фалло (дефект межпредсердной перегородки + сужение устья легочной артерии + гипертрофия (увеличение) правого желудочка).
- « Мужские» пороки – порок в полтора и более раза чаще встречается у мальчиков (мужчин), чем у девочек (женщин). Аортальный стеноз (сужение просвета аорты в области клапана), аномалия соединения легочных вен, коарктация (сужение в области перешейка) аорты, коарктация аорты + открытый артериальный проток, транспозиция (неправильное положение, перемена местами) магистральных (крупнейших) сосудов.
-
Нейтральные пороки – встречаются приблизительно с одинаковой частотой у женщин и мужчин:
- простые пороки – представляют собой « возврат к прошлому», то есть отражают строение сердца предков животных из-за остановки развития части сердца в ранние сроки развития (2-3 месяца беременности) – дефект аорто-легочной перегородки, дефект предсердной перегородки, стеноз (сужение просвета) легочной артерии;
- сложные пороки – развитие сердца нарушается на более поздних стадиях развития плода (4 – 7 месяцы беременности) – дефект предсердно-желудочковой перегородки, аномалия Эбштейна (деформации трехстворчатого клапана из-за неправильного прикрепления его створок), атрезия (отсутствие) трехстворчатого клапана.
В зависимости от характера нарушений в кровообращении, вызванных пороком сердца, выделяют две большие группы врожденных пороков сердца.
-
Белые (бледные) пороки – название пороков произошло от характерной бледности кожных покровов. При этих пороках не происходит смешивания артериальной (обогащенной кислородом) и венозной (насыщенной углекислым газом) крови. К белым порокам относятся:
- пороки с обогащением малого круга кровообращения (задержка крови в легких) – открытый артериальный проток, дефект межпредсердной перегородки, дефект межжелудочковой перегородки;
- пороки с обеднением малого круга кровообращения (недостаточное поступление крови к легким для обогащения кислородом) – стеноз (сужение) легочной артерии;
- пороки с обеднением большого круга кровообращения (недостаточное поступление крови к органам и тканям организма) – аортальный стеноз (сужение просвета аорты в области клапана), коарктация аорты (сужение просвета аорты в области перешейка);
- пороки без существенного нарушения распределения крови в кругах кровообращения (диспозиции (неправильное положение) сердца – декстрокардия (расположение сердца справа), синистрокардия (более левое положение сердца), мезокардия (расположение сердца в середине грудной клетки) и дистопии (нетипичное расположение сердца) – шейное, грудное (в плевральное полости – полости, содержащей легкое), брюшное (в брюшной полости)).
-
Синие пороки – название пороков произошло из-за характерной синюшности кожных покровов. При этих пороках происходит смешивание артериальной и венозной крови, из-за чего органы и ткани организма получают недостаточно обогащенную кислородом кровь. К синим порокам относятся:
- пороки с обогащением малого круга кровообращения (задержкой крови в легких) – транспозиция магистральных сосудов;
- пороки с обеднением малого круга кровообращения (недостаточным поступлением крови к легким для обогащения кислородом) – тетрада Фалло (стеноз (сужение) легочного ствола + дефект межжелудочковой перегородки + декстрапозиция (правое расположение) аорты + гипертрофия (увеличение в размерах) правого желудочка).
Также в зависимости от характера нарушения в строении сердца выделяют:
- гипоплазии (недоразвитие отделов сердца);
- дефекты обструкции (нарушение строения клапанов сердца – специальных заслонок, обеспечивающих правильное поступление крови из одного отдела сердца в другой (из предсердия в желудочек, из желудочка в магистральный сосуд (аорту или легочной ствол));
- дефекты перегородок (отверстия или полное отсутствие перегородок, отграничивающих левые отделы сердца от правых).
Врожденные пороки сердца
Причины врожденных пороков сердца
Как известно, сердце — это важный орган в теле человека, от правильной его работы зависит благополучие всего организма. Сердце состоит из мышечной (миокард) и соединительной ткани (сердечные клапаны, стенки крупных сосудов). Деятельность сердца обусловлена ритмичным и последовательным сокращением составляющих его структур (предсердия и желудочки), в результате чего кровь, протекая через легкие, насыщается кислородом (так называемый малый круг кровообращения) и разносит кислород по всем органам и тканям (большой круг кровообращения).
Когда сердце плода развивается во время беременности, его работа отличается от работы сердца новорожденного ребенка и взрослого человека. В частности, малый круг кровообращения полноценно начинает функционировать только во время родов, когда происходит раскрытие легких новорожденного, и в момент первого крика они наполняются кровью. Поэтому в сердце плода существуют специальные отверстия и протоки, позволяющие циркулировать крови в формирующемся организме в обход легких (артериальный проток, соединяющий аорту и легочную артерию, овальное окно между предсердиями, венозный проток между пупочной веной и нижней полой веной).
Иногда под действием неблагоприятных факторов в период внутриутробного развития происходят грубые нарушения формирования анатомических структур сердца, что сказывается на его деятельности и не всегда совместимо с жизнью ребенка. Тогда либо по УЗИ плода во время беременности, либо в первые дни после родов новорожденному устанавливается диагноз врожденного порока развития сердца. Что это такое, каков прогноз для жизни и какие методы сохранения жизни и здоровья таких малышей предлагает современная медицина, мы и попробуем выяснить в данной статье.
Итак, эти патологические состояния представляют собой многочисленную группу заболеваний сердца, объединенных следующими признаками:
— возникают в период внутриутробного развития;
— характеризуются грубейшими нарушениями архитектоники сердца и крупных сосудов (аорта, нижняя и полая вена, легочные артерия и вены);
— анатомические изменения вызывают значительные нарушения в гемодинамике (циркуляции крови по организму);
— обусловлены недоразвитием анатомических структур или переменой их нормального расположения в сердце.
Частота распространенности варьирует от 6 до 9 на 1000 живых новорожденных. По данным разных авторов, возможных вариантов врожденных пороков развития сердца насчитывается от 50 до 100.
Схематичное изображение некоторых пороков сердца
Причины врожденных пороков сердца
В связи с тем, что во время внутриутробного развития происходит активное формирование всех органов человеческого организма, особенно сердца, плод и беременная женщина уязвимы к действию различных негативных факторов. Так, влияние на неправильное течение органогенеза могут оказать повышенный радиационный фон, ионизирующее излучение, инфекционные заболевания матери, особенно вирусные – краснуха, корь, ветрянка, герпес; прием некоторых лекарственных и токсических веществ (наркотиков, алкоголя) в период беременности, особенно в первом триместре (8 -12 –я недели – период наиболее интенсивного формирования всех органов плода). В 4 – 10% случаев врожденные пороки генетически обусловлены, то есть передаются по наследству.
Симптомы врожденных пороков сердца
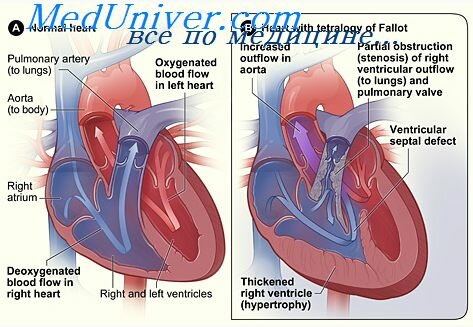
Клиническая симптоматика пороков зависит от их вида. Выделяют пороки «синего» и «белого» типов, а также пороки, создающие препятствие кровотоку.
Основным проявлением «синих» пороков (транспозиция (перемена расположения) магистральных артерий, тетрада Фалло, атрезия – заращение — трикуспидального клапана) является цианоз – синее окрашивание кожи пальцев, кистей, стоп, носогубного треугольника, ушей, носа или, в крайне тяжелых случаях, всего тела. Также проявлением артериальной гипоксемии (пониженного содержания кислорода) являются одышка, потеря сознания с судорогами или без, тахикардия (учащенное сердцебиение), отставание в росте и развитии, частые простудные заболевания, неврологическая симптоматика в связи с отсутствием нормального кровоснабжения головного мозга. Как правило, пороки этого типа проявляют себя уже в первые часы и дни жизни новорожденного ребенка. Транспозиция магистральных артерий (полые вены входят в левое, а не правое предсердие, а аорта отходит от правого, а не левого желудочка) является тяжелым пороком, несовместимым с жизнью, и ребенок, как правило, погибает сразу после родов. Также к несовместимым с жизнью порокам относится трехкамерное сердце (два предсердия и один желудочек, или одно предсердие и два желудочка). Летальность пороков данного типа очень высока, если дети с такими пороками выживают в первые дни жизни, то без лечения погибают к концу первого – второго года.
К порокам белого типа относятся дефект межжелудочковой перегородки, открытый Боталлов (артериальный) проток, дефект межпредсердной перегородки. Клинически эти пороки могут начать проявлять себя не в период раннего, детства, а к 16 – 20 годам. Симптомы пороков белого типа следующие: бледность кожных покровов, отставание в развитии, частые ОРВИ, признаки развивающейся правожелудочковой недостаточности – одышка и тахикардия при физической нагрузке или в покое.
Пороки с препятствием кровотоку: стеноз (сужение просвета) аорты, коарктация (сегментарное сужение) аорты, стеноз легочной артерии клинически проявляются одышкой, тахикардией, болями в грудной клетке, снижением выносливости, отеками, отставанием в развитии и нарушением кровообращения нижней половины туловища. При коарктации аорты дети доживают максимум до 2 –летнего возраста.
Диагностика врожденных пороков развития сердца
Как правило, диагностировать пороки развития плода, в том числе и сердца, возможно еще на этапе ультразвукового обследования беременной женщины. Тогда, в зависимости от вида порока, женщине может быть рекомендовано либо прерывание беременности (при пороках, не совместимых с жизнью, при множественных уродствах и т. д.), либо сохранение беременности с более детальным обследованием беременной и решением вопроса об оперативном лечении ребенка сразу или через некоторое время после родов. Но иногда в силу некоторых причин (не посещение беременной женской консультации и УЗИ кабинета, недостаточное оснащение фельдшерско-акушерских пунктов УЗИ аппаратурой и т. д.) пороки развития могут быть диагностированы только после родов.
Несмотря на то, что симптомы врожденных пороков достаточно яркие, в процессе клинического осмотра новорожденного ребенка диагноз можно только предположить, так как многие симптомы не являются строго специфичными, а могут быть обусловлены другими тяжелыми состояниями новорожденных (респираторный дистресс синдром, внутричерепные кровоизлияния и т. д.). Также не все пороки могут давать характерную аускультативную картину (в процессе выслушивания грудной клетки), и наоборот, шумы, щелчки или иные аускультативные проявления могут встречаться при незначительных отклонениях от нормы в строении сердца (малые аномалии ). Поэтому, если порок сердца не был диагностирован по УЗИ плода, всем деткам с симптомами нарушения кровообращения (диффузный или акроцианоз, одышка при кормлении или в покое, потеря сознания, судороги), должно быть произведено УЗИ сердца во время пребывания в роддоме.
Эхокардиография (УЗИ сердца) это один из самых информативных методов визуализации пороков сердца. Также могут быть назначены ЭКГ (покажет нарушения ритма, гипертрофию предсердий и/или желудочков, если таковые имеются), рентгенография грудной клетки (покажет застой крови в легких, если есть, увеличение тени сердца в связи с расширением его камер). В особо сложных случаях или перед оперативным лечением могут быть назначены вентрикулография (введение рентгенконтрастного вещества в полость желудочков сердца), ангиография (введение контраста через сосуды в полости сердца), зондирование камер сердца с измерением в них давления.
Теперь остановимся подробнее на ультразвуковой диагностике часто встречающихся пороков сердца.
А. Врожденные порки сердца с объемной перегрузкой сосудов в легких (малого круга кровообращения).
1. Дефект межпредсердной перегородки — с помощью одномерной эхокардиографии выявляются признаки объемной перегрузки и дилатации (расширения) правого желудочка, при двухмерной эхокардиографии виден обрыв эхосигнала между предсердиями, а при допплер исследовании оценивается турбулентный (с «завихрениями») поток крови через межпредсердную перегородку и степень нарушений легочного кровотока.
2. Дефект межжелудочковой перегородки — при проведении УЗИ сердца визуализируются отверстие в перегородке между желудочками, дилатация левого и правого желудочков, турбулентный кровоток из левого в правый желудочек, оценивается степень тяжести легочной гипертензии, измеряется разница давления в желудочках.
Так проявляется дефект перегородки между желудочками при проведении эхокардиографии с допплером. Слева — нормальная межжелудочковая перегородка, справа — ее дефект (VSD).
3. Открытый Боталлов проток – проявляется на эхокардиографии непрерывным кровотоком посредством сообщения в аорте и легочной артерии, изменением кровотока в устье легочного ствола.
4. Коарктация аорты – виден сегментарный участок сужения просвета аорты, ускоренный поток крови ниже сегмента.
5. Транспозиция магистральных артерий – визуализируется неправильное отхождение сосудов от сердца.
Б. Пороки сердца с уменьшением объема крови в малом круге кровообращения.
1. Тетрада Фалло – при эхокардиографии помимо стеноза (сужения) легочной артерии и дефекта перегородки между желудочками, определяется гипертрофия правого желудочка и отхождение аорты из правого желудочка, также оценивается степень нарушения внутрисердечной гемодинамики.
2. Стеноз легочной артерии – выявляется сужение просвета легочной артерии, и ускорение кровотока в устье легочной артерии и гипертрофия правого желудочка.
3. Аномалия Эпштейна – патология развития трехстворчатого клапана сердца, когда створки клапана прикрепляются не к фиброзному кольцу между предсердием и желудочком справа, а к стенкам правого желудочка, что вызывает уменьшение его объема. При ЭХО – КГ определяется патология клапана, оценивается степень расширения полостей сердца и нарушения внутрисердечного тока крови.
4. Атрезия трикуспидального клапана – при ЭХО – КГ отсутствует отражение эхосигнала от трикуспидального клапана, регистрируется гипертрофия правого предсердия и левого желудочка.
В. Пороки сердца с уменьшением объема циркулирующей крови в большом круге кровообращения (в сосудах всех жизненно важных органов).
1. Коарктация аорты (см. выше).
2. Изолированный стеноз аорты – оценивается степень сужения, визуализируется ускоренный кровоток через аортальный клапан и деформированные створки клапана.
Г. Пороки сердца без нарушения гемодинамики.
— Декстрокардия (зеркальное расположение сердца справа) – достаточно редкая аномалия, по УЗИ сердца нарушений гемодинамики, как правило, не регистрируется.
Лечение врожденных пороков развития сердца
Полное излечение подавляющего большинства пороков сердца возможно только с помощью их хирургической коррекции. Кардиохирургические операции могут быть проведены в первые часы или дни жизни новорожденного, либо на первом году жизни ребенка. При открытом артериальном протоке допустима выжидательная тактика (при отсутствии симптомов жизнеугрожающих состояний), так как этот проток может самостоятельно закрываться в первые два года жизни.
Операции могут выполняться как на открытом сердце (с рассечением стенки грудной клетки), так и кардиоваскулярным методом (когда доступ к сердцу осуществляется посредством введения в сосуды зонда, достигающего полостей сердца). Последний метод, например, применяется при коррекции дефектов между предсердиями или желудочками, к которым с помощью зонда подводится окклюдер, закрывающий отверстия.
Но при некоторых пороках сердца, не совместимых с жизнью, например, трехкамерное сердце (одно предсердие и два желудочка, или два предсердия и один желудочек) проведение хирургической коррекции, к сожалению, не возможно.
Кроме кардиохирургической операции, пациенту назначается медикаментозная терапия для улучшения сократительной функции сердца и «разгрузки» малого круга кровообращения. Применяются ингибиторы АПФ (эналаприл, периндоприл, лизиноприл, рамиприл и др), диуретики (фуросемид, индапамид и др), В-адреноблокаторы (карведилол, бисопролол и др).
Образ жизни с врожденным пороком сердца
Пациенту необходимо соблюдать следующие рекомендации относительно его образа жизни:
— рациональное сбалансированное питание;
— соблюдение диеты с ограничением поваренной соли и объема потребляемой жидкости (для уменьшения объемной перегрузки сердца и сосудов);
— достаточное пребывание на свежем воздухе;
— исключение любых занятий спортом и ограничение сильных физических нагрузок;
— достаточный по продолжительности сон;
— регулярное наблюдение у кардиолога и кардиохирурга с проведением необходимых лечебно-диагностических мероприятий;
— беременность женщинам с пороками «синего» типа строго противопоказана, но если было проведено хирургическое лечение, то возможность сохранения беременности определяется в каждом конкретном случае индивидуально с совместным ведением беременной кардиохирургом, кардиологом и акушер-гинекологом в специализированном стационаре. Родоразрешение, как правило, проводится путем кесарева сечения.
Прогноз при врожденных пороках сердца
Прогноз для жизни большинства пороков сердца неблагоприятный. Как уже было сказано выше, кардиохирургическое лечение таким деткам требуется в первые дни и месяцы после родов, иначе они погибают в течение первых двух лет из–за прогрессирования сердечной недостаточности или присоединения осложнений (бактериальный эндокардит, фатальные нарушения ритма, повышенный риск тромбообразования и тромбоэмболических осложнений, частые заболевания бронхолегочной системы (затяжные бронхиты, тяжелые пневмонии). Исключение составляют пороки белого типа, при которых в случае отсутствия хирургического лечения в силу каких либо причин дети способны доживать до 16 – 18 лет.
После хирургической коррекции прогноз для жизни благоприятный, но все равно состояние ребенка остается достаточно серьезным, поэтому за такими детьми должно осуществляться усиленное наблюдение родителей и врачей.
В заключение хотелось бы отметить, что данный диагноз у ребенка на современном этапе развития медицины не является приговором, так как возможности отечественной и зарубежной кардиологии детского возраста позволяют выносить, родить и вырастить малыша, способного вести полноценный образ жизни, несмотря на столь тяжелое заболевание.
Врач терапевт Сазыкина О.Ю.
Добавить комментарий
Если Вам это близко, выговоритесь. Поделитесь с товарищами по несчастью, и Вас обязательно поддержат!
Врожденные пороки сердца
Распространенность. Врожденные пороки сердца являются результатом отклонений от нормального внутриутробного развития системы кровообращения ребенка и заключаются в изменениях нормального строения сердца и его сосудов. Данные нарушения могут быть первичными (имеются к моменту рождения ребенка) и вторичными (развиваются как следствие первичною порока). Частота выявляемости врожденных пороков сердца и крупных сосудов составляет 0,5 % всех родившихся детей и 0,2 % у детей после 2 лет жизни. В нашей стране в 2000 г. зарегистрированы 265 000 человек (из них 40 000 выявлены впервые) с врожденными пороками сердца. Почти 50 % новорожденных умирают в течение 1-го месяца жизни, если им не оказывают надлежащую помощь; еще 25 % погибают к концу года. Эти цифры подтверждают высокую актуальность данной проблемы и ее значимость в снижении детской смертности и проблеме демографии населения в целом.
Чаше всего речь идет об отсутствии разделения кровообращения на большой и малый круг вследствие дефектов сердечных перегородок или при функционирующем эмбриональном соустье. Если в венозное русло поступает артериальная кровь, то говорят об артерио-венозном (АВ) сбросе или соустье, а в обратном случае — венозно-артериальном (ВА) сбросе или соустье. Около 20-35 % всех врожденных пороков относятся к нецианотичным порокам, т. с. таким порокам, при которых кожные покровы сохраняют обычный цвет.
В настоящее время известно более 100 видов врожденных пороков. В Москве с населением 8 100 000 человек на 100 000 детей 800-900 имеют врожденные пороки сердца. В данной главе представлены только наиболее частые из них.
Классификация. При врожденных пороках имеются 3 группы изменений- морфологические, гемодинамические и клинические. Согласно этому, различают 3 группы врожденных пороков сердца .
1. Пороки, когда есть внутрисердечное сообщение с АВ-сбросом крови:
— открытый артериальный (боталлов) проток;
— дефект межжелудочковой перегородки (болезнь Голочинова- Роже);
— дефект межпредсердной перегородки, при котором легочный кровоток увеличен («белые» пороки).
2. Пороки, когда есть внутрисердечное сообщение с ВА-сбросом крови:
— триада и тетрада Фалло;
— болезнь Эйзенменгера;
— атрезия трехстворчатого клапана, транспозиция сосудов и др.; легочный кровоток в малом круге уменьшен («синие» пороки).
3. Пороки без внутрисердечного сообщения. при которых нарушение кровообращения вызвано сужением магистральных сосудов, расположенных в средостении:
— изолированное сужение легочной артерии;
— стеноз устья аорты;
— коарктация аорты и др.
Пороки магистральных сосудов
Открытый артериальный (боталлов) проток (ОАП) — представляет собой короткий тонкостенный сосуд, соединяющий аорту (Ао) с легочным стволом (ЛС), составляет 20-25 % всех врожденных пороков сердца. Расположен он внеперикардиально. В норме боталлов проток играет важную роль в кровоснабжении плода. Обычно он облитерируется (закрывается) в первые сутки жизни, в крайнем случае через месяц. Если он продолжает функционировать, возникает артериовенозный сброс, вызывающий гемодинамические нарушения.
Анатомически артериальный проток располагается в верхнем отделе верхнего средостения. Он прикрыт листком париетальной плевры. Диаметр его обычно не превышает 1 -1,5 см. От аорты он отходит на уровне левой подключичной артерии, нередко сливаясь со стволом легочной артерии в месте деления на правую и левую легочную артерии (рис. 1).
Рис. 1. Топографо-анатомическая схема открытого артериального протока.
#image.jpg
Патогенез заболевания заключается в том, что при систоле левого желудочка (ЛЖ) часть артериальной крови из аорты поступает через проток в легочную артерию, где смешивается с венозной кровью. Сброс артериальной крови может достигать 50-70 % ударного объема ЛЖ. В большом круге кровообращения из-за этого возникает гипоперфузия и ухудшается снабжение органов и тканей кислородом, снижается АД.
В малом круге кровообращения, наоборот, давление из-за переполнения кровью повышается (гипертензия легочного круга кровообращения). Возникает фиброз сосудов в легких, что еще больше повышает давление малого круга. Правый желудочек и легочная артерия гипертрофируются и расширяются. Нарастание давления в малом круге ведет к тому, что АД в легочной артерии становится выше, чем в аорте, поэтому направление кровотока меняется в обратную сторону и венозная кровь начинает поступать в аорту. Это ухудшает снабжение кислородом органов и тканей и вызывает их кислородное голодание.
Клиническая картина включает в себя ряд признаков. Визуально дети с таким пороком обычно бледные, отстают в росте и массе тела, но с сохраненным умственным развитием. С возрастом появляется одышка -основная жалоба, которая вначале связана с физической нагрузкой, а со временем становится постоянной. Одновременно с одышкой появляются головная боль, утомляемость, боль в сердце, носовые кровотечения, частые пневмонии. Цианоза обычно нет. При пальпации слева от грудины определяется систолическое дрожание («кошачье мурлыканье»). Аускультативно отмечается непрерывный систолодиастолический «машинный» шум в результате кровотока через открытый артериальный проток и встречи двух потоков крови: из правого желудочка (ПЖ) и из аорты — в легочную артерию. Шум лучше выслушивается на легочной артерии, во втором межреберье слева от грудины и распространяется в подключичное и межлопаточное пространство слева. Если на вдохе задержать дыхание, шум уменьшается, а если задержать на выдохе -усиливается (симптом Вальсальвы). В литературе этот шум описан как «шум грохота поезда в тоннеле» или «шум мельничного колеса». С развитием легочной гипертензии появляется акцент II тона над легочной артерией.
При УЗИ сердца определяются диаметр ОАП и сброс крови по нему (рис. 2).
Рис. 2. УЗИ сердца (цветное допплеровское картирование). Виден сброс-крови по открытому артериальному протоку.
#image.jpg
При рентгенологическом исследовании выявляется умеренное увеличение сердца в поперечнике, выбухает вторая дуга левого контура. Корни легких застойные. Отмечается расширение левого предсердия (ЛП), левого желудочка (ЛЖ), основного ствола и ветвей легочной артерии, усиление легочного рисунка. При рентгеноскопии выявляется усиление пульсации восходящей аорты.
Диагноз подтверждается эхокардиографией и ЭКГ, где регистрируются признаки перегрузки левого желудочка, а при нарастании клинической картины — и правых отделов сердца.
На ФКГ шум имеет характерное расположение во втором межреберье слева от грудины с увеличением амплитуды II тона. Отмечается низкое АДдиаст при нормальном АДсист. Появляется усиленная пульсация сонных артерий — «пляска каротид».
Если диагноз открытого артериального протока сомнителен, применяют зондирование сердца. При этом можно видеть прохождение зонда из легочной артерии в аорту. Одновременно исследуют оксигенацию крови: в пробах крови из легочной артерии она выше, чем в правом желудочке.
Осложнениями данного вида порока может быть воспаление стенок протока или (в более старшем возрасте) его обызвествление.
Лечение данного порока оперативное, спонтанная его облитерация наблюдается редко. Операцию ликвидации открытого артериального протока можно выполнить в любом хирургическом отделении под интубационным наркозом. Следует помнить, что чем раньше выполнена операция, тем лучше результат.
Первую попытку (неудачную) в 1937 г. выполнил Strieder; успешное вмешательство осуществлено в 1938 г. R. Gross. В СССР данное вмешательство сделал впервые А. Н. Бакулев в 1948 г.
Техника операции заключается в торакотомии из левостороннего, в третьем-четвертом межреберье, бокового доступа, перевязки протока двумя лигатурами (иногда с прошиванием) (рис. 3).
Рис. 3. Открытый артериальный проток (операционное поле).
При большой ширине протока его можно прошить аппаратом механического шва типа УАП. В последние годы разработан метод эндоваскулярной окклюзии ОАП. С помошью зонда в артериальный проток проводят полимерную быстротвердеющую массу (обтуратор). Ближайшие и отдаленные результаты хорошие. Следует помнить, что у взрослых операция может осложняться прорезыванием лигатуры вследствие кальциноза стенки артериального протока.
Прогноз заболевания определяют сроки оперативного вмешательства (лучше ее выполнять в возрасте до 5 лет), а также развитие легочной гипертензии и склерозирование легких.
Коарктация аорты
Коарктация аорты (coarctare -прижимать, сужать)- врожденное сужение аорты или даже полное закрытие ее просвета на ограниченном участке; регистрируется у 30 % больных с врожденными пороками сердца.
Чаще (в 95 %) сужение наблюдается в месте перехода дуги в нисходящую грудную аорту, чуть ниже левой подключичной артерии, но может быть в любом месте. Иногда коарктация сочетается с открытым артериальным протоком.
Патогенез заболевания заключается в том, что в аорте, выше места сужения, повышается давление крови. Гипертензия в системе сосудов мозга вызывает церебральные симптомы, систолическую перегрузку левого желудочка и гипертрофию миокарда, вследствие чего появляется диффузный миофиброз с последующей декомпенсацией левого желудочка. АД крови ниже места коарктании значительно снижено. Иногда на периферических артериях не удается определить пальпаторно пульс. В связи с этим ошибочно устанавливается диагноз облитерирующего заболевания артерий конечностей.
Клиническая картина.
Жалобы больных при этой патологии непостоянны: отмечены головокружение, головная боль, утомляемость ног при ходьбе (симптом перемежающейся хромоты). АД крови в артериях рук повышено, а в артериях ног снижено. В результате изменений кровообращения нарушается функция почек. Иногда обнаруживается пульсация межреберных артерий.
При осмотре больных с признаками надклапанного стеноза нередок их характерный внешний вид (выпячивание губы, низко расположенные уши, косоглазие), а также признаки умственной отсталости.
Пальпация может обнаружить приподнимающий верхушечный толчок в пятом-шестом межреберье слева. Определяется систолическое дрожание во втором межреберье справа от грудины. Аускультативно выслушивается систолический шум в проекции места коарктании.
Возможна гипертрофия левого желудочка, которая определяется на рентгенограммах. Контуры первой и второй дуг в прямой проекции напоминают цифру «3» (симптом «тройки»). Характерный признак коарктации аорты — узурация 3 и 4 пар верхних ребер.
Важнейшим методом исследования при аортальном стенозе является левосторонняя вентрикулограмма. При этом на сериях снимков можно видеть местоположение, форму, размер и степень сужения аорты, а также состояние сосудов, отходящих от дуги аорты.
На ЭКГ никаких характерных постоянных изменений не обнаруживают. ФКГ выявляет грубый систолический шум справа от грудины и в яремной ямке, проводящийся на сосуды шеи.Лечение коарктации аорты только оперативное. При сегментарной коарктации аорты выполняют :
— резекцию суженного участка с анастомозом аорты конец в конец;
— резекцию аорты с замещением пораженного участка эндопротезом (экефлоновый, фторлон -лавсановый и др.);
— истмопластику синтетической заплатой.
Прогноз заболевания в значительной степени зависит от возраста больных. Лучшие результаты отмечены у детей в возрасте до 3 лет. У взрослых операция в сочетании с фармакологическим лечением позволяет существенно улучшить качество жизни и продлить ее.
Стеноз легочной артерии — изолированное сужение легочной артерии относится к порокам «белого» (ацианотического) типа и встречается в 2-9 % клинических наблюдений врожденных аномалий.
Стеноз устья легочной артерии создаст препятствие на пути оттока крови из правого желудочка в легочную артерию. По мере нарастания стеноза систолическое давление и работа правого сердца увеличиваются. Вначале наступает гипертрофия правого желудочка, которая в дальнейшем переходит в его недостаточность. Вследствие этого вторично гипертрофируется и расширяется правое предсердие и возникает относительная недостаточность трехстворчатого клапана. В далеко зашедших случаях наблюдается добавочная пульсация вен шеи, пульсация печени и асцит.
Клиническая картина заболевания зависит от степени сужения легочной артерии. В легких случаях отмечается бессимптомное течение. Объективно — кожные покровы бледные («белый» порок), имеется одышка, усиливающаяся при физической нагрузке, выявляется отставание в росте и развитии. В более поздних стадиях одышка появляется в покое и резко усиливается при малейшем движении.
При осмотре области сердца обнаруживается сердечный горб. При пальпации определяется систолическое дрожание, перкуторно — увеличение размеров сердца вправо, при аускультации — грубый «скребущий» систолический шум по левому краю грудины. Интенсивность шума пропорциональна степени стеноза. АД и пульс находятся в пределах нормы.
Рентгенологически выявляется увеличение правого желудочка и второй дуги по левому контуру сердца вследствие постстенотического расширения легочной артерии.
На ЭКГ при сужении легочной артерии отмечаются признаки гипертрофии правого желудочка. ФКГ выявляет систолический шум ромбовидной формы.
При катетеризации сердца типичным признаком является высокий градиент систолического давления между правым желудочком и легочной артерией.
Лечение оперативное. Операцию проводят в условиях гипотермии и ИК. При клапанном стенозе выполняют вальвулотомию (на «открытом» или «закрытом» сердце) или комиссуротомию. При инфундибулярном стенозе осуществляют инфундибулярную резекцию — рассекают выводной тракт правого желудочка и радикально иссекают фиброзное кольцо. Если расширить инфундибулярный отдел не удается, то вшивают в кардиомиотическое отверстие заплаты из синтетического материала.
Продолжительность жизни без операции составляет не более 20 лет.
Пороки перегородок сердца
Дефекты межпредсердной перегородки (ДМПП) составляют 20% всех врожденных пороков. От этого вида порока следует отличать незаращение овальною окна, встречающееся у 30 % практически здоровых людей. ДМПП может сочетаться с расщеплением митрального и трехстворчатого клапанов, являясь компонентом более сложной патологии — открытого атриовентрикулярного канала.
Различают следующие виды порока:
1 — первичные (низкие) дефекты
межпредсердной перегородки -10-20 %
2 — вторичные (высокие) межпредсердные дефекты перегородки -75-90 %.
Нарушения гемодинамики при ДМПП обусловлены сбросом артериальной крови из левого предсердия в правое. В среднем величина сброса составляет 10-15 л/мин. Эта артериальная кровь выключается из нормального кровотока, так как, минуя левый желудочек, попадает в правое сердце, в сосуды легких и возвращается в левое предсердие. Возникают перегрузка правого желудочка, гипертрофия, а затем его дилатация, что ведет к легочной гипертензии. Без коррекции порока она становится необратимой.
Клиническая картина.
Основными симптомами заболевания являются одышка, сердцебиение, утомляемость, отставание в росте, пневмонии и простудные заболевания.
Аускультативно определяется громкий систолический шум в третьем — четвертом межреберье слева у грудины. Определяется акцент II тона в этой области. Визуально может появляться сердечный горб.
На УЗИ сердца визуализируется сброс крови через дефект перегородки (рис. 4).
Рис. 4. Эхокардиограмма (цветное допплеровское картирование) дефекта межпредсердной перегородки.
#image.jpg
На чреспищеводной сонографии четко определяется размер септального дефекта (рис.5) со сбросом через него крови (рис.6).
Рис. 5. Чреспищеводное УЗИ при дефекте межпредсердной перегородки-1.
#image.jpg
Рис. 6. Чреспищеводное УЗИ (цветное допплеровское картирование) при дефекте межпредсердной перегородки-2 (виден сброс крови).
#image.jpg
На рентгенограмме появляются увеличение правых камер сердца и выбухание дуги легочной артерии. Характерным для данного порока является пульсация корней легких.
Окончательный диагноз устанавливают при зондировании: зонд проходит через дефект перегородки сердца. В крови правого предсердия по сравнению с кровью полой вены обнаруживают повышенное содержание кислорода. Контраст, введенный в левое предсердие, появляется сразу в правом.
На ЭКГ определяется правограмма с блокадой ножки пучка Гиса. Решающее значение имеет эхографическое сканирование — изменение размеров желудочков, пароксизмальное движение межпредсердных перегородок.
Лечение данного порока только оперативное. Впервые ушивание дефекта межпредсердной перегородки в условиях обшей гипотермии осуществил J. Louis (1952). Суть операции при ДМПП состоит в ушивании вторичных щелевидных дефектов непрерывным швом синтетической нитью. На большие и первичные дефекты (независимо от величины) накладывают заплату из синтетического материала (тефлон). Результат операции хороший. Как правило, вмешательство выполняют на «сухом» сердце, чаше используя ИК. Операцию можно сделать и без ИК, путем охлаждения тела больного обкладыванием пакетами со льдом и охлаждением головного мозга (например, аппаратом «Холод-2» и др.). При этом необходимы абсолютная ясность патологической анатомии порока и высокая техника работы хирургов, так как общая гипотермия без ИК позволяет остановить сердце не более чем на 30 мин.
В последнее время разрабатывают методы трапскатетерного закрытия дефектов перегородки путем доставки и установки под рентгенологическим контролем специальных дисков и их фиксации в области ДМПП.
Хороший прогноз заболевания зависит от раннего выполнения операции в детском возрасте. При поздних вмешательствах развиваются осложнения порока в виде структурных изменений в сердце, легких и печени. Следует учитывать, что появление легочной гипертензии со сбросом справа налево может явиться противопоказанием к операции.
Дефекты межжелудочковой перегородки (ДМЖП)
Составляют 15-25 % врожденных пороков сердца. Они располагаются в мышечной или мембранозной части межжелудочковой перегородки. Размер отверстий разный — от нескольких миллиметров до 1 -2 см и более. Редко встречается полное отсутствие перегородки -единый желудочек (трехкамерное сердце). Часты сочетания ДМЖП с другими пороками, например с коарктацией аорты.
Так как левый желудочек мощнее по мышечной массе и работе, чем правый, то сброс крови через дефект вправо ведет в конечном итоге к переполнению системы легочной артерии. В правом желудочке и легочной артерии повышается давление. Если это давление превышает 60-80 мм рт. ст. то появляются склероз и фиброз легких и оперативное закрытие дефекта невозможно. Правый желудочек постепенно адаптируется к тому, что за него частично работает левый желудочек. Когда дефект закрывается заплатой, то правый желудочек иногда не справляется с перфузией крови в малом круге кровообращения. При этом может развиваться дилатация правого желудочка уже на операционном столе и сердце останавливается. Таким образом. если упустить время для операции, уже к 6-7 годам ребенок становится сомнительно операбельным, хотя субъективные жалобы, казалось, были небольшими. Об этом надо знать и помнить врачам, особенно педиатрам и детским хирургам. Если дефект мал, иногда он закрывается самостоятельно (в сроки до 4 лет); когда более 1 см, самостоятельное его закрытие сомнительно.
Клиническая картина.
Больные жалуются на одышку при физической нагрузке, сердцебиение и повышенную утомляемость. Кожные покровы детей бледные, они часто болеют пневмонией. Цианоз появляется только в конце заболевания, когда развивается синдром Эйзенменгера — необратимые явления в виде облитерации сосудов легких в результате постоянной гипертензии. В большой круг кровообращения к 6-7 годам попадает венозная кровь и появляется цианоз. Операция становится невозможной. Продолжительность жизни составляет в среднем 25-27 лет.
Аускультативно при ДМЖП определяется грубый систолический шум в третьем-четвертом межреберье слева от грудины. При этом акцент II тона во втором межреберье свидетельствует о легочной гипертензии. Визуально развивается сердечный горб.
При УЗИ сердца определяется дефект межжелудочковой перегородки со сбросом крови (рис. 7).
Рис. 7. УЗИ сердца (цветное допплеровское картирование) при дефекте межжелудочковой перегородки.
#image.jpg
Рентгенологически — расширение камер сердца и усиление сосудистого рисунка легких. Нередко вопрос о диагнозе решают эхокардиографическое сканирование, определяющее размеры дефекта, и зондирование. По сравнению с правым предсердием определяется высокое конечное диастолическое давление в правом предсердии, легочной артерии и более высокое содержание кислорода в правом желудочке. Контрастное вещество из левого желудочка одновременно попадает в аорту и через дефект — в правый желудочек. На ЭКГ часто регистрируется перегрузка обоих желудочков.
Лечение порока только хирургическое. Производят продольную стернотомию и перикардиотомию. Подключают по схеме АИК с общей (до 26-280 в пищеводе) гипотермией. Небольшие дефекты можно ушить под краниоцеребральной или общей гипотермией. Стенку желудочка вскрывают над выходным отделом. Дефект межжелудочковой перегородки либо ушивают непрерывным швом (малые размеры), либо нашивают заплату из тефлона, т. е. производят пластику.
Можно вместо тефлона использовать фасцию или перикард. При своевременно выполненной операции прогноз заболевания хороший.
Тетрада Фалло.
В 1885 г. французский патологоанатом Фалло описал врожденный порок сердца, который относится к наиболее часто встречающемуся «синему» пороку. Среди всех врожденных пороков сердца его обнаруживают у 12-14 % больных, а среди «синих» пороков — у 75-80 %. Характеризуется порок четырьмя постоянными признаками:
— сужением легочной артерии, верхнего выходного отдела правого желудочка (инфундибулярный стеноз). Наиболее тяжелой формой сужения легочной артерии является гипоплазия основного ствола легочной артерии и атрезия ее устья;
— высоким дефектом межжелудочковой перегородки;
— смещением устья аорты в правую сторону (декстропозиция);
— гипертрофией правого желудочка.
Патогенез заболевания заключается в инфундибулярном стенозе, высоком дефекте межжелудочковой перегородки и смещении устья аорты вправо. Это приводит к тому, что кровь из правого и левого желудочков поступает в основном в аорту, «обкрадывая» легочную артерию.
Вследствие этого возникают следующие изменения:
1) в легочном круге кровообращения оксигенируется малая часть крови;
2) в большом круге циркулирует смешанная кровь.
Основную роль в нарушении гемодинамики при тетраде Фалло играет степень сужения легочной артерии. Значительно снижается минутный объем малого круга, кровь сбрасывается в аорту, минуя легкие. Большой круг перегружается балластной венозной кровью с нарушением снабжения организма кислородом (гипоксемия). Это приводит к цианозу кожных покровов за счет увеличения количества редуцированного гемоглобина. Если в 100 г артериальной крови редуцированный гемоглобин достигает 3 г и больше, появляется цианоз (что бывает при многих патологических состояниях). Следует помнить, что на развитие цианоза влияют 4 фактора :
— содержание гемоглобина в крови;
— сброс венозной крови в артериальное русло;
— степень использования кислорода в тканях;
— степень насыщения крови кислородом в легких.
Клиническая картина.
Дети с тетрадой Фалло при рождении имеют нормальную массу тела и рост, так как у плода в большом круге в норме циркулирует смешанная кровь, и в это время порок не приносит большого вреда. Наиболее частым первым симптомом болезни, который выявляют сами родители, является цианоз во время крика ребенка или при кормлении. Далее цианоз и одышка появляются при движении ребенка и с каждым месяцем становятся все более выраженными. В 1-2 года они приобретают постоянный характер, не исчезая даже в покос. Ребенок плохо прибавляет в весе, отстает в развитии. Развивается синдром Мари-Бамбергера («барабанные палочки», «часовые стекла»). Характерна поза больного — «сидит на корточках»; появляется сердечный «горб». Дети поздно начинают ходить (иногда в 3-4 года). Взрослые больные не могут заниматься физическим трудом, так как во время физической нагрузки, а иногда без видимой причины возникают приступы цианоза и одышки, тахикардия. Во время приступа больной может погибнуть от остановки сердца. Эти приступы связывают с ишемией мозга. При развитии ишемии кишечника во время приступов нередко больные принимают коленно-локтевое положение, ложатся на бок, поджав ноги к животу.
Аускультативно тоны и шумы сердца различны, что зависит от разных анатомических вариантов пороков. Чаще определяются грубый систолический шум с максимумом в четвертом межреберье слева, ослабление II тона над легочной артерией.
Различают 3 степени тяжести заболевания .
I степень — общее состояние удовлетворительное, больные день проводят вне постели, кроме часа отдыха (20 %);
II степень — состояние средней тяжести, больные большую часть времени проводят в постели (до 56 %);
III степень — состояние тяжелое, больные прикованы к постели (25 %). Сюда же относятся больные с приступами цианоза и одышки независимо от межприступного состояния.
У больных с тетрадой Фалло в крови увеличено количество эритроцитов до 10-12 млн, содержание гемоглобина достигает 165-200 г/л. Увеличено также содержание лейкоцитов.
Рентгенографически сердце имеет характерную конфигурацию башмака (западает область легочной артерии, высоко приподнята и закруглена верхушка). Легочный рисунок обеднен. На ЭКГ выявляют признаки гипертрофии правого желудочка. Пульс обычно ритмичный, мягкий, малого наполнения. АД часто ниже нормы.
На основании одной клинической картины установить тетраду Фалло трудно. Некоторые формы тетрады Фалло протекают без цианоза (так называемая бледная форма), для которой характерен уравновешенный сброс крови на уровне желудочков, а у некоторых больных выявлен сброс крови слева направо.
Решающее значение для диагностики имеют эхокардиография, зондирование сердца и ангиокардиография. Диагноз подтверждается, если зонд проходит непосредственно из правого желудочка в левый, аорту, в легочную артерию. Ввести зонд из правого желудочка в аорту оказывается легче, чем в легочную артерию. При ангиографии контраст, введенный в правый желудочек, одновременно попадает в аорту и легочную артерию.
Прогноз при тетраде Фалло неблагоприятный: продолжительность жизни зависит от степени кислородною голодания. Больные обычно погибают до совершеннолетня.
Лечение порока только хирургическое. К паллиативным операциям относят создание сообщений между аортой или ветвями дуги аорты и легочной артерией, чтобы усилить приток артериальной крови к легким, минуя суженное устье легочной артерии.
Наиболее целесообразна операция создания подключично-легочного анастомоза по методу Альфреда Блекока (1944). Левосторонним торакальным доступом выделяют левую легочную и левую подключичную артерии. Подключичную артерию пересекают, дистальный конец перевязывают наглухо, а проксимальный вшивают в бок легочной артерии. У 40 % больных можно выполнить только эту операцию, потому что, помимо инфундибулярного стеноза, имеются гипоплазия ствола легочной артерии и ее сужение.
Реже (обычно у детей 2-5 лет) применяют паллиативную операцию Поттса-Смита: анастомоз между нисходящей аортой и ветвью легочной артерии бок в бок без пересечения.
Радикальные операции выполняют с использованием ИК. Этапы операции Лиллехая включают:
— стернотомию;
— вскрытие стенки правого желудочка;
— рассечение сросшихся створок клапана легочной артерии по их комиссурам, иссечение фиброзно-мышечного валика, суживающего выводной отдел правого желудочка, т. е. ликвидацию стеноза легочной артерии;
— наложение заплаты из перикарда или из тефлона на дефект межжелудочковой перегородки;
— такую же заплату вшивают на место разреза правого желудочка для профилактики возможного разрыва выходного отдела.
При невозможности устранения легочного стеноза применяют операцию Растрелли, которая заключается в соединении правого желудочка и легочной артерии клапансодержащим протезом (кондуит).
После одномоментных вмешательств в послеоперационном периоде отмечена высокая летальность. Вследствие этого Б. П. Петровский предложил оперировать в 2 этапа: сначала выполнять паллиативный этап, а по улучшении состояния — радикальное вмешательство, ликвидировав ранее наложенный анастомоз. По такой схеме послеоперационную летальность удалось снизить до 7 %.
Наряду с изложенными более редко встречаются и другие врожденные пороки, такие как общий артериальный ствол, гипоплазия левого сердца, аномалии сосудов сердца и его расположения, единственный желудочек, транспозиции магистральных сосудов, атрезии трехстворчатого клапана, дефект аортолегочной перегородки и др. Следует помнить, что все они приводят к ранним или отсроченным нарушениям гемодинамики. В организме больных с врожденными пороками сердца возникают новые качественные взаимосвязи биохимического, патофизиологического и патоморфологического порядка, что требует постоянного напряжения механизмов компенсации. Указанное требует раннего принятия решения о методе лечения, которое проводят в условиях специализированной кардио-хирургической клиники.