Атеросклеротическое поражение аорты и магистральных артерий головы, верхних и нижних конечностей
Атеросклеротическое поражение аорты и магистральных артерий головы, верхних и нижних конечностей проявляется нарушениями гемодинамики в данных анатомических областях, в связи со снижением растяжимости и сужением просвета крупных и средних артерий вследствие липидной инфильтрации их внутренней оболочки и разрастания в их стенках соединительной ткани.
В отдельных случаях (чаще при атеросклерозе аорты) эластические структуры стенки пораженной артерии разрушаются, и наблюдается ее аневризматическое расширение. Клинические проявления атеросклероза определяются локализацией и степенью стеноза артерий, их закупорки тромботическими массами, наличием таких осложнений, как тромбоэмболия, расслаивание или разрыв аневризмы.
В настоящее время описано более 200 факторов, способствующих возникновению атеросклероза или неблагоприятно влияющих на его течение (в т.ч. наличие таких заболеваний, как сахарный диабет, подагра, псориаз и др.), однако наибольшее значение, кроме гипер- и дислипопротеидемии, имеют артериальная гипертензия, ожирение, недостаточная физическая активность и курение – их относят к так называемым большим факторам риска развития атеросклероза (особенно высокой она считается при сочетании двух и более таких факторов).
Атеросклеротическое поражение аорты при значительном уплотнении ее стенок ограничивает роль их систолического растяжения кровью, в результате чего диастолическое артериальное давление снижается, а систолическое повышается. Наиболее опасные осложнения возникают при развитии аневризмы аорты – расслаивание и разрыв.
Атеросклеротическое поражение артерий головного мозга и внечерепных артерий, питающих мозг (сонных, позвоночных), проявляется снижением памяти, особенно на недавние события, головокружениями, возможны периоды помрачения сознания. Наблюдаются изменения личности: происходит заострение преморбидных черт характера: чувствительный человек становится слезливым, слабодушным; раздражительный – агрессивным и т.д. Выраженный атеросклероз мозговых артерий предрасполагает к развитию инсульта, особенно при сочетании с артериальной гипертонией.
Атеросклеротическое поражение артерий конечностей чаще наблюдается в сосудах ног. Чаще всего облитерация или окклюзия развивается в месте разделения брюшной аорты на подвздошные артерии, реже поражаются бедренные артерии и артерии более мелкого калибра. Острая окклюзия проявляется сильной болью в одной или обеих ногах, побледнением и похолоданием, а также мраморностью кожи.
При медленно нарастающей облитерации, когда развиваются коллатерали в обход пораженных артерий, наблюдается так называемая перемежающаяся хромота при ходьбе и прекращающаяся почти сразу после остановки. На ранних стадиях атеросклеротического поражения аорты и магистральных артерий головы, верхних и нижних конечностей возможно обратное развитие холестериновых бляшек при соблюдении диеты, приеме статинов, гемосорбции.
При значительных стенозах, закупорке или аневризмах крупных артерий показано хирургическое лечение.
УЗИ сосудов шеи (дуплексное ангиосканирование магистральных артерий головы)
Стоимость дуплексного сканирования магистральных сосудов шеи составляет 200 гривен. В стоимость входит исследование сосудов бассейна сонных и позвоночных артерий, путей венозного оттока и проведение функциональных проб. Подробный отчет об исследовании, печать снимков и запись на электронный носитель.
Акция: при исследовании сосудов головы и шеи (дуплексное сканирование) — эхокардиография (узи сердца) — бесплатно! Экономия 250 гривен!
Цели проведения узи сосудов шеи
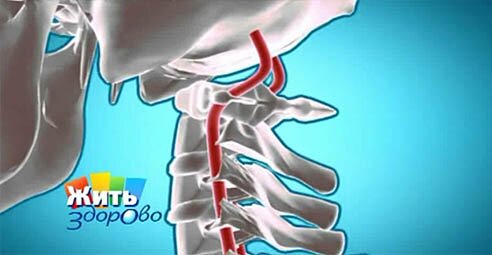
Узи сосудов шеи применяют для диагностики изменений сосудов. которые отходят от дуги аорты и несут кровь к головному мозгу, мышцам шеи и головы и к щитовидной железе. Узи сосудов шеи позволяет диагностировать изменения в таких артериях как брахиоцефальный ствол справа, общие сонные артерии с обеих сторон, позвоночные артерии с обеих сторон, наружные и внутренние сонные артерии с обеих сторон. При узи сосудов шеи оценивают диаметр артерий, состояние стенок сосудов, изменения просвета вследствие присутствия тромбов, заболеваний стенки сосуда, атеросклеротических бляшек или сдавления сосудов извне. Можно диагностировать аномалии строения сосудов – например патологическую извитость, отсутствие сосуда, его сужение или расширение. Главный вопрос, который ставится при назначении узи сосудов шеи оценка способности сосудов обеспечить питание головного мозга. Любой процесс, который протекает как внутри сосуда, так и извне может привести у сужению просвета артерии – стенозу или к полоному закрытию просвета сосуда – окклюзии. Задачей узи сосуда является оценка степени стеноза, а при окклюзии – оценка развития коллатеральной системы кровообращения. Коллатеральная система кровообращения развивается путем возникновения обходных путей доставки крови к тем участкам, которые кровоснабжались закупоренной артерией. Наиболее яркий пример – атеросклероз подключичной артерии, когда кровоснабжение руки осуществляется по позвоночной артерии и движения рукой могут вызвать ухудшение кровоснабжения головного мозга. Для диагностики такого состояния необходимо знать не только диаметр сосудов шеи, но и направление движения крови в них. При узи сосудов шеи оценивают характеристики кровотока — скорость движения крови по сосудам,характер кровотока (ламинарный или турбулентный), перепады скорости на различных участках сосуда,эластичность стенки сосуда, симметричность всех перечисленных характеристик с обеих сторон.
Такое исследование сосудов шеи называют дуплексным ангиосканированием, так как применяется одновременно исследование в двумерном режиме и в режиме допплера (цветного и/или спектрального).
Оценка сужения артерий при узи сосудов шеи
Для оценки степени стеноза сонных артерий Американское общество радиологов в 2003 году рекомендовало использовать следующие критерии
- Норма — пиковая систолическая скорость во внутренней сонной артерии не превышает 125 см/с, при этом не визуализируются бляшки или утолщение внутреннего слоя сосуда
- Стеноз от 50-69% — пиковая систолическая скорость составляет 125-230 см/с
- Стеноз более 70% — пиковая систолическая скорость выше 230 см/с
- Стеноз более 90% — при дуплексном сканировании регистрируется значительное сужение просвета сосуда и падение скорости кровотока
- При полной окклюзии (закупорке) сосуда – кровоток не регистрируется.
- Вспомогательное значение имеет определение соотношения пиковой систолической скорости во внутренней и общей сонной артерии. При стенозе внутренней сонной артерии соотношение увеличивается более, чем в 3 раза. Особенно полезно вычисление этого отношения у больных с сердечной недостаточностью и снижением фракции выброса сердечной мышцы (левого желудочка сердца). По тем же причинам необходимо измерение артериального давления на обоих руках у пациента перед началом обследования.
Прогностические критерии при узи сосудов шеи
На современных аппаратах с высоким разрешением при узи сосудов шеи оценивают состояние комплекса интима-медиа. Это самый внутренний слой артериальных сосудов, который первым начинает изменяться при атеросклерозе. Изменение толщины и структуры комплекса интима-медиа является очень важным прогностическим признаком при узи сосудов шеи. Считается, что превышение толщины комплекса интима-медиа в общей сонной артерии свыше 0,87 мм, а во внутренней сонной артерии больше,чем 0,9 мм является фактором, который ассоциирован с высоким риском кардиоваскулярных заболеваний (инфаркта миокарда и инсульта). Образно говоря оценка толщины комлекса интим-медиа в сонных артериях является окном, в которое можно заглянуть для диагностики атеросклеротического поражения всех сосудов. Значение предельной толщины этого комплекся колеблется в зависимости от пола, возраста и расы.
Что можно выявить при узи сосудов шеи
Самая частая патология, выявляемая при узи сосудов шеи – наличие атеросклеротических бляшек в просвете сосудов. Так как симптомы нарушения кровообращения, заметные для пациента, развиваются только после перекрытия просвета сосуда более, чем на 60%, процесс образования бляшек и тромбов может протекать длительное время бессимптомно. Бляшки при узи сосудов шеи могут быть различной формы и состава. Задача исследователя – по возможности подробно описать состав бляшки и ее локализацию.
Часто атеросклеротические бляшки распадаются, на них образуются тромбы, которые могут перекрывать полностью просвет артерии или отрываться, вызывая закупорку других, более мелких сосудов. Эти состояния часто заканчиваются развитием инсульта (отмирание участка ткани мозга) вследствие острого нарушения мозгового кровообращения. Инсульт – заболевание сопровождающееся высокой летальностью (около 40%), а более половины людей, перенесших инсульт становятся инвалидами. В последнее время инсульты развиваются у людей во все более молодом возрасте (до 60 лет).
Факторы способствующие развитию мозгового инсульта: курение, сахарный диабет, повышенное артериальное давление, избыточная масса тела, женский пол, наличие подобного заболевания у кровных родственников.
Если такие факторы присутствуют у человека, ему необходимо пройти исследование сосудов шеи как можно раньше. Также исследование сосудов шеи необходимо пройти, если беспокоит головокружение,хронические головные боли, нарушения координации, памяти и речи.
К редким случаям, которые диагностируются при узи сосудов шеи, является диссекция стенки сонной артерии- отслоение ее участка с последующим тромбозом.
Обязательной информацией, получаемой при узи сосудов шеи, является исследование объема крови, который поступает по всем сосуда шеи в головной мозг в единицу времени. Адекватное поступление крови к головному мозгу – главный фактор, который принимается во внимание при оценке патологии мозгового кровообращения. В норме у здорового человека около 15% крови, которое сердце перекачивает за минуту, попадает в сосуды головного мозга. При помощи узи сосудов шеи можно очень точно вычислить сколько именно крови попадает в головной мозг. Для этого складывают объемную скорость кровотока во всех четырех сосудах, питающих головной мозг, а именно во внутренних сонных артериях и в позвоночных артериях с обеих сторон. Корректно проведенное исследование приближается по точности к результатам, полученным при проведении позитронно-эмиссионной томографии.
Подготовка и проведение исследования
Подготовки при проведении узи сосудов шеи не требуется. Нужно только по возможности отказаться от приема лекарств, влияющих на артериальное давление.
При исследовании пациент не испытывает каких-либо неудобств или болевых ощущений. Исследование сосудов шеи осуществляют в нескольких плоскостях сначала в черно-белом режиме, затем переходят к дуплексному сканированию и к импульсной допплерометрии. При этом оценивают вначале форму сосуда и его геометрию, измеряют линейные размеры и площади при наличии стенозов. Цветовой допплер исползуют прежде всего для диагностики невидимых в черно-белом режиме бляшек. При низких скоростях кровотока, например при почти полной окклюзии сосуда используют энергетический допплер. При помощи импульсного допплера проводят измерения линейной и объемной скорости кровотка.
Очень часто узи сосудов шеи проводят как исследование, предшествующее узи сосудов головного мозга. Связано это с тем, что при поиске причин нарушения мозгового кровообращения вначале логичнее убедиться в том, что по магистральным сосудам поступает достаточное количество крови.
женская консультация Наталии Петрик 2©08-2015
АТЕРОСКЛЕРОТИЧЕСКОЕ ПОРАЖЕНИЕ МАГИСТРАЛЬНЫХ АРТЕРИЙ ГОЛОВЫ
ПОКАЗАНИЯ К ХИРУРГИЧЕСКОМУ ЛЕЧЕНИЮ
Среди сосудистых заболеваний мозговой инсульт занимает одно из ведущих мест как по частоте возникновения и тяжести течения, так и по инвалидизации населения и летальности.
В России ежегодно переносят нарушения мозгового кровообращения 35 человек на 10 тыс. населения, т.е. до 700 тыс. в год, причем ведущее место среди них занимает ишемический инсульт. В настоящее время более 1 млн человек в стране являются глубокими инвалидами вследствие перенесенного инсульта. Только в Москве за последние пять лет ишемические нарушения мозгового кровообращения возросли на 40 проц. Летальность после мозгового инсульта сохраняется высокой и составляет 30-35 проц. Только 10-20 проц. пациентов, переживших острую стадию заболевания, восстанавливают трудоспособность, остальные становятся инвалидами со стойким неврологическим дефицитом. Сейчас по тяжести экономических потерь мозговой инсульт прочно занял первое место, превосходя даже инфаркт миокарда. Затраты на лечение и социальное обеспечение больных, перенесших мозговой инсульт, огромны; в США, например, они составляют 7,5 млрд $ в год.
Сам факт развития церебрального ишемического инсульта не может рассматривается как показание к оперативному вмешательству. В частности, инсульт, развившийся вследствие материальной эмболии на фоне эндокардита либо диффузного атеросклероза на сегодняшний день не имеет реальных перспектив хирургического лечения. Способы реваскуляризации на пиально-капиллярном уровне артериального русла пока не вышли за рамки экспериментальных лабораторий, и основная нагрузка по лечению этой категории пациентов ложится на неврологический стационар.
Хирургическое лечение инсульта, явившегося следствием поражения интракраниальных магистральных сосудов, нередко возможно путем создания обходных шунтов — наложения экстра-интракраниальных анастомозов в условиях нейрохирургических и сосудистых стационаров.
Лечение церебрального инсульта вследствие патологии экстракраниальных магистральных сосудов является одной из важнейших задач сосудистой хирургии и нейрохирургии.
Особого внимания заслуживает проблема хирургического лечения атеросклеротических поражений магистральных артерий на "доинсультной" стадии, когда больные переносят лишь транзиторные ишемические атаки или имеют дефицит кровоснабжения мозга.
Современный этап решения проблем диагностики и лечения мозгового инсульта характеризуется достаточно высокой разрешающей способностью диагностического комплекса и операционного оборудования. В то же время арсенал медикаментозных средств воздействия на патогенетические звенья инсульта не претерпел существенных изменений. Это обстоятельство обусловило значительное возрастание роли хирургических методов лечения заболеваний сосудов головного мозга и магистральных артерий головы, следствием либо осложнением которых является мозговой инсульт. Оперативные вмешательства реваскуляризирующего характера занимают существенное, а в ряде случаев и ведущее место в комплексном лечении нарушений мозгового кровообращения и их остаточных явлений, успешно выполняя задачу восстановления нарушенной церебральной функции и оптимизации показателей мозгового кровотока.
Проведены мультицентровые изучения результатов комплексного лечения церебрального инсульта в Европе (European Trial of Carotid Surgery — ECST), в Северной Америке при участии нескольких европейских центров (North American Simptomatic Carotid Endarterectomy Trial -NASCET). Кроме того, среди лиц с атеросклерозом сонных артерий без сопутствующей мозговой симптоматики в североамериканских центрах выполнено третье исследование (Asymptomatic Carotid Atherosclerosis Study — ACAS). Эти исследования, каждое из которых включало не менее 1,5 тыс. случаев, позволили сформулировать показания к хирургической коррекции магистральных артерий головы. На основе рандомизированных исследований сравнивались два способа лечения: каротидная эндартерэктомия в сочетании с медикаментозной профилактикой инсульта и только медикаментозное лечение. Было доказано несомненное преимущество каротидной эндартерэктомии, особенно при возрастании степени стеноза у больных с клиническими проявлениями дисциркуляции в бассейне внутренней сонной артерии при всех прочих равных условиях. При асимптомном течении заболевания хирургическая профилактика дает незначительное, но статистически достоверное снижение частоты инсульта у лиц с сужением диаметра внутренней сонной артерии более чем на 60 проц.
Лечение и клиническое наблюдение за больными с цереброваскулярной патологией, обусловленной поражениями магистральных артерий головы, должно проводиться под контролем неврологов — нейрохирургов и сосудистых хирургов.
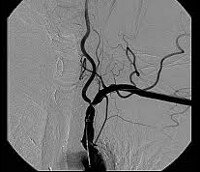
Диагностический алгоритм включает физикальное и неврологическое исследование, ультразвуковую допплерографию магистральных вне- и внутричерепных сосудов, дуплексное сканирование; компьютерную томографию головного мозга или магнитно-резонансную томографию головного мозга, церебральную селективную ангиографию; исследование центральной гемодинамики, функции внешнего дыхания, почек; биохимические и клинические лабораторные исследования.
Объем диагностических исследований на поликлиническом этапе может быть сокращен для пациентов с повторными транзиторными атаками и острыми тромбозами артерий сетчатки при наличии допплерографического гемодинамически значимого стеноза магистральных артерий головы (МАГ), снабжающих данный бассейн, до оценки кардиологом переносимости операции.
В случаях острой или прогрессирующей церебро-васкулярной патологии интегративная схема должна быть значительно сокращена, и такие больные направляются из поликлиники в специализированное отделение в экстренном порядке.
Больные с клиническими проявлениями цереброваскулярной недостаточности по результатам обследования должны быть отнесены в группы консервативного или оперативного лечения.
Оперативному лечению подвергаются пациенты с различными вариантами поражений каротидного и вертебрально-базилярного бассейнов. Определены абсолютные и относительные показания и противопоказания к хирургическим методам лечения.
Абсолютные показания к каротидной эндартерэктомии (КЭАЭ):
— каротидные стенозы с клиникой транзиторных ишемических атак или проявлениями декомпенсации дисциркуляторной энцефалопатии (у пациентов с тяжелым, более 70 проц. ипсилатеральным стенозом, приведшим к нарушению мозгового кровообращения и инфаркту мозга).
— наличие гетерогенной бляшки в устье внутренней сонной артерии ВСА, даже при асимптомном стенозе.
В этой группе также должны быть учтены факторы риска развития мозгового инсульта, такие, как возраст, артериальная гипертензия, повышенный уровень липидов крови, курение, диабет.
Относительные показания к КЭАЭ:
— асимптомные стенозы (до 70 проц.) сонных артерий;
— асимптомные стенозы сонных артерий с допплерографическими признаками стеноза более 90 проц.;
стенозы сонных артерий от 30 до 69 проц. с неврологическими проявлениями;
быстро прогрессирующий каротидный стеноз (пациенты, у которых полгода назад отмечался асимптомный стеноз);
грубый каротидный стеноз с ипсилатеральной неврологической симптоматикой и контрлатеральным тромбозом сонной артерии;
грубый каротидный стеноз с единственным симптомом — ипсилатеральным амоврозом fugax;
грубый каротидный стеноз, осложненный инсультом с проявлениями гемипареза или афазии (не ранее, чем через месяц после инсульта);
грубый каротидный стеноз с завершенным инсультом в бассейне пораженной артерии;
грубый каротидный стеноз с ипсилатеральной симптоматикой и кардиальной эмбологенной причиной инсульта (подтвержденной при ЭхоКГ или фибриляцией предсердий);
грубый каротидный стеноз, асимптомно протекающий перед операцией аорто-коронарного шунтирования.
Противопоказания к каротидной эндартерэктомии:
— каротидный стеноз менее 30 проц. с ипсилатеральным неврологическим дефицитом;
— тромбоз сонной артерии с ипсилатеральной неврологической симптоматикой;
— негемисферная симптоматика, такая, как головная боль, повышенная утомляемость, синкопальные состояния и т.п. при верифицированном грубом каротидном стенозе;
— транзиторные ишемические атаки в вертебро-базилярном бассейне;
— грубый каротидный стеноз с симптомами поражения противоположного полушария мозга;
— грубый каротидный стеноз с ипсилатеральным тяжелым инсультом с гемиплегией и/или комой;
-грубый каротидный стеноз с ипсилатеральными симптомами и тяжелой сопутствующей патологией (метастазы рака, органическое поражение ЦНС и т.д.).
Существуют несколько видов каротидных эндартерэктомий — открытая, эверсионная, различные варианты протезирования артерии с применением вен и протезов (гомо- и гетеротрансплантаты). Выбор метода операции зависит от степени поражения каротидного бассейна, его протяженности. Наиболее оптимальными являются прямая и эверсионная эндартерэктомии — при последней значительно сокращается время операции, а также минимально изменяются геометрические показатели реконструированного сосуда.
Для адекватной защиты мозга во время каротидной эндартерэктомии необходимо осуществлять тщательный отбор больных, быструю хирургическую технику, общую анестезию, системную гепаринизацию, допплерографический мониторинг в до- и интраоперационном периоде. В некоторых случаях необходимо использовать временный внутрипросветный шунт, показания к применению которого следующие:
1) контралатеральная окклюзия внутренней сонной артерии;
2) грубый стеноз или окклюзия позвоночной или основной артерии при неполноценном виллизиевом круге (отсутствие ПСоА или А1 сегмента).
3) низкая толерантность головного мозга к ишемии даже на фоне превентивного наложенного экстра-интракраниального микроанастомоза.
Показания к реконструкции позвоночной артерии:
Симптомы нестабильной гемодинамики в вертебрально-базилярном бассейне:
— стеноз доминантной позвоночной артерии более 75 проц.;
— стенозирующий процесс при той же степени стеноза обеих позвоночных артерий;
— сегментарная окклюзия второго сегмента позвоночной артерии при наличии гипоплазии другой.
2. Клиника стволовой дисциркуляции тромбэмболического генеза при выявлении источника эмболии из позвоночной артерии.
3. Стенозы каротидного бассейна, подлежащие реконструкции при наличии патологии в вертебрально-базилярном бассейне, перечисленные в п.1.
4. Значительно влияющая на вертебральный кровоток экстравазальная компрессия (шейное ребро, аномалия Киммерле, унковертебральные и другие спондилогенные причины).
Хирургическая реконструкция патологии первого сегмента позвоночной артерии заключается в стандартной эндартерэктомии устья артерии через надключичный доступ, а при невозможности ее выполнения (при протяженном поражении позвоночной и/или подключичной артерий) необходимо использовать методы перемещения артерии — позвоночно-каротидное анастомозирование (шунтирование) и т.д.
Показания к хирургическому лечению поражений подключичной артерии:
1. Наличие феноменов внутримозгового "обкрадывания", состоящих из признаков ишемии в вертебрально-базилярном бассейне и/или верхней конечности. Признаки сочетанного поражения сонных и вертебрально-базилярных артерий одновременно.
Наиболее частый механизм формирования этих симптомов — любое серьезное ограничение потока крови из-за критического стеноза или эмболии магистрального артериального сосуда в результате изъязвления атероматозной бляшки.
2. Гетерогенные атеросклеротические бляшки в первом сегменте подключичной артерии при отсутствии проявлений внутричерепной артериальной патологии, клинически проявляющиеся вертебрально-базилярной дисциркуляцией.
3. Гемодинамически значимые (75 проц. и более) стенозы первого сегмента подключичной артерии.
4. Асимптомные поражения первого сегмента подключичной артерии (>75 проц. ее диаметра) у пациентов, которым показано наложение маммарно-коронарного анастомоза с целью профилактики развития синдрома коронарно-маммарно-подключичного "обкрадывания".
5. Реваскуляризация подключичной артерии также показана пациентам, которым выполнен маммарно-коронарный анастомоз, а прогрессирование ИБС связано с возникшим феноменом коронарно-маммарно-подключичного "обкрадывания".
6. Двусторонние бессимптомные окклюзии подключичной артерии с целью создания адекватного магистрального кровотока у пациентов, которым показан системный гемодиализ или выполнение подключично(аксиально)-бедренного шунтирования.
Выбор между чрезгрудинным и надключичным доступом зависит от локализации поврежденных сегментов магистрального ствола. При астеническом телосложении и умеренном питании пациента предпочтительнее накладывать каротидно-подключичный анастомоз. У лиц же с нормостеническим или гиперстеническим телосложением на фоне повышенного питания предпочтительнее использовать каротидно-подключичное протезирование.
Показания к наложению экстра-интракраниального анастомоза:
— тромбоз ВСА с истощением резервов коллатерального кровообращения;
— гемодинамически значимый стеноз интракраниальных сегментов в бассейнах средней, передней или заднемозговой артерий;
— как первый этап перед каротидной эндартерэктомией на ипсилатеральной стороне при отсутствии адекватного коллатерального кровотока по вилизиевому кругу;
— при тандемных поражениях внутренней сонной артерии с низкой степенью толерантности головного мозга к ишемии, когда показано многоэтапное хирургическое лечение;
— при бикаротидных стенозах с тандемным поражением одной из каротид: вначале первый этап — восстановление адекватной проходимости сонной артерии, контрлатеральной тандемному поражению, затем — поэтапное наложение ЭИКМА.
Рентген-эндоваскулярная ангиопластика должна выполняться лишь при адекватной технической оснащенности. Предпочтительнее использовать эндоваскулярную ангиопластику при локальных стенозах.
Строгая оценка показаний и противопоказаний к оперативному лечению, детализация этапов операции, наличие технически высокооснащенной специализированной хирургической бригады, интраоперационного мониторинга мозговой гемодинамики, адекватного реанимационного пособия — основные факторы, позволяющие минимизировать риск возникновения послеоперационных осложнений и адекватно восстановить церебральную перфузию.
В заключение необходимо отметить, что лечение острой и хронической цереброваскулярной патологии, безусловно, должно проводиться общепринятыми методами. Не вызывает сомнения приоритетное значение традиционной терапии в лечении данной категории больных.
Опыт свидетельствует, что существует строго определенная категория больных с патологией сосудистой системы магистральных артерий головы, которая несомненно входит в группу риска развития мозговой сосудистой катастрофы или уже страдает мозговыми дисциркуляторными нарушениями, оптимальное лечение которой может быть достигнуто только оперативным путем. Международными кооперативными исследованиями подтверждено несомненное преимущество хирургического лечения стенозирующих поражений магистральных артерий головы для предупреждения развития инсульта или его прогрессирования.
Правильный клинический подход к этой группе больных может оказаться решающим в предотвращении развития болезни, сохранении качества жизни, да и самой жизни, если своевременно будет решен вопрос о диагнозе и показаниях к оперативному лечению. Выбор показаний к операции, наиболее адекватного хирургического метода коррекции, профилактики постоперационных осложнений во многом зависит как от возможностей детального изучения патологического процесса, его верификации, строгой оценки противопоказаний к ней, так и от наличия высокооснащенной специализированной хирургической бригады и адекватного реанимационного пособия.
Георгий МИТРОШИН, начальник Центра
сердечно-сосудистой хирургии ЦВКГ им.
А.А.Вишневского, заслуженный врач РФ.
Валерий ЛАЗАРЕВ, ведущий научный сотрудник
сосудистого отделения НИИ нейрохирургии
им. Н.Н.Бурденко РАМН, доктор медицинских наук.
Геннадий АНТОНОВ, начальник отделения
ангионейрохирургии ЦВКГ им.А.А.Вишневского,



у миня 70/ забиты сонные артериистеноз что делать
мои т,89874124778