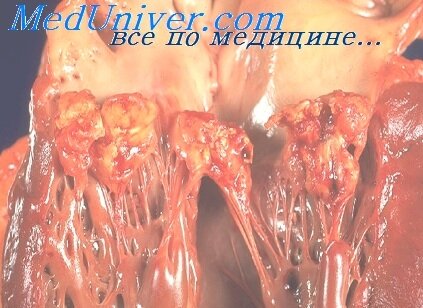
Грибковый энтерокардит (грибковый эндокардит)
Возбудителями инфекционного эндокардита естественных клапанов грибы бывают редко. У больных, подвергавшихся катетеризации сосудов, особенно если они получали глюкокортикоиды. антибиотики широкого спектра действия или цитостатики. встречаются эндокардиты, обычно подострые, вызванные Candida spp. или Aspergillus spp. Они сопровождаются образованием обильных крошащихся вегетации и крупных эмболов, поражающих преимущественно артерии ног. Прогноз неблагоприятный, отчасти из-за отсутствия действенных противогрибковых препаратов.
Статья Эндокардит
Эндокардит (новолат. endocarditis; от др.–греч. ἔνδον — внутри, καρδία — сердце, + itis) — воспаление внутренней оболочки сердца — эндокарда.
В большинстве случаев эндокардит не является самостоятельным заболеванием, а представляет собой частное проявление других заболеваний. Самостоятельное значение имеет подострый бактериальный эндокардит, вызываемый чаще стрептококком.
Причины
При диффузных болезнях соединительной ткани и ревматизме эндокардит связан с воспалительной реакцией на иммунные комплексы, локализованные в эндокарде и обычно сочетается с миокардитом. Эти эндокардиты имеют хроническое течение и отличаются бедностью клинических проявлений. При локализации процесса на створках клапана может сформироваться порок сердца. Среди других вторичных эндокардитов (встречаются редко) выделяют аллергический, фибропластический с эозинофилией, травматический (в том числе послеоперационный), интоксикационный, тромбоэндокардит. Инфекционные эндокардиты возникают при внедрении в ткань эндокарда бактерий, грибов, редко — вирусов и простейших. Часто развивается как проявление острого сепсиса (наряду с другими его симптомами), иногда бывает проявлением специфического поражения при туберкулёзе, сифилисе, бруцеллёзе. Острый септический эндокардит рассматривается как осложнение общего сепсиса, по этиологии, патогенезу и клинике такая форма заболевания существенно не отличается от подострой формы, характеризуется лишь более острым течением.
Подострый бактериальный эндокардит (син. — эндокардит инфекционный; уст. назв. — затяжной септический эндокардит, sepsis lenta) — системный инфекционно–воспалительный процесс с иммунными нарушениями и преимущественным поражением клапанов сердца, реже париетального эндокарда или протезированных клапанов. Возбудителями чаще всего оказываются микробы — представители «нормальной» флоры дыхательных путей, кишечника и кожи, а также окружающей среды. Чаще всего это — зеленящий стрептококк. Он обусловливает до 80 % бактериологически подтверждённых случаев. Нередко заболевание вызывается золотистым стафилококком и энтерококком, однако они чаще выявляются при остросептическом процессе, чем при подостром эндокардите. Реже среди возбудителей эндокардита выделяют кишечную палочку, протей, синегнойную палочку, другие стрептококки (например, β–гемолитические), патогенные грибы. В последнее время в связи с изменением чувствительности микрофлоры и появлением новых антибиотиков изменился и спектр возможных возбудителей (напр. уменьшился удельный вес зеленящего стрептококка, чаще стали выявлять грамотрицательные бактерии и пенициллиназопродуцирующий стафилококк).
Для возникновения заболевания необходим более или менее длительный период бактериемии, которая может быть связана как с очагом инфекции в организме (тонзиллит, периодонтит, фурункул), так и с различными манипуляциями, нарушающими тканевый барьер: хирургическая операция, катетеризация, удаление зуба, бронхоскопия, внутривенное введение лекарственных или наркотических веществ и др. Процесс локализуется главным образом на ранее изменённых клапанах, наслаиваясь на уже существующие пороки сердца: врождённые, ревматические, или на ранее протезированные клапаны. Локализация (в порядке убывающей частоты) — аортальный, митральный, трёхстворчатый и лёгочный. Поражение двух последних клапанов более характерно для инъекционных наркоманов.
Основа патологического процесса болезни — деструктивно–язвенный эндокардит со значительными тромботическими наложениями, состоящими из фибрина, тромбоцитов, бактерий, и частичек ткани. Это обусловливает такое проявление болезни как тромбоэмболия. Кроме того, в развитии эндокардита большую роль играют иммунные (точнее аутоиммунные) механизмы. В крови часто обнаруживаются антитела к соответствующему возбудителю в высоких титрах (и некоторые другие типы антител) и циркулирующие иммунные комплексы. С наличием последних связывают, в частности, таких осложнений как гломерулонефрит и васкулит.
Классификация
Симптомы
Проявления болезни складываются из симптомов инфекционного процесса, иммунных нарушений и признаков поражения клапанов сердца.
Начало заболевания может быть как отчетливым, так и относительно постепенным. Сравнительно редко удается выявить связь эндокардита с предшествующей инфекцией дыхательных путей, экстракцией зубов, катетеризацией уретры и т. д. В анамнезе пациентов часто имеются указания на ревматизм. При выраженном начале отмечается лихорадка неправильного типа (температура t 38,5 — 39,5° С) с потрясающими ознобами и обильным потоотделением, боли в суставах и мышцах, слабость, похудание. Нередко, особенно при длительном течении, наблюдается своеобразная бледно–сероватая с лёгкой желтизной окраска кожи (т. наз. субиктеричность, или «цвет кофе с молоком»). Иногда на коже выявляются петехии, редко другие элементы сыпи. Характерно появление на кистях и стопах узелков Ослера (мелких вишнево–красных узелков), повышенная ломкость сосудов, мелкие кровоизлияния в слизистые оболочки, особенно в конъюнктиву.
Концевые фаланги пальцев рук и ног у многих больных утолщаются, приобретают вид барабанных палочек, а ногти — часовых стёкол (так называемый симптом «барабанных пальцев», весьма характерный для инфекционного эндокардита).
Часто при пальпации определяется увеличенная селезёнка, иногда печень. У многих больных наблюдаются признаки поражения почек (гематурия, протеинурия) вследствие эмболий или аутоиммунного гломерулонефрита. В крови — циркулирующие иммунные комплексы, выраженная гипохромная анемия, лейкоцитоз или лейкопения, увеличение СОЭ, иногда — моноцитоз, тромбоцитопения, С–реактивный белок, повышенная α2 — и γ–глобулинемия. Иногда возникают инфаркты (селезёнки, почек, миокарда, лёгких, реже кишечника, вещества мозга — геморрагический инсульт). В некоторых случаях картина болезни стёрта.
Ведущий признак — выраженные шумы в сердце, связанные с образованием тромботических наложений. Признаки сердечной недостаточности выявляются позднее, как правило по мере образования клапанного порока сердца. Чаще наблюдается недостаточность аортального клапана, реже — митрального. При длительном течении часто возникают васкулиты, различные тромбоэмболические осложнения, декомпенсация сердца.
Диагностика
Диагноз устанавливают при возникновении признаков поражения клапанного аппарата сердца, в частности при сочетании порока (чаще аортального) с лихорадкой, увеличением селезёнки, гематурией, кожными геморрагиями, анемией, повышением СОЭ, иногда эмболиями. Положительный результат посева крови существенно облегчает диагностику и позволяет выбрать наилучшую стратегию лечения.
Существенную помощь оказывают фонокардиография и эхокардиография. При подозрении на инфекционный эндокардит необходимо исключить прежде всего ревматизм. Особенно сложна диагностика при отрицательных результатах посева крови. В этих случаях проводят эмпирическую терапию с последующими повторными посевами (используя другие методики); при особо тяжелом течении иногда прибегают к хирургическому лечению, не дожидаясь результатов повторного анализа, иногда с использованием биопсии эндокарда.
Дифференциальную диагностику необходимо проводить с ревмокардитом и другими асептическими эндокардитами (системная красная волчанка, системная склеродермия, ревматоидный артрит), фибропластическим эндокардитом и тромбоэндокардитом. При этих заболеваниях отсутствуют выраженные признаки инфекционного процесса (лихорадка, повышение СОЭ, нейтрофилёз, бактериемия и др.) и меньшая степень разрушения клапанов. При остром бактериальном эндокардите картина болезни более тяжелая, он чаще вызывается микробами с выраженной патогенностью (стафилококки, стрептококки группы А и др.), сочетается с множественными септическими очагами — абсцессами в лёгких, почках, костях и др.(при подостром эндокардите вторичные септические заносы практически отсутствуют), гектической лихорадкой, нарушениями сознания и другими признаками септического состояния, меньшей выраженностью иммунных нарушений и большими разрушениями клапанов.
Лечение
Основой терапии подострого бактериального эндокардита является возможно более раннее и достаточно длительное (не менее 4 недель) назначение эффективных бактерицидных доз адекватных антибиотиков, наиболее надежный выбор которых определяется чувствительностью выделенных из крови микроорганизмов. При отрицательных результатах выделения из крови микробов проводят анализ ситуации, позволяющий предположить наиболее вероятный возбудитель и тем самым определить его чувствительность к антибиотикам.
В большинстве случаев, вызванных зеленящим стрептококком лечение начинают с применения умеренных доз бензилпенициллина (порядка 4 000 000 — 6 000 000 ЕД в сутки) внутривенно в течение 4 недель. У пожилых людей, а также если заболевание вызвано энтерококком назначают высокие дозы бензилпенициллина (12 000 000 — 24 000 000 ЕД в сутки), часто в сочетании с гентамицином (3—5 мг/кг) или амикацином (10—15 мг/кг) в сутки внутримышечно. Дозы указаны для взрослых.
При стафилококковом эндокардите препаратами выбора являются полусинтетические пенициллины (оксациллин, ампициллин, метициллин, амоксициллин и др.) по 10 г в сутки в сочетании с цефалоспоринами (цефалоридин, цефамизин, клафоран) или аминогликозидами. При непереносимости пенициллинов можно назначать макролиды (эритромицин, олеандомицин и др.), а также аминогликозиды. Такое же лечение показано при выявлении грамотрицательных бактерий (Escherichia, Proteus и др.).
Высокой эффективностью обладает ванкомицин, а также фторхинолоны.
В случае неэффективности терапии проводят повторное исследование крови и назначение других антибиотиков с учётом их чувствительности. Отсутствие положительной динамики в течение двух недель является показанием к хирургическому лечению — удалению пораженного клапана с последующим протезированием его.
Попутно проводится симптоматическое лечение (детоксикация, сердечные гликозиды, тромболитические средства). Кортикостероиды не показаны, так как они способствуют угнетению иммунитета (лишь при очень бурных аллергических реакциях назначают короткий курс преднизолона).
Наиболее тяжело протекает грибковый эндокардит — он плохо поддаётся терапии и даёт высокую летальность. В этих случаях основой лечения является хирургическое иссечение клапанов и их протезирование, проводимое на фоне лечения противогрибковым антибиотиком амфотерицином В (внутривенно капельно по 250—1000 ЕД на 1 кг массы тела).
Прогноз
Прогноз условно неблагоприятный, до введения в практику антибиотиков широкого спектра действия в большинстве случаев заболевание заканчивалось смертью, однако и сейчас в 30 % случаев наступает летальный исход. Смерть может наступить от сердечной или почечной недостаточности, тромбоэмболий, интоксикации.
Ранняя энергичная антибиотикотерапия при условии правильного определения возбудителя и его чувствительности делает возможным практически полное излечение (с более или менее выраженными остаточными склеротическими изменениями клапанов). Трудоспособность медленно восстанавилвается, зачастую развиваются необратимые морфологические изменения клапанного аппарата сердца.
Рецидивы эндокардита обычно возникают в течение 4 недель после окончания лечения. Их развитие является отражением неадекватности или недостаточной активности (малые дозы) антибиотиков, либо (реже) является показанием к хирургическому лечению. Рецидивы приводят к тяжелым повреждениям клапанов и прогрессированию сердечной недостаточности. Появление симптомов эндокардита позже 6 недель после окончания лечения свидетельствует не о рецидиве, а о новом инфицировании.
Профилактика
Профилактика заключается в активном лечении хронических инфекционных заболеваний, своевременной санации очагов инфекции, лечении интеркуррентных заболеваний у больных с пороками сердца (врожденными, ревматическими и прочими).
Кроме того этим больным необходимо назначать антибиотики длительного действия при обострениях тонзиллита, пиелонефрита, ангинах, пневмонии, а также при любых вмешательствах, которые могут сопровождаться бактериемией (экстракция зуба, тонзиллэктомия, аборт, аппендэктомия, бронхоскопия, катетеризация уретры и др.). С этой целью применяют, например, бициллин–3 или бициллин–5 по 1 000 000 ЕД однократно или по 500 000 ЕД два раза в неделю в течение 2 — 4 недель (в зависимости от показаний, вида сопутствующей патологии, хирургического вмешательства и реактивности организма). Возможно применение с профилактической целью клиндамицина или эритромицина.
Важно избегать переохлаждений, гриппа и других провоцирующих заболевание инфекций.
Хирургическое лечение инфекционного эндокардита
… инфекционный эндокардит продолжает представлять серьезную социальную проблему.
Инфекционный (бактериальный) эндокардит является тяжелым инфекционным процессом, который в отсутствие лечения всегда приводит к летальному исходу.
К сожалению, и в «эру антибиотиков» инфекционный эндокардит продолжает оставаться серьезной причиной общей смертности. Заболеваемость инфекционным эндокардитом не снижается, хотя ее структура за последние десятилетия претерпела определенные изменения — в настоящее время инфекционный эндокардит чаще встречается у лиц старше 50 лет. Патологический процесс по-прежнему в основном локализуется на левом предсердно-желудочковом (митральном) клапане, на втором месте по частоте поражения следует аортальный клапан. В то же время наблюдается рост частоты развития инфекционного эндокардита правых отделов сердца, что связано с распространением наркомании и широким применением венозных катетеров. В странах с высоким уровнем развития сердечно-сосудистой хирургии увеличивается частота развития внутрибольничных инфекционных эндокардитов. Наблюдаются изменения в структуре этиологических факторов заболевания, в частности увеличивается частота стафилококковых, грамотрицательных инфекций, а также инфекций, вызванных редкими микроорганизмами и штаммами, резистентными к антибиотикам.
Современная лечебная программа инфекционного эндокардита включает антибактериальную, патогенетическую, симптоматическуютерапию и экстракорпоральную гемокоррекцию, также современная терапия инфекционного эндокардита не мыслима без своевременного оперативного лечения, которое при остром инфекционном эндокардите выполняется в ранние сроки при сохраняющейся лихорадке и бактериемии после непродолжительного курса антибактериальной терапии. Указанный подход позволяет снизить госпитальную летальность до 11,5%, увеличить пятилетнюю выживаемость больных с инфекционным эндокардитом до 76,8%.
Вообще же, всегда лучше вылечить инфекционный эндокардит антибиотиками, без протезирования клапана, однако клиническая ремиссия должна быть достигнута достаточно быстро. В противном случае наступает генерализация процесса, развитие общего сепсиса, и прибегать к хирургическому лечению становится слишком поздно.
В то же время успех хирургического лечения возможен лишь там, где есть взаимосвязь и четкое взаимодействие между кардиологами и кардиохирургами. У больных инфекционным эндокардитом чрезвычайно важно определить тот момент, когда консервативная терапия исчерпала свой ресурс и продолжение её ведет только лишь к снижению функциональных резервов больного. В ряде же случаев любое консервативное лечение абсолютно нежелательно ввиду полной его бесперспективности и, можно даже сказать, что оно вредно для больного, так как отдаляет срок проведения жизненно необходимой операции. Для больных с острым разрушением аортального клапана или нескольких клапанов такая тактика не только неправильна, но и просто опасна. Быстрое развитие порока сердца не позволяет обеспечить компенсацию расстройств кровообращения, и очень скоро резервы миокарда истощаются, несмотря на консервативную терапию. В подобных ситуациях срабатывает правило: «Чем дольше живет больной до операции, тем меньше он проживет после нее».
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Лечение инфекционного эндокардита невозможно без своевременной операции, которая выполняется в ранние сроки или по завершении 4-6-недельного курса антибактериальной терапии. Недостаточность кровообращения при современном инфекционном эндокардите чаще всего связана с быстрым разрушением клапанного аппарата, поэтому хирургическое лечение в последнее десятилетие применяется все чаще. Хирургическое вмешательство является эффективным методом восстановления внутрисердечной гемодинамики и санации полостей сердца, без чего больные погибали бы.
Хирургический метод лечения, как правило, заключается в удалении пораженного клапана и имплантации искусственного механического или биологического протеза. Новыми методами хирургического лечения являются применение криосохраненных аллографтов, ксенографтов и разработка реконструктивных вмешательств на клапанах сердца, что снижает частоту реинфекции.
По данным Ю.Л.Шевченко, Г.Г.Хубулава, Н.Н.Шихвердиева, С.А.Матвеева (Клиника хирургии усовершенствания врачей имени П.А. Куприянова Военно-медицинской академии). «… в основу хирургического лечения инфекционного эндокардита должна быть положена щадящая по своему характеру операция на сердце с целью санации его камер и радикальной коррекции нарушений внутрисердечной гемодинамики. Щадящий принцип операции продиктован особой тяжестью состояния таких больных и заключается в максимальном уменьшении всех видов лекарственной и общей хирургической агрессии по отношению к пациентам. Этот принцип начинает реализоваться уже с оперативного доступа. Несмотря на то, что во всем мире стандартным доступом к сердцу является срединная стернотомия, мы в клинике используем правостороннюю передне-боковую торакотомию. Как доказывает наш многолетний клинический опыт, этот доступ менее травматичен, лучше переносится больными и в последующем дает меньше осложнений. Из этого доступа возможно выполнение протезирования практически любого клапана сердца, которые пока остаются наиболее частыми вариантами коррекции нарушений внутрисердечной гемодинамики при инфекционном эндокардите.
Более выгодным для больного вариантом является клапаносохраняющая операция. Но пластические клапаносохраняющие операции требуют опыта, хороших мануальных навыков и творчества в их выполнении. Тем не менее, именно эти виды коррекции нарушений внутрисердечной гемодинамики (клапаносохраняющие операции) дают наиболее благоприятные результаты. Однако такие вмешательства, как правило, возможны у больных на относительно ранней стадии заболевания, когда клапанные разрушения еще не столь обширные. Чаще, чем при других локализациях, возможны пластические вмешательства при инфекционном поражении трикуспидального клапана.
В среднем, клапаносохраняющие операции возможны у 7-15% больных. Безусловно, по мере развития диагностики этот процент будет увеличиваться соответственно увеличению количества больных инфекционным эндокардитом, выявленным на ранних стадиях заболевания.»
В Национальном институте сердечно-сосудистой хирургии им. Н.М. Амосова АМН Украины выработаны такие подходы к хирургическому лечению инфекционного эндокардита. (1) раннее хирургическое вмешательство; (2) радикальное иссечение инфицированных тканей; (3) выполнение реконструктивных пластических операций; (4) использование аутотканей для реконструкции; (5) применение общей управляемой гипертермической перфузии.
Количество больных, нуждающихся в оперативном лечении, зависит от своевременной диагностики, эффективности антибактериальной терапии, осложнений, вида возбудителя. При стрептококковом инфекционном энокардите протезирование клапанов сердца выполняют 17% больных, при стафилококковом — 51,7-70%. Лечение инфекционного эндокардита на современном этапе состоит в расширении показаний к хирургическому вмешательству и, соответственно, уменьшении ограничений для его проведения.
Основными показаниями к проведению хирургического лечения при остром инфекционном эндокардите являются. (1) острая аортальная и митральная недостаточность; (2) деструкция клапанного аппарата (разрыв хорд, разрушение или отрыв створки, перфорации); (3) прогрессирующая сердечная недостаточность; (4) неконтролируемая инфекция, в том числе диагностика абсцесса фиброзного кольца; (5) также хирургическое вмешательство показано и тогда, когда течение эндокардита естественных клапанов осложняется повторными системными эмболиями, аневризмой синуса Вальсальвы, прогрессирующими нарушениями проводимости.
Согласно данным Шевченко Ю.Л. Хубулава Г.Г. 1995; Тюрина В.П. (1999) показаниями к хирургическому лечению инфекционного эндокардита являются. (1) прогрессирующая сердечная недостаточность (60-81%); (2) высокая активность инфекционного эндокардита, некупируемая медикаментозной терапией (10-19%); (3) грибковый эндокардит (75-86%), инфекционный эндокардит протеза клапана (11-26%); (4) эмболические осложнения или высокий риск рецидивов эмболий (3,4-14%); (5) быстрое разрушение аортального клапана (88-91%).
Показаниями для операции по поводу инфекционного эндокардита на фоне протезированного клапана считаются. (1) развитие инфекционного эндокардита менее чем через год после протезирования; (2) развитие осложнений с дисфункцией протеза – стенозирование или существенная регургитация; (3) персистирующая бактериемия, формирование абсцессов, нарушения проводимости и крупные вегетации, особенно если они вызваны стафилококком.
По данным Крикунова А. А. (кандидат медицинских наук, заведующий отделением хирургии инфекционного эндокардита Национального института сердечно-сосудистой хирургии им. Н.Н. Амосова АМН Украины). «… в настоящее время абсолютными показаниями к хирургическому лечению инфекционного эндокардита считаются: (1) отсутствие эффекта от проводимой антибиотикотерапии в течение двух недель; (2) развитие выраженных нарушений гемодинамики (хроническая недостаточность кровообращения, острая сердечная недостаточность, сепсис-индуцированная гипотензия); (3) наличие внутрисердечного абсцесса, микотических аневризм корня аорты; (4) повторные эмболии.
Относительным показанием к операции считается наличие вегетаций при отсутствии клиники активного воспалительного процесса и без гемодинамических нарушений. Наличие вегетаций, даже при отсутствии других проявлений клапанного инфекционного эндокардита, значительно повышает риск смерти от эмболии периферических сосудов, однако некоторые авторы не находят статистически достоверной связи между наличием вегетации и частотой эмболии. Учитывая противоречивость результатов различных исследований, риск операции, а также потенциальный риск тромбоэмболии в отдаленные сроки после протезирования клапанов в таких случаях, к выбору метода лечения следует подходить дифференцированно. При больших вегетациях необходимо отдавать предпочтение хирургическому методу, стараясь сохранить собственный клапан пациента. В большинстве случаев грибковый эндокардит и инфекционного эндокардита, вызванный грамнегативными микроорганизмами, также являются показаниями к хирургическому лечению, так как медикаментозное лечение заболевания данной этиологии, как правило, безуспешно.»
Эхокардиографические данные, указывающие на необходимость хирургического лечения. ЭхоКГ позволяет оценить гемодинамический статус и выявить внутрисердечные осложнения инфекционного эндокардита, что может быть важно при определении показаний к хирургическому лечению.
Основными моментами являются следующие. (1) количественная оценка степени регургитации через поврежденные клапаны, оценка функциональных возможностей левого желудочка; (2) мониторинг преждевременного закрытия клапана (до начала систолы), что является признаком острого переполнения левого желудочка и тяжелой декомпенсации сердца, указывает на необходимость хирургического лечения; (3) появление патологических фистул, указывающих на неклапанные поражения сердца; (4) трансэзофагеальная ЭхоКГ позволяет более точно выявлять абсцессы, расположенные около клапанов и в перегородке (перикардит является косвенным указанием на формирование абсцесса кольца аортального клапана); (5) обнаружение вегетаций, особенно значительного размера, может указывать на возможность массивной эмболии (во многих исследованиях показана прямая корреляционная зависимость между частотой обнаружения вегетаций и частотой сердечной недостаточности, тяжелых эмболических поражений; критическим является размер вегетаций более 10 мм в диаметре; подвижность вегетаций и их локализация также имеют определенное значение с точки зрения возможности эмболии).
Полный курс антимикробной терапии должен быть проведен в течение не менее 7–15 дней после оперативного вмешательства независимо от длительности терапии до операции.
Очень важным является время проведения оперативного вмешательства при остром инфекционном эндокардите. желательно провести какое-то время антибактериальную терапию с целью уменьшения микробного инфицирования ткани, куда будет имплантироваться клапан (и тем самым уменьшить риск реинфекции на протезе), а с другой стороны – при неэффективности медикаментозной терапии необходимо оперировать до развития полиорганной недостаточности. В современных условиях основной тенденцией в хирургическом лечении инфекционного эндокардита стало раннее проведение операции на сердце при минимальных внутрисердечных разрушениях, а порой и без них до развития других тяжелых осложнений. К сожалению, до сих пор доля таких операций невелика. Больше поступает больных с развившимися тяжелыми осложнениями.
Инфекционный эндокардит – заболевание, угрожающее жизни пациента. Поэтому, наличие онкологических заболеваний, внесердечных осложнений (эмболических инсультов, ишемий) при инфекционном эндокардите не являются противопоказанием к операции на сердце. При наличии экстракардиальных осложнений инфекционного эндокардита тактика лечения должна быть активной. В случае возникновения эмболии в сосуды головного мозга, например, операция на сердце может быть выполнена уже через две недели после возникновения данного эпизода (при отсутствии геморрагии в зоне поражения). Но даже в случаях развития геморрагического инсульта через два месяца возможно проведение операции в условиях искусственного кровообращения.
Развитие острой аортальной или митральной недостаточности является показанием к неотложному хирургическому вмешательству, а отсутствие эффекта от проводимой антибактериальной терапии в течение 10-14 дней (сохранение лихорадки, лейкоцитоза, бактериемии) диктуют необходимость раннего оперативного вмешательства до развития гнойных очагов других органах и тканях.
Также раннее хирургическое вмешательство может рассматриваться и при крупных вегетациях митрального клапана – более 10 мм; при продолжающемся росте вегетаций на фоне антибиотикотерапии и при наличии соприкасающихся вегетаций створок митрального клапана. Прогноз при инфекционном эндокардите правых отделов более благоприятен и хирургическое вмешательство требуется только при вегетациях размером более 20 мм и после повторных легочных эмболий.
В связи с этим лечение больных острым инфекционным эндокардитом должно проводиться совместно терапевтами (кардиологами, ревматологами) и кардиохирургами с целью выработки оптимальной тактики лечения.
* * *
Таким образом. инфекционный эндокардит в значительной степени является хирургической проблемой и требует для своего лечения интеграции усилий специалистов самых различных направлений: кардиологов, кардиохирургов, микробиологов, инфекционистов, специалистов по лучевой диагностике, реаниматологов и многих других. Основой успешного хирургического лечения этого тяжелого недуга является ранняя диагностика и ранняя операция. Поэтому необходимо расценивать инфекционный эндокардит как хирургическую патологию, включая рассмотрение этой нозологической формы во всех учебниках по общей хирургии, а также включить в программу подготовки врачей изучение инфекционного эндокардита на хирургических циклах.