Сердечная недостаточность при алкоголизме. Алкогольная кардиомиопатия и сердечная недостаточность
В качестве примеров приведем несколько наблюдений над больными с алкогольной кардиопатией. осложненной сердечной недостаточностью различных форм и стадий.
Больной В. 39 лет, слесарь автобазы «Скорой помощи » поступил в психиатрическую больницу для противоалкогольного лечения. Злоупотребляет алкоголем около 15 лет, последние 6 лет опохмеляется, пьет преимущественно водку. Считает себя физически здоровым, жалоб не предъявляет. При осмотре несколько повышенного питания, умеренный цианоз губ. Над легкими ясный перкуторный звук, везикулярное дыхание. Пульс 106 в минуту (12-й день воздержания), ритмичный. Правая и верхняя границы сердца в норме. Левая на 1 см кнаружи от срединно-ключичной линии.
Ритм правильный, тоны глухие. Артериальное давление 130/100 мм рт. ст. Язык влажный. Живот мягкий, печень выступает на 2 см, плотная. При попытке использовать больного на нетяжелой работе обращала внимание одышка, несоответствующая степени нагрузки. На ЭКГ у больного выявлена полная блокада правой ножки пучка Гиса и возможные очаговые изменения в передне-боковой стенке левого желудочка.
При рентгенологическом исследовании органов грудной клетки выявлена умеренная гипертрофия левого желудочка сердца, патологических изменений в легких не обнаружено. Лабораторные показатели без существенных отклонений от нормы. При повторных осмотрах оставалась тахикардии до 100 в минуту, ЭКГ без существенной динамики. У больного была диагностирована алкогольная кардиопатия, осложненная сердечной недостаточностью НА стадии, назначен дигоксин по 0,25 мг 3 раза в день, фуросемид по 40 мг через день, неробол 15 мг в день.
Лечение проводилось в терапевтическом стационаре. Через пять недель у больного состояние заметно улучшилось, уменьшилась тахикардия до 80 в минуту, артериальное давление 120/80 мм рт. ст. исчезла одышка при небольшой нагрузке, губы приобрели нормальную окраску, перестал выслушиваться ритм галопа на верхушке сердца. На ЭКГ сохраняется картина блокады правой ножки пучка Гиса. Выписан для продолжения лечения сердечными гликозидами в амбулаторных условиях.
При осмотре через 4 мес состояние больного удовлетворительное. Вернулся к работе, алкоголь не употребляет, хорошо справляется с нагрузкой, одышки нет. Пульс 76 в минуту, ритм сердца правильный. На ЭКГ остается блокада правой ножки пучка Гиса. За 3 нед до осмотра по совету врачей перестал принимать сердечные гликозиды.
Таким образом, у больного с алкогольной кардиопатией в исходе дистрофии миокарда развился кардиосклероз с блокадой правой ножки пучка Гиса, осложненный сердечной недостаточностью преимущественно по левожелудочковому типу. При соблюдении режима, воздержании и адекватной кардиотонической терапии удалось добиться достаточной компенсации сердца, позволившей отказаться от дальнейшей терапии сердечными гликозидами.
Оглавление темы «Алкогольное поражение органов»:
Похоронный Портал
Статьи о похоронах
Кардиомиопатия
Группа заболеваний, при которых в первую очередь страдает мышца сердца и которые проявляются нарушением функции сердечной мышцы.
Известны три вида кардиомиопатий:
— дилатационная
При этом заболевании нарушается основная функция мышцы сердца – сократительная. Она ослабляется. При этом диффузно (во все стороны) расширяются камеры сердца. Значительно реже поражается только одна из камер сердца. Согласно статистике дилатационные кардиомиопатии составляют 9% от всех случаев сердечной недостаточности. Частота заболеваний дилатационной кардиомиопатией от 3 до 10 случаев на 100 000 человек.
Причины возникновения этого вида кардиомиопатий до конца не изучены. Считается возможной наследственная природа болезни, так как нередко встречается несколько случаев заболевания у близких родственников. Возможно способствуют болезни нарушения в иммунной системе, но подтверждение этому не найдено у всех больных. Многие исследователи уверены в вирусном происхождении дилатационной кардиомиопатии, однако выделить вирус ее вызывающий никто пока не смог. Болезнь обычно развивается постепенно. Иногда человек несколько лет не замечает болезни. И расширенные контуры левого желудочка обнаруживают случайно при рентгеновском исследовании.
Первые признаки болезни: они не специфичны, т.е. по ним нельзя сразу догадаться, что это именно кардиомиопатия. Это повышенная утомляемость при физической нагрузке, слабость. Позже появляется одышка, сначала при нагрузке затем она усиливается и в разгаре болезни появляется сердечная астма. Очень часто возникают боли в сердце различного характера: ноющие, колющие, сжимающие. Но стенокардия встречается редко. Оттого что внутренние камеры сердца расширены и по другим до конца не выясненным причинам часто в полости сердца и в больших венах возникают тромбы. Эти тромбы могут отрываться и с током крови попадать в легкие. Тогда возникает грозное осложнение — тромбэмболия легочной артерии (ТЭЛА). В 33% случаев внезапной смерти виновницей оказывается именно ТЭЛА.
При осмотре у больного обнаруживается холодная кожа, расширение границ сердца. При выслушивании выявляется систолический шум, различные нарушения ритма. При значительном расширении полости левого желудочка и снижении объема выбрасываемой им из-за слабости сердечной мышцы объема крови – прогноз у пациента неблагоприятный.
Диагноз дилатационной кардиомиопатии устанавливается на основании рентгеновского исследования, лектрокардиограммы, ангиографии. Но основным методом диагностики кардиомиопатии служит эхокардиография. При эхокардиографическом исследовании выявляют увеличение левого желудочка, расширение остальных камер сердца, определяется нормальная или уменьшенная толщина стенки левого желудочка. При подозрении на дилатационную кардиомиопатию эхокардиография проводится обязательно. Уже при первом обследовании устанавливается диагноз. В последующем обследования проводятся для контроля лечения и состояния сердца. Может быть проведена биопсия. Исследование под микроскопом маленького кусочка сердечной мышцы. В ней находят обширные изменения – погибшие клетки сердечной мышцы, замещение мышечной ткани на соединительную (склероз мышцы сердца).
Специфического лечения кардиомиопатий нет. Лечение направлено на борьбу с осложнениями. Прежде всего, это сердечная недостаточность, которая с течением времени развивается у всех пациентов.
Больным даются рекомендации по изменению образа жизни: необходимо снизить физическую активность, уменьшить потребление соли, животных жиров, исключить вредные привычки. Это позволяет снизить нагрузку на сердце и замедлить развитие сердечной недостаточности.
Медикаментозное лечение направлено на снижение артериального давления. Для этого используются ингибиторы ангиотензинпревращающего фермента (эналаприл, берлиприл, лизиноприл и другие). Эти препараты уменьшают системное артериальное давление и снижают давление в левом предсердии, уменьшая нагрузку на сердце. Доказано, что их применение увеличивает продолжительность жизни больных дилатационной кардиомиопатией. Иногда применяются сердечные гликозиды и малые дозы бета-адреноблокаторов.
Почти всем пациентам назначаются диуретики (мочегонные). Они снижают объем циркулирующей в сосудах крови.
При нарушениях сердечного ритма обязательно назначаются препараты для нормализации ритма сердечных сокращений.
Поскольку у больных часто образуются тромбы, назначаются препараты, препятствующие тромбообразованию (аспирин, варфарин).
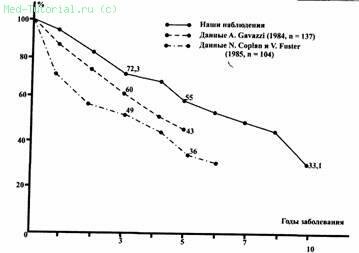
Возможны случаи, когда сердечная недостаточность не поддается медикаментозному лечению, тогда единственный выход это трансплантация сердца. Прогноз при этой болезни серьезный. Постепенно, несмотря на лечение, функция сердца ухудшается. В первые 5 лет от начала заболевания умирает
около 70% больных. Однако, есть данные, что при регулярном контроле и лечении возможна стабилизация состояния у 20-50% больных и даже улучшение. Выздоровление при дилатационной кардиомиопатии происходит очень редко. Женщинам-пациенткам следует избегать беременности, так как при этом состоянии очень высока материнская смертность.
— гипертрофическая
Характеризуется значительным утолщением и увеличением в объеме (гипертрофией) стенки левого желудочка сердца, при этом его внутренняя полость не расширяется. В большинстве случаев утолщается еще и межжелудочковая перегородка.
Частота гипертрофических кардиомиопатий составляет 0,2%. Болеют чаще молодые люди. Заболевание неуклонно прогрессирует. При гипертрофической кардиомиопатии существует самая большая угроза внезапной смерти. Смертность при этом заболевании 2-4%. Доказана наследственная природа гипертрофической кардиомиопатии. Это так называемая «семейная гипертрофическая кардиомиопатия».
Но бывают случаи, когда не удается доказать наследственную природу. Когда заболевание не обнаруживается у близких родственников заболевшего, считается, что произошла мутация генов, кодирующих белки сердечной мышцы.
Сердечная мышца при гипертрофической кардиомиопатии утолщена и менее растяжима. Миокард может быть утолщен равномерно или преимущественно в каких-либо отделах. От этого зависит вариант течения болезни:
— Если сердечная мышца гипертрофируется в большей степени в зоне под отхождением аорты, в этом случае может сужаться выход из левого желудочка. Это сопровождается утолщением внутренней оболочки сердца, из которой состоят клапаны, и нарушается функция митрального и аортального клапанов. Чаще это происходит при неравномерном утолщении межжелудочковой перегородки. Возможен вариант несимметричного утолщения перегородки без нарушения клапанного аппарата сердца и сужения выхода из левого желудочка.
— Верхушечная гипертрофическая кардиомиопатия возникает, если увеличивается сердечная мышца только на верхушке сердца.
— Симметричная гипертрофическая кардиомиопатия с круговой гипертрофией миокарда левого желудочка.
Чаще гипертрофической кардиомиопатией болеют молодые люди. Заболевание протекает очень разнообразно. У некоторых пациентов длительное время не бывает жалоб. У других с самого начала состояние тяжелое и высок риск внезапной смерти. Самое частое проявление кардиомиопатии боли в сердце различного характера от колющих и ноющих до типичного приступа стенокардии. Часто у больных с гипертрофической кардиомиопатией возникает стенокардия. Это происходит оттого, что в условиях гипертрофии коронарные сосуды сдавливаются, а увеличенной сердечной мышце требуется больше кислорода и питательных веществ. Возникает несоответствие между потребностью миокарда в кислороде и его доставкой.
Очень частое проявление – нарушение сердечного ритма. Проводящая система сердца сдавливается, нормальное распространение электрического импульса нарушается и возникают самые разнообразные нарушения ритма сердечных сокращений. Больные жалуются на перебои в сердце, сердцебиения, провалы в сердце.
Из-за нарушений ритма и снижения кровоснабжения мозга возникают обмороки. У одних больных такой обморок может быть единственным на протяжении жизни, у других может быть несколько обмороков каждый день.
Иногда первым симптомом болезни может стать одышка.
При осмотре пациента выявляют расширение границ сердца, систолический шум над сердцем. На рентгенограмме находят увеличение левого желудочка сердца.На электрокардиограмме находят специфические изменения, по которым можно поставить диагноз гипертрофической кардиомиопатии. Но основным методом диагностики служит эхокардиография. С ее помощью выявляют утолщение сердечной мышцы, утолщение межжелудочковой перегородки, снижение двигательной активности миокарда. Иногда проводят биопсию сердечной мышцы (исследование кусочка миокарда под микроскопом).
Направлено на уменьшение симптомов со стороны сердечно-сосудистой системы. Применяют бета-блокаторы и верапамил. Эти препараты используются как при лечении возникшего заболевания, так и при обнаружении гипертрофической кардиомиопатии при безсимптомном течении (пока не появились жалобы). При неэффективности медикаментозного лечения проводят хирургические операции по удалению части гипертрофированной сердечной мышцы. Прогноз гипертрофической кардиомиопатии благоприятный по сравнению с другими видами кардиомиопатий. Заболевание может протекать десятилетиями. Больной длительное время остается трудоспособным. Возможны даже беременности и роды у женщин с гипертрофической кардиомиопатией. Больной должен помнить, что ему противопоказаны значительные физические нагрузки.
— рестриктивная
Заболевание, вызванное изменением внутренней оболочки сердца – эндокарда и характеризующейся нарушением диастолической функции сердца.
Внутренняя оболочка сердца (эндокард) состоит из соединительной ткани. Она утолщается и уплотняется, при этом такой измененный эндокард не может растягиваться в фазу диастолы (расслабления). Это нарушает нормальное наполнение кровью желудочков сердца и в итоге возникает недостаточность кровообращения. Кроме того, сердечная мышца не может полноценно расслабиться в фазу диастолы, а это нарушает ее кровоснабжение и питание.
Рестриктивная кардиомиопатия – наиболее редкая форма кардиомиопатий. Она может быть как самостоятельным заболеванием, так и одной из составляющих различных болезней (амилоидоз, гемохроматоз, эндомиокардиальный фиброз, болезнь Фабри, болезнь Леффлера, склеродермия).
Выделяют две формы рестриктивной кардиомиопатии:
— Облитерирующая, когда во внутренней оболочке сердца и под ней откладываются патологические белки. Затем происходит уплотнение и утолщение эндокарда (стадия фиброза), на стенках полостей сердца образуются тромбы и происходит облитерация (уменьшение, сужение) внутренних полостей сердца. Поражаться может правая, левая или обе половины сердца.
— Диффузная инфильтрация миокарда. При этом патологические субстанции откладываются равномерно по всей сердечной мышце.
Происхождение рестриктивной кардиомиопатии остается невыясненным, как и многих из тех заболеваний, которые сопровождаются возникновением такого вида кардиомиопатий. Предполагается вирусное или наследственное происхождение. Но доказанных теорий пока нет.
В начале болезни пациенты могут жаловаться на слабость, снижение переносимости физической нагрузки, одышку. Боль в области сердца или грудной клетки встречается редко. В дальнейшем постепенно возникает сердечная недостаточность, в зависимости от места поражения эндокарда по левому или по правожелудочковому типу. Часто заболевание обнаруживается лишь тогда, когда у больного уже возникают признаки сердечной недостаточности: отеки на ногах, асцит (накопление жидкости в животе), цианоз лица, набухание шейных вен.
При аускультации выслушиваются приглушенные тоны сердца, иногда систолический шум. На электрокардиограмме обнаруживают различные нарушения ритма, низкие зубцы сердечных комплексов.
На рентгенограмме чаще увеличение правого предсердия и правого желудочка, изменения в легких. На эхокардиограмме определяют утолщение внутренней оболочки сердца, уменьшение объема полостей желудочков, неправильное движение межжелудочковой перегородки, часто нарушения клапанного аппарата сердца. При ангиокардиографии (исследование с помощью контрастных веществ) обнаруживают уменьшение размеров, неровность контуров желудочков сердца, снижение сердечного выброса. Иногда проводят биопсию эндокарда – исследование под микроскопом маленького кусочка внутренней оболочки сердца.
Лечение
Эффективного лечения этого заболевания пока не найдено. Проводится симптоматическое лечение при возникновении сердечной недостаточности небольшими дозами мочегонных и дигоксина. Остальные препараты применяются с большой осторожностью. Пересадка сердца чаще всего неэффективна, так как через некоторое время в трансплантированном сердце развивается тот же процесс. Состояние больных обычно средней тяжести и тяжелое. 70% больных погибает в течение 5 лет.
4) аритмическая дисплазия правого желудочка;
5) сочетание одного из 4 видов кардиомиопатий с артериальной гипертензией.
2. Дилатационная кардиомиопатия
Дилатационная кардиомиопатия (ДКМП) – заболевание сердечной мышцы, характеризующееся диффузным расширением всех камер сердца (преимущественно левого желудочка), при котором на первом плане стоит патология насосной функции сердца и как следствие – хроническая сердечная недостаточность (отсю-
да второе название – застойная, когда сердце не способно полноценно перекачивать кровь и она «застаивается» в тканях и органах организма). Мышечная стенка сердца при этом остается либо неизмененной, либо в различной степени гипертрофируется.
Заболевания и факторы, предшествовавшие развитию ДКМП, описаны в приведенной ниже таблице (см. табл. 5).
Таблица 5
Заболевания и факторы, предшествовавшие развитию ДКМП
Это самая распространенная форма поражения сердечной мышцы. Заболеваемость составляет 5–8 случаев на 100 000 человек в год. Точного семейного анамнеза у этих пациентов не прослеживается. Мужчины болеют в 2–3 раза чаще женщин.
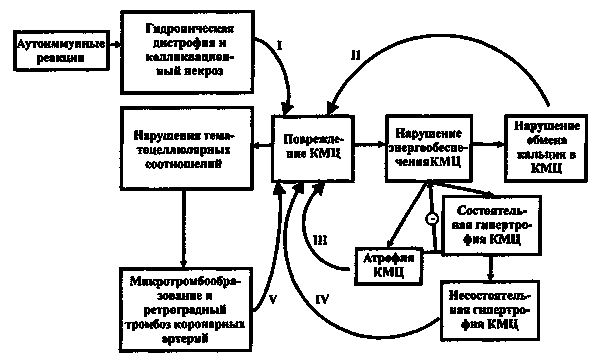
Патогенез. В результате воспалительного процесса в сердечной мышце (миокардита) происходит гибель отдельных клеток в различных ее участках. Воспаление при этом носит вирусный характер, а клетки, пораженные вирусом, становятся чужеродными агентами для организма. Соответственно, при появлении в организме антигенов развивается комплекс реакций иммунного ответа, направленных на их уничтожение. Постепенно происходит замещение погибших мышечных клеток на соединительную ткань, которая не обладает способностью к растяжимости и сократимости, присущей миокарду. В результате потери основных функций миокарда сердце теряет способность функционировать, как насос. В ответ на это (как компенсаторная реакция) камеры сердца расширяются (т. е. происходит их дилатация), а в оставшейся части миокарда происходит утолщение и уплотнение (т. е. развивается его гипертрофия). Для увеличения доставки кислорода органам и тканям организма возникает стойкое учащение сердечного ритма (синусовая тахикардия).
Данная компенсаторная реакция лишь на время улучшает насосную функцию сердца. Однако возможности дилатации и гипертрофии миокарда ограничиваются количеством жизнеспособного миокарда и являются индивидуальными для каждого конкретного случая заболевания. При переходе процесса в стадию декомпенсации развивается хроническая сердечная недостаточность. Однако на этом этапе вступает в действие еще один компенсаторный механизм: ткани организма увеличивают экстракцию кислорода из крови по сравнению со здоровым организмом.
Но этот механизм недостаточен, так как снижение насосной функции сердца ведет к уменьшению поступления в органы и ткани кислорода, который является необходимым для их нормальной жизнедеятельности, при этом количество углекислого газа в них увеличивается.
У 2/3 больных в полостях желудочков на поздних стадиях болезни образуются пристеночные тромбы (вследствие снижения насосной функции сердца, а также при неравномерности сокращения миокарда в камерах сердца) с последующим развитием эмболии по малому или большому кругу кровообращения.
Патогистологические и патоморфологические изменения в сердце. Форма сердца становится шаровидной, масса его увеличивается от 500 до 1000 г, в основном за счет левого желудочка. Миокард становится дряблым, тусклым, с заметными белесоватыми прослойками соединительной ткани, имеется характерное чередование гипертрофированных и атрофичных кардиомиоцитов.
Микроскопически выявляется диффузный фиброз, он может сочетаться как с атрофией, так и с гипертрофией кардиомиоцитов, в которых отмечаются значительное увеличение объема ядер, количества митохондрий, гиперплазия аппарата Гольджи, увеличение количества миофибрилл, свободных и связанных с эндоплазматическим ретикулумом рибосом, обилие гранул гликогена.
Клиническая картина. Специфических признаков заболевания нет. Клиническая картина полиморфна и определяется:
1) симптомами сердечной недостаточности;
2) нарушениями ритма и проводимости;
3) тромбоэмболическим синдромом.
Все эти явления развиваются в терминальной стадии болезни, в связи с чем распознавание ДКМП до появления перечисленных симптомов представляет значительные трудности.
В большинстве случаев прогноз заболевания определяется поражением левого желудочка сердца. До наступления сердечной недостаточности ДКМП протекает латентно. Наиболее частыми жалобами уже наступившей сердечной недостаточности являются жалобы на снижение работоспособности, повышенную утомляемость, одышку при физической нагрузке, а затем в покое. По ночам беспокоит сухой кашель (эквивалент сердечной астмы), позже – типичные приступы удушья. У больных наблюдаются характерные ангинозные боли. При развитии застойных явлений в большом круге кровообращения появляются тяжесть в правом подреберье (вследствие увеличения печени), отеки ног.
Диагностика. При диагностике заболевания важным признаком является значительное увеличение сердца (признаки клапанного порока сердца или артериальной гипертензии отсутствуют). Кардиомегалия проявляется расширением сердца в обе стороны, определяемым перкуторно, а также смещением верхушечного толчка влево и вниз. В тяжелых случаях выслушиваются ритм галопа, тахикардия, шумы относительной недостаточности митрального или трехстворчатого клапанов. В 20 % случаев развивается мерцание предсердий. Артериальное давление обычно нормальное или слегка повышено (вследствие сердечной недостаточности).
Биохимические исследования крови и мочи позволяют обнаружить различные токсические вещества, а также дефицит витаминов. Инструментальные методы исследования позволяют обнаружить:
1) признаки кардиомегалии;
2) изменения показателей центральной гемодинамики;
3) нарушения ритма и проводимости.
На ЭКГ не отмечается каких-либо характерных изменений или сдвиги носят неспецифический характер. Это признаки увеличения размеров сердца, нарушения проводимости в виде блокады передней ветви левой ножки предсердно-желудочкового пучка (пучка Гиса) или полной блокады левой ножки (15 % случаев); а также стойкая синусовая тахикардия (частота сердечных сокращений часто превышает 100 ударов в 1 мин).
Фонокардиограмма подтверждает аускультативные данные в виде ритма галопа, довольно частого обнаружения систолического шума (вследствие относительной недостаточности митрального или трехстворчатого клапана). При застойных явлениях в малом круге кровообращения выявляют акцент II тона.
Рентгенологически обнаруживаются значительное увеличение желудочков (часто в сочетании с умеренным увеличением левого предсердия) и застой крови в легочном (малом) круге кровообращения. Нарушения в малом круге кровообращения проявляются усилением легочного сосудистого рисунка, а также появлением транссудата в плевральных полостях, который образуется вследствие повышения давления в сосудах легких.
Метод эхокардиографии – один из основных в диагностике заболевания. ЭхоКГ помогает выявить дилатацию обоих желудочков, гипокинезию задней стенки левого желудочка, парадоксальное движение межжелудочковой перегородки во время систолы. Помимо этого, ЭхоКГ позволяет уточнить увеличение амплитуды движения неизмененных створок митрального клапана.
Дополнительные инструментальные исследования не являются обязательными для постановки диагноза, однако их результаты позволяют детализировать степень расстройств гемодинамики и характер морфологических изменений миокарда.
Радиоизотопное исследование сердца (сцинтиграфия миокарда) производится для уточнения состояния насосной функции сердца, а также для определения зон погибшего миокарда. Исследование показателей центральной гемодинамики выявляет низкий минутный и ударный объем (минутный и ударный индексы), повышение давления в легочной артерии.
Ангиокардиографически обнаруживаются те же изменения, что и на эхокардиограмме. Прижизненная биопсия миокарда неинформативна для определения этиологии кардиомиопатии. В некоторых случаях в биоптате можно обнаружить вирусный антиген или увеличение содержания ЛДГ, а также ухудшение энергопродукции митохондриями. Однако этот хирургический метод можно использовать для уточнения этиологии заболевания и дальнейшей терапии. Манипуляция проводится следующим образом: под местным наркозом прокалывают (пунктируют) крупные артерию и вену, затем по их ходу к сердцу проводят специальный инструмент с маленькими ножницами на конце. При сочетании биопсии миокарда с коронароангиографией (введением контрастного вещества в кровоснабжающие сердце коронарные артерии) появляется возможность исключить у больного ИБС как одно из заболеваний, которое имеет схожие с ДКМП симптомы.
Эти два исследования производят под рентгенотелевизионным контролем.
Дифференциальная диагностика. Производится в первую очередь с миокардитом и миокардиодистрофиями, т. е. с теми состояниями, которые иногда необоснованно называются вторичными кардиомиопатиями.
Биопсия миокарда оказывает существенную помощь при дифференциальной диагностике дилатационной кардиомиопатии и заболеваний сердца, протекающих с выраженным его увеличением:
1) при тяжелых диффузных миокардитах обнаруживается клеточная инфильтрация стромы в сочетании с дистрофическими и некротическими изменениями кардиомиоцитов;
2) при первичном амилоидозе, протекающем с поражением сердца (так называемый кардиопатический вариант первичного амилоидоза), наблюдается значительное отложение амилоида в интерстициальной ткани миокарда, сочетающееся с атрофией мышечных волокон;
3) при гемохроматозе (заболевании, обусловленном нарушением обмена железа) в миокарде находят отложения железосодержащего пигмента, наблюдаются различной степени дистрофия и атрофия мышечных волокон, разрастание соединительной ткани. Как вариант ДКМП можно рассмотреть медикаментозные и токсические кардиомиопатии.
Многочисленные агенты могут вызвать токсические повреждения миокарда: этанол, эметин, литий, кадмий, кобальт, мышьяк, изпротеренол и другие яды. Патогистологические изменения в тканях сердечной мышцы проявляются в виде очаговых дистрофий. В дальнейшем происходит развитие микроинфарктов, сопровождающееся периферической воспалительной реакцией. Самым ярким примером токсической кардиомиопатии является кардиомиопатия, которая наблюдается у людей, избыточно потребляющих пиво. Она обусловлена наличием в нем кобальта, который добавляют в пиво для улучшения пенности. Кобальт блокирует действие витамина В1. а также непосредственно воздействует на изменение энзимных процессов клетки. В острой стадии течения кобальтовой кардиомиопатии отмечаются наличие гидропической и жировой дистрофии, деструкция внутриклеточных органелл, очаговый некроз кардиомиоцитов.
В дальнейшем происходит развитие диффузного или мелкоочагового интерстициального фиброза, заключительным итогом является формирование обширных рубцов. Кобальтовая кардиомиопатия тяжелее алкогольной кардиомиопатии. Если постановка диагноза происходит вовремя, то наблюдается клиническое излечение больных.
Алкогольная кардиомиопатия. Этанол оказывает прямое токсическое влияние на кардиомиоциты. К тому же при хронической этиловой интоксикации часто наблюдается недостаток питания. Доказано, что алкоголь ведет к коммуляции в кардиомиоцитах жирных кислот, так как имеется недостаток энергии, которая является необходимой для их деятельности. Ацетальдегид, образующийся при метаболизме алкоголя, может быть фактором прямого токсического воздействия на протеиновый синтез. Алкоголизм также сопровождается активацией латентных вирусов.
Макроскопически миокард дряблый, глинистого вида, иногда наблюдаются маленькие рубчики. Коронарные артерии интактны. При микроскопическом исследовании отмечается сочетание дистрофии (гидропической и жировой), атрофии и гипертрофии кардиомиоцитов, возможно наличие очажков лизиса кардиомиоцитов и склероза. Пораженные участки миокарда контрастируют с неизмененными. При электронно-микроскопическом исследовании биоптатов сердца наблюдается кистозное расширение саркоплазматической сети и Т-системы кардиомиоцитов, что является характерным для алкогольной кардиомиопатии. Осложнения алкогольной кардиомиопатии – внезапная смерть в результате фибрилляции желудочков или хроническая сердечная недостаточность, тромбоэмболический синдром.
Лечение. Терапия кардиомиопатий представляет трудную задачу, так как не известны конкретные причины их возникновения. Общие принципы лечения ДКМП не имеют значительных отличий от лечения хронической сердечной недостаточности. В случаях вторичной ДКМП дополнительно проводится лечение предшествующего заболевания (порока клапана сердца и т. д.), а также предпринимаются все меры для устранения причин возникновения ДКМП.
По существу, можно говорить о лечении больных кардиомиопатией лишь при появлении клинических признаков. При сердечной недостаточности сердечные гликозиды малоэффективны. У больных быстро развиваются явления непереносимости препаратов (гликозидная интоксикация), в связи с чем приходится применять гликозиды, быстро выводящиеся из организма (строфантин, изоланид). Достаточно эффективны периферические вазодилататоры, особенно при сопутствующем ангинозном синдроме (нитронг, сустак, нитросорбид). Эти препараты следует назначать при выраженной сердечной недостаточности, плохо поддающейся лечению гликозидами и мочегонными средствами. При ангинозном синдроме возникает необходимость применять антиангинальные препараты, предпочтительнее пролонгированные нитраты (сустак, нитронг, нитросорбид). Эффективны адреноблокаторы (их назначают при отсутствии признаков сердечной недостаточности).
Из современных методов хирургического лечения ДКМП наиболее эффективным является пересадка (трансплантация) сердца. Однако возможности проведения данной операции существенно ограничены. По этой причине как альтернатива пересадке сердца при современном лечении для увеличения продолжительности жизни больным ДКМП разработаны и производятся реконструктивные операции, которые направлены на ликвидацию недостаточности митрального и трикуспидального клапанов сердца. Оперативное устранение недостаточности этих клапанов позволяет на некоторое время «затормозить» наступление конечной стадии заболевания. Еще одной альтернативой пересадке сердца у больных ДКМП стало частичное удаление левого желудочка с целью уменьшения его размеров (операция Батиста).
Не так давно для лечения больных ДКМП были разработаны специальные модели электрокардиостимуляторов, они позволяют сделать работу желудочков сердца синхронной. Это приводит к улучшению наполнения желудочков сердца кровью и увеличению насосной функции сердца.
Отдельным вопросом следует рассмотреть ДКМП у детей, которая составляет 5—10 случаев на 100 000 детского населения в год. Примечательно, что болезнь может развиться у различных возрастных групп, в том числе у грудных детей. Данные, полученные при исследовании группы детей, следующие: больные получали 3 варианта терапии (монотерапия преднизолоном, монотерапия дигоксином или преднизолон + дигоксин). Эффективность лечения оценивали по следующим критериям: определяли частоту сердечных сокращений до и после проведенного лечения, частоту дыхания, состояние фракции выброса и фракции сократимости. Анализ полученных результатов свидетельствует, что наибольший эффект лечения дилатационной кардиомиопатии у детей раннего возраста достигается с помощью комбинации кортикостероидов и гликозидов (преднизолона и дигоксина). После завершения основного курса лечения (преднизолон назначают 2 мг/кг в день в течение 28 дней, дигоксин) наблюдались выраженное снижение частоты сердечных сокращений, уменьшение одышки. На фоне монотерапии преднизолоном происходит уменьшение частоты сердечных сокращений. Монотерапия дигоксином приводит к уменьшению тахикардии и одышки. Учитывая нецелесообразность назначения цитостатических препаратов у детей раннего возраста, так как наблюдалось значительное количество осложнений лечения, более оптимальным в педиатрии является использование при дилатационной кардиомиопатии сердечных гликозидов пролонгированного действия в сочетании с кортикостероидными гормонами.
Профилактика. Профилактика ДКМП заключается в исключении алкоголя, кокаина, а также проведении тщательного контроля показателей сердечной деятельности при химиотерапии опухолей.
Полезно проводить закаливание организма с раннего возраста. Полный отказ от употребления алкоголя при алкогольной разновидности ДКМП способствует улучшению сократительной функции сердца и может устранить необходимость его пересадки.
К отрицательным результатам в лечении может привести и тот факт, что в большинстве случаев заболевания постановка диагноза происходит на стадии сердечной недостаточности. Ранняя диагностика дилатационной кардиомиопатии может производиться при случайной (скрининговой) ЭхоКГ, которая выполняется при ежегодной диспансеризации, а также при обследовании лиц с отягощенной по данному заболеванию наследственностью. Именно в этом случае возможно повышение эффективности медикаментозного лечения ДКМП.