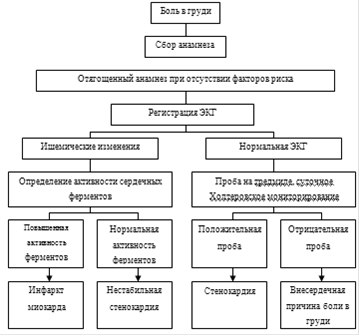
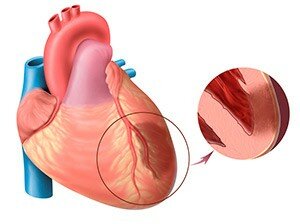
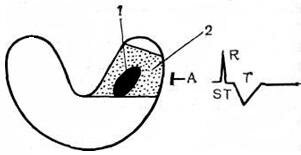
3. Инфаркт миокарда
Как указывалось выше без нормальной работы сердца не может быть нормального кровообращения. И мудрая Природа позаботилась, сделав сердечную мышцу вечной, неснашиваемой [19]. Почему же инфаркт сердечной мышцы (миокарда) – одно из самых распространенных заболеваний, а часто и причина смерти?
Мышца сердца человека содержит исключительно большое количество капилляров. На 1 кв.мм поперечного сечения миокарда желудочков взрослого человека приходится 3342-3400 капилляров [9]. То есть масса капилляров и сосудов в сердечной мышце практически соизмерима с массой самой сердечной мышцы – огромная масса, сопоставимая с массой миокарда. Поражение любой части капилляров и сосудов существенно влияет на прочность стенок сердца, на работу сердца и на кровообращение как в самом сердцае, так и организма в целом, принимая во внимание прямые и обратные связи.
Например, поражение ствола левой коронарной артерии обнаруживается при ангиографии примерно у 2-13% больных ИБС. Этот вариант поражения коронарного русла крайне неблагоприятен в прогностическом отношении, поскольку имеет высокий риск обширного поражения в случае развития инфаркта, а при благоприятном течении заболевания со временем развиваются явления ишимической кардиомиопатии [17]. Так что этиология инфаркта миокарда носит глобальный характер для сердечно-сосудистых заболеваний.
Без громкого обсуждения, незаметно появилась публикация, что наряду с БКК и МКК наличествует и СКК. Он начинается артериями сердца, отходящими от аорты на уровне полулунных клапанов и заканчивается венами, впадающими или непосредственно в правое предсердие, или в венечный синус, который открывается непосредственно в правое предсердие [11]. Так что, время открытий в физиологии еще не закрыто. НТК и эта книжка тому свидетельство.
ЭТИОЛОГИЯ. Об этиологии инфаркта миокарда до сих пор нет единого мнения. В связи с этим рассмотрение некоторых аспектов этиологии инфаркта миокарда (как наиболее изученный феномен) может, на наш взгляд, пролить свет на проблему инфарктов других органов, а также на проблему этиологии в целом для других заболеваний.
Различают три вида инфаркта миокарда: белый (ишемический), красный (геморрагический), белый с геморрагическим поясом [3].
В отдельную группу выделяют близкие к геморрагическим так называеиые застойные, или венозные инфаркты, обусловленные закрытием просвета и прекращением оттока крови по сравнительно крупным венозным стволам или тромбозом большого количества мелких вен. Застой крови, отек и массивные кровоизлияния создают условия, не совместимые с жизнедеятельностью тканей, – возникает инфаркт. Такие венозные застойные инфаркты наблюдаются в кишечнике при тромбозе брыжеечных вен, в почках при нарастающем тромбозе почечных вен, в селезенке при закупорке просвета селезеночной вены [3].
Нас же в данном случае больше интересуют застойные, венозные инфаркты, обусловленные закрытием просвета и прекращением оттока крови по сравнительно крупным венозным стволам или тромбозом большого количества мелких вен – это является ни чем иным как нарушением венозного возврата по причине длительного стационарного, однообразного положения тела, увеличения вязкости крови в десятки и сотни раз и все это прекрасно коррелируется с НТК.
Как видим, наука наблюдения и фиксации объективной реальности опережает попытки объяснить наблюденное. Считается, что факторы риска развития инфаркта миокарда во многом совпадают с факторами риска возникновения и прогрессирования атеросклероза, о которых мы указывали выше.
Опять же медицина расписывается в абсолютном незнании и непонимании истинных причин возникновения инфаркта миокарда. Да и как можно объяснить "застойные, или венозные инфаркты, обусловленные закрытием просвета и прекращением оттока крови", когда считается непогрешимым установка, что вся кровь постоянно циркулирует. Это тот самый случай, когда "Идея существующей теори кровообращения" давлеет над многкратно наблюденными фактами – телега поставлена впереди лошади. Такая постановка вопроса хорошо известна в мире, особено в нашей стране, однако. рассыпались суперимперии, но Принцип оставался непоколебим.
Небольшие инфаркты (микроинфаркты) в течение 3-4 дней замещаются молодой соединительной тканью. В обширных инфарктах некротические массы в центре очага могут сохраняться в течение недель и даже месяцев. Обширные инфаркты вызывают интоксикацию организма продуктами тканевого распада: отмечаются повышение температуры, лихорадочное состояние, дистрофические изменения внутренних органов [3].
Как уже отмечалось, повторные эпизоды острой транзиторной коронарной недостаточности с длительностью периодов ишемии миокарда до 10 мин. и более могут происходить у любого человека. Частота таких эпизодов может достигать 3-8 в течение суток. [13].
Причиной частой смены периода ишемии органов периодом возобновления кровотока в ранее ишимизированной зоне может являться нарушение и восстановление кровообращения, которые могут возникнуть в любой момент за счет смены полноценного кровообращения в отдельных частях органов и тканей на неполноценное и наоборот, что может происходить ежедневно и многократно в течение одного дня. Причиной могут выступать: длительное пребывание в одной позе, стрессы, переедание, неактивность и активность поведения и многое другое.
Повторная реперфузия миокарда характерна не только для тех форм ИБС, которые сопровождаются преходящим снижением коронарного кровотока в магистральных коронарных артериях. Феномен реперфузии отдельных зон ранее ишимизированного миокарда наблюдается и при необратимом нарушении тока крови в какой-либо ветви венечных артерий сердца [12]. Это чрезвычайно важное наблюдение. И оно находит объяснение в нашем толковании НТК.
Свидетельством тому может служить способность капилляров и мелких сосудов как отмирать при затухании кровотока, так восстанавливаться и прорастать при возрастании кровотока [9]. Понятен смысл феномена более лучшего и более быстрого выздоровления больных, которые на следующий день после операции начинают по возможности двигать,руками, ногами, поворачиваться, ходить, улучшая тем самым кровоток и расширяя зону охвата полноценного кровообращения.
C читается, что постишимическое возобновление или увеличение локального венечного кровотока может быть обусловлено спонтанным или медикаментозным прекращением коронароспазма, лизисом тромба или дезагрегацией форменных элементов крови, хирургической реваскуляризацией ранее ишимизированной зоны сердца в остром (ишимическом) периоде инфаркта миокарда или при "трансформирующейся" в инфаркт нестабильной стенокардии. При указанных состояниях ранний этап периода реперфузии сопровождается существенными расстройствами сердечной деятельности, дестабилизацией системной гемодинамики, микргемоциркуляции и нередко нарушением функции других физиологических систем [12]. Обращаем внимание на выражение: "прекращение коронароспазма может быть спонтанным" – согласно НТК это любые движения, изменение положения тела, физические нагрузки и упражнения, любые растирания и разминания тела и т.д. которые могут обеспечить венозный возврат в данной зоне (а следовательно и полноценное кровообращение). Однако они и поныне не принимаются во внимание, как и во многих других случаях.
"Застойные, или венозные инфаркты, обусловленные закрытием просвета и прекращением оттока крови" заслуживают гораздо большего внимания при изучении этиологии инфарктов сердца и других органов. Основы учения о свертывании крови были разработаны нашим соотечественником А.А.Шмидтом (1831-1894). Он впервые установил ферментативный характер процесса свертывании крови. Основным положением предложенной им теории свертывании крови явилось признание существования фибрина и фибрин-фермента, который впоследствии он назвал тромбином. Кроме всего прочего им было экспериментально показано, что тромбин отсутствует в циркулирующей крови и образуется при повреждении сосудов из неактивного предшественника – протромбина.
Но последующие исследования снова идут по "ложному следу" – пристальному изучению подвергаются вопросы тромбообразования, их искусственного разрушения. Кажется им, что познав химико-физиологическую сущность процесса свертывания крови, можно будет решить проблему инфарктов сердца и других органов. Было установлено, что свертывание крови – сложный, многоступенчатый механизм, действующий по принципу обратной связи, и выявлены с I по аж XIII факторы свертывания крови. Затем к ним прибавились еще факторы XIV и XV, Это такая сложная наука, что далеко не всякому специалисту окажется “по зубам”. Но главнейшее заключение А.А.Шмидта о том, что тромбин отсутствует в циркулирующей крови и образуется при повреждении сосудов из неактивного предшественника – протромбина, просто выкинули из сложной теории свертывания крови – из-за простоты, наверное. Действительно: зачем говорить об этом – ведь вся кровь циркулирует. Может быть потому и "забыли" утверждение А.А.Шмидта, поскольку. тромбы-то образуются в сосудах, их видят воочию при вскрытии, а ведь их не должно быть, т.к. кровь-то циркулирует однозначно! То, что какая-то часть крови может не циркулировать в живом организме – это нонсенс, который не допускался даже "горячими головами". В этом, наверное, разница между специалистами широкого профиля XIX века и узкими специалистами второй половины XX века: ни в коем случае нельзя перешагивать через существующие табу.
Сложный, многоступенчатый механизм свертывания крови – ни на иоту не приблизил к решению проблему инфарктов сердца и других органов. Тогда все стали валить на атеросклероз, на холестерин, но и здесь оптимистические прогнозы не оправдались – ждало очередное разочарование.
И не удивительно. По словам академика Е.И.Чазова школа А.Л.Мясникова доказала возможность образования тромбов в сердечно-сосудистой системе не только при отсутствии бляшек, но и вообще при отсутствии в них атеросклеротических изменений. Затем А.М.Вихерт (1982) писал: "К долипидным изменениям относятся также пристеночные тромбы, возникающие в различных отделах артериальной системы и обнаруживаемые лишь при микроскопических исследованиях. Тромбы могут состоять из одних тромбоцитов, одного фибрина или обоих компонентов". "Наши исследования (1961) показали возможность воспроизведения тромба в различных артериях животных при отсутствии в них атеросклеротических изменений. Так, например, при одновременном введении животным тромбина и питунтрина, воздействующего, помимо других эффектов, на состояние стенки сосудов, удавалось обнаружить тромбоз, который не воспроизводился при введении одного тромбина. Все это указывает на то, что не только атеросклеротические изменения, но и любые нарушения состояния стенки сосудов может способствовать формированию тромбов" [13]. Безусловно, атеросклероз существенно усугубляет ситуацию с инфарктами, но.
В этом смысле характерно исследование коронарной болезни сердца, возникающей у женщин в возрасте до 65 лет. Есть все основания подозревать, что в тех случаях, когда коронарная болезнь сердца развивается у женщин 45-55 лет, она развивается достаточно рано, "преждевременно". Наряду с классическими факторами определенную роль в "преждевременной" болезни играют и какие-то, пока еще "нетрадиционные" факторы риска [9].
Таким "нетрадиционным" фактором риска, по нашему мнению, является необеспечение венозного возврата, то бишь циркуляции крови [8] как в самом миокарде, так и в других органах и тканях организма. Это приводит к увеличению вязкости крови в сотни раз (возможно до 1000 [10]), что также сильно сказывается на кровоток в отдельных участках тела, на кровообращение в целом, т.к. в этом случае кровь (застойная ее часть, например) из жидкости превращается в кашицеобразную массу, из которой могут образовываться бляшки, могут образовываться пролежни, она может прорастать соединительной тканью, могут прирастать к стенкам сосудов, а при ее распаде могут образовываться тромбы. Своего рода "микропролежни" могут образовываться по всему телу – там, где длительно отсутствует циркуляция крови. Тромбы – в крупных венах, главным образом ног.
Частота тромбоза коронарных артерий, выявляемого при инфаркте миокарда, варьирует по данным разных авторов, от 30 до 92%, но его роль как непосредственной причины инфаркта миокарда оценивается по-разному, т.к. не исключено, что в ряде случаев тромбоз по отношению к инфаркту миокарда развивается вторично [4].
Сердце расположено у большинства людей практически по оси симметрии человека, что усложняет кровообращение в миокарде, т.к. при любом положении тела часть миокарда остается в неблагоприятной зоне, с неполноценным венозным возвратом, И достаточно всего лишь не произвести смену положения своевременно (на что никогда не обращалось внимания), чтобы не избежать застоя крови в отдельных участках миокарда со всеми вытекающими из этого последствиями – местное увеличение вязкости крови, трансформация эпителиальных клеток коронарных артерий, образование и налипание бляшек, образования микроинфарктов и инфарктов. Так что необеспечение венозного возврата в равной степени может наблюдаться как в БКК и МКК, так и в СКК. Все это чревато образованием обширных сгустков крови в венах и даже пролежней в отдельных участках тела. Особенно опасно образование обширных сгустков крови в крупных венах ног, чему способствует характер работы многих людей.
Характерно для фактора "смены положения тела" имеющая место смена ишемии миокарда периодом возобновления коронарного кровотока в ранее ишимизированной зоне сердца, что говорит о не необратимости этого процесса. Характерно также, что все перечисленные факторы риска для инфаркта миокарда в равной степени распространяются на инфаркты почек, селезенки, мозга, легких и др.
Однако, как уже отмечалось, самым распространенной причиной возникновения инфаркта миокарда является окклюзия магистральных венечных артерий, которая наблюдается у всех больных крупноочаговым инфарктом миокарда [3,4]. При этом причина возникновения тромбоза не имеет однозначного толкования.
Согласно НТК сгустки крови могут образовываться по тем же причинам во всех органах, железах и тканях, прежде всего в венозной их части. При нормализации кровообращения в данной зоне (по причине смены положения, физической нагрузке и т.д.) кровяной сгусток разрушается и его части транспортируется с потоком крови. Окклюзия происходит в ветвящейся части венечных артерий или в артериях, подверженных атеросклерозу. Как видим, коронарные артерии удовлетворяют обоим этим требованиям. Более того, сгустки крови, по мере удаления от места их возникновения (чаще всего в ножных венах), все более и более разрушаются в потоке крови и сокращаются в объеме, а коронарные артерии – в самом начале движения крови от сердца и они имеют сечение во много раз меньше артерий и поэтому опасными становятся более мелкие тромбы, которых, кстати, гораздо больше, чем крупных.
Самый легкий и невинный способ получить инфаркт миокарда или отек легких – длительное нахождение тела в неподвижном состоянии (ни рукой, ни ногой), без изменения положения тела достаточно длительное время. По этой причине большинство смертей наступает именно ночью, в результате длительной неподвижности истощенного больного или "здорового". Необеспечение полноценного венозного возврата, на наш взгляд, служит главнейшей первопричиной подавляющего числа инфарктов миокарда и других инфарктов, а также других заболеваний, прежде всего сердечно-сосудистых.
ПРОФИЛАКТИКА. Смена положений тела с таким расчетом, чтобы выше горизонтальной оси сердца регулярно оказывались все органы и части тела, – является обязательным требованием, чтобы избежать (предотвратить) инфаркт миокарда, и инфаркты других органов.
Как показано, насчитывается более двух дюжин факторов, способствующих нормализации венозного возврата и любой из них может послужить причиной отрыва тромба, при его наличии. Но при регулярном их выполнении эти же факторы предотвращают застойные явления и образования тромбов в органах, железах, тканях. Основными из них и как уже было сказано, доступными для собственного человеческого воздействия факторами, обеспечивающими венозный возврат, являются – физические нагрузки и упражнения, регулярные периодические изменения положения тела, растирание и разминание тела, смех, хохот, крик, пение. Отсюда столь полезны и целебны всевозможные физические нагрузки, движения, массаж и самомассаж, особенно, если выполняются они ежедневно и регулярнов течение дня. Особенно это важно в период депрессии, после стресса. Как нетрудно убедиться, при одновременном воздействии двух или нескольких "факторов риска" – возрастает опасность инфарктов. Вероятно поэтому Природа заложила потребность в движении при срессах, обидах, ссорах (стучать кулаком, махать руками, кричать, ходить из угла в угол и т.д.). Вспомним, как благотворно действует на подчиненных в Японии, когда он в гневе "отведет душу" на чучеле своего начальника. Считалось, что это психологическая разгрузка. Однако, помимо этого, при одновременном воздействии двух или нескольких факторов, обеспечивающих венозный возврат, создаются условия наименьшего риска возникновения инфаркта миокарда и других инфарктов – много движения не бывает.
Вот почему так опасно находиться, к примеру, только в вертикальном, только в горизонтальном – в любом другом положении – длительно и неподвижно. Создаются самые благоприятные условия не только для инфаркта миокарда, но и для отека легких (лежа на спине), инфаркта других органов.
Физические упражнения, обеспечивающие венозный возврат в организме (кроме указанных выше), следует дополнить специальными для сердца: это т.н."шнурки", "полумостик" – приподять таз, "полустойка" у стены. Любое из них необходимо выполнить хотя бы пару раз в день повторяя по 2-3 раза.
Ишимическая болезнь сердца (ИБС) – сердечно-сосудистое заболевание, характеризующееся нарушением коронарного кровообращения и ишимий миокарда. Формы ИБС: стенокардия, инфаркт миокарда, кардиосклероз и др. Ишимия – по определению ЭСМТ – уменьшение кровоснабжения участка тела, органа или ткани вследствие ослабления или прекращения притока артериальной крови.
Смерть американцев с искусственным сердцем – не случайность, а закономерность. Можно создать искусственный аппарат-насос. Но нельзя создать аппарат, способный гибко воспринимать и адекватно реагировать на сигналы ЦНС, рецепторов всех органов, желез, сосудов и капилляров, давать соответствующие команды. Да и в искусственном сердце вообще нет никакой необходимости: сердечно-сосудистые заболевания исчезнут навсегда – достаточно устранить грубейшие, очевидннейшие ошибки в существующей теории кровообращения.
Стенокардия (грудная жаба) – форма ИБС, приступы сжимающих, давящих болей в центре или в левой половине грудной клетки с иррадиацией в левую руку, чувством страха, слабостью. Приступы наступают при физ нагрузке, волнении, реже – в покое, длятся обычно несколько минут. Первая помощь валидол, горчичники на грудину и др. Мы предлагаем растирание грудины каждый час (можно чаще) по одной минуте.
Инсульт – вызванное патологическим процессом острое нарушение кровообращения в головном или спинном мозге с развитием стойких симптомов поражения ЦНС. Различают:
Инсульт геморрогический (апоплексический удар) – инсульт, обусловленный кровоизлиянием в головной мозг или под его оболочки. Профилактика: то же, что для атеросклероза и инфарктов.
Ишемический инсульт – инсульт, обусловленный прекращением или значительным уменьшением кровоснабжения участка мозга. Профилактика: то же, что для атеросклероза и инфарктов.
Инсульт тромбический – инсульт, обусловленный закупоркой сосуда мозга тромбом. Профилактика: то же, что для атеросклероза и инфарктов.
Инсульт эмболический – инсульт, обусловленный закупоркой сосуда мозга эмболом ЭСМТ, с 331. Профилактика: то же, что для атеросклероза и инфарктов.
Мы пока выдвигаем гипотезу: наряду с БКК, МКК, СКК в голове также имеется свой круг кровоображения.
Ни в коем случае нельзя лежать на спине без подушки длительное время. Следить, чтобы голова была всегда выше горизонтальной оси сердца. Недопускать запоров и чрезмерного напряжения при дефикации. Остальное – вполне достаточным является регулярное выполнение системы ГОЛФИ. Даже при постельном режиме – возможно чаще менять положение различных участков тела относительно горизонтальной оси, проходящей через всасывающие клапаны предсердий сердца. Стараться совершать движения руками и ногами, разговаривать, по возможности смеяться и т.д.
Самый простой и доступный способ поддержания полноценного венозного возврата даже при постельном режиме – возможно чаще менять положение различных участков тела относительно горизонтальной оси, проходящей через всасывающие клапаны предсердий сердца. Стараться совершать движения руками и ногами, разговаривать, по возможности смеяться, растирать и разминать все участки тела и т.д.
Часто в медицине изначально заложено ошибочное представлении об ишимии: принимается во внимание только фактор “кровоснабжение” и игнорируются факторы поддержания полноценного венозного возврата и качества крови. В этом, как в зеркале, отражается вся ошибочность представлений медиков и медицины о кровообращении. Отсюда все ошибки и невозможность как понять причины возникновения болезней так и излечить их. Вошедшая в моду чистка крови – тоже бесперспективное занятие. Она необходима при каках-то экстремальных ситуациях, но для профилактики абсолютно бесполезна, т.к. в следующую секунду после ее окончания начинается накопление шлаков.
Лучшее средство от инфаркта – это мытье пола с тяпкой в руках. Однако такой способ давно сошел на нет, чем человек гордится. А надо ли? Инстикнктивно сознавая потребность, мой товарищ по палате в больнице N 15 Э.Н.Островский – задого до моих "открытий" просил персонал больницы разрешения мыть пол на этаже и чувствовал себя отлично при наличии лишь одого легкого. Моет регулярно пол он и в квартире. Кстати, вменяя такую обязанность членам семьи, особенно детям, как это делают наши ташкенстские друзья, достигается хорошая воспитательная практика.
Инфаркт миокарда — это ограниченный некроз сердечной мышцы. Некрозы в большинстве случаев коронарогенные или ишемические. Реже встречаются некрозы без коронарного повреждения: при стрессе — глюкокортикоиды и катехоламины резко повышают потребность миокарда в кислороде; при некоторых эндокринных нарушениях; при нарушениях электролитного баланса. Сейчас инфаркт миокарда рассматривается только как ишемический некроз, т.е. как повреждение миокарда вследствие ишемии, обусловленной окклюзией коронарных артерий. Самая частая причина — тромб, реже — эмбол. Возможен также инфаркт миокарда при длительном спазме коронарных артерий.
Тромбоз чаще всего наблюдается на фоне атеросклеротического повреждения венечных артерий. При наличии атероматозных бляшек происходит завихрение потока крови. Кроме того, вследствие нарушенного липидного обмена при атеросклерозе увеличивается свертываемость крови, что отчасти связано также со снижением активности тучных клеток, вырабатывающих гепарин. Повышенная свертываемость крови + завихрения способствуют образованию тромбов. Кроме того, к образованию тромбов может вести распад атероматозных бляшек, кровоизлияния в них. Примерно в 1% случаев инфаркт миокарда развивается на фоне коллагенеза, сифилитического поражения артерий, при расслаивающейся аневризме аорты. Выделяют предрасполагающие факторы: сильное психоэмоциональное перенапряжение, инфекции, резкие изменения погоды. Инфаркт миокарда — очень распространенное заболевание, является самой частой причиной внезапной смерти. Проблема инфаркта до конца не решена, смертность от него продолжает увеличиваться. Сейчас все чаще инфаркт миокарда встречается в молодом возрасте. В возрасте от 35 до 5О лет инфаркт миокарда встречается в 5О раз чаще у мужчин, чем у женщин. У 6О-8О% больных инфаркт миокарда развивается не внезапно, а имеет место прединфарктный (продромальный) синдром, который встречается в трех вариантах: 1) стенокардия в первый раз, с быстрым течением — самый частый вариант; 2) стенокардия протекает спокойно, но вдруг переходит в нестабильную — возникает при других ситуациях, не стало полного снятия болей;
3) приступы острой коронарной недостаточности;
4) стенокардия Принцметалла. Клиника инфаркта Миокарда: Заболевание протекает циклически, необходимо учитывать период болезни. Чаще всего инфаркт миокарда начинается с нарастающих болей за грудиной, нередко носящих пульсирующий характер. Характерна обширная иррадиация болей — в руки, спину, живот, голову и т.д. Больные беспокойны, тревожны, иногда отмечают чувство страха смерти. Часто присутствуют признаки сердечной и сосудистой недостаточности — холодные конечности, липкий пот и др. Болевой синдром длительный, не снимается нитроглицерином. Возникают различные расстройства ритма сердца, падение АД.
Указанные выше признаки характерны для 1 периода — болевого
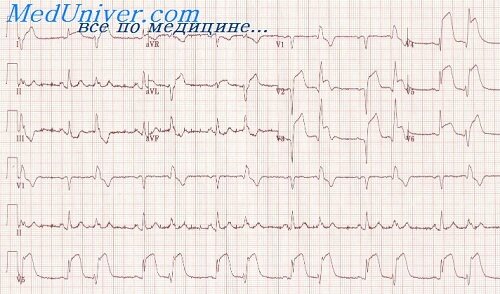
или ишемического. Длительность 1 периода от нескольких часов до 2-х суток. Объективно в этот период можно найти: увеличение АД (затем снижение); увеличение частоты сердечных сокращений; при аускультации иногда слышен патологический 4-й тон; биохимических изменений крови практически нет, характерные признаки на ЭКГ.
2-й период — острый (лихорадочный, воспалительный), характеризуется возникновением некроза сердечной мышцы на месте ишемии. Появляются признаки асептического воспаления, начинают всасываться продукты гидролиза некротизированных масс. Боли, как правило. проходят. Длительность острого периода до 2-х недель. Самочувствие больного постепенно улучшается, но сохраняется общая слабость, недомогание, тахикардия. Тоны сердца глухие. Повышение температуры тела, обусловленное воспалительным процессом в миокарде, обычно небольшое, до 38оС, появляется обычно на 3-й день заболевания. К концу первой недели температура, как правило, нормализуется. При исследовании крови во 2-м периоде находят: лейкоцитоз, возникает к концу 1-х суток, умеренный, нейтрофильный (1О-15 тыс.) со сдвигом до палочек: эозинофилы отсутствуют или эозинопения; постепенное ускорение СОЭ с 3-5 дня заболевания, максимум ко 2-й неделе, к концу 1-го месяца приходит к норме; появляется С-реактивный белок, который сохраняется до 4 недели; повышается активность трансминазы, особенно ГЩУ — через 5-6 часов и держится 3-5-7 дней, достигая 5О ЕД. В меньшей степени увеличивается глутаминовая трансминаза. Повышается также активность лактатдегидрогеназы (5О ЕД), которая возвращается к норме на 1О сутки. Исследования последних лет показали, что более специфичной по отношению к миокарду является креатинфосфокиназа, ее активность повышается при инфаркте миокарда до 4-х ЕД на 1 мл и сохраняется на высоком уровне 3-5 дней. Считается, что существует прямая пропорциональная зависимость между уровнем креатинфосфокиназы и протяженностью зоны очага некроза сердечной мышцы. На ЭКГ ярко представлены признаки инфаркта миокарда. а) при проникающем инфаркте миокарда (т.е. зона некроза распространяется от перикарда до эндокарда): смещение сегмента ST выше изолинии, форма выпуклая кверху — это первый признак проникающего инфаркта миокарда; слияние зубца Т с сегментами ST на 1-3 день; глубокий и широкий зубец Q — основной, главный признак; уменьшение величины зубца R, иногда форма QS; характерные дискордантные изменения — противоположные смещения ST и Т (например, в 1 и 2 стандартном отведениях по сравнению с 3 стандартным отведением); в среднем с 3-го дня наблюдается характерная обратная динамика изменений ЭКГ: сегмент ST приближается к изолинии, появляется равномерный глубокий Т. Зубец Q также претерпевает обратную динамику, но измененный Q и глубокий Т могут сохраняться на всю жизнь. б) при интрамуральном инфаркте миокарда: нет глубокого зубца Q, смещение сегмента ST может быть не только вверх, но и вниз. Для правильной оценки важно повторное снятие ЭКГ. Хотя ЭКГ-признаки очень помогают диагностике, диагноз должен опираться на все признаки (в критерии) диагностики инфаркта миокарда:
1. Клинические признаки.
2. Электрокардиографические признаки.
3. Биохимические признаки.
3 период (подострый или период рубцевания) длится 4-6 недель. Характерным для него является нормализация показателей крови (ферментов), нормализуется температура тела и исчезают все другие признаки острого процесса: изменяется ЭКГ, на месте некроза развивается соединительно-тканный рубец. Субъективно больной чувствует себя здоровым.
4. период (период реабилитации, восстановительный) — длится от 6-ти месяцев до 1 года. Клинически никаких признаков нет. В этот период происходит компенсаторная гипертрофия интактных мышечных волокон миокарда, развиваются другие компенсаторные механизмы. Происходит постепенное восстановление функции миокарда. Но на ЭКГ сохраняется патологический зубец Q.
АТИПИЧНЫЕ ФОРМЫ ТЕЧЕНИЯ ИНФАРКТА МИОКАРДА
1. Абдоминальная форма. Протекает по типу патологии ЖКТ с болями в подложечной области, в животе, с тошнотой, рвотой. Чаще всего гастралгическая форма (абдоминальная) инфаркта миокарда встречается при инфаркте задней стенки левого желудочка. В целом вариант редкий. ЭКГ отведения II, III, AVL.
2. Астматическая форма: начинается с сердечной астмы и провоцирует отек легких как исход. Боли могут отсутствовать. Астматическая форма встречается чаще у пожилых людей с кардиосклерозом или при повторном инфаркте, или при очень обширных инфарктах.
3. Мозговая форма: на первом плане симптомы нарушения мозгового кровообращения по типу инсульта с потерей сознания, встречается чаще у пожилых людей со склерозом сосудов головного мозга.
4. Немая или безболевая форма иногда является случайной находкой при диспансеризации. Из клинических проявлений: вдруг стало «дурно», возникла резкая слабость, липкий пот, затем все, кроме слабости, проходит. Такая ситуация характерна для инфаркта в пожилом возрасте и при повторных инфарктах миокарда.
5. Аритмическая форма: главный признак пароксизмальная тахикардия, болевой синдром может отсутствовать.
6. Тромбоэмболическая.
Инфаркт миокарда очень тяжелое заболевание с частым летальным исходом, особенно часты осложнения в I и II периодах.
Осложнения инфаркта Миокарда:
I период
1. Нарушения ритма сердца, особенно опасны все желудочковые аритмии (желудочковая форма пароксизмальной тахикардии, политропные желудочковые экстрасистолии и т.д.) Это может привести к фибрилляции желудочков (клиническая смерть), к остановке сердца. При этом необходимы срочные реабилитационные мероприятия, фибрилляция желудочков может произойти и в прединфарктный период.
2. Нарушения атриовентрикулярной проводимости: например, по типу истинной электро-механической диссоциации. Чаще возникает при передне- и заднеперегородочных формах инфаркта миокарда.
3. Острая левожелудочковая недостаточность: отек легких, сердечная астма.
4. Кардиогенный шок:
а) Рефлекторный — происходит падение АД, больной вялый, заторможенный, кожа с сероватым оттенком, холодный профузный пот. Причина — болевое раздражение.
б) Аритмический — на фоне нарушения ритма.
в) Истинный — самый неблагоприятный, летальность при нем достигает 9О%. В основе истинного кардиогенного шока лежит резкое нарушение сократительной способности миокарда при обширных его повреждениях, что приводит к резкому уменьшению сердечногог выброса, минутный объем падает до 2,5 л/мин. Чтобы сдержать падение АД, компенсаторно происходит спазм периферических сосудов, однако он недочтаточен для поддержания микроциркуляции и нормального уровня АД. Резко замедляется кровоток на периферии, образуеются микротромбы (при инфаркте миокарда повышена свертываемость + замедленный кровоток). Следствием микротромбообразования является капилляростаз, появляются открытые артериовенозные шунты, начинают страдать обменные процессы, происходит накопление в крови и в тканях недоокисленных продуктов, которые резко увеличивают проницаемость капилляров. Начинается пропотевание жидкой части плазмы крови вследствие тканевого ацидоза. Это приводит к уменьшению ОЦК, уменьшается венозный возврат к сердцу, минутный объем падает еще больше — замыкается порочный круг. В крови наблюдается ацидоз, который еще больше ухудшает работу сердца. Клиника истинного шока: Слабость, заторможенность — практически ступор. АД падает до 8О мм рт.ст. и ниже, но не всегда так четко. Пульсовое давление обязательно меньше 25 мм рт.ст. Кожа холодная, землисто-серая, иногда пятнистая, влажная вследствие капилляростаза. Пульс нитевидный, часто аритмичный. Резко падает диурез, вплоть до анурии.
5. Нарушения ЖКТ: парез желудка и кишечника чаще при кардиогенном шоке, желудочное кровотечение. Связаны с увеличением количества глюкокортикоидов.
II период
Возможны все 5 предыдущих осложнений + собственно осложнения II периода.
1. Перикардит: возникает при развитии некроза на перикарде, обычно на 2-3 день от начала заболевания. Усиливаются или вновь появляются боли за грудиной, постоянные, пульсирующие, на вдохе боль усиливается, меняется при изменении положения тела и при движении. Одновременно появляется шум трения перикарда.
2. Пристеночный тромбоэндокардит: возникает при трансмуральном инфаркте с вовлечением в некротический процесс эндокарда. Длительно сохраняются признаки воспаления или появляются вновь после некоторого спокойного периода. Основным исходом данного состояния является тромбоэмболия в сосуды головного мозга, конечности и в другие сосуды большого круга кровообращения. Диагностируется при вентрикулографии, сканировании.
3. Разрывы миокарда, наружные и внутренние.
а) Наружный, с тампонадой перикарда. Обычно имеет париод предвестников: рецидивирующие боли, не поддающиеся анальгетикам. Сам разрыв сопровождается сильнейшей болью, и через несколько секунд больной теряет сознание. Сопровождается резчайшим цианозом. Если больной не погибает в момент разрыва, развивается тяжелый кардиогенный шок, связанный с тампонадой сердца. Длительность жизни с момента разрыва исчисляется минутами, в некоторых случаях часами. В исключительно редких случаях прикрытой перфорации (кровоизлияние в осумкованный участок полости перикарда), больные живут несколько дней и даже месяцев.
б) Внутренний разрыв — отрыв папиллярной мышцы, чаще всего бывает при инфаркте задней стенки. Отрыв мышцы приводит к острой клапанной недостаточности (митральной). Резчайшая боль и кардиогенный шок. Развивается острая левожелудочковая недостаточность (отек легких), границы сердца резко увеличены влево. Характерен грубый систолический шум с эпицентром на верхушке сердца, проводящийся в подмышечную область. На верхушке часто удается обнаружить и систолическое дрожание. На ФКГ лентообразный шум между I и II тонами. Часто наступает смерть от острой левожелудочковой недостаточности. Необходимо срочное оперативное вмешательство.
в) Внутренний разрыв межпредсердной перегородки встречается редко. Внезапный коллапс, вслед за которым быстро нарастают явления острой левожелудочковой недостаточности.
г) Внутренний разрыв межжелудочковой перегородки: внезапный коллапс, одышка, цианоз, увеличение сердца вправо, увеличение печени, набухание шейных вен, грубый систолический шум над грудиной + систолическое дрожание + диастолический шум — признаки острой застойной правожелудочковой недостаточности. Нередки нарушенияы ритма сердца и проводимости (полная поперечная блокада). Часты летальные исходы.
4. Острая аневризма сердца: по клиническим проявлениям соответствует той или иной степени острой сердечной недостаточности. Наиболее частая локализация постинфарктных аневризм — левый желудочек, его передняя стенка и верхушка. Развитию аневризмы способствуют глубокий и протяженный инфаркт миокарда, повторный инфаркт миокарда, артериальная гипертония, сердечная недостаточность. Острая аневризма сердца возникает при трансмуральном инфаркте миокарда в период миомаляции. Признаки: нарастающая левожелудочковая недостаточность, увеличение границ сердца и его объема; надверхушечная пульсация или симптом коромысла (надверхушечная пульсация + верхушечный толчок), если аневризма формируется на передней стенке сердца; протодиастолический ритм галопа, добавочный III тон; систолический шум, иногда шум «волчка»; несоответствие между сильной пульсацией сердца и слабым наполнением пульса; на ЭКГ нет зубца Р, появляется широкий Q, отрицательный зубец Т — то есть сохраняются ранние призхнаки инфаркта миокарда. Наиболее достоверна вентрикулография. Лечение оперативное. Аневризма часто приводит к разрыву, смерти от острой сердечной недостаточности, может перейти в хроническую аневризму.
III период
1. Хроническая аневризма сердца возникает в результате растяжения постинфарктного рубца. Появляются или долго сохраняются признаки воспаления. Увеличение размеров сердца, надверхушечная пульсация. Аускультативно двойной систолический или диастолический шум — систоло-диастолический шум. На ЭКГ застывшая форма кривой острой фазы. Помогает нерентгенологическое исследование.
2. Синдром Дресслера или постинфарктный синдром. Связан с сенсибилизацией организма продуктами аутолиза некротизированных масс, которые в данном случае выступают в роли аутоантигенов. Осложнение появляется не раньше 2-6 недели от начала заболевания, что доказывает аллергический механизм его возникновения. Возникают генерализованные поражения серозных оболочек (полисерозиты), иногда вовлекаются синовиальные оболочки. Клинически это перикардит, плеврит, поражение суставов, чаще всего левого плечевого сустава. Перикардит возникает вначале как сухой, затем переходит в экссудативный. Характерны боли за грудиной, в боку (связаны с поражением перикарда и плевры). Подъем температуры до 4ОоС. лихорадка часто носит волнообразный характер, Болезненность и припухлость в грудинно-реберных и грудинно-ключичных сочленениях. Часто ускоренное СОЭ, лейкоцитоз, эозинофилия. Объективно признаки перикардита, плеврита. Угрозы для жизни больного данное осложнение не представляет. Может также протекать в редуцированной форме, в таких случаях иногда трудно дифференцировать с-м Дресслера с повторным инфарктом миокарда. При назначении глюкокортикоидов симптомы быстро исчезают.
3. Тромбоэмболические осложнения: чаще в малом кругу кровообращения. Эмболы при этом в легочную артерию попадают из вен при тромбофлебите нижних конечностей, вен таза. Осложнение возникает, когда больные начинают лдвигаться после длительного постельного режима. Проявления тромбоэмболии легочной артерии: коллапс, легочная гипертензия с акцентом II тона над легочной артерией, тахикардия, перегрузка правого сердца, блокада правой ножки пучка Гисса. Рентгенологически выявляются признаки инфаркт-пневмонии. Необходимо провести ангиопульмонографию, так как для своевременного хирургического лечения необходим точный топический диагноз. Профилактика заключается в активном ведении больного.
4. Постинфарктная стенокардия. О ней говорят в том случае, если до инфаркта приступов стенокардии не было, а впервые возникли после перенесенного инфаркта миокарда. Она делает прогноз более серьезным.
IV период
Осложнения периода реабилитации относятся к осложнениям ИБС. Кардиосклероз постинфарктный. Это уже исход инфаркта миокарда, связанный с формированием рубца. Иногда его еще называют ишемической кардиопатией. Основные проявления: нарушения ритма, проводимости, сократительной способности миокарда. Наиболее частая локализация — верхушка и передняя стенка.
Дифференциальная диагностика инфаркта Миокарда:
1. Стенокардия. При инфаркте боли носят нарастающий характер, большей интенсивности, больные возбуждены, беспокойны, а при стенокардии — заторможены. При инфаркте нет эффекта от нитроглицерина, боли длительные, иногда часами; при стенокардии четкая иррадиация болей, при инфаркте — обширная. Наличие сердечно-сосудистой недостаточности более свойственно инфаркту миокарда. Окончательная диагностика — по ЭКГ.
2. Острая коронарная недостаточность. Это — затянувшийся приступ стенокардии с явлениями очаговой дистрофии миокарда. то есть промежуточная форма. Длительность болей от 15 мин до 1 часа, не более: эффекта от нитроглицерина тоже нет. Изменения ЭКГ характеризуются смещением сегмента ST ниже изолинии, появляется отрицательный зубец Т. В отличие от стенокардии, после окончания приступа изменения ЭКГ остаются, а в отличие от инфаркта миокарда изменения держатся только 1-3 дня и полностью обратимы. Нет повышения активности фермсентов, так как нет некроза.
3. Перикардит. Болевой синдром весьма сходен с таковым при инфаркте миокарда. Боль длительная, постоянная, пульсирующая, но нет нарастающего, волнообразного характера боли. Нет предвестников (нестабильной стенокардии). Боли четко связаны с дыханием и положением тела. Признаки воспаления: повышение температуры, лейкоцитоз. Появляются не после начала болей, а предшествуют, или появляются вместе с ними. Шум трения перикарда долго сохраняется. На ЭКГ смещение сегмента ST выше изолинии, как и при инфаркте миокарда, но нет дискордантности и патологического зубца Q — главного признака инфаркта миокарда; подъем сегмента ST происходит практически во всех отведениях, так как изменения в сердце носят диффузный характер, а не очаговый, как при инфаркте. При перикардите при возвращении сегмента ST на изолинию зубец Т остается положительным, при инфаркте — отрицательным.
4. Эмболия ствола легочной артерии (как самостоятельное заболевание, а не осложнение инфаркта миокарда). Возникает остро, резко ухудшается состояние больного. Острые загрудинные боли, охватывающие всю грудную клетку, на первый план выступает дыхательная недостаточность: приступ удушья, диффузный цианоз. Причиной эмболии бывают мерцательная аритмия, тромбофлебит, оперативные вмешательства на органах малого таза и др. Чаще наблюдается эмболия правой легочной артерии, поэтому боли больше отдают вправо, а не влево. Признаки острой сердечной недостаточности по правожелудочковому типу: одышка, цианоз, увеличение печени. Акцент II тона на легочной артерии, иногда набухание шейных вен. ЭКГ напоминает инфаркт в правых I и II грудных отведениях, есть признаки перегрузки правого сердца, может быть блокада ножки пучка Гисса. Изменения исчезают через 2-3 дня. Эмболия часто приводит к инфаркту легкого: хрипы, шум трения плевры, признаки воспаления, реже наблюдается кровохарканье. Рентгенологически изменения клиновидной формы, чаще справа внизу.
5. Расслаивающаяся аневризма аорты. Чаще всего возникает у больных с высокой артериальной гипертензией. Нет периода предвестников, боль сразу же носит острый характер, кинжальная. Характерен мигрирующий характер болей: по мере расслаивания боли распространяются вниз в поясничную область, в нижние конечности. В процесс начинают вовлекаться другие артерии — возникают симптомы окклюзии крупных артерий, отходящих от аорты. Отсутствует пульс на лучевой артерии, может наблюдаться слепрота. На ЭКГ нет признаков инфаркта. Боли атипичные, не снимаются наркотиками.
6. Печеночная колика. Необходимо дифференцировать с абдоминальной формой инфаркта миокарда. Чаще у женщин, есть четкая связь с приемом пищи, боли не носят нарастающего волнообразного характера, иррадиируют вправо вверх. Часто повторная рвота. Локальная болезненность, однако это бывает и при инфаркте миокарда вследствие увеличения печени. Помогает ЭКГ. Повышена активность ЛДГ 5, а при инфаркте — ЛДГ 1.
7. Острый панкреатит. Тесная связь с едой: прием жирной пищи, сладкого, алкоголя. Опоясывающие боли, повышена активность ЛДГ 5. Повторная, часто неукротимая рвота. Помогает определение активности ферментов (амилаза мочи), ЭКГ.
8. Прободная язва желудка. На рентгенограмме воздух в брюшной полости (серп над печенью).
9. Острый плеврит. Связь болей с дыханием, шум трения плевры.
1О. Острые корешковые боли (рак, туберкулез позвоночника, радикулит). Боли связаны с изменением положения тела.
11. Спонтанный пневмоторакс. Признаки дыхательной недостаточности, коробочный перкуторый звук, отсутствие дыхания при аускультации (не всегда).
12. Диафрагмальная грыжа. Сопутствует пептический эзофагит. Боли связаны с положением тела, больше в горизонтальном положении тела, срыгивание, чувство жжения, усиленная саливация. Боли появляются после приема пищи. Тошнота, рвота.
13. Крупозная пневмония. В случае захвата в патологический процесс медиастенальной плевры боли могут быть за грудиной. Высокая лихорадка, данные со стороны легких.
Формулировка диагноза
1. ИБС. 2. Атеросклероз коронарных артерий. 3. Инфаркт миокарда с указанием даты (от. ) и локализация патологического процесса (какой стенки). 4. Осложнения.
Лечение инфаркта Миокарда
Две задачи: 1. Профилактика осложнений. 2. Ограничение зоны инфаркта. Необходимо, чтобы лечебная практика соответствовала периоду заболевания.
1. Предынфарктный период. Главная цель лечения в этот период — предупредить возникновение инфаркта миокарда: — постельный режим (до тех пор, пока есть признаки нарастания коронарной недостаточности); — прямые антикоагулянты: — гепарин, можно вводить в/в, но чаще применяют п/к по 5-1О тыс. ЕД через каждые 4-6 часов. — антиаритмические средства: поляризующая смесь. Если — глюкоза 5% 2ОО-5ОО мл у больного сахарный диа- — хлорид калия 1О% — 3О,О бет, то глюкозу заменить — сульфат магния 25% — 2О,О физраствором. — инсулин 4-12 ЕД — кокарбоксилаза 1ОО мг — бета-адреноблокаторы /Anaprillini О,О4; — нитраты пролонгированного действия (Sustak-forte). иногда проводят экстренную реваскуляризацию миокарда.
2. Острейший период. Основная цель лечения — ограничить зону повреждения миокарда. Снятие болевого синдрома: начинать правильнее с нейролептанальгезии, а не с наркотиков, т.к. при этом меньше осложнений; фентанил 1-2 мл в/в на глюкозе /О,ОО5% 2 мл; дроперидол 2,О мл О,25% 2 мл на 4О мл 5% р-ра глюкозы; таламонал (содержит в 1 мл О,О5 мг фентанила и 2,5 мг дроперидола) 2-4 мл в/в струйно. Аналгетический эффект наступает немедленно после в/в введения (у 6О% больных) и сохраняется 3О мин. Фентанил, в отличие от опиатов, очень редко угнетает дыхательный центр. После нейролептанальгезии сознание быстро восстанавливается. Не нарушается кишечная перистальтика и мочеотделение. Нельзя сочетать с опиатами и барбирутатами, т.к. возможно потенцирование пробочных эффектов При неполном эффекте повторно вводят через 6О мин. морфин 1% 1,5 п/к или в/в струйно; омнопон 2% — 1,О п/к или в/в; промедол 1% — 1,О п/к. Побочные явления препаратов группы морфина: а) угнетение дыхательного центра — налорфин 1-2 мл в/в. б) снижение рН крови и индуцирование синдрома электрической нестабильности сердца; в) способствует депонированию крови, снижению венозного возврата, приводя к относительной гиповолении; г) мощное ваготропное действие — усугубляется брадикардия, может быть тошнота, рвота, угнетение перистальтики кишечника и парез мускулатуры мочевого пузыря. В связи с возможностью указанных осложнений применение морфинов и его аналогов при инфаркте миокарда должно быть сведено к минимуму. Закисно-кислородная аналгезия. Ее применение при инфаркте миокарда — приоритет советской медицины. Применяют по следующей схеме: а) Премедикация. Введение пипольфена, атропина, морфина, дроперидола (в том числе и на догоспитальном этапе). б) Денитрогенизация. Вентиляция легких чистым кислородом в течение 3-5 мин. в) Период аналгезии. Ингаляция закисью азота и кислородом в соотношении 2,5:1 в течение 1О мин. г) 2-й период аналгезии. Ингаляция закисью азота и кислородом в соотношении 1:1 до 5 часов. д) Выведение из наркоза. Вентиляция легких чистым кислородом в течение 1О мин. Для усиления обезболивающего эффекта, снятия тревоги, беспокойства, возбуждения: — анальгин 5О% — 2,О в/м или в/в; — димедрол 1% — 1,О в/м (седативный эффект) + аминазин 2,5% — 1,О в/м в/в (потенцирование наркотиков). Кроме того, аминазин оказывает гипотензивное действие, поэтому при нормальном или пониженном давлении вводят только димедрол. Аминазин может вызывать тахикардию. При локализации инфаркта на задней стенке левого желудочка болевой синдром сопровождается брадикардией — ввести холинолитик: атропина сульфат О,1% — 1,О (при тахикардии не вводить!). Возникновение инфаркта часто связано с тромбозом коронарных артерий, поэтому необходимо введение антикоагулянтов, которые особенно эффективны в первые минуты и часы заболевания. Они также ограничивают зону инфаркта + обезболивающий эффект. Дополнительно: гепарин 1О-15 тыс. (около 2 мл), в 1 мл — 5 тыс.ЕД; фибринолизин 6 тыс. в/в кап.; стрептаза 25О тыс. на физ. р-ре в/в кап. Гепарин вводят в течение 5-7 дней под контролем свертывающей системы крови, вводят 4-6 раз в сутки (т.к. длительность действия 6 час.), лучше в/в. Также повторно вводится фибринолизин в течение 1-2 сут. (т.е. только в течение 1-го периода). Профилактика и лечение аритмий а) Поляризующая смесь (состав см. выше), входящие в нее ингридиенты способствуют проникновению калия внутрь клеток. б) Лидокаин — препарат выбора, более эффективен при желудочковых аритмиях. 5О-75 мг струйно. в) Новокаинамид 1ОО мг в/в струйно, через 5 мин. до достижения эффекта, далее капельно (1О% р-р 5 мл). г) Обзидан до 5 мг в/в медленно (О,1% р-р 1 мл). д) Хинидин по О,2-О,5 через 6 час. внутрь. Применяют также нитраты пролонгированного действия — вследствие коронарооасширяющего действия они улучшают коллатеральное кровообращение и тем самым ограничивают зону инфаркта. Препараты: Нитросорбит таб. О.О1; Эринит таб. О,О1; Сустак митте 2,6 мг и сустак форте 6,4 мг.
III Острый период инфаркта миокарда.
Цель лечения в острый период — предупреждение осложнений. При неосложненном инфаркте миокарда со 2-3 дня начинают ЛФК. Отменяют фибринолизин (на 1-2 день), но гепарин оставляют до 5-7 дней под контролем времени свертывания. За 2-3 дня до отмены гепарина назначают антикоагулянты непрямого действия; при этом обязателен контроль протромбина 2 раза в неделю, рекомендуется снижать протромбин до 5О%. Исследуется моча на эритроциты (микрогематурия). Фенилин (список А) О,О3 по 3 раза в день, отличается от других препаратов быстрым эффектом: 8 часов. Неодикумарин таб.О,О5 в 1 день по 4 т. 3 раза, на 2-й день 3 т. 3 раза и далее по О,1-О,2 в сутки индивидуально. Фепромарон таб. О,ОО5 (О,ОО1) Синкумар таб. О,ОО4 (О,ОО2) Нитрофарин таб. О,ОО5 Омефин таб. О,О5 Дикумарин таб. О,О1.
Показания к назначению антикоагулянтов непрямого действия: 1) Аритмии. 2) Трансмуральный инфаркт (почти всегда есть коронаротромбоз). 3) У тучных больных. 4) На фоне сердечной недостаточности.
Противопоказания к назначению антикоагулянтов непрямого действия: 1) Геморрагические осложнения, диатезы, склонность к кровотечениям. 2) Заболевания печени (гепатит, цирроз). 3) Почечная недостаточность, гематурия. 4) Язвенная болезнь. 5) Перикардит и острая аневризма сердца. 6) Высокая артериальная гипертензия. 7) Подострый септический эндокардит. 8) Авитаминозы А и С.
Цель назначения непрямых антикоагулянтов — предупреждение повторного гиперкоагуляционного синдрома после отмены прямых антикоагулянтов и фибринолитических средств, создание гипокоагуляции с целью профилактики повторных инфарктов миокарда или рецидивов, предупреждение тромбоэмболических осложнений.
В остром периоде инфаркта миокарда наблюдаются два пика нарушения ритма — в начале и конце этого периода. Для профилактики и лечения дают антиаритмические средства: поляризующую смесь и другие препараты (см.выше). По показаниям назначают преднизолон. Применяют также анаболические средства: Ретаболил 5% 1,О в/м — улучшает ресинтез макроэргов и синтез белков, благоприятно влияет на метаболизм миокарда. Нераболил 1% 1,О Нерабол таб. О,ОО1 (О,ОО5).
С 3-го дня заболевания начинают довольно быстро расширять режим. К концу 1 недели больной должен садиться, через 2 недели ходить. Обычно через 4-6 недель больного переводят в отделение реабилитации. Еще через месяц — в специализированный кардиологический санаторий. Далее больные переводятся под амбулаторное наблюдение и лечение у кардиолога.
Диета.
В первые дни заболевания питание резко ограничивают, дают малокалорийную, легко усвояемую пищу. Не рекомендуются молоко, капуста, другие овощи и фрукты, вызывающие метеоризм. Начиная с 3 дня заболевания необходимо активно опорожнять кишечник, рекомендуются масляное слабительное или очистительные клизмы, чернослив, кефир, свекла. Солевые слабительные нельзя — из-за опасности коллапса.
IV период реабилитации.
Реабилитации различают: а) Физическая — восстановление до максимально возможного уровня функции сердечно-сосудистой системы. Необходимо добиваться адекватной реакции на физическую нагрузку, что достигается в среднем через 2-6 недель физических тренировок, которые развивают коллатеральное кровообращение. б) Психологическая — у больных, перенесших инфаркт миокарда, нередко развивается страх перед повторным инфарктом. При этом может быть оправдано применение психотропных средств. в) Социальная реабилитация — больной после перенесенного инфаркта миокарда считается нетрудоспособным 4 месяца, затем его направляют на ВТЭК. 5О% больных к этому времени возвращается к работе, то есть трудоспособность практически полностью восстанавливается. Если возникают осложнения, то временно устанавливается группа инвалидности, обычно II, на 6-12 месяцев.
Лечение осложненного инфаркта миокарда
I. Кардиогенный шок. а) Рефлекторный (связан с болевым синдромом). Необходимо повторное введение анальгетиков: Морфин 1% 1,5 мл п/к или в/в струйно. Анальгин 5О% 2 мл в/м, в/в. Таломонал 2-4 мл в/в струйно. Сосудотонизирующие средства: Кордиамин 1-4 мл в/в (фл. по 1О мл); Мезатон 1% 1,О п/к, в/в, на физ.растворе; Норадреналин О,2% 1,О в/в; Ангиотензинамид 1 мг в/в капельно.
б) Истинный кардиогенный шок. Повышение сократительной деятельности миокарда: Строфантин О,О5% О,5-О,75 в/в медленно на 2О,О изотонического раствора. Корглюкон О,О6% 1,О в/в, также на изотоническом растворе или на поляризующей смеси. Глюкагон 2-4 мг в/в капельно на поляризующем растворе. Имеет значительное преимущество перед глюкозидами: обладая, как и гликозиды, положительным инотропным действием, в отличие от них не оказывает аритмогенного действия. Может быть использован при передозировке сердечных гликозидов. Обязательно вводить на поляризующей смеси или вместе с другими препаратами калия, так как он вызывает гипокалиемию.
Нормализация АД:
Норадреналин О,2% 2-4 мл на 1 л 5% р-ра
глюкозы или изотонического раствора. АД поддерживается на уровне 1ОО мм рт.ст. Мезатон 1% 1,О в/в; кордиамин 2-4 мл; Гипертензинамид 2,5-5 мг на 25О мл 5% глюкозы в/в капельно, под обязательным контролем АД, так как обладает резко выраженным прессорным действием. При нестойком эффекте от вышеуказанных препаратов: Гидрокортизон 2ОО мг, Преднизолон 1ОО мг. Вводить на физиологическом растворе.
Нормализация реологических свойств крови (так как обязательно образуются микрососудистые тромбы, нарушается микроциркуляция). Применяют в общепринятых дозах: гепарин; фибринолизин; низкомолекулярные декстраны. Устранение гиповолемии, так как происходит пропотевание жидкой части крови: реополиглюкин, полиглюкин — в объеме до 1ОО мл со скоростью 5О,О в мин. Коррекция кислотно-щелочного равновесия (борьба с ацидозом): натрия бикарбонат 5% до 2ОО,О; натрия лактат. Повторное введение обезболивающих средств. Восстановление нарушений ритма и проводимости. Также иногда используют аортальную контрапульсацию — один из видов вспомогательного кровообращения, операцию иссечения зоны некроза в остром периоде, гипербарическую оксигенацию.
II. Атония желудка и кишечника. Связаны с введением больших доз атропина, наркотических анальгетиков и с нарушением микроциркуляции. Для ликвидации необходимы: промывание желудка через тонкий зонд с использованием раствора соды; постановка газоотводной трубки; введение в/в гипертонического раствора NaCl 1О% 1О,О; паранефральная новокаиновая блокада. Эффективен прозерин О,О5% 1,О п/к.
III. Постинфарктный синдром. Это — осложнение аутоиммунной природы, поэтому дифференциально-диагностическим и лечебным средством является назначение глюкокортикоидов, которые дают при этом отличный эффект. Преднизолон 3О мг (6 таб.), лечить до исчезновения проявлений заболевания, затем дозу очень медленно снижать в течение 6 недель — поддерживающая терапия по 1 таб. в день. При такой схеме лечения рецидивов не бывает. Также десенсибилизирующая терапия.
Реферат: Инфаркт миокарда 3
Название: Инфаркт миокарда 3
Тип: реферат Добавлен 19:31:15 10 июня 2011 Похожие работы
Просмотров: 347 Комментариев: 0 Оценило: 0 человек Средний балл: 0 Оценка: неизвестно Скачать
Инфаркт миокарда.
Инфаркт миокарда развивается в результате обтурации просвета сосуда кровоснабжающего миокард (коронарная артерия). Причинами могут стать (по частоте встречаемости):
- Атеросклероз коронарных артерий (тромбоз, обтурация бляшкой) 93-98 %
- Хирургическая обтурация (перевязка артерии или диссекция при ангиопластике)
- Эмболизация коронарной артерии (тромбоз при коагулопатии, жировая эмболия т. д.)
Отдельно выделяют инфаркт при пороках сердца (аномальное отхождение коронарных артерий от легочного ствола)
Патогенез
Различают стадии:
- Ишемии
- Повреждения (некробиоза)
- Некроза
- Рубцевания
Ишемия может являться предиктором инфаркта и длиться сколь угодно долго. При исчерпывании компенсаторных механизмов говорят о повреждении, когда страдает метаболизм и функция миокарда, однако изменения носят обратимый характер. Стадия повреждения длится от 4 до 7 часов. Некроз характеризуется необратимостью повреждения. Через 1-2 недели после инфаркта некротический участок начинает замещаться рубцовой тканью. Окончательное формирование рубца происходит через 1-2 месяца.
Клиническая картина
Основной клинический признак — интенсивная боль за грудиной (ангинозная боль). Однако болевые ощущения могут носить вариабельный характер. Пациент может жаловаться на чувство дискомфорта в груди, боли в животе, горле, руке, лопатке и т. п. Нередко заболевание имеет безболевой характер, что характерно для больных сахарным диабетом. Болевой синдром сохраняется более 15 минут и купируется через несколько часов, либо после применения наркотических анальгетиков, нитраты неэффективны. Бывает профузный пот. В 20-30 % случаев при крупноочаговых поражениях развиваются признаки сердечной недостаточности. Пациенты отмечают одышку, непродуктивный кашель. Нередко встречаются аритмии. Как правило это различные формы экстрасистолий или фибрилляция предсердий. Нередко единственным симптомом инфаркта миокарда является внезапная остановка сердца. Предрасполагающим фактором является физическая нагрузка, психоэмоциональное напряжение, состояние утомления, гипертонический криз.
Атипичные формы инфаркта миокарда
В некоторых случаях симптомы инфаркта миокарда могут носить атипичный характер. Такая клиническая картина затрудняет диагностику инфаркта миокарда. Различают следующие атипичные формы инфаркта миокарда:
- Абдоминальная форма — симптомы инфаркта представлены болями в верхней части живота, икотой, вздутием живота, тошнотой, рвотой. В данном случае симптомы инфаркта могут напоминать симптомы острого панкреатита.
- Астматическая форма — симптомы инфаркта представлены нарастающей одышкой. Симптомы инфаркта напоминают симптомы приступа бронхиальной астмы.
- Атипичный болевой синдром при инфаркте может быть представлен болями локализованными не в груди, а в руке, плече, нижней челюсти, подвздошной ямке.
- Безболезненная форма инфаркта наблюдается редко. Такое развитие инфаркта наиболее характерно для больных сахарным диабетом, у которых нарушение чувствительности является одним из проявлений болезни (диабета).
- Церебральная форма — симптомы инфаркта представлены головокружениями, нарушениями сознания, неврологическими симптомами.
Диагностика
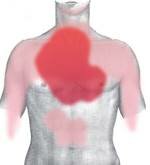
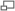
Болевые зоны при инфаркте миокарда: темно-красный = типичная область, светло-красный = другие возможные области.
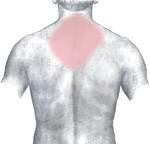
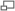
Вид со спины.
- Ранняя:
- Электрокардиография
- Эхокардиография
- Анализ крови на кардиотропные белки (MB-КФК, АсАТ, ЛДГ1. тропонин)
- Отсроченая:
- Коронарография
- Сцинтиграфия миокарда
Осложнения
ранние:
- острая сердечная недостаточность
- кардиогенный шок
- нарушения ритма и проводимости
- тромбоэмболические осложнения
- разрыв миокарда с развитием тампонады сердца
- перикардит
поздние:
- постинфарктный синдром (синдром Дресслера)
- тромбоэмболические осложнения
- хроническая сердечная недостаточность
- аневризма сердца
Лечение
Лечение на ранних этапах при возможности сводится к устранению боли, восстановлению коронарного кровотока (тромболитическая терапия, ангиопластика коронарных артерий, АКШ). При выраженной сердечной недостаточности в условиях клиники возможна постановка внутриаортальной баллонной контрпульсации.
В случае остановки сердца (в результате фибрилляции желудочков) необходимо немедленно начать сердечно-лёгочную реанимацию. Доступность автоматических наружных дефибрилляторов увеличивает выживаемость в таких ситуациях.
Устранение боли, одышки и тревоги
Если приступ ангинозной боли не ослабевает через несколько минут после прекращения физической нагрузки или он возник в покое, больной должен принять нитроглицерин в виде таблетки под язык (0,5 мг) или в виде аэрозоля (0,4 мг в дозе). Если приступ не исчезает через 5 мин, то можно принять нитроглицерин повторно. Если симптомы сохраняются в течении следующих 5 минут после повторного приёма, следует вызвать бригаду скорой медицинской помощи и принять нитроглицерин ещё раз. Если боль сохраняется на момент приезда бригады скорой медицинской помощи, врач применяет морфин. Предварительно 10 мг морфина гидрохлорида разводят в 10 мл 0,9 % раствора хлорида натрия или дистиллированной воды. Первую дозу 2-5 мг (то есть 2-5 мл раствора) вводят внутривенно струйно. Затем дополнительно вводят 2-5 мг каждые 5-15 минут до устранения боли или возникновения побочных эффектов. Также с обезболивающей целью возможно применение нейролептанальгезии — сочетание наркотического анальгетика фентанила (0,05-0,1 мг) и нейролептикадроперидола (2,5-10 мг в зависимости от уровня артериального давления). При необходимости нейролептанальгезию повторяют в более низкой дозе.
При наличии у больного артериальной гипоксемии (насыщение артериальной крови кислородом <90 %), одышки или других признаков сердечной недостаточности вводят кислород (через маску или носовой катетер) со скоростью 2-5 л/мин. Артериальную гипоксемию по возможности определяют с помощью пульсоксиметрии.
Больному с выраженным возбуждением, тревогой, страхом (которые не исчезают после введения наркотического анальгетика) можно назначить транквилизатор (например, диазепам внутривенно 2,5-10 мг). Также важно успокоить пациента и его близких.
Антитромбоцитарная терапия
Всем больным инфарктом миокарда следует принять ацетилсалициловую кислоту, предварительно разжевав, в нагрузочной первой дозе 150—300 мг. Для этих целей не подходит кишечно-растворимая форма, так как начало его действия медленное. При выраженной тошноте, рвоте, сопутствующих заболеваниях желудка возможно внутривенное введение ацетилсалициловой кислоты в дозе 250—500 мг. Далее ацетилсалициловая кислота показана таким больным пожизненно в дозе 75-150 мг/сут. При наличии противопоказаний к ацетилсалициловой кислоте применяют клопидогрел в нагрузочной первой дозе 300 мг и в последующем 75 мг/сут.
Антикоагулянты
Применяют нефракционированный гепарин в течении 48 ч. В начале вводят внутривенно струйно 60 МЕ/кг (но не более 4000 МЕ), затем постоянно внутривенно со начальной скоростью 13 МЕ/кг/ч (но не более 100 МЕ/ч) Дальнейшую дозу подбирают, ориентируясь на АЧТВ, который должен в 1,5-2 раза быть больше нормы и контролироваться через 3, 6, 12, 24 ч.
Также возможно применение низкомолекулярного гепарина (эноксапарина), который вводят под кожу живота в дозе 1 мг/кг 2 раза в сутки до 5-7 дней. За 15 мин до первой п/к инъекции необходимо внутривенно струйно ввести 30 мг данного препарата. Доза первых 2 п/к инъекций — не более 100 мг. Преимущества низкомолекулярного гепарина перед нефракционированным: простота введения и нет необходимости в постоянном контроле свёртывания крови.
Иногда применяют фондапаринукс в дозе 2,5 мг под кожу живота 1 раз в сутки. Данный препарат наиболее удобен в применении и в отличие от гепарина не вызывает тромбоцитопению.
[Тромболитическая терапия
Тромболитическая терапия показана при инфаркте миокарда с подъёмом сегмента ST на ЭКГ. Эффективность её убедительно доказана, позволяет восстановить коронарный кровоток, ограничить размер инфаркта и снизить смертность. Тромболизис проводят как можно раньше и в пределах 12 ч от начала заболевания. Для этого применяют стрептокиназу в дозе 1,5 млн МЕ внутривенно на 100 мл 0,9% раствора хлорида натрия в течении 30-60 мин. Также используют альтеплазу на 100-200 мл изотонического раствора по схеме: 15 мг внутривенно струйно, затем 0,75 мг/кг в течении 30 мин (но не более 50 мг) и далее 0,5 мг/кг в течении 60 мин (но не более 35 мг). Альтеплаза имеет преимущества перед стрептокиназой в виде более эффективного восстановления коронарного кровотока за счёт тропности к фибринутромба, а также отсутствии антигенности.
Бета-адреноблокаторы
При отсутствии противопоказаний применяют метопролол, пропранолол или атенолол. Однако эффективность внутривенного применения бета-адреноблокаторов на ранних этапах не доказана и повышает риск развития кардиогенного шока.
Опасные предрассудки и дезинформация
- Через электронную почту массово рассылают некую презентацию (на русском и английском языках), в которой утверждается о якобы имеющихся рекомендациях «сильно кашлять при угрозе инфаркта» (якобы для «улучшения кровообращения»). Никаких научных данных такого рода нет, наоборот, больному необходим покой и срочная медицинская помощь. Ссылки на публикацию, приведенные в статье, являются фальсификацией.
- Среди населения существует заблуждение, что после инфаркта следует максимально снизить физическую активность, что не вполне верно. При возникновении инфаркта миокарда жесткое ограничение физической активности необходимо в первые часы и дни с момента возникновения инфаркта. Данная мера вызвана необходимостью снижения нагрузки на пораженный миокард. Однако впоследствии — ранняя активизация больного в сочетании с лечебной физкультурой значительно облегчают реабилитацию и снижают риск осложнений. Следует помнить, что при длительной иммобилизации тела увеличивается риск образования внутрисосудистых тромбов. Отсутствие же нагрузки существенно повышает риск повторного инфаркта. Это не означает, что больной, перенесший инфаркт миокарда, может сразу же вернуться к уровню физических нагрузок, которые были доступны ему за месяц до инфаркта. Подбор интенсивности безопасной физической нагрузки после инфаркта — задача для специалиста.
Прогноз
Прогноз заболевания условно неблагоприятный, после возникновения инфаркта в миокарде развиваются необратимые ишемические изменения, что может привести к осложнениям различной степени тяжести.
Источники
- Здоровая тема.ru — Инфаркт миокарда на сайте медицинского справочника «Здоровая тема» ztema.ru (Проверено 14 марта 2009)
- Инфаркт миокарда: причины, симптомы, классификация, диагностика и лечение www.polismed.ru (Проверено 14 марта 2009)
- Все об инфаркте миокарда доступным языком www.libemed.ru (Проверено 23 мая 2010)
- Принципы медикаментозной терапии больных, которые прошли реваскуляризацию миокарда. Видео-лекция www.chil.com.ua (Проверено 23 мая 201
Медицинская сестра должна владеть техникой съемки ЭКГ и такими методами, как закрытый массаж сердца, искусственное дыхание способом рот в рот, уметь обращаться с электрическим дефибриллятором, простейшими наркозными и дыхательными аппаратами, иметь навыки операционной сестры и уметь произвести некоторые простейшие лабораторные исследования (определение сахара или ацетона в моче, тромбоэластрография и т. п.).
Как видно из этого перечня, медицинская сестра палаты интенсивного наблюдения должна быть высококвалифицированным разносторонним специалистом с широким кругом обязанностей. Это ставит особые задачи по отбору, подготовке и воспитанию кадров. Весьма существенная в этом процессе роль врачей блока и кардиологического отделения, которые должны регулярно проводить соответствующие групповые и индивидуальные занятия с медицинскими сестрами, следить за повышением их квалификации.
Для более эффективной работы целесообразно разделить обязанности между медицинскими сестрами, если одновременно дежурят две или более. Одна контролирует ритм сердца по кардиоскопу (а также следит за другими параметрами, если они измеряются) и осуществляет общее наблюдение за больными. Другая обеспечивает непосредственный уход и выполняет врачебные назначения.
Естественно, что при необходимости все медицинские сестры подключаются к проведению, например, реанимации. Это же относится к вспомогательному медицинскому персоналу, так как в эти моменты чрезвычайно дорога каждая пара рук. Младший медицинский персонал, особенно работающий в палатах интенсивного наблюдения, также должен быть знаком с основами техники и порядком проведения реанимационных мероприятий (закрытый массаж сердца, дыхание рот в рот).
В штате специализированного отделения необходимо иметь инженера или техника, в задачу которого входит контроль за состоянием аппаратуры, чтобы она всегда была готова к работе. В некоторых стационарах бригады медицинских сестер сменяются 2 — 3 раза в сутки, в других — реже.
Недостаток первого варианта: относительно короткий период наблюдения за конкретным больным, что обычно отрицательно сказывается на преемственности диагностических и лечебных процедур.
Недостаток второго варианта: значительная усталость к концу смены, влекущая за собой снижение качества контроля. Особого внимания за работой среднего медицинского персонала требует момент перевода больного в обычную палату отделения (соблюдение преемственности лечения). Клиника инфаркта миокарда
Заболевание протекает циклически, необходимо учитывать период болезни.
I период
Чаще всего инфаркт миокарда начинается с нарастающих болей за грудиной, нередко носящих пульсирующий характер. Характерна обширная иррадиация болей – в руки, спину, живот, голову и т. д. Больные беспокойны, тревожны, иногда отмечают чувство страха смерти. Часто присутствуют признаки сердечной и сосудистой недостаточности – холодные конечности, липкий пот и др. Болевой синдром длительный, не снимается нитроглицерином. Возникают различные расстройства ритма сердца, падение АД. Указанные выше признаки характерны для I периода – болевого, или ишемического. Длительность I периода от нескольких часов до 2 суток. Объективно в этот период можно найти: увеличение АД (затем снижение); увеличение частоты сердечных сокращений; при аускультации иногда слышен патологический 4-й тон; биохимических изменений крови практически нет, характерные признаки на ЭКГ.
II период
II период – острый (лихорадочный, воспалительный), характеризуется возникновением некроза сердечной мышцы на месте ишемии. Появляются признаки асептического воспаления, начинают всасываться продукты гидролиза некротизированных масс. Боли, как правило, проходят. Длительность острого периода до 2 недель. Самочувствие больного постепенно улучшается, но сохраняются общая слабость, недомогание, тахикардия. Тоны сердца глухие. Повышение температуры тела, обусловленное воспалительным процессом в миокарде, обычно небольшое, до 38 оС, появляется обычно на 3-й день заболевания. К концу первой недели температура, как правило, нормализуется. При исследовании крови во 2-м периоде находят: лейкоцитоз, возникает к концу первых суток, умеренный, нейтрофильный (10—15 тыс.) со сдвигом до палочек: эозинофилы отсутствуют или эозинопения; постепенное ускорение СОЭ с 3—5-го дня заболевания, максимум ко 2-й неделе, к концу первого месяца приходит к норме; появляется С-реактивный белок, который сохраняется до 4 недели; повышается активность трансминазы, особенно ГЩУ – через 5—6 ч и держится 3—5—7 дней, достигая 50 ЕД. В меньшей степени увеличивается глутаминовая трансминаза. Повышается также активность лактатдегидрогеназы (50 ЕД), которая возвращается к норме на 10-е сутки. Исследования последних лет показали, что более специфичной по отношению к миокарду является креатинфосфокиназа, ее активность повышается при инфаркте миокарда до 4 ЕД на 1 мл и сохраняется на высоком уровне 3—5 дней. Считается, что существует прямая пропорциональная зависимость между уровнем креатинфосфокиназы и протяженностью зоны очага некроза сердечной мышцы.
На ЭКГ ярко представлены признаки инфаркта миокарда.
1. При проникающем инфаркте миокарда (т. е. зона некроза распространяется от перикарда до эндокарда): смещение сегмента ST выше изолинии, форма, выпуклая кверху, – это первый признак проникающего инфаркта миокарда; слияние зубца Т с сегментами ST на 1—3-й день; глубокий и широкий зубец Q – основной, главный признак; уменьшение величины зубца R, иногда форма QS; характерные дискордантные изменения – противоположные смещения ST и Т (например, в 1 и 2 стандартном отведениях по сравнению с 3 стандартным отведением); в среднем с 3-го дня наблюдается характерная обратная динамика изменений ЭКГ: сегмент ST приближается к изолинии, появляется равномерный глубокий Т. Зубец Q также претерпевает обратную динамику, но измененный Q и глубокий Т могут сохраняться на всю жизнь.
2. При интрамуральном инфаркте миокарда: нет глубокого зубца Q, смещение сегмента ST может быть не только вверх, но и вниз.
Для правильной оценки важно повторное снятие ЭКГ. Хотя ЭКГ-признаки очень помогают диагностике, диагноз должен опираться на все признаки (в критерии) диагностики инфаркта миокарда:
– клинические признаки;
– электрокардиографические признаки;
– биохимические признаки.
III период
III период (подострый, или период рубцевания) длится 4—6 недель. Характерным для него является нормализация показателей крови (ферментов), нормализуется температура тела и исчезают все другие признаки острого процесса: изменяется ЭКГ, на месте некроза развивается соединительно-тканный рубец. Субъективно больной чувствует себя здоровым.
IV период
IV период (период реабилитации, восстановительный) – длится от 6 месяцев до 1 года. Клинически никаких признаков нет. В этот период происходит компенсаторная гипертрофия интактных мышечных волокон миокарда, развиваются другие компенсаторные механизмы. Происходит постепенное восстановление функции миокарда.
Также инфаркт миокарда может протекать по следующим типам.
? Абдоминальная форма. Протекает по типу патологии ЖКТ с болями в подложечной области, в животе, с тошнотой, рвотой. Чаще всего гастралгическая форма (абдоминальная) инфаркта миокарда встречается при инфаркте задней стенки левого желудочка. В целом вариант редкий. ЭКГ отведения II, III, AVL.
? Астматическая форма: начинается с сердечной астмы и провоцирует отек легких как исход. Боли могут отсутствовать. Астматическая форма встречается чаще у пожилых людей с кардиосклерозом, или при повторном инфаркте, или при очень обширных инфарктах.
? Мозговая форма: на первом плане симптомы нарушения мозгового кровообращения по типу инсульта с потерей сознания, встречается чаще у пожилых людей со склерозом сосудов головного мозга.
? Немая или безболевая форма иногда является случайной находкой при диспансеризации. Из клинических проявлений: вдруг стало «дурно», возникла резкая слабость, липкий пот, затем все, кроме слабости, проходит. Такая ситуация характерна для инфаркта в пожилом возрасте и при повторных инфарктах миокарда.
? Аритмическая форма: главный признак пароксизмальная тахикардия, болевой синдром может отсутствовать.
? Тромбоэмболическая. Инфаркт миокарда – очень тяжелое заболевание с частым летальным исходом, особенно часты осложнения в I и II периодах.
Течение инфаркта миокарда, как и других острых заболеваний, имеет определенную цикличность. Между подострым периодом инфаркта миокарда, который больной проводит в стационаре, и постинфарктным кардиосклерозом, когда ишемическая болезнь сердца приобретает более или менее спокойное течение, отчетливо прослеживается еще один период – период выздоровления. В это время больные лечатся в кардиологических санаториях (загородных филиалах больниц) при кардиологических кабинетах поликлиник. Терапия направлена главным образом на постепенное повышение физических и психологических возможностей больного, на возвращение его к труду.
Период выздоровления после перенесенного инфаркта миокарда характеризуется постепенной реадаптацией больного к внешним условиям среды при сниженных резервных возможностях сердечно-сосудистой системы, в частности, при уменьшении массы активно сокращающегося миокарда. В этот период постепенно развивается компенсаторная гипертрофия сохранившегося миокарда, происходит перестройка коронарного кровообращения путем образования коллатералей, после длительного пребывания в постели и гиподинамии восстанавливает тонус и силу скелетная мускулатура. Инфаркт миокарда является тяжелой психической травмой для больного. Нередко еще в стационаре больной задает себе вопросы, сможет ли он работать, как сложатся его отношения с коллективом после возвращения, каким будет материальное положение его семьи и т. д. Эти вопросы с еще большей остротой встают перед ним после выписки из больницы. Это нередко приводит к соматогенно обусловленным невротическим состояниям, требующим психотерапии, назначения седативных, психотропных средств и т. д. Детальное изучение восстановительного периода помогает разработать реабилитационные мероприятия, улучшить экспертизу трудоспособности.
Таким образом, в лечении больных соблюдается принцип этапности и преемственности. Согласно многочисленным исследованиям это одно из важнейших условий успешной реабилитации лиц, перенесших инфаркт миокарда.
Как показали динамические наблюдения за больными в восстановительном периоде инфаркта миокарда, вскоре после выписки из стационара у подавляющего большинства отмечается субъективное ухудшение. Оно складывается в основном из четырех синдромов.
? Главным остается сердечно-болевой синдром.
? Второй синдром состоит преимущественно из клинико-функциональных признаков, характерных для ранней стадии сердечной недостаточности.
? Третий синдром проявляется в общей детренированности организма (утомляемость, слабость, снижение мышечной силы, боли в мышцах ног при ходьбе, головокружение и т. д.).
? Четвертый состоит в основном из жалоб и симптомов невротического происхождения (плохой сон, раздражительность, подавленное настроение, различные фобии, в основном кардиофобии, импотенция и т. д.).
Наибольшую тревогу у больных, перенесших инфаркт миокарда, вызывает сердечно-болевой синдром. Возобновление болей по миновании острого периода заболевания больные обычно связывают с угрозой повторного инфаркта миокарда, это порождает сомнения в эффективности лечения, подавляет стремление вернуться на работу и т. д. Возникновение приступов стенокардии после инфаркта миокарда обычно свидетельствует о распространенном стенозирующем атеросклерозе коронарных артерий и является неблагоприятным прогностическим признаком в отношении как жизни, так и трудоспособности. Сердечно-болевому синдрому у больных, перенесших инфаркт миокарда, следует уделять серьезное внимание. Однако не все боли в области сердца и за грудиной у больных, перенесших инфаркт миокарда, следует рассматривать как грудную жабу, проявление хронической коронарной недостаточности. Наряду с типичными приступами стенокардии в виде сжимающих, давящих болей за грудиной и в области сердца с иррадиацией в нижнюю челюсть, левое плечо, руки и быстрым эффектом от приема нитроглицерина у больных, перенесших инфаркт миокарда, нередко наблюдаются боли невротического происхождения. Они могут быть как незначительными, так и весьма интенсивными. Такие боли приковывают к себе внимание больных и часто служат основной жалобой при обращении к врачу. Невротические боли обычно локализуются в области левого соска, могут распространяться на всю предсердечную область и нередко иррадиируют в левую лопатку, левое плечо и руку. Эти боли, как правило, не связаны с физической нагрузкой, чаще возникают после психоэмоционального перенапряжения, могут длиться от нескольких секунд до нескольких часов, не купируются нитроглицерином и лучше уступают приему седативных средств. При болях в области сердца невротического происхождения практически всегда можно выявить ряд симптомов, указывающих на изменения центральной нервной системы в виде повышенной раздражительности, неустойчивости настроения, снижения внимания, работоспособности и т. д.
По интенсивности можно выделить 3 степени кардиалгии.
? При I степени больные жалуются на сравнительно редкие, слабые колющие, ноющие боли в области левого соска без иррадиации. Эти боли возникают спонтанно либо после волнения, переутомления, при перемене погоды, обычно проходят самостоятельно и легко купируются седативными средствами (валидол, валериана, валокордин). Такие больные сравнительно редко обращаются к врачу по поводу этих болей, у них нет невротических расстройств или они незначительно выражены, преимущественно имеют тревожно-депрессивную окраску.
? При II степени больные жалуются на частые ноющие, колющие или давящие боли в области сердца, иррадиирующие в левую лопатку и плечо. Боли продолжаются от нескольких минут до 3—4 ч. Иногда боли длятся 2—3 дня, периодически ослабевая и вновь усиливаясь. Невротические расстройства у больных этой группы умеренно выражены, преобладают ипохондрические явления. Как правило, больные жалуются на повышенную раздражительность, плохой сон, общую слабость, сердцебиение, сниженную работоспособность, нередко на одышку, которая при уточнении без труда квалифицируется как чувство неудовлетворенности вдохом. Иногда больные говорят о покалывании в левом боку при глубоком вдохе, что весьма напоминает боли при левостороннем сухом плеврите. У некоторых лиц приступы болей в области сердца сочетаются с ознобом, похолоданием конечностей, сухостью во рту, одышкой, учащением пульса и полиурией, что указывает на их симпатико-адреналовое происхождение. Эти больные часто жалуются на боли, но коронароактивные препараты не приносят им облегчения. Болезненной оказывается также кожа, особенно неприятные ощущения вызывает разминание кожной складки в левой части межлопаточного пространства. Такое разминание, хотя и весьма болезненное, быстро снимает или уменьшает боль в области сердца, что в свою очередь подтверждает ее экстракардиальное происхождение.
? При III степени интенсивности болей невротического происхождения больные жалуются на постоянные, периодически усиливающиеся боли в области сердца, которые иррадиируют в левое плечо, лопатку, руку, левую половину головы, изредка даже в левую ногу. Ярко выражено общее невротическое состояние. Преобладают истерические и ипохондрические нарушения. Отмечается резкая и весьма распространенная болезненность мышц, кожи, межреберий, паравертебральных точек, над– и подключичных ямок слева. Болезненны мышцы левой руки (больше на плече), места выхода нервов, имеется болезненность в области затылочной точки, точек выхода тройничного нерва слева. Иногда при пальпации отмечается легкая болезненность левой сонной и левой височной артерий. При длительном существовании кардиалгии значительно снижается сила в левой руке, возможна легкая атрофия мышц пояса верхних конечностей (чаще дельтовидной мышцы). Толерантность к физической нагрузке у этих больных нередко снижена, они прекращают работу на велоэргометре из-за резкой слабости, усталости или боязни сердечного приступа.
Если боли по типу кардиалгии локализуются в области грудины, то обнаруживается симметричное повышение чувствительности мягких тканей и паравертебральных точек в соответствующих зонах.
Общими чертами невротических болей в области сердца являются их распространенность, широкая иррадиация, связь с эмоциональными и метеорологическими факторами, частое возникновение в покое, ночью, отсутствие отчетливых изменений соматической иннервации, преимущественное нарушение глубокой чувствительности, а также ряд трофических расстройств.
Выявление зон нарушения чувствительности в области грудной клетки и пояса верхних конечностей можно использовать как для дифференциальной диагностики при болях в области сердца и за грудиной, так и для объективной характеристики интенсивности кардиалгии. При типичной стенокардии гипералгезия мягких тканей и вегетативных точек в левой половине грудной клетки отсутствует, что повышает дифференциально-диагностическое значение объективного обследования больных, предъявляющих жалобы на боли в области сердца. Специальное изучение психического статуса больных с типичными приступами стенокардии выявило незначительные невротические расстройства. Причина сочетанного сердечно-болевого синдрома у больных ишемической болезнью сердца вообще и у перенесших инфаркт миокарда, в частности, остается неясной. В патогенезе атипичных болей определенное значение придают явлениям реперкуссии. Специальное изучение этого вопроса на нашем контингенте больных показало, что нет соответствия между тяжестью, величиной и локализацией перенесенного инфаркта миокарда и степенью хронической коронарной недостаточности, с одной стороны, и интенсивностью кардиалгии – с другой, среди больных, перенесших инфаркт миокарда.
Среди предъявляющих жалобы на атипичные боли в области сердца можно выделить еще одну небольшую группу. У лиц этой группы боли локализуются в области сердца и шейно-грудном отделе позвоночника, усиливаются при длительном лежании, при изменении положения тела. Характер болевого синдрома и объективные данные позволяют диагностировать шейно-грудной радикулит вследствие остеохондроза позвоночника. Появление атипичных болей в области сердца у больных этой группы обусловлено, по-видимому, раздражением спинальных корешков измененными межпозвоночными дисками. Касаясь динамики сердечно-болевого синдрома у больных в восстановительном периоде инфаркта миокарда, необходимо отметить следующее.
После выписки из больницы в связи с постепенным расширением двигательного режима значительно возрастает частота стенокардии. и она выявляется приблизительно у 50 % больных. При этом в половине случаев она остается типичной стенокардией, а у другой половины больных сочетается с кардиалгией. Число больных, у которых в восстановительном периоде заболевания выявляется постинфарктная стенокардия, не изменяется, хотя под влиянием лечебных мероприятий несколько уменьшается ее тяжесть. Стенокардия чаще встречается в старших возрастных группах, у больных, перенесших повторный инфаркт миокарда, и наиболее редко – у больных в восстановительном периоде после обширного трансмурального инфаркта миокарда. У лиц, занятых физическим трудом, стенокардия встречается несколько реже, чем у служащих, что можно объяснить, по-видимому, благоприятным влиянием предшествующей заболеванию мышечной деятельности на состояние коронарного резерва и, в частности, на развитие коллатерального кровообращения.
Клинические данные свидетельствуют о том, что среди больных, у которых в течение первого месяца амбулаторного лечения появилась стенокардия, в дальнейшем удается ее устранить лишь в 16—18 % случаев. Однако стенокардия в этих случаях, как правило, не бывает тяжелой. Это отражает прогрессирование атеросклероза коронарных артерий в восстановительном периоде после инфаркта миокарда. У большинства больных в периоде выздоровления после инфаркта миокарда периодически возникают или остаются постоянно невротические боли в области сердца различной интенсивности. Динамическое изучение болей в области сердца невротического происхождения показало, что наиболее редко они встречаются у больных перед выпиской из стационара (35,3 % случаев).
В период амбулаторного лечения частота кардиалгии увеличивается до 50 % и остается без существенных изменений на протяжении последующего наблюдения. На возникновение и интенсивность кардиалгии не влияют возраст больных, обширность перенесенного инфаркта миокарда и сопутствующая гипертоническая болезнь. У женщин кардиалгия бывает значительно чаще и интенсивнее, чем у мужчин. Однако параллельно нарастанию интенсивности кардиалгии отчетливо увеличиваются частота и выраженность изменений личности больного.
Нередко у больных, перенесших инфаркт миокарда, наблюдаются боли в плечевых суставах, чаще в левом, чувство онемения в руке. Может развиться картина выраженного периартрита. При рентгенологическом исследовании иногда обнаруживается остеопороз костей, образующих плечевой сустав. Описанный симптомокомплекс в литературе называется плечевым синдромом, или синдромом «плечо – рука». Он наблюдается у 5—20 % больных постинфарктным кардиосклерозом. Нередко плечевой синдром развивается уже в остром периоде инфаркта миокарда, а иногда лишь через несколько лет после него.
Появление застойной сердечной недостаточности – сигнал о неблагоприятном прогнозе. Так, например, среди больных, перенесших инфаркт миокарда в трудоспособном возрасте, у которых уже перед выпиской из стационара или в ближайшие дни после нее появились признаки застойной сердечной недостаточности, летальный исход в течение ближайших 3 месяцев наступил в 35 % случаев. Большее практическое значение и большие трудности представляет собой распознавание начальной стадии сердечной недостаточности. В этой стадии нет истинных признаков декомпенсации, гемодинамические показатели в покое еще не изменены, но сократительная способность миокарда слегка снижена, выполнялась больным без труда. При опросе важно выяснить, не возникла ли у больного потребность спать в последнее время на высоких подушках или склонность к никтурии. Следует обращать внимание на появление кашля по ночам, что может быть одним из первых симптомов застойной левожелудочковой недостаточности. Другим классическим симптомом является сердцебиение. Оно возникает на ранних этапах развития недостаточности миокарда и обусловлено стремлением к компенсации путем увеличения частоты сокращений. Однако жалобы на одышку и сердцебиение не могут служить достаточно точными диагностическими ориентирами, так как в значительной мере зависят от нагрузок, которым подвергается больной в повседневной жизни. Поскольку больные, перенесшие инфаркт миокарда, обычно ведут размеренный образ жизни и избегают перегрузок, на одышку при ходьбе и подъеме по лестнице или сердцебиение они жалуются редко.
Значительно большую роль в распознавании скрытой (латентной) сердечной недостаточности у больных, перенесших инфаркт миокарда, играют инструментальные методы. Их можно разделить на две группы: неинвазивные (электрокардиография, реография, рентгенография и др.) и инвазивные (катетеризация левых и правых полостей сердца, вентрикулография).
Важную роль в диагностике начальной стадии сердечной недостаточности может играть велоэргометрическое исследование. Появление тахикардии, относительно малый прирост пульсового давления, удлинение восстановительного периода, значительное повышение диастолического давления в легочной артерии, а также конечного диастолического давления в полости левого желудочка под влиянием дозированной физической нагрузки можно считать важными признаками скрытой недостаточности кровообращения.