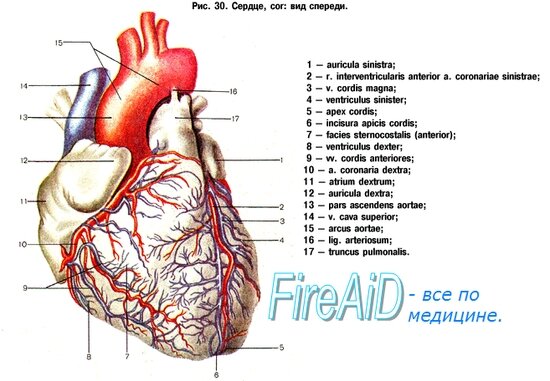
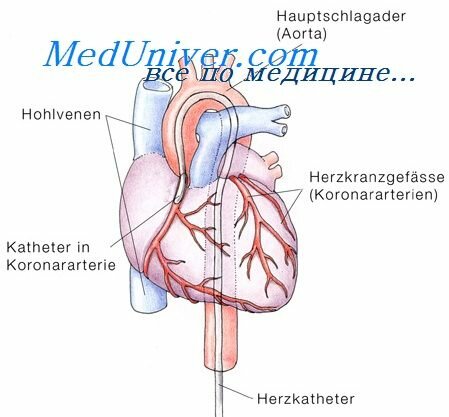
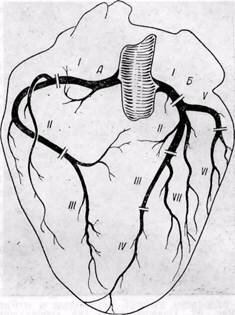
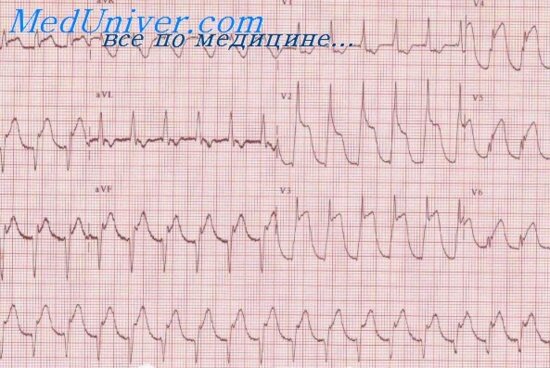
Острая ишемическая болезнь сердца, или инфаркт миокарда
Выражением острой ишемической болезни является инфаркт миокарда, который занимает примерно 8 нед с момента приступа ишемии миокарда. Инфаркт миокарда, развившийся спустя 8 нед после первого (острого), называют повторным инфарктом, а развившийся в течение 8 нед существования первого (острого) инфаркта — рецидивирующим.
За время своего существования инфаркт проходит три стадии: ишемическую (донекротическую), некротическую и стадию организации, морфология которых хорошо изучена. Инфаркт миокарда локализуется чаще всего в области верхушки, передней и боковой стенок левого желудочка и передних отделов межжелудочковой перегородки, т. е. в бассейне передней межжелудочковой ветви левой коронарной артерии, которая функционально более отягощена и сильнее других ветвей поражается атеросклеротическим процессом.
Реже инфаркт возникает в области задней стенки левого желудочка и задних отделов межжелудочковой перегородки, т. е. в бассейне огибающей ветви левой коронарной артерии. Нередко атеросклеротической окклюзии подвергаются основной ствол лев ой венечной артерии и обе его ветви.
В таких случаях нередко развивается обширный инфаркт миокарда. В правом желудочке и особенно в предсердиях инфаркт развивается редко. Атеросклероз в правой коронарной артерии по сравнению с левой, как правило, выражен меньше. Топография и размеры инфаркта определяются не только преимущественной заинтересованностью и степенью поражения ветвей коронарных артерий, но и типом кровоснабжения сердца.
Различают три типа кровоснабжения сердца: левый, правый и средний. При левом типе преобладает развитие левой венечной артерии, которая снабжает все стенки левого, заднюю стенку правого желудочка и всю межжелудочковую перегородку. При правом типе хорошо развита правая венечная артерия, которая снабжает кровью стенки правого желудочка, задний отдел межжелудочковой перегородки и заднюю стенку левого желудочка.
Средний тип характеризуется равномерным развитием обеих венечных артерий. Поскольку атеросклеротические изменения обычно интенсивнее выражены в более развитой и функционально отягощенной артерии, инфаркт миокарда чаще наблюдается при крайних типах кровоснабжения — левом или правом.
Эти особенности кровоснабжения сердца позволяют понять, почему, например, при тромбозе нисходящей ветви левой венечной артерии в разных случаях инфаркт имеет различную локализацию (передняя или задняя стенка левого желудочка, передний или задний отдел межжелудочковой перегородки).
«Патологическая анатомия», А.И.Струков
ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ И ГЕМАТОЛОГИЯ
Макроскопическая диагностика инфаркта миокарда.
Написал Красницкий Евгений в 19 Июль 2011, 17:39
Ишемия миокарда начинается в субэндокардиальной зоне и распространяется к эпикарду, что обусловлено особенностью кровоснабжения миокарда. На вскрытии наибольшие трудности вызывает определение наличия инфаркта сроком до 6 часов. Для начала необходимо определить тип кровоснабжения сердца, наличие и степень атеросклероза коронарных артерий, состояние стенки и просвета коронарных артерий, наличие гипертрофии миокарда.
Морфология инфаркта миокарда сроком 30 минут до 3-х часов – миокард дряблый, влажный, отмечается бледность, небольшое западение над поверхностью разреза с нечеткой границей, эти признаки наблюдаются до 5 часа после начала ишемии.
Инфаркт сроком от 5 часов до суток имеет отчетливые границы, миокард бледный, отечный, зона повреждения выступает над поверхностью разреза.
Инфаркт сроком от 1 суток до 2 суток – проявляется очагом с четкой границей, желтоватого цвета, дряблый, немного выступает над поверхностью разреза.
Инфаркт на 2 – 3 сутки представляет очаг с четкими границами, сухой, желто-коричневого цвета.
Инфаркт от 4 до 6 дня темно-желтого цвета, отмечается дряблость стенки.
Инфаркт от 7 до 14 дня серо-розового цвета, с западающими зонами и красным ободком по краю.
Морфология инфаркта миокарда к концу 3 недели определяется появлением грануляционной ткани, при созревании которой рубец сокращается и образуется белый плотный слегка западающий рубец.
Особенности танатогенеза при остром инфаркте миокарда 14. 00. 15 патологическая анатомия
На правах рукописи
НЕФЕДОВА Галина Александровна
Особенности танатогенеза
при остром инфаркте миокарда
14.00.15 – патологическая анатомия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2007
Работа выполнена в Московском научно-исследовательском институте скорой помощи имени Н.В. Склифосовского
НАУЧНЫЙ РУКОВОДИТЕЛЬ:
доктор медицинских наук, профессор Галанкина Ирина Евгеньевна
ОФИЦИАЛЬНЫЕ ОППОНЕНТЫ:
доктор медицинских наук, профессор Михалева Людмила Михайловна
доктор медицинских наук, профессор Рогов Константин Аркадьевич
ВЕДУЩАЯ ОРГАНИЗАЦИЯ: ГОУ ВПО «Московский государственный медико-стоматологический Университет Росздрава»
Защита диссертации состоится « » 2007 г. в часов на заседании диссертационного совета Д 001. 004. 01 ГУ НИИ морфологии человека РАМН по адресу: 117418, Москва, ул. Цюрупы, д. 3
С диссертацией можно ознакомиться в библиотеке ГУ НИИ морфологии человека РАМН
Автореферат разослан « » 2007 г.
Ученый секретарь диссертационного совета
д.м.н. Михайлова Л.П.
Актуальность проблемы
Ишемическая болезнь сердца (ИБС) – одно из основных заболеваний человека, значительно ухудшающее качество жизни и приводящее к летальному исходу (Беринская А.Н. и соавт. 1958; Кактурский Л.В. 1982; Лукомский П.Е. 1964; Fagin D. 1966; McQuay N. 1955; Терновой С.К. и соавт. 2003). Статистические исследования свидетельствуют о том, что более 50% населения в возрасте от 65 лет страдают сердечно-сосудистыми заболеваниями. В России, по данным разных авторов, ежегодно ишемическая болезнь сердца диагностируется у 2,8-5,8 млн. человек, смертность же составляет до 30% общей смертности (Ганелина И.Е. и соавт. 1968; Goldberg RJ и соавт. 1988). Острый инфаркт миокарда (ОИМ) – заболевание, которое может закончиться выздоровлением больного без вмешательства врачей, и наоборот, привести к смерти, несмотря на все их усилия. Однако между этими крайностями находится многочисленная группа больных, судьба которых зависит от своевременного вмешательства врача и использования современных методов лечения (Мазур Н.А. 1985; Руда М.Я. 1977). Поиск путей снижения летальности от ОИМ является постоянным стимулом для анализа летальных исходов с учетом новых возможностей современных методов лечения и представляет собой актуальную проблему современной медицины.
Несомненно, что основными факторами, определяющими исход ОИМ, являются: распространенность стенозирующего атеросклероза коронарных артерий (КА) с тромботической окклюзией просвета или без нее; обширность некроза, влияющая на степень нарушения функции ЛЖ и являющаяся основным фактором, определяющим летальность и выживаемость; а также выраженность и степень компенсации сопутствующей патологии: гипертонической болезни, сахарного диабета, ожирения и др.
В то же время имеются сведения, свидетельствующие о том, что все вышеперечисленные условия не всегда могут объяснить летальность и выживаемость при ОИМ. Далеко не во всех случаях летального исхода от ОИМ обнаруживаются распространенный стенозирующий атеросклероз КА, окклюзирующий просвет тромб, значительное количество летальных исходов происходит при небольшой площади ОИМ (Беляев А.А. 2001; Руда М.Я. 1977; Терновой С.К. 2003). Несмотря на прогресс в медикаментозном лечении, активном внедрении методов интервенционной кардиоангиологии и хирургического вмешательства (Бузиашвили Ю.И. и соавт. 2002; Иоселиани Д.Г. и соавт. 2003) цифры летальности от ОИМ остаются неизменными и достаточно высокими. Объяснить причину этого пока не удается.
В 1925 году ленинградский патологоанатом Георгий Владимирович Шор представил обоснованную концепцию о смерти человека, в которой поставил перед патологоанатомами задачу глубокого анализа причин и механизмов наступления смерти в конкретных условиях, обосновал необходимость клинико-анатомического анализа предпосылок невозможности в этих условиях дальнейшей жизни, изложил пути изучения механизмов смерти больного человека. Г.В. Шор (1925) подчеркивал, что «главнейшей задачей танатологии должно быть выяснение всех условий, приведших к смерти организм, как индивидуальное целое».
В настоящее время анализ всех условий наступления смерти с учетом разных этапов болезни, как правило, не проводится, а заключение о причине смерти часто носит статистический характер. Этого недостаточно ни для клиницистов, ни для патологоанатомов, так как не дает представления о причинах летального исхода у данного конкретного больного. Изучение зарубежной литературы по данному вопросу свидетельствует о том, что вопросы танатологии в широком смысле не являются предметом обсуждения. Анализ летальных исходов чаще проводится в связи с изучением влияния новых подходов к лечению острого инфаркта миокарда (Flather M. et al, 1996, Reynolds G. et al, 1996).
Таким образом, вопросы, касающиеся механизмов развития смертельных осложнений при ОИМ, до сих пор остаются спорными. Несмотря на многочисленные клинико-анатомические исследования, аспекты танатогенеза в основном сведены к основному заболеванию либо непосредственной причине смерти. Однако изучение танатогенеза, как считал Г.В. Шор, является «той частью танатологии, которая направлена к практической деятельности врачей. и которая разрабатывает меры предупреждения фатальных осложнений болезни».
Цель исследования – выявление особенностей танатогенеза при остром инфаркте миокарда в зависимости от обширности его, степени и распространенности атеросклеротического поражения коронарных артерий в свете поиска путей снижения летальности.
Задачи исследования:
Определить обширность (площадь) и особенности локализации острого инфаркта миокарда в зависимости от распространенности и тяжести атеросклеротического поражения коронарных артерий.
Оценить особенности морфогенеза острого инфаркта миокарда в зависимости от распространенности атеросклеротического поражения коронарных артерий.
Выявить основные факторы, определяющие развитие смертельных осложнений острого инфаркта миокарда: наружный разрыв сердца, аритмический шок, истинный кардиогенный шок, острая левожелудочковая недостаточность.
Выделить основные механизмы танатогенеза с учетом обширности острого инфаркта миокарда, особенностей поражения коронарного русла сердца и роли других заболеваний на основе клинико-анатомического анализа.
Научно-практическая значимость работы
Впервые на основе сопоставления площади острого инфаркта миокарда и выраженности и распространенности стенозирующего атеросклероза коронарных артерий представлены механизмы развития основных смертельных осложнений, обоснованы особенности танатогенеза с учетом роли других заболеваний, что способствует поиску путей снижения летальности от острого инфаркта миокарда. Обширный острый инфаркт миокарда (более 50% рабочей поверхности левого желудочка) чаще возникает в условиях тяжелого атеросклеротического стеноза всех ветвей коронарных артерий. Необширный острый инфаркт миокарда (менее 30% рабочей поверхности левого желудочка), как правило, развивается при локальном атеросклеротическом стенозе одной из ветвей коронарных артерий.
При развитии обширного острого инфаркта миокарда летальный исход наступает от истинного кардиогенного шока, либо острой левожелудочковой недостаточности. При развитии необширного острого инфаркта миокарда летальный исход в половине наблюдений наступает от наружного разрыва сердца, реже – тромбоэмболических осложнений (12%) либо декомпенсации другого заболевания (13%). При развитии острого инфаркта миокарда с площадью поражения 30-50% рабочей поверхности левого желудочка летальный исход чаще наступает от аритмического шока.
В большинстве случаев острый инфаркт миокарда, завершающийся летально, развивается при сочетанном атеросклеротическом стенозе двух либо трех ветвей коронарных артерий, в трети случаев – при изолированном атеросклеротическом стенозе одной из ветвей, чаще передней межжелудочковой ветви левой коронарной артерии. Частота тромбоза существенно уменьшается с увеличением числа пораженных ветвей, а также с вовлечением в атеросклеротический процесс их средних и дистальных сегментов.
Темпы формирования демаркационной зоны при остром инфаркте миокарда зависят от его площади и от степени выраженности и распространенности стенозирующего атеросклероза в коронарных артериях. При необширном инфаркте миокарда (в условиях изолированного атеросклеротического стеноза одной из ветвей коронарных артерий) демаркационная зона формируется раньше; при многососудистом поражении коронарных артерий – позднее, особенно в условиях декомпенсации других соматических заболеваний у лиц пожилого и старческого возраста.
Дано обоснование необходимости обязательного (а не желательного, как принято в настоящее время) включения в патологоанатомический диагноз рубрики «клинико-анатомический эпикриз», в котором на основе клинико-анатомического анализа должны быть изложены представления о механизмах танатогенеза данного конкретного умер- шего.
Внедрение в практику
Полученные результаты внедрены в практическую работу регулярно проводимых клинико-анатомических конференций в НИИ Скорой помощи им. Н.В. Склифосовского и в Научно-практическом центре интервенционной кардиоангиологии.
Апробация работы
Основные положения работы доложены: на I Московской городской конференции молодых ученых «Медицина на пороге XXI века, актуальные проблемы и вопросы» (Москва, 2001); симпозиуме «Патогенез и патологическая анатомия критических, терминальных и постреанимационных состояний» (Москва, 2003); IY и Y Международных симпозиумах «Сердечно-сосудистая и интервенционная радиология» (Москва, 2001, 2004); Втором Российском Съезде Интервенционных Кардиоангиологов (Москва, 2005); на заседании Московского отделения Российского общества патологоанатомов (Москва, 2005); II Съезде Российского общества патологоанатомов (Москва, 2006); на ежегодно проводимых городских научно-практических конференциях НИИ Скорой Помощи им. Н.В. Склифосовского (Москва, 2000 – 2005); на межлабораторной конференции в НИИ скорой помощи им. Н.В. Склифосовского (Москва, декабрь 2006); межлабораторной конференции в ГУ НИИ морфологии человека РАМН (Москва, декабрь 2006).
Публикации
По теме диссертации опубликовано 11 научных работ, в том числе 5 работ на Российском, международном и региональном уровнях, 2 публикации представлены в изданиях, включенных в утвержденный ВАКом «Перечень периодических изданий».
Структура и объем диссертации
Диссертация изложена на 162 страницах машинописного текста, состоит из введения, трех глав, обсуждения, заключения, выводов, практических рекомендаций, списка литературы, включающего 167 источников (128 на русском и 39 на иностранных языках). Диссертация содержит 2 таблицы, 30 рисунков, 6 схем.
^ СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования
Изучены 180 наблюдений летальных исходов от острого инфаркта миокарда за период с 1998 по 2005 годы (все вскрытия произведены автором). Исследования проводили на материале объединенной прозектуры НИИ скорой помощи им. Н.В. Склифосовского, в которой концентрируются умершие в институте и нескольких городских клинических больницах, имеющих специализированные кардиологические отделения. Во всех случаях ОИМ был диагностирован клинически. Все больные были полноценно обследованы с помощью клинических, функциональных и лабораторных методов, необходимых для больных кардиологического профиля. Всем пациентам проводили интенсивную лекарственную терапию. Из исследуемого материала исключены случаи, в которых применялись методы современной интервенционной кардиоангиологии и хирургического лечения. В анализ вошли только те наблюдения, в которых на аутопсии была выявлена четкая граница некроза, т.е. сроки ОИМ во всех случаях превышали 18 часов.
Детально изучали распространенность и степень стеноза коронарных артерий (КА) по сегментам. Степень стеноза просвета КА определяли на поперечных срезах каждого сегмента артерии путем визуальной оценки бляшки, выступающей в просвет. Использовали коронарографическую классификацию атеросклеротических поражений артерий, предложенную в 1974 г. Ю.С. Петросяном и Л.С. Зингерманом: 0 – без сужения просвета, 1 – умеренный стеноз до 50% площади просвета – гемодинамически незначимые стенозы, 2 – выраженный стеноз от 50 до 75%, 3 – резкий стеноз свыше 75%, 4 – резкий стеноз до 90% (гемодинамически значимые стенозы), 5 – атеросклеротическая окклюзия или обтурирующий просвет тромб. Определяли характер атеросклеротического поражения КА, тип коронарного кровоснабжения сердца.
Во всех случаях проводили микроскопическое исследование миокарда и коронарных артерий: после фиксации материала в 10% растворе нейтрального формалина, забуференном по Лилли, и заливки в парафин, срезы окрашивали гематоксилином и эозином, по ван Гизону, по Lie (ГОФП). Гистохимическое исследование включало выявление нейтральных жиров (жировым красным О), гликогена (PAS-реакция), фибрина (MSB).
Во всех исследуемых случаях проводился детальный клинико-анатомический анализ данных истории болезни и результатов секционного и гистологического исследований. В 80% наблюдений аутопсии обсуждались на клинико-анатомических конференциях.
Результаты исследования и их обсуждение
Данные проведенного анализа 180 умерших от ОИМ свидетельствуют о том, что в большинстве случаев (77,8%) больные умирали от обширного острого инфаркта миокарда (площадь более 30% рабочей поверхности ЛЖ) (рис.1.). В подавляющем большинстве случаев (78%) обширность ОИМ обусловлена тяжелым атеросклеротическим стенозом всех ветвей КА.
Рис. 1. Частота ОИМ в зависимости от его площади
1 КА
2 КА
3 КА
иброзные и кальцинированные атеросклеротические бляшки, суживающие просвет на 75-90% площади, выявляли во всех сегментах пораженных КА, в дистальных отделах, в ветвях второг
днако в 22,2% случаев больные умирали от необширного ОИМ (менее 30% рабочей поверхности ЛЖ). Чаще, в 67,5% этих случаев, он развивался при изолированном атеросклеротическом стенозе одной из ветвей КА (рис. 3). Атеросклеротическая бляшка, иногда единственная, суживающая просвет на 75-90% площади, как правило, локализовалась в проксимальном сегменте пораженной КА. Дистальные отделы артерии, а также другие ветви КА не были стенозированы более 50% площади просвета, т. е. имели гемодинамически незначимые стенозы.
#image.jpg
Рис. 3. Распространенность стенозирующего поражения КА
при ОИМ площадью до 30%
2 КА
1 КА
3 КА
80 летальных исходов были условно разделены на 3 группы по количеству пораженных ветвей КА: изолированное поражение одной ветви КА, сочетанное поражение двух ветвей КА, сочетанное поражение трех ветвей КА. Такое распределение наших наблюдений оправдано тем, что с возрастанием распространенности поражения КА усложняется не только морфология коронарного атеросклероза, но и проявления компенсаторных процессов, в совокупности ведущих к существенной перестройке всей коронарной системы. По нашим данным, в 32,2% случаев ОИМ, завершившийся летально, развивался при изолированном атеросклеротическом стенозе одной из ветвей КА, в 67,8% — при сочетанном атеросклеротическом стенозе двух либо трех ветвей КА. Частота тромбоза просвета КА существенно уменьшалась с увеличением числа пораженных ветвей, а также с вовлечением в атеросклеротический процесс средних и дистальных сегментов коронарных артерий и составляет 58,7%. При изолированном стенозе одной из ветвей КА она высокая – 82,8% случаев.
Исходя из особенностей типа кровоснабжения сердца, в каждом конкретном случае была проанализирована зависимость обширности и локализации ОИМ и постинфарктного рубца от пораженной (либо пораженных) КА и наличия тромбоза просвета. Интересные сведения получены в наблюдениях с изолированным поражением одной из ветвей КА. В 46% наблюдений этой группы ОИМ развивался необширный (до 30% рабочей поверхности ЛЖ); вне зависимости от пораженной ветви КА и типа кровоснабжения сердца первичный ОИМ локализовался в бассейне ее кровоснабжения и не выходил за его пределы. Однако в 54% наблюдений при изолированном атеросклерозе одной ветви КА ОИМ развивался обширный, площадь его превышала 30%, а в большинстве наблюдений была свыше 50% рабочей поверхности ЛЖ. Локализовался первичный ОИМ не только в бассейне пораженной КА, но и выходил за его пределы. Например, в случаях изолированного атеросклеротического стеноза передней межжелудочковой ветви (ПМЖВ) ОИМ захватывал не только переднюю, боковую стенки левого желудочка, переднюю папиллярную мышцу и межжелудочковую перегородку, но и, нередко, заднюю стенку левого желудочка и заднюю папиллярную мышцу, а также распространялся на миокард правого желудочка. Согласно данным литературы (Смольянников А.В. Наддачина Т.А. 1960, 1963 гг.), при стенозирующем поражении ПМЖВ вблизи от устья главную роль играют коллатерали и анастомозы ее верхушечной, боковой и перегородочной ветвей, которые относятся к межкоронарным. Кровь в дистальные отделы пораженной ПМЖВ поступает главным образом через эти анастомозы, вследствие чего зона кровоснабжения второй, компенсирующей артерии, изменяется или расширяется. По-видимому, в данной ситуации основную нагрузку несет та артерия, которая в большей степени определяет тип кровоснабжения сердца. Также большой интерес представляет анализ локализации повторного ОИМ при изолированном стенозе одной ветви КА. Мы столкнулись с парадоксальным фактом – очаг постинфарктного кардиосклероза находился в бассейне изолированно пораженной КА, в то время как повторный ОИМ имел другую локализацию, т.е. обнаруживался в бассейне кровоснабжения нестенозированной ветви КА. По-видимому, в этих случаях имеет место, описанное в литературе функциональное изменение типа кровоснабжения сердца (Смольянников А.В. Наддачина Т.А. 1960, 1963 гг.). То есть при тромбозе или выраженном стенозе в одной магистральной КА, кровь в ее дистальные отделы может поступать главным образом через межкоронарные анастомозы, вследствие чего зона кровоснабжения второй, компенсирующей артерии, изменяется или расширяется. По-видимому, в данной ситуации основную нагрузку несла хорошо развитая нестенозированная КА.
Анализируя механизмы танатогенеза при ОИМ, 180 летальных исходов были условно разделены на 5 групп по развитию того или иного смертельного осложнения: наружный разрыв сердца (НРС), аритмический шок (АШ), истинный кардиогенный шок (ИКШ), острая левожелудочковая недостаточность (ОЛЖН) и комплекс причин, связанных с декомпенсацией второго основного заболевания (рис. 4).
Рис. 4. Частота смертельных осложнений при ОИМ.
Представленный материал свидетельствует в пользу того, что механизмы танатогенеза при ОИМ во многом определяются его площадью. Необширный ОИМ (до 30% рабочей поверхности ЛЖ) преимущественно завершался НРС (55% наблюдений необширного ОИМ), либо смерть наступала от комплекса причин, связанных с декомпенсацией другого основного заболевания, либо в результате тромбоэмболических осложнений инфаркта миокарда (25%). Средний по площади ОИМ (30-50% рабочей поверхности ЛЖ) преимущественно (67,7%) завершался аритмическим шоком. Обширный ОИМ (более 50% рабочей поверхности ЛЖ) осложнялся ИКШ (71,8%) или ОЛЖН (24,4%).
^ Наружный разрыв сердца (14,4% набл. ОИМ) чаще развивается при необширном (до 30% площади) первичном ОИМ. Прогностически неблагоприятными факторами, способствующими его развитию, следует считать наличие гипертонической болезни или гипертензионного синдрома иного генеза Чаще он возникает у женщин 60-80 лет, имеющих изолированное атеросклеротическое поражение одной из ветвей КА (53,8%) и тромбоз ее просвета (78,6%).
13,3% наблюдений ОИМ составили случаи, причина смерти в которых была многофакторна. т.е. обусловлена сочетанием поражения сократительного миокарда либо с экстракардиальными тромбоэмболическими осложнениями инфаркта, либо с декомпенсацией второго (сочетанного или конкурирующего) основного заболевания (сахарного диабета, хронической обструктивной болезни легких и т.д.). Прогностически неблагоприятными факторами, приведшими к летальному исходу в данной группе, следует считать сочетание таких заболеваний, которыми одновременно страдал умерший и которые, взаимно отягощая друг друга, привели к смерти. В значительном числе случаев (41,7%) площадь первичного ОИМ была менее 30% рабочей поверхности ЛЖ, ни в одном из наблюдений не превысила 50%, чаще он развивался в условиях многососудистого стенозирующего поражения КА с тромбозом просвета в 64,7% наблюдений. В трети наблюдений ОИМ развивался у мужчин в возрасте 50-54-х лет при изолированном атеросклеротическом стенозе одной из ветвей КА и тромбозе ее просвета (85,7%).
Из вышеизложенного следует, что для развития смертельного осложнения при необширном ОИМ (с площадью до 30% рабочей поверхности ЛЖ) недостаточно только поражения сократительного миокарда, необходимы дополнительные факторы и условия, во многом определяющие танатогенез. В связи с этим основным направлением реального снижения летальности у больных с ОИМ менее 30% площади рабочей поверхности ЛЖ является, наряду с консервативной интенсивной терапией ОИМ, устранение гипертензионного синдрома при НРС, ранняя диагностика и интенсивная терапия сочетанных и конкурирующих заболеваний.
В 26,7% всех умерших ОИМ осложнился аритмическим шоком. Площадь его в этих случаях была в пределах 30-50% рабочей поверхности ЛЖ, чаще он развивается у мужчин в возрасте 60-65 лет, при тяжелом неравномерно выраженном стенозирующем атеросклерозе ветвей КА. Во всех этих наблюдениях ОИМ был единственным основным заболеванием, как правило, отсутствовали признаки хронической сердечной недостаточности. Несомненным преимуществом снижения летальности и лечения таких больных ОИМ в блоке кардиореанимации является возможность постоянного контроля над нарушениями ритма и проводимости сердца и немедленное использование другой необходимой аппаратуры.
31,2% всех наблюдений ОИМ составили инфаркты, завершившиеся ИКШ. Прогностически неблагоприятными факторами, приведшими к летальному исходу в данной группе, следует считать: обширный ОИМ (площадью более 50% рабочей поверхности ЛЖ во всех случаях), нередко распространяющийся на миокард правого желудочка, нередко повторный, развивающийся в условиях тяжелого атеросклеротического поражения ветвей КА (75% наблюдений). Как правило, ИКШ развивался при наличии многочисленных других заболеваний, нередко с явлениями их декомпенсации и признаками предсуществующей хронической сердечной недостаточности. Средний возраст умерших составил 63,8 года. Совокупность всех перечисленных факторов определяла закономерно высокую летальность в этой группе.
14,4% всех наблюдений составили инфаркты, осложнившиеся ОЛЖН. Прогностически неблагоприятными факторами, приведшими к летальному исходу в данной группе (57,7%), следует считать обширный, нередко повторный, ОИМ (площадью более 50% рабочей поверхности ЛЖ), развившийся в условиях тяжелого атеросклеротического поражения ветвей КА. В некроз, как правило, вовлечены папиллярные мышцы. ОЛЖН, также как и ИКШ, развивалась при наличии многочисленных других заболеваний, нередко с явлениями их декомпенсации и признаками предсуществующей хронической сердечной недостаточности. Средний возраст умерших составил 64 года. Также как и при ИКШ, все выше перечисленные факторы определяли закономерно высокую летальность в этой группе.
Иные перспективы снижения летальности имеют 25% больных с ИКШ и 42,3% больных с ОЛЖН, развивающихся при ОИМ в условиях изолированного стеноза и тромбоза одной из ветвей КА. Как правило, это мужчины работоспособного возраста, без наличия других тяжелых соматических заболеваний. Наиболее эффективным направлением снижения летальности у данного контингента больных является активное использование современных методов интервенционной кардиологии до развития острого инфаркта миокарда, т.е. профилактически. Только тесная взаимосвязь между кардиологом, рентгенэндоваскулярным хирургом и кардиохирургом, преемственность лечебных мероприятий на всех этапах медицинской помощи могут обеспечить конечный успех лечения.
Данные проведенного морфологического исследования свидетельствуют о том, что темпы формирования демаркационной зоны при ОИМ находятся в зависимости от степени выраженности и распространенности стенозирующего атеросклероза в КА. При необширном (до 30% рабочей поверхности ЛЖ) ОИМ в условиях изолированного атеросклеротического стеноза одной КА демаркационная зона формируется раньше. В последующем при необширном ОИМ (до 30% площади просвета) к концу первого месяца его развития имеются морфологические признаки начальных этапов формирования рубца за счет раннего (после 2-й недели) проникновения отрогов грануляционной ткани с потерей монолитности очага некроза. При многососудистом поражении коронарных артерий демаркационная зона формируется позднее, в основном это относится к больным пожилого и старческого возраста, страдающим полипатиями, нередко с декомпенсацией другого заболевания. К концу первой недели (максимальный срок наблюдений) обширного ОИМ макрофагальная и фибробластическая реакции, как правило, отсутствовали. И только у умерших с изолированным атеросклеротическим стенозом одной КА (как правило, мужчины работоспособного возраста) можно было выявить периваскулярно их начальные проявления.
Мнение врача-патологоанатома о танатогенезе, механизме наступления смерти с учетом клинических и морфологических данных должно излагаться в клинико-анатомическом эпикризе (КАЭ). содержащем суждение врача о причине смерти. КАЭ обязателен в каждом случае, потому что врач-патологоанатом должен попытаться ответить, а клиницист должен найти ответ на вопрос «Почему же умер конкретный больной?», так как именно в ответе на этот вопрос лежит перспектива поиска путей снижения летальности. В КАЭ должны быть отражены: обоснование условий развития смертельного осложнения и последовательность развития других осложнений (танатогенез), оценка своевременности диагностики и лечебных мероприятий, анализ проявлений патоморфоза в связи с проводившимся лечением, осложнения лечения и оценка их роли в танатогенезе, результаты сличения клинического и патологоанатомического диагнозов основного заболевания и смертельных осложнений. Клинико-анатомический эпикриз, помимо установления основного заболевания и его осложнений, должен отражать суждение о типе и механизме смерти. В нем должна быть дана оценка тех факторов, которые явились непосредственной причиной или способствовали ускорению летального исхода.
Выводы
Особенности танатогенеза у каждого умершего от острого инфаркта миокарда определяются патогенетическими механизмами смертельного осложнения, которые в первую очередь обусловлены обширностью поражения сократительного миокарда. Обширный (более 30% рабочей поверхности левого желудочка) острый инфаркт миокарда чаще возникает в условиях тяжелого атеросклеротического стеноза всех ветвей коронарных артерий. Однако локальный атеросклеротический стеноз в одной коронарной артерии (чаще передней межжелудочковой ветви) также может завершаться развитием обширного острого инфаркта миокарда (22,2% набл.). Необширный острый инфаркт миокарда (до 30% площади), как правило, развивается при локальном атеросклеротическом стенозе одной из коронарных артерий.
При развитии необширного острого инфаркта миокарда (22,2% от числа умерших) летальный исход наступает от наружного разрыва сердца (55% набл.), тромбоэмболических осложнений (12%) либо декомпенсации другого заболевания (13%): сахарного диабета, хронической язвы желудка, хронической обструктивной болезни легких и др. При развитии острого инфаркта миокарда с площадью поражения 30-50% рабочей поверхности левого желудочка (34,5% от числа умерших) летальный исход чаще наступает от аритмического шока (68%), либо декомпенсации другого заболевания (19%). При развитии обширного (более 50% рабочей поверхности левого желудочка) острого инфаркта миокарда (43,3% от числа умерших) летальный исход наступает от истинного кардиогенного шока, либо острой левожелудочковой недостаточности.
В 67,8% случаев острый инфаркт миокарда, завершающийся летально, развивается при сочетанном атеросклеротическом стенозе двух либо трех ветвей коронарных артерий, в 32,2% случаев – при изолированном атеросклеротическом стенозе одной из ветвей коронарных артерий, чаще передней межжелудочковой ветви левой коронарной артерии. Частота тромбоза просвета коронарных артерий существенно уменьшается с увеличением числа пораженных ветвей, а также с вовлечением в атеросклеротический процесс средних и дистальных сегментов коронарных артерий и составляет 58,7%. При изолированном стенозе одной из ветвей коронарных артерий она высокая – 82,8% случаев.
Темпы организации острого инфаркта миокарда зависят от площади инфаркта миокарда и от степени выраженности и распространенности стенозирующего атеросклероза в коронарных артериях. При необширном остром инфаркте миокарда она протекает активно. Многососудистое поражение коронарных артерий снижает ее темпы особенно в условиях декомпенсации других соматических заболеваний у лиц пожилого и старческого возраста. У умерших с изолированным атеросклеротическим стенозом одной из ветвей коронарных артерий организация, вне зависимости от обширности острого инфаркта миокарда, выражена.
Практические рекомендации
I. Смертельные осложнения острого инфаркта миокарда развиваются при наличии определенных условий, в профилактике которых лежат пути снижения летальности.
1) Наружный разрыв сердца – как правило, при небольшом первичном остром инфаркте миокарда (площадь до 30% рабочей поверхности левого желудочка), развивающемся при атеросклеротическом стенозе одной коронарной артерии с тромбозом ее просвета, преимущественно у женщин 60-80 лет, во всех случаях – страдающих гипертонической болезнью либо артериальной гипертензией другого генеза и часто с наличием гипертензионного синдрома во время развития острого инфаркта миокарда. Признаки декомпенсации другого соматического заболевания и предсуществующей сердечной недостаточности при этом, как правило, отсутствуют.
2) Аритмический шок – при среднем по площади первичном остром инфаркте миокарда (в пределах 30-50% рабочей поверхности левого желудочка), развивающемся в условиях тяжелого многососудистого поражения коронарных артерий, преимущественно у мужчин в возрасте 60-65 лет. Во всех наблюдениях острый инфаркт миокарда является единственным основным заболеванием, и признаки предсуществующей сердечной недостаточности отсутствуют.
3) Для истинного кардиогенного шока во всех случаях характерен обширный, нередко – повторный, острый инфаркт миокарда (более 50% площади рабочей поверхности левого желудочка), часто с вовлечением миокарда правого желудочка. при тяжелом многососудистом стенозе коронарных артерий. В большинстве случаев истинный кардиогенный шок развивается при декомпенсации других соматических заболеваний (комбинированное основное заболевание), в условиях предсуществующей сердечной недостаточности.
4) Острая левожелудочковая недостаточность чаще возникает при обширном остром инфаркте миокарда (более 50% площади рабочей поверхности левого желудочка), с поражением папиллярных мышц. в половине наблюдений – при тяжелом многососудистом стенозе коронарных артерий. В большинстве случаев острая левожелудочковая недостаточность развивается при декомпенсации других соматических заболеваний (комбинированное основное заболевание), в условиях предсуществующей сердечной недостаточности.
II. Для определения площади при макроскопической оценке острого инфаркта миокарда в практической работе может быть использован метод ориентировочной оценки ее (упрощенный и ускоренный). Принимая за 100% площадь рабочей поверхности левого желудочка (передняя, боковая, задняя стенки и межжелудочковая перегородка), площадь каждой из них составляет 25%. Разделив каждую стенку на три условных сегмента – верхушечный, средний и базальный (≈ по 8%), можно вычислить площадь поражения сократительного миокарда у секционного стола. (Например, острый инфаркт миокарда всей передней стенки левого желудочка и верхушечных сегментов остальных стенок (часто – при локальном проксимальном стенозе и тромбозе передней межжелудочковой ветви левой коронарной артерии): 25%+8%+8%+8%=49% площади рабочей поверхности левого желудочка).
III. Условия развития смертельного осложнения острого инфаркта миокарда в каждом конкретном случае должны быть обсуждены в клинико-анатомическом эпикризе с учетом площади поражения сократительного миокарда, состояния коронарного русла сердца и, что особенно важно, наличия других дополнительных факторов (фонового и (или) сочетанного (конкурирующего) другого основного заболевания, с отражением сроков диагностики и всех возможностей современных методов лечения. Такой полноценный ретроспективный анализ способствует профилактике осложнений острого инфаркта миокарда в последующем, а также обосновывает необходимость обязательного введения рубрики «Клинико-анатомический эпикриз» в патологоанатомический диагноз.
Список работ, опубликованных по теме диссертации
Нефедова Г.А. Галанкина И.Е. Особенности пато- и морфогенеза острого инфаркта миокарда при изолированном стенозирующем атеросклерозе коронарной артерии. // Сб. трудов 1 Московской городской конференции молодых ученых «Медицина на пороге ХХI века, актуальные проблемы и вопросы». М. – 2001. – С. 56 – 57.
Галанкина И.Е. Нефедова Г.А. Особенности танатогенеза и обширность инфаркта миокарда при однососудистом поражении коронарных артерий. // Сб. трудов: Проблемы подострого периода неотложных состояний в кардиологии. М. – 2000. – С. 15 – 19.
Галанкина И.Е. Власов Г.П. Нефедова Г.А. Дейнека К.С. и др. Морфологическая документация возможности трансмиокардиальной лазерной васкуляризации (экспериментальные исследования). // Архив патологии. 2001. – № 3. – С. 35 – 39.
Нефедова Г.А. Галанкина И.Е. Обширность инфаркта миокарда в зависимости от распространенности и степени поражения коронарных артерий. // Сб. трудов: Актуальные проблемы неотложной кардиологии. М. – 2001. – С. 28 – 32.
Нефедова Г.А. Галанкина И.Е. Особенности танатогенеза и обширность инфаркта миокарда в зависимости от распространенности атеросклеротического стенозирования коронарных артерий. // «Архив патологии». – 2004. – № 4. – С. 17 – 20.
Галанкина И.Е. Нефедова Г.А. Патанатомические особенности истинного кардиогенного шока при инфаркте миокарда. // Материалы симпозиума «Патогенез и патологическая анатомия критических, терминальных и постреанимационных состояний». М. – 2003. – С. 23 – 26.
Газарян Г.А. Бранд Я.Б. Захаров И.В. Галанкина И.Е. Санфирова Е.Ю. Природова О.Ф. Нефедова Г.А. Чепкий Д.А. Спасский А.А. Долгов И.М. Голиков А.П. Сроки и степень восстановления кровотока в инфарктзависимой артерии, течение и прогноз заболевания у больных с первичным инфарктом миокарда. // Сб. трудов: Современные подходы диагностики и лечения острого коронарного синдрома. М. – 2003. – С. 4 – 7.
Нефедова Г.А. Галанкина И.Е. Особенности танатогенеза при остром инфаркте миокарда в свете поиска путей снижения летальности. // Сб. трудов: 85-летие патологоанатомической службы НИИ СП им. Н.В. Склифосовского. М. – 2005. – С. 68 – 75.
Нефедова Г.А. Анализ смертельных исходов при остром инфаркте миокарда в свете поиска путей снижения летальности. // Материалы Второго Российского съезда интервенционных кардиоангиологов. М. – Международный журнал интервенционной кардиоангиологии. – 2005. – № 7. – С. 67.
Нефедова Г.А. Особенности танатогенеза при комбинации острого инфаркта миокарда с другими заболеваниями. // Сб. трудов: Эндоваскулярные коронарные вмешательства при острых проявлениях ишемической болезни сердца. М. – 2005. – С. 40 – 42.
Нефедова Г.А. Галанкина И.Е. Механизмы развития смертельных осложнений при остром инфаркте миокарда. // Труды II Российского съезда патологоанатомов. М. – 2006. – Т. 2. – С. 128 – 131.
Соискатель Нефедова Г.А.