Экстрасистолия
Экстрасистолы — это самая распространенная аритмия. Экстрасистолы возникают как у больных, так и у практически здоровых людей. Частой причиной является стресс, переутомление, под действием кофеина, табака и алкоголя.
Статистической нормой для здорового человека считается до 200 наджелудочковых и 200 желудочковых экстрасистол в сутки. У некоторых здоровых людей отмечается гораздо больше экстрасистол — до нескольких десятков тысяч в сутки.
Сами по себе экстрасистолы совершенно безопасны. Их называют «косметические аритмии». Однако, у лиц с органическим поражением сердца (постинфарктный кардиосклероз, гипертрофия миокарда) наличие экстрасистол является дополнительным прогностически неблагоприятным фактором.
Экстрасистолия — дифференциальный диагноз
Экстрасистолия — преждевременные сокращения сердца, обусловленные возникновением импульса вне синусового узла.
Этиологический дифференциальный диагноз экстрасистолии затруднен, особенно если экстрасистолия является ведущим синдромом, или когда заболевание начинается с экстрасистолии, а другие признаки отсутствуют.
Целесообразно разграничение экстраситолии на функциональные и органические.
Функциональные экстрасистолы
— возникают у молодых, практически здоровых людей, но нередко с невротическими расстройствами или признаками вегетативной дисфункции.
Они появляются в покое, при отрицательных эмоциях, после физической нагрузки могут прекратиться.
Чаще всего больной ощущает экстрасистолы, что становится дополнительным психотравмирующим фактором.
По данным ЭКГ экстрасистолы обычно желудочные, монотопные, отсутствуют постэкстрасистолические изменения интервала ST и зубца Т.
Органические экстрасистолы
— возникают обычно у лиц старше 50 лет, при тщательном обследовании у них можно выявить признаки заболеваний сердца, хронических интоксикаций, эндокринных расстройств.
Экстрасистолы появляются после физической нагрузки, в покое исчезают или урежаются. Больные в большинстве случаев их не ощущают.
Электрокардиографически это различные по топике экстрасистолы — предсердные, атриовентрикулярные, желудочковые, политопные, групповые.
Экстрасистолы высоких градаций практически всегда органические.
Функциональные экстрасистолы наблюдаются у курильщиков, лиц, употребляющих в большом количестве крепкий чай или кофе.
Так называемые «психогенные» экстрасистолы бывают у больных со скрытой, ларвированной депрессией. Они возникают преимущественно или только по утрам в соответствии с суточными колебаниями настроения, при пробуждении, по пути на работу, особенно в ожидании значимых для больного конфликтных ситуаций.
Прекращаются при перемене обстановки, в периоды эмоционального подъёма, во время отпуска.
Условно к функциональным экстрасистолам можно отнести те, которые развиваются вследствие патологических висцеро-кардиальных рефлексов — у больных с заболеванием брюшной полости, лёгких, средостения.
Окончательно убедиться в рефлекторном происхождении экстрасистолии можно при её исчезновении после излечения больного от основного заболевания, что не всегда возможно.
Необходимо подчеркнуть, что диагноз функциональной экстрасистолии можно поставить лишь после тщательного обследования больного для исключения органических причин.
Наиболее вероятными причинами изолированной органической экстрасистолии в молодом возрасте является миокардит, у лиц среднего и пожилого возраста — ИБС, атеросклеротический кардиосклероз; во всех случаях стойкой экстрасистолии необходимо помнить о тиреотоксикозе.
Экстрасистолия как ведущий синдром характерна для лёгких, очаговых форм миокардита. Другие его признаки надо тщательно искать.
К ним прежде всего относятся указания больного о перенесённом незадолго до появления экстрасистол острого респираторного заболевания, ангины.
С помощью эхографии можно выявить начальные признаки нарушения сократительной способности миокарда.
Большое значение придаётся ферментной диагностике — у больных миокардитом закономерно повышается активность некоторых ферментов и изоферментов — ЛДГ и ЛДГ1, КФК и МВ-КФК.
Если экстрасистолия является ведущим проявлением ИБС, необходимо искать атипичные проявления стенокардии напряжения, признаки нарушения питания миокарда на ЭКГ, особенно при мониторировании, после велоэргометрии, чреспищеводной стимуляции, некоторых фармакологических проб.
При подозрении на тиреотоксикоз следует исследовать содержание тиреоидных гормонов Т3 и Т4, что сразу позволяет подтвердить или исключить этот диагноз.
Терапия
С помощью приема антиаритмических препаратов можно устранить экстрасистолы, но после отмены препаратов экстрасистолия возобновляется.
Кроме того, самое главное, у лиц с органическим поражением сердца на фоне эффективного лечения экстрасистолии антиаритмическими препаратами выявлено увеличение смертности более, чем в 3 раза! Только при лечении бета-блокаторами или амиодароном не было отмечено повышения риска смертности. Однако, у ряда больных наблюдались осложнения, включая опасные для жизни.
При этом, назначение бета-блокаторов оказывает довольно слабое антиаритмическое действие, а прием амиодарона является высокоэффективным, но сопровождается частым возникновением побочных эффектов.
Эффективность и безопасность применения препаратов калия и магния или т.н. «метаболических» препаратов окончательно не установлены.
Предсердные экстрасистолы
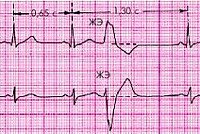
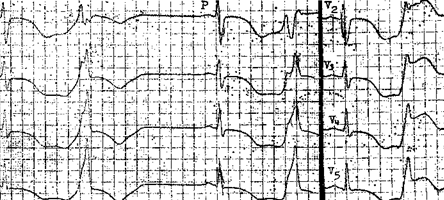
Внеочередной несинусовый зубец P, за которым следует нормальный или аберрантный комплекс QRS. Интервал PQ — 0,12—0,20с. Интервал PQ ранней экстрасистолы может превышать 0,20с. Причины: бывают у здоровых лиц, при усталости,стрессе, у курильщиков, под действием кофеина и алкоголя, при органических поражениях сердца,легочном сердце. Компенсаторная пауза обычно неполная (интервал между пред- и постэкстрасистолическим зубцами P меньше удвоенного нормального интервала PP).
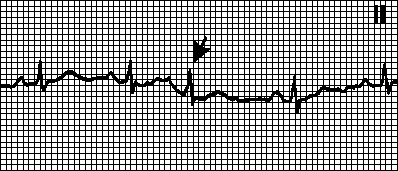
Блокированные предсердные экстрасистолы
Внеочередной несинусовый зубец P, за которым не следует комплекс QRS. Через «атриовентрикулярный» АВ-узел, находящийся в периоде рефрактерности, предсердная экстрасистола не проводится. Экстрасистолический зубец P иногда наслаивается на зубец T, и распознать его трудно; в этих случаях блокированную предсердную экстрасистолу ошибочно принимают за синоатриальную блокаду или остановку синусового узла.
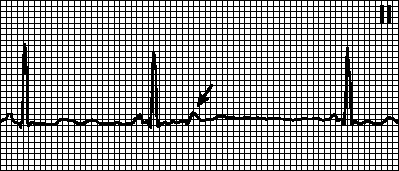
АВ-узловые экстрасистолы
Внеочередной комплекс QRS с ретроградным (отрицательным в отведениях II, III, aVF) зубцом P, который может регистрироваться до или после комплекса QRS либо наслаиваться на него. Форма комплекса QRS обычная; при аберрантном проведении может напоминать желудочковую экстрасистолу. Причины: бывают у здоровых лиц и при органических поражениях сердца. Источник экстрасистолии — «атриовентрикулярный» АВ-узел. Компенсаторная пауза может быть полной или неполной.
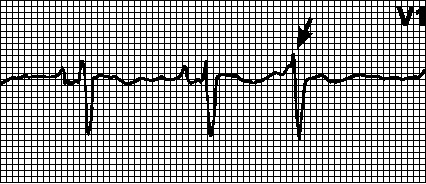
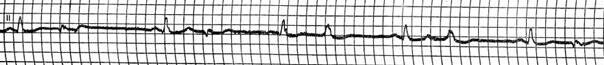
Желудочковые экстрасистолы
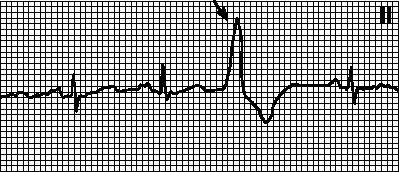
Внеочередной, широкий ( 0,12с) и деформированный комплекс QRS. Сегмент ST и зубец T дискордантны комплексу QRS. Зубец P может быть не связан с экстрасистолами («атриовентрикулярный» АВ-диссоциация) либо быть отрицательным и следовать за комплексом QRS (ретроградный зубец P). Компенсаторная пауза обычно полная (интервал между пред- и постэкстрасистолическим зубцами P равен удвоенному нормальному интервалу PP).
Реабилитация сердца по Бутейко
Август Ревзон
Два года назад мы с женой, как обычно, проводили лето в деревеньке Бредки, что затаилась в северо-западных лесах Тверской области. Ягод и грибов было видимо-невидимо. И мы без устали занимались сбором и заготовкой этих даров природы.
И вот лето закончилось, стали мы готовиться к отъезду домой. Собрались и что же видим? Баки и целлофановые мешки в рюкзаках с груздями, волнушками и лисичками потрясающей засолки, герметично упакованные ведра с «живой» земляникой и черникой. Вместительные коробки с перебранной брусникой. Емкости с сушеными грибами и травами. Всего-то 30 мест.
Увы, в назначенный срок машина, заранее оговоренная, не приходит. А это значит, что уезжать придется на перекладных. С приключениями добираемся до станции, потом — поезд, потом, уже в Москве, перебежками от него до такси. Так добираемся до дома. С трудом заносим свою поклажу на наш второй этаж.
Под душем мне делается плохо. Сильно кружится голова. Жена вовремя подхватывает меня под руки и укладывает на диван. Ощущаю то бешеное учащение пульса, то его резкое замедление. Сердце кувыркается в груди и работает, как неисправный мотор захудалого трактора. «Скорая помощь» доставляет меня, пока еще тепленького, в больницу.
Врачи ставят диагноз — мерцательная аритмия. В старину ее называли «бредом сердца» (какая поразительно удачная ассоциация с моими Бредками!). Болезнь эта характеризуется фибрилляцией (мерцанием) предсердий и несогласованностью сокращений предсердий и желудочков сердца. Для нее типичны спонтанно возникающие приступы, чередующиеся светлыми промежутками правильного синусового ритма.
Медикам довольно быстро удалось снять приступы аритмии и завести мой «мотор», поэтому уже на второй день я поднялся с постели. Через три недели я был дома и мог самостоятельно провести курс реабилитации.
Главные причины моей болезни были очевидны. После погони за дарами леса и финальных дорожных мытарств налицо было явное физическое и психоэмоциональное перенапряжение. К тому же все события разворачивались на фоне давно заработанных атеросклеротических изменений в сердце (они иногда давали о себе знать незначительным стенокардическими болями). Короче говоря, стало ясно, что дальнейшие «шутки» с сердцем плохи, а для реабилитации понадобится целый комплекс мер.
Начал с питания. Резко ограничил употребление сливочного масла и соли, так как натрий является антагонистом калия, столь необходимого при сердечных коллизиях. Сделал акцент на употребление содержащих калий продуктов: печеного картофеля, кураги, бананов, абрикосов, черники.
Для выведения лишнего холестерина ввел в свой рацион отруби, добавляя их в каши. Старался больше употреблять овощей и зелени. Ежедневно ем чеснок (2—3 зубчика). Его очищающие сосуды свойства широко известны.
Очень пригодилась брусника. Употреблял ее в разных вариантах (как гарнир к мясным и рыбным блюдам, просто с чаем). С ее помощью снизил уровень протромбина со 100 единиц (верхняя граница для мужчин) до 80, сделав кровь жиже. И всего-то за один месяц без всякого аспирина.
Подключил и фитотерапию. Лечебных трав мы набрали в деревне предостаточно. Использовал такой сбор: мята — 10 г, подорожник — 20 г, пустырник — 20 г, брусничный лист — 20 г, бессмертник — 20 г, семя льна — 20 г, шиповник (толченый) — 50 г. 2 ст. ложки смеси заваривал вечером в пол-литровом термосе и оставлял томиться на ночь. По полстакана теплого отвара пил 3 раза в день за 15—20 минут до еды. На следующий год, летом в деревне, готовил салаты из сныти, медуницы и листьев одуванчика (с добавлением вареного яйца и репчатого лука), ел без ограничения землянику и чернику.
Теперь перехожу к своей двигательно-дыхательной терапии, сыгравшей, на мой взгляд, одну из решающих ролей в моей реабилитации.
На страницах нашего журнала я уже не раз называл себя давним сторонником системы дыхания по К. Бутейко. Дело в том, что гипоксия (недостаток кислорода), создаваемая искусственным затруднением дыхания, расширяет сосуды благодаря избыточному насыщению крови углекислым газом. А это в моем случае было важно для устранения сосудистых спазмов, лечения и надежной профилактики мерцательной аритмии.
Используя идеи К. Бутейко, я разработал и стал применять в повседневной ходьбе три алгоритма дыхания.
Легкий: 3+6+6+3. Расшифровываю: на 3 шага — полный вдох, на 6 шагов — пауза (задержка дыхания), еще на 6 шагов — полный выдох и далее на 3 шага — пауза.
Средней трудности. 3+6+6+6. Здесь заключительная пауза увеличена по сравнению с предыдущим алгоритмом до 6 шагов.
Трудный: 3+8+8+3. На 3 шага — полный вдох, на 8 шагов — пауза, еще 8 шагов — полный выдох и далее на 3 шага — пауза.
Начал, конечно, с двух первых алгоритмов. А месяца через два вкрапливал в ходьбу и последнее сочетание движений и дыхания. Все дыхательные упражнения выполнял до тех пор, пока не испытывал потребности отдышаться, что делал, не прибегая к гипервентиляции, а за счет спокойного, сдержанного дыхания по К. Бутейко.
Уже через три месяца после выписки из больницы я приступил к полноценной аэробной тренировке, состоящей из чередования обычной ходьбы и бега трусцой на носовом дыхании. При этом в ходьбе часто использовал первый алгоритм дыхания. В беге же, как всегда, на 3 шага — вдох, на 4 — выдох. Такие смешанные тренировки продолжительностью 30—40 минут проводил через день.
Постепенно я расширял перечень аэробных упражнений. Это были катание на велосипеде и лыжах по равнине, домашнее плавание — аквааэробика в своем персональном бассейне с морской водой (моя статья «Примите ванну за бассейн» опубликована в «ФиС», 2004, № 10) и бег трусцой с лыжными палками (моя статья «Из осени в зиму. на лыжных палках», «ФиС», 2006, № 10).
На этом, собственно, и заканчивается история с мерцательной аритмией. Приведенные алгоритмы дыхания использую и теперь — хорошая штука для профилактики, опробированная на собственном сердце.
Правда, в прошлом году пришлось познакомиться еще с одной разновидностью сердечных аритмий. Как это ни смешно (а скорее грустно!), виной тому была одна из моих безуспешных попыток убедить собственную жену в пользе дыхания по Бутейко. Испытать, к примеру, когда у нее разыгрывается мигрень, ну уж совсем легкий, на мой взгляд, алгоритм дыхания — 3+4+4+3.
«Галя, — как-то говорю ей на прогулке, — это же так просто. Я же не предлагаю тебе длительную задержку дыхания. Вот смотри, я ее сейчас сделаю». После обычного вдоха делаю на паузе 30 медленных шагов. Реакция со стороны жены нулевая. Наскоро отдышавшись, выполняю 40 неспешных шагов. Но опять реакции никакой! Аргументы, видно, не убедительны.
Тогда, переведя дух, отваживаюсь на 50 шагов. Жена несколько удивлена моей живучестью. Я же чувствую себя неважно. Ощущаю какие-то перебои в работе сердца и одышку. Понимаю, что допустил принципиальную ошибку, о которой ведь предупреждал К. Бутейко. Глубоко дышать после затянутой паузы опасно. Я же после трех запальчиво-азартных и следующих друг за другом заходов (с прогрессивно нарастающим кислородным долгом!) бдительность как-то утратил.
Электрокардиограмма выявила картину экстрасистолии напряжения. При этой сердечной патологии вслед на нормальной систолой (то есть сокращением сердца или его отделов) следует добавочная. Этакая «выскочка». Это и есть экстрасистола. А вслед за ней обычно наступает компенсаторная пауза. Более продолжительная, так как после экстрасистолы очередное сокращение сердца выпадает.
Пальпаторно (например, нащупав пульс на левой руке) я стал ощущать экстрасистолу даже при, казалось бы, легкой физической нагрузке. При небольшом ускорении в ходьбе или медленном подъеме по лестнице на свой второй этаж.
«Ну что, несчастный экспериментатор, популяризатор бутейковских идей, — бичевал я себя, — мало тебе эпопеи с мерцательной аритмией? Вот борись теперь и с экстрасистолической!»
Я вновь использовал почти весь арсенал средств, задействованных в лечении мерцательной аритмии, но кое-что откорректировал и добавил.
В фитотерапию включил боярышник, антиаритмические свойства которого известны со времен древнеримского врача Диоскорида. Летом в деревне приналег на землянику, которая тоже полезна при экстрасистолии.
Пользуясь тем, что экстрасистолу можно «ловить» пальпаторно, стал ежедневно выполнять комплекс упражнений, согласовывая движения с ритмом сердца и до первой экстрасистолы.
Итак, нащупываем пульс на шее или левой руке (прекрасно, что экстрасистолы пока нет!) и приступаем к выполнению простых упражнений.
1. Стоя, ноги вместе, чуть-чуть согнув колени. Высокие поднимания на носки, вытягиваясь «в струнку» вверх с последующим акцентированным, в заданном сердцем метрономном режиме, опусканием на пятки и незначительным сгибанием коленей, ударно посылая к сердцу ножной кровоток. Порция за порцией! Ритмично! Блокируя самозарождение экстрасистолы.
2. Стоя, ноги вместе. Неглубокие полуприседания.
3. Стоя, ноги врозь, левая рука отведена в сторону (правая-то на пульсе). Повороты туловища влево-вправо.
4. Стоя, ноги врозь. Наклоны вперед и возвращение в и. п.
5. Лежа на спине. «Велосипед».
В синусовом ритме можно выполнять и другие простейшие упражнения, а также ходьбу по ровной и слегка пересеченной местности.
В своей двигательно-дыхательной терапии по Бутейко ограничился использованием первых двух алгоритмов: 3+6+6+3 и 3+6+6+6. Причем на второй алгоритм переходил только после освоения — без экстрасистолы — первого.
• В лечебно-оздоровительной ходьбе с успехом использовал и метод прерывистого (порциального) дыхания бийского врача В. Дурыманова. Сочетание этого дыхания и шагов выглядело так. Короткий прерывистый (но в итоге — полный диафрагмально-грудной) вдох через нос делал в три приема, а акцентированный полнейший выдох («чтобы живот прилип к спине») через чуть приоткрытый рот — в четыре. Паузы во время и по завершении вдоха и выдоха заполнялись тремя шагами ходьбы. Схематично весь алгоритм прерывистого дыхания можно представить так: 1/3 вдоха + 3 шага на паузе + 1/3 вдоха + 3 шага на паузе + 1/3 вдоха + 3 шага на паузе + 1/4 выдоха + 3 шага на паузе + 1/4 выдоха + 3 шага на паузе + 1/4 выдоха + 3 шага на паузе + 1/4 выдоха + 3 шага на паузе и т. д.
Через полгода я вновь вышел на привычный для себя уровень двигательной активности. Мне уже не нужно было во время зарядки или разминки держать руку на пульсе, так как каждое упражнение я уже испытал «на прочность». Оно не должно было провоцировать появление экстрасистолы ни темпом движений, ни величиной физических усилий. В итоге, не выдержав настойчивых, методичных атак, моя экстрасистола куда-то сгинула.
Вот на этой оптимистичной ноте и завершаю свой, надеюсь, поучительный рассказ о том, как можно довольно легко и быстро заработать (из-за форс-мажорных обстоятельств или собственного легкомыслия) серьезные сердечные недуги, а затем уже долгим и далеко не легким, кропотливым и каждодневным трудом избавиться от них. Как не пасть духом и все-таки добиться того, чтобы аритмия перестала мерцать, а пульс — выпадать. Мне это, к счастью, удалось.
Август РЕВЗОН, кандидат педагогических наук
ЭКСТРАСИСТОЛИЯ: клиническое значение, диагностика и лечение
РЕКЛАМА
Экстрасистолами называют преждевременные комплексы (преждевременные сокращения), выявляемые на ЭКГ. По механизму возникновения преждевременные комплексы подразделяются на экстрасистолы и парасистолы. Различия между экстрасистолией и парасистолией являются чисто электрокардиографическими или электрофизиологическими. Клиническое значение и лечебные мероприятия при экстрасистолии и парасистолии абсолютно одинаковы. По локализации источника аритмии электросистолы разделяют на наджелудочковые и желудочковые.
Экстрасистолы, несомненно, являются самым распространенным нарушением ритма сердца. Они часто регистрируются и у здоровых лиц. При проведении суточного мониторирования ЭКГ статистической «нормой» экстрасистол считается примерно до 200 наджелудочковых экстрасистол и до 200 желудочковых экстрасистол в сутки. Экстрасистолы могут быть одиночными или парными. Три и более экстрасистолы подряд принято называть тахикардией («пробежки» тахикардии, «короткие эпизоды неустойчивой тахикардии»). Неустойчивой тахикардией называют эпизоды тахикардии продолжительностью менее 30 с. Иногда для обозначения 3–5 экстрасистол подряд используют определение «групповые», или «залповые», экстрасистолы. Очень частые экстрасистолы, особенно парные и рецидивирующие «пробежки» неустойчивой тахикардии, могут достигать степени непрерывно-рецидивирующей тахикардии, при которой от 50 до 90% сокращений в течение суток составляют эктопические комплексы, а синусовые сокращения регистрируются в виде единичных комплексов или коротких кратковременных эпизодов синусового ритма.
В практической работе и научных исследованиях основное внимание уделяют желудочковой экстрасистолии. Одной из наиболее известных классификаций желудочковых аритмий является классификация B. Lown и M. Wolf (1971).
- Редкие одиночные мономорфные экстрасистолы — менее 30 в час.
- Частые экстрасистолы — более 30 в час.
- Полиморфные экстрасистолы.
- Повторные формы экстрасистол: 4А — парные, 4Б — групповые (включая эпизоды желудочковой тахикардии).
- Ранние желудочковые экстрасистолы (типа «R на Т»).
Предполагалось, что высокие градации экстрасистол (классы 3–5) являются наиболее опасными. Однако в дальнейших исследованиях было установлено, что клиническое и прогностическое значение экстрасистолии (и парасистолии) практически целиком определяется характером основного заболевания, степенью органического поражения сердца и функциональным состоянием миокарда. У лиц без признаков поражения миокарда с нормальной сократительной функцией левого желудочка (фракция выброса больше 50%) экстрасистолия, включая эпизоды неустойчивой желудочковой тахикардии и даже непрерывно-рецидивирующей тахикардии, не влияет на прогноз и не представляет опасности для жизни. Аритмии у лиц без признаков органического поражения сердца называют идиопатическими. У больных с органическим поражением миокарда (постинфарктный кардиосклероз, дилатация и/или гипертрофия левого желудочка) наличие экстрасистолии считается дополнительным прогностически неблагоприятным признаком. Но даже в этих случаях экстрасистолы не имеют самостоятельного прогностического значения, а являются отражением поражения миокарда и дисфункции левого желудочка.
В 1983 г J. T. Bigger предложил прогностическую классификацию желудочковых аритмий.
- Безопасные аритмии — любые экстрасистолы и эпизоды неустойчивой желудочковой тахикардии, не вызывающие нарушений гемодинамики, у лиц без признаков органического поражения сердца.
- Потенциально опасные аритмии — желудочковые аритмии, не вызывающие нарушений гемодинамики, у лиц с органическим поражением сердца.
- Опасные для жизни аритмии («злокачественные аритмии») — эпизоды устойчивой желудочковой тахикардии, желудочковые аритмии, сопровождающиеся нарушениями гемодинамики, или фибрилляция желудочков. У больных с опасными для жизни желудочковыми аритмиями, как правило, имеется выраженное органическое поражение сердца (или «электрическая болезнь сердца», например синдром удлиненного интервала Q–T, синдром Бругада).
Однако, как было отмечено, независимого прогностического значения желудочковая экстрасистолия не имеет. Сами по себе экстрасистолы в большинстве случаев безопасны. Экстрасистолию даже называют «косметической» аритмией, подчеркивая этим ее безопасность. Даже «пробежки» неустойчивой желудочковой тахикардии тоже относят к «косметическим» аритмиям и называют «энтузиастическими выскальзывающими ритмами» (R. W. Campbell, K. Nimkhedar, 1990). В любом случае лечение экстрасистолии с помощью антиаритмических препаратов (ААП) не улучшает прогноз. В нескольких крупных контролируемых клинических исследованиях было выявлено заметное повышение общей смертности и частоты внезапной смерти (в 2–3 раза и более) у больных с органическим поражением сердца на фоне приема ААП класса I, несмотря на эффективное устранение экстрасистол и эпизодов желудочковой тахикардии. Наиболее известным исследованием, в котором впервые было выявлено несоответствие клинической эффективности препаратов и их влияния на прогноз, является исследование CAST. В исследовании CAST («исследование подавления аритмий сердца») у больных, перенесших инфаркт миокарда, на фоне эффективного устранения желудочковой экстрасистолии препаратами класса I С (флекаинид, энкаинид и морицизин) выявлено достоверное увеличение общей смертности в 2,5 раза и частоты внезапной смерти в 3,6 раза по сравнению с больными, принимавшими плацебо. Результаты исследования заставили пересмотреть тактику лечения не только пациентов с нарушениями ритма, но и кардиологических больных вообще. Исследование CAST является одним из основных в становлении «медицины, основанной на доказательствах». Только на фоне приема β- адреноблокаторов и амиодарона отмечено снижение смертности больных с постинфарктным кардиосклерозом, сердечной недостаточностью или реанимированных пациентов. Однако положительное влияние амиодарона и особенно β-адреноблокаторов не зависело от антиаритмического действия этих препаратов.
Выявление экстрасистолии (как и любого другого варианта нарушений ритма) является поводом для обследования, направленного прежде всего на выявление возможной причины аритмии, заболевания сердца или экстракардиальной патологии и определения функционального состояния миокарда.
ААП не излечивают от аритмии, а только устраняют ее на период приема препаратов. При этом побочные реакции и осложнения, связанные с приемом практически всех препаратов, могут быть гораздо более неприятными и опасными, чем экстрасистолия. Таким образом, само по себе наличие экстрасистолии (независимо от частоты и «градации») не является показанием для назначения ААП. Бессимптомные или малосимптомные экстрасистолы не требуют проведения специального лечения. Таким больным показано диспансерное наблюдение с проведением эхокардиографии примерно 2 раза в год для выявления возможных структурных изменений и ухудшения функционального состояния левого желудочка. Л. М. Макаров и О. В. Горлицкая (2003) при длительном наблюдении за 540 больными с идиопатической частой экстрасистолией (более 350 экстрасистол в час и более 5000 в сутки) выявили у 20% больных увеличение полостей сердца («аритмогенная кардиомиопатия»). Причем более часто увеличение полостей сердца отмечалось при наличии предсердной экстрасистолии.
Показания для лечения экстрасистолии:
- очень частые, как правило, групповые экстрасистолы, вызывающие нарушения гемодинамики;
- выраженная субъективная непереносимость ощущения перебоев в работе сердца;
- выявление при повторном эхокардиографическом исследовании ухудшения показателей функционального состояния миокарда и структурных изменений (снижение фракции выброса, дилатация левого желудочка).
Лечение экстрасистолии
Необходимо объяснить больному, что малосимптомная экстрасистолия безопасна, а прием антиаритмических препаратов может сопровождаться неприятными побочными эффектами или даже вызвать опасные осложнения. Прежде всего необходимо устранить все потенциально аритмогенные факторы: алкоголь, курение, крепкий чай, кофе, прием симпатомиметических препаратов, психоэмоциональное напряжение. Следует немедленно приступить к соблюдению всех правил здорового образа жизни.
При наличии показаний для назначения ААП у больных с органическим поражением сердца используют β-адреноблокаторы, амиодарон и соталол. У больных без признаков органического поражения сердца, кроме этих препаратов, применяют ААП класса I: Этацизин, Аллапинин, Пропафенон, Кинидин Дурулес. Этацизин назначают по 50 мг 3 раза в день, Аллапинин — по 25 мг 3 раза в день, Пропафенон — по 150 мг 3 раза в день, Кинидин Дурулес — по 200 мг 2–3 раза в день.
Лечение экстрасистолии проводят методом проб и ошибок, последовательно (по 3–4 дня) оценивая эффект приема антиаритмических препаратов в средних суточных дозах (с учетом противопоказаний), выбирая наиболее подходящий для данного больного. Для оценки антиаритмического эффекта амиодарона может потребоваться несколько недель или даже месяцев (применение более высоких доз амиодарона, например по 1200 мг/сут, может сократить этот период до нескольких дней).
Эффективность амиодарона в подавлении желудочковых экстрасистол составляет 90–95%, соталола — 75%, препаратов класса I C — от 75 до 80% (B. N. Singh, 1993).
Критерий эффективности ААП — исчезновение ощущения перебоев, улучшение самочувствия. Многие кардиологи предпочитают начинать подбор препаратов с назначения β-адреноблокаторов. У больных с органическим поражением сердца при отсутствии эффекта от β-адреноблокаторов применяют Амиодарон, в том числе в комбинации с первыми. У больных с экстрасистолией на фоне брадикардии подбор лечения начинают с назначения препаратов, ускоряющих ЧСС: можно попробовать прием пиндолола (Вискен), эуфиллина (Теопек) или препаратов класса I (Этацизин, Аллапинин, Кинидин Дурулес). Назначение холинолитических препаратов типа белладонны или симпатомиметиков менее эффективно и сопровождается многочисленными побочными явлениями.
В случае неэффективности монотерапии оценивают эффект комбинаций различных ААП в уменьшенных дозах. Особенно популярны комбинации ААП с β-адреноблокаторами или амиодароном.
Есть данные, что одновременное назначение β-адреноблокаторов (и амиодарона) нейтрализует повышенный риск от приема любых антиаритмических средств. В исследовании CAST у больных, перенесших инфаркт миокарда, которые наряду с препаратами класса I C принимали β-адреноблокаторы не было отмечено увеличения смертности. Более того, было выявлено снижение частоты аритмической смерти на 33%!
Особенно эффективна комбинация β-адреноблокаторов и амиодарона. На фоне приема такой комбинации наблюдалось еще большее снижение смертности, чем от каждого препарата в отдельности. Если ЧСС превышает 70–80 уд./мин в покое и интервал P–Q в пределах 0,2 с, то проблемы с одновременным назначением амиодарона и β-адреноблокаторов нет. В случае брадикардии или АВ-блокады I–II степени для назначения амиодарона, β-адреноблокаторов и их комбинации необходима имплантация кардиостимулятора, функционирующего в режиме DDD (DDDR). Есть сообщения о повышении эффективности антиаритмической терапии при сочетании ААП с ингибиторами АПФ, блокаторами рецепторов ангиотензина, статинами и препаратами омега-3-ненасыщенных жирных кислот.
Некоторые противоречия существуют в отношении применения амиодарона. С одной стороны, некоторые кардиологи назначают амиодарон в последнюю очередь — только при отсутствии эффекта от других препаратов (считая, что амиодарон довольно часто вызывает побочные явления и требует длительного «периода насыщения»). С другой стороны, возможно, более рационально начинать подбор терапии именно с амиодарона как наиболее эффективного и удобного для приема препарата. Амиодарон в малых поддерживающих дозах (100–200 мг в день) редко вызывает серьезные побочные явления или осложнения и является скорее даже более безопасным и лучше переносимым, чем большинство других антиаритмических препаратов. В любом случае при наличии органического поражения сердца выбор небольшой: β-адреноблокаторы, амиодарон или соталол. При отсутствии эффекта от приема амиодарона (после «периода насыщения» — как минимум по 600–1000 мг/сут в течение 10 дней) можно продолжить его прием в поддерживающей дозе — 0,2 г/сут и, при необходимости, оценить эффект последовательного добавления препаратов класса I С (Этацизин, Пропафенон, Аллапинин) в половинных дозах.
У больных с сердечной недостаточностью заметное уменьшение количества экстрасистол может отмечаться на фоне приема ингибиторов АПФ и Верошпирона.
Следует отметить, что проведение суточного мониторирования ЭКГ для оценки эффективности антиаритмической терапии утратило свое значение, так как степень подавления экстрасистол не влияет на прогноз. В исследовании CAST выраженное увеличение смертности отмечено на фоне достижения всех критериев полного антиаритмического эффекта: уменьшения общего количества экстрасистол более чем на 50%, парных экстрасистол — не менее чем на 90% и полное устранение эпизодов желудочковой тахикардии. Основным критерием эффективности лечения является улучшение самочувствия. Это обычно совпадает с уменьшением количества экстрасистол, а определение степени подавления экстрасистолии не имеет значения.
В целом последовательность подбора ААП у больных с органическим заболеванием сердца, при лечении рецидивирующих аритмий, включая экстрасистолию, можно представить в следующем виде.
- β-адреноблокатор, амиодарон или соталол.
- Амиодарон + β-адреноблокатор.
- Комбинации препаратов:
- β-адреноблокатор + препарат класса I;
- амиодарон + препарат класса I С;
- соталол + препарат класса I С;
- амиодарон + β-адреноблокатор + препарат класса I С.
У больных без признаков органического поражения сердца можно использовать любые препараты, в любой последовательности или использовать схему, предложенную для больных с органическим заболеванием сердца.
Краткая характеристика ААП
β-адреноблокаторы. После исследования CAST и опубликования результатов метаанализа исследований по применению ААП класса I, в котором было показано, что практически все ААП класса I способны увеличивать смертность у больных с органическим поражением сердца, β-адреноблокаторы стали самыми популярными антиаритмическими препаратами.
Антиаритмический эффект β-адреноблокаторов обусловлен именно блокадой β-адренергических рецепторов, т. е. уменьшением симпатико-адреналовых влияний на сердце. Поэтому β-адреноблокаторы наиболее эффективны при аритмиях, связанных с симпатико-адреналовыми влияниями — так называемые «катехоламинзависимые» или «адренергические аритмии». Возникновение таких аритмий, как правило, связано с физической нагрузкой или психоэмоциональным напряжением.
Катехоламинзависимые аритмии в большинстве случаев одновременно являются «тахизависимыми», т. е. возникают при достижении определенной критической частоты сердечных сокращений, например во время физической нагрузки частая желудочковая экстрасистолия или желудочковая тахикардия возникают только при достижении частоты синусового ритма 130 сокращений в минуту. На фоне приема достаточной дозы β-адреноблокаторов больной не сможет достичь частоты 130 уд./мин при любом уровне физической нагрузки, таким образом предотвращается возникновение желудочковых аритмий.
β-адреноблокаторы являются препаратами выбора для лечения аритмий при врожденных синдромах удлинения интервала Q–T.
При аритмиях, не связанных с активацией симпатической нервной системы β-адреноблокаторы гораздо менее эффективны, но добавление β-адреноблокаторов нередко значительно увеличивает эффективность других антиаритмических препаратов и снижает риск аритмогенного эффекта ААП класса I. Препараты класса I в сочетании с β-адреноблокаторами не увеличивают смертность у больных с им поражением сердца (исследование CAST).
При так называемых «вагусных» аритмиях β-адреноблокаторы оказывают аритмогенное действие. «Вагусные» аритмии возникают в состоянии покоя, после еды, во время сна, на фоне урежения ЧСС («брадизависимые» аритмии). Вместе с тем в некоторых случаях при брадизависимых аритмиях эффективно применение пиндолола (Вискен) — β-адреноблокатора с внутренней симпатомиметической активностью (ВСА). Кроме пиндолола к β-адреноблокаторам с ВСА относятся окспренолол (Тразикор) и ацебутолол (Сектраль), однако в максимальной степени внутренняя симпатомиметическая активность выражена именно у пиндолола.
Дозы β-адреноблокаторов регулируют в соответствии с антиаритмическим эффектом. Дополнительным критерием достаточной β-блокады является снижение ЧСС до 50 уд./мин в состоянии покоя. В прежние годы, когда основным β-адреноблокатором был пропранолол (Анаприлин, Обзидан), известны случаи эффективного применения пропранолола при желудочковых аритмиях в дозах до 960 мг/сут и более, например до 4 г в день! (R. L. Woosley et al. 1979).
Амиодарон. Амиодарон таблетки 0,2 г. (оригинальным препаратом является Кордарон) обладает свойствами всех четырех классов ААП и, кроме того, оказывает умеренное a-блокирующее действие. Амиодарон, несомненно, является самым эффективным из существующих антиаритмических препаратов. Его даже называют «аритмолитическим препаратом».
Основным недостатком амиодарона является высокая частота экстракардиальных побочных эффектов, которые при длительном приеме наблюдаются у 10–75% больных. Однако необходимость в отмене амиодарона возникает у 5–25% (J. A. Johus et al. 1984; J. F. Best et al. 1986; W. M. Smith et al. 1986). К основным побочным эффектам амиодарона относятся: фотосенсибилизация, изменение цвета кожи, нарушение функции щитовидной железы (как гипотиреоз, так и гипертиреоз), повышение активности печеночных трансаминаз, периферические нейропатии, мышечная слабость, тремор, атаксия, нарушения зрения. Большинство этих побочных эффектов обратимы и исчезают после отмены или при уменьшении дозы амиодарона. Гипотиреоз можно контролировать с помощью приема левотироксина. Наиболее опасным побочным эффектом амиодарона является поражение легких («амиодароновое поражение легких») — возникновение интерстициального пневмонита или, реже, легочного фиброза. У большинства больных поражение легких развивается только при длительном приеме сравнительно больших поддерживающих доз амиодарона — более 400 мг/сут. Такие дозы крайне редко применяют в России. Поддерживающая доза амиодарона в России обычно составляет 200 мг/сут или даже меньше (по 200 мг в день 5 дней в неделю). B. Clarke и соавторы (1985) сообщают лишь о трех случаях из 48 наблюдений возникновения этого осложнения на фоне приема амиодарона в дозе 200 мг в сутки.
В настоящее время изучается эффективность дронедарона, деривата амиодарона без йода. Предварительные данные свидетельствуют об отсутствии экстракардиальных побочных эффектов у дронедарона.
Соталол. Соталол (Соталекс, Сотагексал) таблетки 160 мг применяется в средней суточной дозе 240–320 мг. Начинают с назначения 80 мг 2 раза в день. При рефрактерных аритмиях иногда используют прием соталола до 640 мг/сут. β-адреноблокирующее действие соталола проявляется начиная с дозы 25 мг.
На фоне приема соталола имеется повышенный риск развития желудочковой тахикардии типа «пируэт». Поэтому прием соталола желательно начинать в стационаре. При назначении соталола необходимо тщательно контролировать величину интервала Q–T, особенно в первые 3 дня. Корригированный интервал Q–T не должен превышать 0,5 с. В этих случаях риск развития тахикардии типа «пируэт» менее 2%. С увеличением дозы соталола и степени удлинения интервала Q–T значительно увеличивается риск развития тахикардии типа «пируэт». Если корригированный интервал Q–T превышает 0,55 с — риск тахикардии типа «пируэт» достигает 11%. Поэтому при удлинении интервала Q–T до 0,5 с необходимо уменьшить дозу соталола или отменить препарат.
Побочные эффекты соталола соответствуют типичным побочным эффектам β-адреноблокаторов.
Этацизин. Этацизин таблетки 50 мг. Наиболее изученный отечественный препарат (создан в СССР). Для лечения аритмий применяется с 1982 г. Быстрое достижение клинического эффекта позволяет с успехом использовать Этацизин у лиц без органического поражения сердца для лечения желудочковых и наджелудочковых нарушений ритма: экстрасистолии, всех вариантов пароксизмальных и хронических тахиаритмий, в том числе мерцательной аритмии, при синдроме Вольфа–Паркинсона–Уайта. Наиболее эффективен Этацизин у пациентов с ночными аритмиями, а также при желудочковой экстрасистолии.Средняя суточная доза Этацизина составляет 150 мг (по 50 мг 3 раза в день). Максимальная суточная доза — 250 мг. При назначении этацизина для предупреждения рецидивирования мерцательной аритмии, наджелудочковых и желудочковых тахикардий его эффективность, как правило, превосходит эффективность других АПП класса I. Препарат хорошо переносится, необходимость в отмене возникает примерно у 4% больных. Основные побочные эффекты: головокружение, головная боль, «онемение» языка, нарушение фиксации взора. Обычно побочные реакции наблюдаются сравнительно редко, и их выраженность уменьшается после первой недели приема Этацизина.
Аллапинин. Отечественный препарат Аллапинин, таблетки 25 мг (создан также в СССР) применяется в клинической практике с 1986 г. Назначают по 25–50 мг 3 раза в день. Максимальная суточная доза составляет 300 мг. Аллапинин довольно эффективен при наджелудочковых и желудочковых аритмиях. Основные побочные явления — головокружение, головная боль, нарушение фиксации взора. Необходимость в отмене возникает примерно у 6% больных. Одной из особенностей аллапинина и теоретически его недостатком является наличие β-адреностимулирующего действия.
Пропафенон (Ритмонорм, Пропанорм), таблетки 150 мг, ампулы 10 мл (35 мг). Назначают по 150–300 мг 3 раза в день. При необходимости дозу увеличивают до 1200 мг/сут. Пропафенон, кроме замедления проведения, слегка удлиняет рефрактерные периоды во всех отделах сердца. Кроме того, пропафенон обладает небольшим β-адреноблокирующим действием и свойствами антагонистов кальция.
К основным побочным эффектам пропафенона относятся головокружение, нарушение фиксации взора, атаксия, тошнота, металлический вкус во рту.
Хинидин. В настоящее время в России используют в основном Кинидин Дурулес, табл. по 0,2 г. Разовая доза составляет 0,2–0,4 г, средняя суточная доза — от 0,6 до 1,0 г. Максимальная суточная доза хинидина в прежние годы (когда хинидин был основным антиаритмическим препаратом) достигала 4,0 г! В настоящее время такие дозы не используются и примерной максимальной суточной дозой хинидина можно считать 1,6 г.
В небольших дозах (600–800 мг/сут) хинидин хорошо переносится. Побочные явления возникают обычно при более высоких дозах. К наиболее частым побочным эффектам при приеме хинидина относятся нарушения функции желудочно-кишечного тракта: тошнота, рвота, понос. Реже отмечаются головная боль, головокружения, ортостатическая гипотония. Самое опасное осложнение от приема хинидина — возникновение желудочковой тахикардии типа «пируэт». По данным литературы, это осложнение наблюдается у 1–3% больных, принимающих хинидин.
П. Х. Джанашия. доктор медицинских наук, профессор
С. В. Шлык. доктор медицинских наук, профессор
Н. М. Шевченко. доктор медицинских наук, профессор