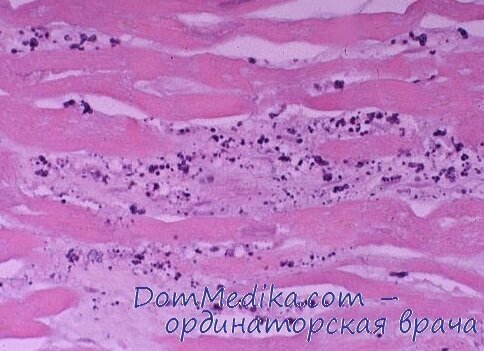
Инфаркт миокарда
16. Инфаркт миокарда
Способность принимать любую нагрузку близко к сердцу
Инфаркт миокарда возникает в результате закупорки коронарных артерий (рис. 22). Если прерывается кровообращение, то пораженная сеть сердечных сосудов перестает получать кислород; это приводит к разрушению тканей сердечной мышцы. В медицинской литературе приводятся следующие факторы риска: наследственная предрасположенность, повышенное содержание жиров в крови (холестерин, триглицериды), повышенное систолическое и диастолическое кровяное давление, курение, избыточная масса тела и малоподвижный образ жизни.
Инфаркт миокарда обычно случается внезапно, иногда даже при физическом покое, часто даже ночью. Почти всегда он сопровождается сильными болями. Однако бывают и «немые» инфаркты, которые протекают безболезненно и могут быть замечены только по преходящей слабости и недомоганию.
Транскультурный аспект и эпидемиология
С 1987 г. в Германии ежегодно коронарной болезнью сердца заболевали около 500 000 человек, из них 250 000 переносили инфаркт миокарда, от которого умирают примерно 100 000 человек.
Статистика ВОЗ фиксирует отчетливый рост ишемической болезни сердца в различных европейских странах. Исследование, проведенное в 7 странах показало, согласно данным Keys (1970), различную частоту коронарной болезни сердца. По данным Европейской Согласительной конференции (EEC), ежегодно в Германии можно было бы избежать при помощи превентивных мероприятий около 10 500 инфарктов, что составляет 23 % всех случаев. Если раньше соотношение между заболевшими мужчинами и женщинами было 4:1, то в последние годы риск заболевания изменился к новому соотношению 1,3:1. Различные авторы объясняют это возросшим числом женщин, выполняющих типично мужскую работу и связанным с этим стрессорным фактором.
Обзор литературы
Уже Siebeck (1949) и Weizsacker (1949) допускали, что психический фактор наряду с органическим может играть роль в возникновении инфаркта миокарда.
Dunbar (1948) на основании глубиннопсихологического анализа был составлен типичный личностный профиль пациента с коронарными заболеваниями. Подобные особенности обнаружили Roscnman и Friedman (1968) в проспективном эпидемиологическом исследовании.
Пословицы и народная мудрость
Принимать близко к сердцу; это разрывает мне сердце; сердце разрывалось от радости; этот груз лежит у меня на сердце, чистосердечно признаться; удар в самое сердце.
Притча: «Нужное слово»
Смотри ч.1, гл. 3.
Аспекты самопомощи: развитие инфаркта миокарда с точки зрения позитивной психотерапии.
Наблюдение, что люди с отдельными факторами риска или вообще без них также могут страдать инфарктом миокарда и что, напротив, люди несмотря на факторы риска, могут не подвергнуться инфаркту, способствовало появлению первого сомнения в чисто соматической природе этого заболевания. Было сделано предположение, что и физические факторы риска могут иметь психическую предысторию (ср. напр. Kornitzer et al. 1982). Предпочитаемой сферой переработки конфликтов у пациентов с инфарктом миокарда является тело. Оно полностью поставлено на службу концепции достижения. Фирма, партия или другие институты часто занимают при этом место межличностных отношений. Контакты в этой связи имеют значение только тог’да, когда они важны для стремления к профессиональному росту или социальному признанию. Установку по отношению к настоящей жизни и к будущему можно охарактеризовать как «постояннуюозабоченность» и «требующую какой-либо активности». При анализе ситуации в семье пациентов с инфарктом миокарда часто обнаруживается недостаток материнской любви, обусловленный разлукой или смертью. По отношению к отцу выясняется, что он не являлся авторитетом или помощником. Отношения родителей между собой нередко характеризовались конфликтом доминантности. Общение с людьми вне семьи было ограниченным. Надежда родителей концентрировалась на достижениях детей. Как чутко и разнообразно сердце реагирует на чувство, очень хорошо подмечено людьми и отражено в различных крылатых выражениях. При инфаркте миокарда можно сказать, что у человека «разбивается сердце».
#image.jpg
Практическое дополнение к этому аспекту самопомощи содержится в опроснике в конце этой главы.
Трудности при проведении обезболивания у пациентов с инфарктом миокарда
Основные проблемы обезболивания при инфаркте миокарда:
— побочные эффекты наркотических анальгетиков (угнетение дыхания, тошнота, нарушения гемодинамики);
— недостаточный анальгетический эффект;
— отсутствие наркотических средств (отсутствие разрешения на применение наркотических анальгетиков);
— особые состояния, не поддающиеся традиционным методам лечения (медлешготекущий разрыв миокарда).
Побочные эффекты при использовании наркотических анальгетиков прежде всего проявляются угнетением дыхания, тошнотой, реже артериальной гипотензией.
Угнетение дыхания может развиваться вследствие неправильного выбора препарата или его дозы (не учтены возраст пациента, сопутствующие заболевания, осложнения, предшествующая или сопутствующая терапия и т. п.). В подавляющем большинстве случаев нарушение дыхания обусловлено быстрым
внутривенным введением наркотического анальгетика, причем вероятность нарушения дыхания возрастает при применении наркотических анальгетиков в сочетании с транквилизаторами (диазепам). Однако несмотря на угнетение дыхания больные, как правило, остаются доступными для словесного контакта, поэтому прежде всего следует попытаться использовать команды "вдох — выдох".
Применять для стимуляции дыхания дыхательные аналепти-ки (кордиамин, коразол и др ) недопустимо!
Чрезвычайно редко для восстановления дыхания может потребоваться назначение специфического антагониста наркотических анальгетиков налоксона.
Налоксон (нарканти) — конкурентный антагонист опиоидов без морфиноподобной активности. Налоксон блокирует связывание агонистов и агонистов-антагонистов или вытесняет их из опиатных (прежде всего |х) рецепторов.
При выраженной депрессии дыхания налоксон вводят внут ривенно медленно (в течение 3 мин) в дозе 0,4 мг. Нормализация дыхания начинается через 2-3 мин, уменьшение степени угнетения сознания происходит значительно позже. При недостаточном эффекте инъекции налоксона по 0,4 мг повторяют до нормализации дыхания (до 4 мг/ч). Следует учитывать, что продолжительность действия налоксона меньше, чем у опиатов, и нарушения дыхания могут возобновляться.
Артериальная гипотензия чаще встречается при применении морфина. Вероятность ее возникновения увеличивается при ги-поволемии, нижнем инфаркте миокарда, поражении правого желудочка, а также у пациентов пожилого возраста.
Недостаточная анальгетическая эффективность, как правило, является следствием неадекватного выбора препарата, его дозы или способа применения. В качестве примера можно привести назначение наркотических анальгетиков с умеренной болеутоляющей активностью (промедол) молодым пациентам с сильной болью, введение анальгетиков подкожно или внутримышечно и пр. В ряде случаев недостаточный анальгетический эффект обусловлен особой тяжестью боли, связанной с медлен-нотекущим разрывом сердечной мышцы (см. ниже).
Необходимо иметь в виду, что даже при полноценном обезболивании у пациентов могут оставаться ощущения дискомфорта в грудной клетке (так называемые остаточные боли). При этом
к остаточным можно относить только слабые болевые ощущения ограниченной локализации, без иррадиации, гемодинамических или моторной реакций. Больные характеризуют такие ощущения словом "наболело". Во избежание развития тяжелых побочных эффектов не следует стремиться к получению абсолютного (100 %) болеутоляющего эффекта. Чрезвычайно важно предупреждать пациентов о необходимости сообщать о любых изменениях болевых ощущений!
Если боль не укладывается в рамки остаточной, то нужно принять дополнительные меры. Прежде всего, анальгетичес-кую активность наркотических анальгетиков можно усилить с помощью нейролептиков и транквилизаторов, а при артериальной гинертензии с помощью клонидина. Имеет значение использование ненаркотических анальгетиков, особенно анальгина.
Анальгин. Болеутоляющая активность анальгина при выраженном ангинозном статусе у пациентов молодого и среднего возраста явно недостаточна. При этом анальгин отчетливо потенцирует действие других обезболивающих средств, что является общим свойством препаратов этого класса [Варрасси Дж. Пироли А. 1995]. Поэтому при инфаркте миокарда анальгин может быть показан либо для потенцирования действия наркотических анальгетиков (особенно на фоне артериальной гипотен-зии), либо самостоятельно при исходно слабой боли у пациентов старческого возраста. В этих случаях внутривенное введение анальгина в дозе 2,5 г с 10 мг диазепама может оказаться достаточно эффективным. Дополнительное внутривенное введение 5000 ЕД гепарина заметно усиливает болеутоляющую активность анальгина. Анальгин может устранить перикардиальную боль, а нередко — и боль при ранней постинфарктной стенокар дии. У некоторых больных внутривенное введение анальгина сопровождается легкой эйфорией.
У пациентов с сохраняющейся артериальной гипертеизией для потенцирования анальгетической активности наркотических анальгетиков эффективно внутривенное введение клонидина (клофелипа).
Клонидин (клофелин) — гипотензивный препарат, стимулятор а2 -адренорецепторов ЦНС. Помимо основного гипотензивного действия клофелин обладает обезболивающей и седа-тивной активностью, устраняет эмоционально-аффективные,
моторные и гемодинамические реакции на боль. Наши совместные исследования применения клофслина в остром периоде инфаркта миокарда [Зайцев А. А. и соавт. 1988; Кузнецова О. Ю. и соавт. 1990] доказали, что медленное внутривенное введение 0,1 мг препарата (1 мл 0,01 % раствора) через 5-10 мин приводило к полному подавлению или значительному уменьшению боли. У всех пациентов отмечался выраженный седативный эффект. Гипотензивное действие препарата проявлялось только при повышенном уровне артериального давления, уменьшение ЧСС было также прямо пропорционально его исходной величине.
Безусловно, наличие самостоятельной (адренергической) анальгетической активности у клофелина не следует понимать как основание для замены традиционных наркотических анальгетиков. Болеутоляющее действие клофелина при инфаркте миокарда необходимо использовать только для потенцирования действия наркотических анальгетиков у больных с сохраняющейся артериальной гипертензией.
Наши дальнейшие наблюдения подтвердили, что особенно ярко проявляется болеутоляющая активность клофелина на фоне предшествующего применения наркотических анальгетиков. В этих случаях у подавляющего большинства пациентов удавалось достичь полноценного обезболивания.
Отсутствие наркотических анальгетиков обычно обусловлено тем, что нет соответствующего разрешения на использование наркотических лекарственных средств (невозможно обеспечить требуемые условия хранения, негосударственные лечебные учреждения и пр.). В этих случаях для экстренного обезболивания приходится использовать лекарственные препараты, которые не находятся на специальном учете.
Буторфанол (стадол, морадол) — агонист-антагонист опи-атных рецепторов. По нашим данным, стадол в дозе 2 мг при медленном внутривенном введении с 2,5-5 мг дроперидола эффективен при ангинозной боли у 76,5 % больных с инфарк том миокарда (в 60 % случаев эффект был хорошим, в 16,5 % — удовлетворительным). Обезболивающее действие стадола при внутривенном введении начинает развиваться через 2 мин, достигает максимума к 10-20-й минуте и продолжается до 2-4 ч. Во избежание угнетения дыхания препарат (особенно пожилым пациентам) необходимо вводить внутривенно медленно и
дробно (за 2 приема в течение 5 мин). Учитывая влияние ста-дола на кровообращение [Авруцкий М. Я. и соавт, 1994; Ли-товченко В С, 1994], назначение его прежде всего показано больным с инфарктом нижней локализации и синдромом "брадикардия—гипотензия". При необходимости применения стадола у пациентов с артериальной гипертензией увеличивают дозу дроперидола. Болеутоляющее действие стадола может быть усилено дополнительным назначением анальгина, а при артериальной гипертензии — клонидина. Следует особо подчеркнуть, что эффективность и безопасность буторфанола зависят от фирмы-изготовителя. При остром инфаркте миокарда используют буторфанол исключительно (!) при отсутствии возможности применения традиционных наркотических средств.
Болеутоляющее действие трамадола при ангинозной боли несколько слабее, чем буторфанола, а введение препарата в вену нередко вызывает тошноту. Хотя этот побочный эффект можно предотвратить предварительным внутривенным введением диа-зепама, болеутоляющая активность трамадола при инфаркте миокарда часто недостаточна.
Боль при медленнотекущем разрыве сердечной мышцы. Серьезная проблема при обезболивании возникает в случае осложнения инфаркта миокарда медленнотекущим разрывом сердечной мышцы. При этой разновидности боли полноценного обезболивания добиться чрезвычайно трудно.
Как показали исследования, проведенные на кафедре неотложной медицины СПбМАПО [Михайлович В. А. и соавт. 1990], в этих случаях (при соответствующей квалификации врача!) методом выбора является перидуральиая анестезия на уров не Thin _! V с использованием малых доз наркотических анальгетиков (фентанил).
На догоспитальном этапе временный результат может быть получен с помощью внутривенного введения малых доз кеталара.
Кеталар (кетамин). При невозможности проведения периду-ральной анестезии, уверенности в диагнозе и соответствующей квалификации врача приходится вводить субнаркотические дозы препарата для общей анестезии — кетамина. По методике, разработанной на кафедре неотложной медицины СПбМАПО [Кузнецова О. Ю. Ландер Н. М. 1989], для этого 50 мг кетамина и 10 мгдиазепама в 100 мл изотонического раствора натрия хлорида вводят внутривенно капельно, начиная со скорости 50-60 кап/мин и снижая ее по мере наступления эффекта. Средняя скорость инфузии составляет 0,04 мг/<�кг X мин), а общая доза кетамина, необходимая для обезболивания,— 0,75 мг/кг. Значительно менее эффективно назначение наркотических анальгетиков и натрия оксибутирата. Натрия оксибутират вводят внутривенно в дозе до 40 мг/кг в течение 5-10 мин.
При остаточных и перикардиальных болях интенсивное обезболивание обычно не требуется. При этом очень важно предупредить больного о необходимости сообщать о любых изменениях болевых ощущений. На пике перикардиальной боли, а также при умеренном усилении остаточной назначают ненаркотические анальгетики: анальгин 2,5 г (5 мл 50 % раствора) в сочетании с диазепамом (седуксен, реланиум) в дозе 5-10 мг.
При болях, связанных с ранней постинфарктной стенокардией, лечение начинают с сублингвального назначения 0,5 мг нитроглицерина, показана оксигенотерапия. При необходимости проводят коррекцию артериального давления и ЧСС. Если боль сохраняется, то внутривенно вводят 2,5 г анальгина в сочетании с 5-10 мг диазепама. Болеутоляющий эффект анальгина усиливает внутривенное введение 5000 ЕД гепарина, а при артериальной гипертензии — ОД мг клонидина. При тяжелом приступе стенокардии сразу назначают наркотические анальгетики.
В заключение нельзя не остановиться на возможности использования при инфаркте миокарда закиси азота.
Закись азота при ангинозном статусе недостаточно эффективна, а масочная методика обезболивания плохо переносится пациентами. Закись азота целесообразно применять только в качестве дополнения к нейролептанальгезии, особенно при возобновлении или усилении ангинозной боли в процессе транспортировки.
Обезболивание закисью азота должно начинаться с ингаля ции чистого кислорода в течение 5 мин (денитрогенизация), после чего подается закись азота с кислородом в соотношении 3. 1, а затем 1. 1; в конце необходима ингаляция чистого кислорода в течение 5 мин.
Возможные варианты обезболивания при различных видах болевого синдрома у пациентов с острым инфарктом миокарда обобщены в табл. 6.2.

Результат поиска
1. Сестринское дело в клинике внутренних болезней 5
1.1 Научные теории сестринского дела 5
1. 2.Понятие сестринского процесса 8
2. Особенности реабилитации при инфаркте миокарда 15
2.2.Характеритсика заболевания 15
2.2.Реабилитация при инфаркте миокарда 17
2.3. Особенности работы медсестры с больными, перенесшими инфаркт миокарда 22
Заключение 27
Список использованной литературы 29
Приложение 30
Введение
Главным понятием в сестринском деле является сестринский процесс. Эта реформаторская концепция родилась в США в середине 50-х годов и за почти пять десятилетий апробации в клинических условиях полностью доказала свою целесообразность. В настоящее время сестринский процесс является сердцевиной сестринского образования и практики, создавая научную базу сестринской помощи.
Известно большое количество моделей сестринского дела, но наиболее значимые из них: В. Хендерсон, Д. Орэм, К. Рой, Д. Джонсон, Н. Роупер и др. В каждой модели авторы по-разному видят:
— пациента, как объект деятельности сестринского персонала;
— направленность сестринского вмешательства;
— цель ухода;
— способы сестринского вмешательства;
— роль сестры;
— оценку качества и результатов ухода.
Единой модели на сегодняшний день нет, это мешает взаимопониманию в обучении медсестер и их практической деятельности, особенно у нас, где реформирование сестринского дела только начинается. Модель сестринского ухода — это средство, которое помогает медсестре при обследовании пациента выбрать цели и сестринское вмешательство.
В нашей стране получила развитие модель ухода В. Хендерсон, которая рассматривает пациента в целом, считая его независимым совершенным существом, имеющим 14 фундаментальных потребностей. Чтобы жить, быть здоровым и счастливым, люди нуждаются в пище, воздухе, сне и т. д. Эти потребности человек удовлетворяет на протяжении всей своей жизни. Обеспечиваются они функцией различных органов и систем организма. А. Маслоу разработал одну из теорий потребностей человека. Удовлетворены жизненные потребности человека — значит, не будет проблем. В уходе за пациентом медсестра должна ежедневно выявлять проблемы пациента и способствовать их ликвидации. Модели сестринского дела (ухода) по-разному определяют роль медсестры в сестринском процессе. В России общепринята врачебная модель сестринского ухода, где медсестра только технический исполнитель, в других моделях ухода медсестра самостоятельный член лечебной бригады, а в некоторых моделях она сочетает зависимую от врача роль с независимой.
Поэтому, чтобы быть едиными в осуществлении характеристик алгоритма сестринского вмешательства в лечебных учреждениях, нужно четко представлять, что такое сестринский процесс.
Инфаркт миокарда — обусловленное ишемической болезнью сердца заболевание, в основе которого лежит острое нарушение кровообращения по одной или нескольким коронарным (венечным) артериям с развитием очагового повреждения, некроза (инфаркта) сердечной мышцы (миокарда), что клинически проявляется выраженной, длительной (30 и более минут) и плохо поддающейся лечению болью за грудиной с возможным развитием одного или нескольких жизненно опасных состояний. К ним следует отнести сердечную недостаточность, нарушения сердечного ритма и проводимости, кардиальный шок, остановку сердца, внезапную смерть.
Данное заболевание требуют выхаживания и последующей реабилитации пациентов, поэтому тема данной работы является достаточно актуальной и востребованной. Целью данной работы является исследование особенностей реабилитации при инфаркте миокарда. Объект исследования — сестринский процесс. Предмет – его особенности при инфаркте миокарда. Задачи:
-рассмотреть понятие сестринского процесса, его основные этапы
-изучить составляющие реабилитационного процесса при инфаркте миокарда.
1. Сестринское дело в клинике внутренних болезней
1.1 Научные теории сестринского дела
Если содержание процесса или явления слишком вели¬ко и абстрактно, тогда оно заменяется моделью, которая облегчает его изучение и анализ. Различают политические модели, экономические, социальные, медицинские и т. д. Медицинская модель существует на протяжении веков, она ориентирована на заболевание, когда усилия врача на¬правлены на постановку диагноза и лечение патологиче¬ского состояния. Все его внимание сосредоточено на по¬иске и лечении отклонений, дисфункций и дефектов. Боль¬шинство видов деятельности врача — лечение, преподава¬ние или научно-исследовательская работа, так или иначе направлены на различные аспекты заболеваний и недугов.
Модель сестринского дела ориентирована на человека, а не на болезнь. Эта модель должна быть приложима к нуж¬дам пациентов, их семей и общества, предоставлять меди¬цинским сестрам широкий выбор ролей и функций для работы не только с больными и умирающими пациентами, но и со здоровым контингентом населения. Модели сестринской помощи отражают существующую действительность, дают возможность сравнивать различные концепции сестринского дела на протяжении длительного времени.
Например, до XIX века сестринское дело было сведено к уходу за пациентом. Как правило, не было никаких попыток активно повлиять на течение болезни. Модель сестринского дела, сложившаяся в США в конце XIX
начале XX века, отражает деятельность Флоренс Найтингейл, которая считала, что состояние пациента можно улучшить, воздействуя на окружающую обстановку, для этого обеспечивался свежий воздух, тепло, свет, питание и соответствующая гигиена. Постепенно эти факторы стали важными для всех, а не только для больных, это заложило основы профилактики.
С развитием медицинской помощи многие обязанности врача стали переходить к медицинской сестре (измерение температуры, артериального давления, выполнение ряда про¬цедур и т. д.). Кроме ухода за пациентом, сестра принимает активное участие в реабилитации и профилактике. В связи с этим появились другие модели сестринской помощи. В каж¬дой модели отражаются мировоззрения и убеждения меди¬цинских сестер, занимающихся се построением.
В настоящее время в мировой практике сестринского дела насчитывается более 30 концептуальных моделей сестринской помощи. Они содержат следующие основные положения: определение пациента, источник проблем пациента, приоритетная задача сестры, роль сестры, фокус вмешательства, способы вмешательства, ожидаемый результат.
Наибольшее распространение получили пять моделей: эволюционно-адаптационная (Канадская Ассоциация сестер), добавочно-дополняющая (Хендерсон), модель поведенческой системы (Джонсон), адаптационная модель (Рай); модель дефицита самоухода (Орэм).
Эволюционно-адаптационная модель рассматривает пациента как личность, индивидуум. Источником проблем пациента являются настоящие или будущие изменения в его жизни, особенно в ее критические периоды, которые оказывают негативное влияние на состояние здоровья. Приори¬тетной задачей сестры является оказание помощи пациенту в достижении и поддержании оптимального уровня здоровья в критические периоды жизни. Здесь сестра выступает в роли наставника-координатора. Фокусом вмешательства медицин¬ской сестры являются способы адаптации пациента к окру-жающей обстановке во время происходящих изменений в его жизни, требующие усилия или изменения для поддержа¬ния оптимального уровня здоровья. Способы вмешательства медсестры включают применение различных способов сти¬мулирования пациента. Ожидаемый результат — достижение оптимального уровня здоровья пациента в критические пе-риоды его жизни.
Следующая модель рассматривает пациента как пове¬денческую систему. Источником проблем пациента является функциональный и структурный стресс. Приоритетная задача сестры в данной модели — обеспечение равновесия поведенческой системы и функциональной стабильности пациента. Медсестра выступает в роли регулятора и кон-тролера. Фокусом вмешательства сестры являются меха¬низмы контроля и регуляции, а также требования, предъявляемые к пациенту — Способы вмешательства подразуме¬вают действия предупреждающие, защищающие, сдержи¬вающие и расслабляющие пациента в ситуациях функци¬онального или структурного стресса. Ожидаемый резуль¬тат — адекватное поведение пациента в ответ на стрессо¬вую ситуацию.
Адаптационная модель рассматривает пациента как челове¬ка, находящегося в постоянном взаимодействии с окружающей средой и приспосабливающегося к ней с помощью различных адаптационных способов. Источником проблем пациента является дефицит активности (пассивность) в ре-зультате имеющегося заболевания. Приоритетной задачей медицинской сестры является обучение пациента адаптироваться к окружающей обстановке в период болезни. Сестра играет роль педагога-организатора. Фокусом вмешатель¬ства является использование всевозможных способов стиму¬лирования пациента обучению приспосабливанию к окружа¬ющей его обстановке. Способы сестринского вмешательства и ожидаемый результат — адаптация нациста в результате адекватного восприятия применяемых стимулов.
Модель дефицита самоухода рассматривает пациента как существо, обеспечивающее деятельность по самообслужи¬вани.
**************************************************************