Мозговой инсульт и ночной сон
Мозговой инсульт (МИ), развиваясь в различные периоды цикла сон — бодрствование, является классической иллюстрацией медицины сна. Статистика свидетельствует о том, что в течение суток МИ распределяется следующим образом: от 0 до 6 ч — 17%, от 6 до 12 ч — 46%, от 12 до 18 ч — 20%, от 18 до 24 ч — 17%. По данным Pressman и соавт. (1995), от 25 до 45% случаев МИ встречается в ночное время. По результатам наших исследований, распределение МИ представляется таким образом: утреннее время — 45%, днем — 32% и во время ночного сна — 23%. Некоторые авторы особое внимание уделяют временному переходу "конец ночного сна — начало утра". Первые несколько часов после пробуждения являются особенно опасными в плане возникновения инсульта.
Несмотря на очевидную связь МИ со сном и ранним постсомническим периодом, до сих пор эти взаимоотношения остаются наименее изученными в клинике цереброваскулярной патологии. Большинство проведенных исследований носит характер чисто клинических наблюдений, в которых наряду с характерными для МИ неврологическими изменениями описываются различные расстройства в цикле сон — бодрствование. С развитием полиграфических методов исследования в неврологии появилась возможность объективного регистрирования особенностей ночного сна у больных, перенесших МИ. Особую динамику исследованиям в этом направлении дала развиваемая проф. А. М. Вейном особая отрасль медицины — медицина сна.
Объективное изучение ночного сна у больных МИ представляет не только академический интерес, но также имеет достаточно серьезное практическое значение в плане лечебных, реабилитационных мероприятий, вопросов прогноза. Расстройства в структуре ночного сна являются одним из факторов, приводящих к возникновению МИ. По нашим данным, незначительные, клинически не определяемые изменения мозговой гемодинамики (в сторону улучшения или же ухудшения), имеют свое отражение в особенностях структуры сна у больных МИ. Обнаружение у коматозных больных отдельных сонных феноменов, в частности периодов десинхронизации, сопровождающихся быстрыми движениями глаз и снижением мышечного тонуса, указывает на относительную сохранность стволово-диэнцефальных структур мозга, что прогностически является благоприятным фактором.
Для всех форм и стадий МИ облигатны грубые расстройства механизмов как генерации сна и его стадий, так и их поддержания, проявляющиеся в сокращении длительности сна, частых пробуждениях, продолжительных сегментах бодрствования и дремоты среди ночи, дисбалансе между отдельными стадиями. Причиной этого являются не только повреждение и гибель мозговой ткани локального характера, но и расстройства общей и местной гемодинамики, возникновение отека и смещения вещества головного мозга, попадание крови в ликворные пути, и как следствие — раздражение различных структур, находящихся в пределах ствола мозга. Факторами, оказывающими наибольшее влияние на ночной сон, являются характер, размер, локализация процесса, стадии развития заболевания. Геморрагический инсульт по сравнению с ишемическим приводит к наиболее грубым расстройствам ночного сна. Это проявляется в резком сокращении продолжительности сна, частых и длительных пробуждениях, увеличении представленности первой стадии. Однако при благоприятном исходе заболевания степень восстановления структуры сна происходит быстрее, чем при ишемическом инсульте. Это объясняется тем, что в отличие от ишемического инсульта, при котором имеет место очаг некротического распада ткани головного мозга, при геморрагии повреждение происходит вследствие расслоения структур мозга излившейся кровью. Поэтому восстановление как клинической картины, так и ночного сна происходит относительно лучше.
С развитием нейровизуализационных методов исследования появилась возможность более точно определять размер очага поражения, глубины его нахождения. Размер очага МИ играет существенную роль в формировании расстройств сна. Крупный очаг приводит к распространенному отеку полушария головного мозга, иногда даже противоположного, возникновению процессов сдавления ствола. Логичны наиболее грубые расстройства сна при крупных очагах МИ, что было подтверждено нами в проведенных исследованиях. Исследования также показали, что максимальная приближенность очага к срединным структурам и ликвороносным путям, т. е. медиальное расположение процесса приводит к более грубым расстройствам сна. При этом отмечают не только количественные, а также и качественные изменения в структуре сна. Так, медиальный очаг с захватом таламических структур характеризуется исчезновением на стороне поражения "сонных веретен" (электроэнцефалографических признаков II стадии сна). Латерально расположенные процессы сопровождаются относительно негрубыми расстройствами сна.
Острейшая стадия инсульта (1-я неделя) характеризуется целым рядом клинических и полисомнографических особенностей. Клинически это наличие грубых, трудно контролируемых гемодинамических, общемозговых и локальных неврологических процессов. В зависимости от направления развития болезни при полисомнографии отмечается различная картина. Грубые расстройства сознания (сопор, кома), как правило, сопровождаются диффузной медленноволновой активностью, исключающей возможность выделения отдельных стадий сна, а в большинстве случаев — из-за отсутствия таковой. Однако, как было указано выше, на фоне диффузной общемозговой электрической активности появление отдельных стадий и феноменов сна является прогностически благоприятным признаком.
При сохранном сознании в острейший период достаточно часто встречается как полифазность, так и инверсия цикла сон — бодрствование вследствие циркадных расстройств. Если в первом случае больные в течение суток засыпают по нескольку раз, то во втором отмечается смещение цикла сон — бодрствование: дневной сон и ночное бодрствование.
По нашим данным, характерными признаками острейшего периода, сопровождающегося общемозговой симптоматикой, являются уменьшение d-сна, частые пробуждения и отсутствие фазы быстрого сна (ФБС).
Расположение очага поражения в различных полушариях или же в стволе мозга вносит специфические изменения в структуру сна. Более грубые расстройства отмечают при правополушарных процессах. Нарушения заключаются в уменьшении длительности d-сна и ФБС, росте длительности периода бодрствования и I стадии, длительности засыпания, количества пробуждений, низком коэффициенте эффективности сна. Причину грубых нарушений сна у правополушарных больных следует искать в глубинных механизмах взаимосвязи правого полушария и гипногенных структур мозга. Кроме расстройств сна, у этих больных отмечают более грубые изменения в вегетативной регуляции. Это проявляется в тахикардии, различных сердечных аритмиях, высоких цифрах артериального давления. Левое полушарие наиболее тесно связано с активирующими системами мозга. Существует точка зрения, что в этом заключается причина частого нарушения сознания при левополушарных инсультах.
Особый интерес представляют инсульты с различной стволовой локализацией. При возникновении процесса в Варолиевом мосту резко уменьшается длительность ФБС, увеличивается ее латентный период. Бульбарная симптоматика сопровождается уменьшением d-сна.
Нами были изучены особенности структуры ночного сна у больных МИ в группах с исходно хорошим и плохим сном. Исследование показало, что больные, которые преморбидно имели определенные проблемы со сном (долгое засыпание, частые пробуждения, раннее пробуждение, неудовлетворенность сном), независимо от других факторов имели худшие показатели качества сна. Это говорит о том, что в формирование структурных изменений сна, кроме основной причины (инсульт), определенный вклад вносит исходная особенность регуляции цикла сон — бодрствование.
Структура сна, больных МИ, возникшим в различное время суток, также различается. Характерным для инсульта, возникшего во время сна, является, высокая представленность ФБС, что с учетом сопровождающей эту фазу "вегетативной бури" (резкие колебания частоты сердечных сокращений, артериального давления и частоты дыхания, повышение свертываемости крови) может быть одной из причин возникновения МИ в это время суток. По нашим данным, у больных с "утренним инсультом" по сравнению с "ночным" и "дневным" наблюдается наименьшее время быстрого сна.
Таким образом, результаты наших исследований и данные литературы показывают, что изучение структуры ночного сна является необходимым как у больных МИ, так у контингента с так называемыми доинсультными заболеваниями. Человек является частью природы и как все живые существа подвергается воздействию определенных природных ритмических колебаний. Для нормального функционирования организма требуется гармоничное подстраивание к природным ритмам. Однако современный ритм жизни все более сдвигает эту "подстройку". Нарушение циркадной ритмики (биоритма сон — бодрствование) приводит к так называемому синдрому десинхроноза — рассогласованной динамике различных показателей внутренней среды, что является потенциальной базой возникновения различной сосудистой патологии. Поэтому для профилактики и лечения сосудистой патологии необходимо восстановление биоритма сон — бодрствование с помощью медикаментозных (снотворные препараты) иили физических (фототерапия) методов лечения.
Нарушения цикла “сон-бодрствование” охватывают от 28% до 45% популяции, являясь для половины из них существенной клинической проблемой, требующей специальной диагностики и лечения.
Представленность нарушений сна в популяции неврологических больных еще большая и достигает 70-85%. При этом чаще встречаются инсомнии; гиперсомнии занимают второе место, и значительную их часть составляет синдром апноэ во сне. В МКБ-10 под инсомнией, гиперсомнией и нарушениями ритма сна совокупно подразумеваются “первично психогенные состояния с эмоционально обусловленным нарушением качества, длительности или ритма сна”. Мозговой инсульт, развиваясь в различные периоды цикла “сон – бодрствование”, является классическим примером того, как нарушения сна влияют на течение неврологического заболевания, и как развитие заболевания провоцируется теми физиологическими изменениями, которые характерны для различных фаз сна. Статистика свидетельствует о том, что в течение суток мозговой инсульт развивается наиболее часто с 6 ч утра до 12 ч дня — 46%, у 20% — с 12 ч до 18 ч, в 17% случаев – с 0ч до 6 ч утра и с 18 ч до 24 ч. По данным Pressman и соавт. (1995), от 25 до 45% случаев мозгового инсульта регистрируется в ночное время. По результатам исследований Центра сомнологических исследований и кафедры нервных болезней ФППО Московской медицинской академии им. И.М.Сеченова и сомнологического центра Министерства здравоохранения РФ инсульт развивается в утреннее время — у 45% больных, днем – у 32% и во время ночного сна — у 23%.
Некоторые авторы особое внимание уделяют временному переходу “конец ночного сна — начало утра”. Первые несколько часов после пробуждения являются особенно опасными в плане возникновения инсульта.
Несмотря на очевидную связь мозгового инсульта со сном и ранним постсомническим периодом, до сих пор эти взаимоотношения остаются наименее изученными в клинике цереброваскулярной патологии. Большинство проведенных исследований носят характер чисто клинических наблюдений, в которых наряду с характерными для мозгового инсульта клиническими изменениями, описываются различные расстройства в цикле “сон-бодрствование”. Объективное исследование больных инсомнией обязательно включает полисомнографию. Эта методика предполагает одновременную регистрацию нескольких параметров, таких как электроэнцефалограмма (ЭЭГ), электромиограмма (ЭМГ), электроокулограмма (ЭОГ), что является минимально необходимым набором для оценки структуры сна. Развитие полиграфических методов исследования позволило регистрировать особенности ночного сна у больных, перенесших мозговой инсульт.
Объективное изучение ночного сна у больных инсультом представляет не только академический интерес, но также имеет достаточно серьезное практическое значение в плане выработки лечебных, реабилитационных мероприятий, в оценке прогноза заболевания. Незначительные, клинически не определяемые изменения мозговой гемодинамики (в сторону улучшения или же ухудшения), имеют свое отражение в особенностях структуры сна у больных мозговым инсультом. Обнаружение у коматозных больных отдельных сонных феноменов, в частности периодов десинхронизации, сопровождающихся быстрыми движениями глаз и снижением мышечного тонуса, указывает на относительную сохранность стволово-диэнцефальных структур мозга, что прогностически является благоприятным фактором.
Для всех форм и стадий мозгового инсульта облигатны грубые расстройства механизмов как генерации сна и его стадий, так и их поддержания, проявляющиеся в сокращении длительности сна, частых пробуждениях, продолжительных включениях бодрствования и дремоты среди ночи, дисбалансе между отдельными стадиями.
Причиной этого являются не только гибель и повреждение мозговой ткани локального характера, но и расстройства общей и местной гемодинамики, возникновение отека и смещения вещества головного мозга, попадание крови в ликворные пути, и как следствие – раздражение различных структур, находящихся в пределах ствола мозга. Факторами, оказывающими наибольшее влияние на ночной сон, являются характер, размер, локализация процесса, стадия развития заболевания. Геморрагический инсульт по сравнению с ишемическим приводит к наиболее грубым расстройствам ночного сна. Это проявляется в резком сокращении продолжительности сна, частых и длительных пробуждениях, увеличении представленности первой стадии сна (поверхностный сон). Однако при благоприятном исходе заболевания степень восстановления структуры сна происходит быстрее, чем при ишемическом инсульте. Это объясняется тем, что в отличие от ишемического инсульта, при котором развивается очаг некротического распада ткани головного мозга, при геморрагии повреждение происходит вследствие расслоения структур мозга излившейся кровью. Поэтому восстановление как клинической картины, так и ночного сна, происходит относительно лучше.
С развитием нейровизуализационных методов исследования появилась возможность более точно определять размер очага поражения, глубину его нахождения. Размер очага инсульта играет существенную роль в формировании расстройств сна.
Крупный очаг приводит к распространенному отеку вещества головного мозга, иногда даже противоположного полушария, возникновению дислокационного синдрома. Логичны наиболее грубые расстройства сна при крупных очагах мозгового инсульта, что подтверждено исследованиями сомнологического центра МЗ РФ. Кроме того, максимальная приближенность очага инсульта к ликворным путям и срединным структурам головного мозга, т. е. медиальное расположение процесса, приводит к более грубым расстройствам сна. Так, медиальный очаг с захватом таламических структур характеризуется исчезновением на стороне поражения “сонных веретен” (ЭЭГ признаков второй стадии сна); латерально расположенные процессы сопровождаются относительно негрубыми расстройствами сна.
Острейшая стадия инсульта (1 неделя) характеризуется целым рядом клинических и полисомнографических особенностей. Клинически — это наличие грубых, трудно контролируемых гемодинамических, общемозговых и локальных неврологических процессов. Грубые расстройства сознания (сопор, кома), как правило, сопровождаются медленноволновой активностью, исключающей возможность выделения отдельных стадий сна, а в большинстве случаев — из-за отсутствия таковых. Однако появление отдельных стадий и феноменов сна на фоне диффузной общемозговой электрической активности является прогностически благоприятным признаком.
При сохранном сознании в острейший период достаточно часто встречается как полифазность, так и инверсия цикла “сон-бодрствование” вследствие циркадных расстройств. Если в первом случае больные засыпают несколько раз в течение суток, то во втором — отмечается смещение цикла “сон-бодрствование”: дневной сон и ночное бодрствование. Характерными признаками острейшего периода, сопровождающегося общемозговой симптоматикой, являются: нарушение инициации, поддержания и изменение целостной картины сна: уменьшение количества дельта — сна, уменьшение его времени, увеличение латентного периода сна, увеличение времени поверхностного сна, увеличение времени бодрствования во сне с частыми пробуждениями и отсутствие фазы быстрого сна (ФБС), т.е. дисфункция неспецифических систем мозга, отвечающих за сон.
Наибольшие нарушения сна наблюдаются при поражении правого полушария, что объясняется глубинными механизмами взаимосвязи правого полушария головного мозга и гипногенных структур мозга. Кроме расстройств сна у этих больных отмечают более грубые изменения в вегетативной регуляции. Это проявляется в тахикардии, различных сердечных аритмиях, высоких цифрах артериального давления. Левое полушарие наиболее тесно связано с активирующими системами мозга.
Существует точка зрения, что именно это является причиной частого нарушения сознания при левополушарных инсультах. Отмечено, что при поражении левого полушария головного мозга, существует связь между степенью сохранности речевой функции и ФБС, что говорит в пользу благоприятного прогноза заболевания. Усугубляет нарушение сна и различная локализация очага инсульта в стволе мозга (в зависимости от уровня): при локализации в продолговатом мозге наблюдается редукция дельта — сна в связи с увеличением активирующего влияния ретикулярной формации и бульбарными расстройствами дыхания; при поражении Варолиева моста резко уменьшается длительность ФБС, увеличивается ее латентный период; поражение мезэнцефальных структур сопровождается урежением активационных сдвигов во сне. Чем грубее нарушена структура сна в остром периоде инсульта, тем хуже прогноз в дальнейшем восстановительном периоде. Интересно, что больные, преморбидно имевшие определенные проблемы со сном (долгое засыпание, частые пробуждения, раннее пробуждение, неудовлетворенность ночным сном), независимо от других факторов, имели и худшие показатели качества сна во время ОНМК.
Это говорит о том, что в формировании структурных изменений сна, кроме основной причины ( инсульт), определенный вклад вносит исходная особенность регуляции цикла “сон-бодрствование”. Важным является также и то, что в проблему нарушений сна во время инсульта вплетается проблема нарушений дыхания во сне у этих больных. От 20 до 40% больных мозговым инсультом имеют патологическое число апноэ — гипопноэ во сне, причем в случае геморрагических инсультов их больше. Синдром апноэ во сне (САС) определяется как потенциально летальное состояние, характеризующееся множественными эпизодами остановок дыхания во сне и сочетающееся с повторными эпизодами взрывного храпа и дневной сонливостью. Апноэ во сне — это дыхательная пауза во время сна, т.е. отсутствие воздушного потока на уровне рта и носа длительностью не менее 10 секунд, гипопноэ представляет собой уменьшение воздушного потока более чем на 50% также в течение не менее 10 секунд.
Выраженность возникающих дыхательных расстройств оценивают на основании индекса апноэ, который определяется как среднее число эпизодов апноэ, или индекса апноэ / гипопноэ, который отражает среднее число всех респираторных событий за 1 час сна. Наиболее часто встречающееся в литературе количественное определение для постановки диагноза САС соответствует индексу апноэ более 5 или индексу апноэ / гипопноэ более 10.
Каждый эпизод апноэ сопровождается повышением АД. Связанная с САС артериальная гипертензия характеризуется преимущественным повышением диастолического давления, также наблюдается циклическое колебание давления в легочной артерии. Клинически значимая правопредсердная недостаточность развивается у 12%-13% пациентов с САС. Для больных с САС характерны ночные нарушения сердечного ритма. Практически у всех пациентов во время эпизода апноэ наблюдают синусовую аритмию с выраженной брадикардией вплоть до короткого периода асистолии, которая резко сменяется тахикардией после его окончания. У пациентов с САС возможна выраженная предсердная и желудочковая экстрасистолия, преходящая атриовентрикулярная блокада разных степеней, суправентрикулярная и желудочковая тахикардия. Не исключено, что фибриляция желудочков у больных с САС может явиться причиной внезапной смерти во сне. Вероятно, эти нарушения возникают на фоне значительного снижения сатурации кислорода у пациентов с сопутствующей сердечно- легочной патологией, особенно на фоне мозгового инсульта.
У больных с САС восстановительный период инсульта протекает медленнее, так как важную роль здесь играет дополнительная гипоксия за счет САС.
Нарушения сна во время мозгового инсульта могут протекать в виде ночного ухудшения поведения и ажитации, ночных блужданий и неадекватности, разрушающих сон больного — “синдром заходящего солнца” — «sundown syndromе». Это не делирий, а расстройство поведения, связанное со скоростью развития ментального дефекта. Однако при сочетании нескольких факторов, разрушающих сон у больного с инсультом, могут возникнуть более тяжелые расстройства поведения, в т.ч. делирий. Развивается подобное состояние поздним вечером либо ранним утром и связано с расстройством циркадианных ритмов. В палате интенсивной терапии неврологического отделения ОКБ №1 в течение 6 месяцев 2001 года наблюдалось 17 больных с ОНМК, имевших выраженные нарушения цикла “сон-бодрствование”, из них 12 больных с ишемическим и 5 — с геморрагическим характером инсульта.
Это были больные пожилого возраста (55-75 лет) со средней степенью тяжести течения заболевания. Клиническое наблюдение за больными проводилось круглосуточно медперсоналом отделения. Проводился постоянный мониторинг температуры, АД, пульса, ЧСС, ЧДД, подсчет количества “апноэ – гипопноэ”, лабораторный контроль КЩС (в т.ч. сатурации кислорода в крови), биохимических изменений в крови (в т.ч. электролитов крови).
Выявлены следующие нарушения цикла “сон-бодрствование”:
1. Уменьшение времени сна до 4-5 часов (в норме 6-10 часов в зависимости от возраста).
2. Поверхностный сон с частыми пробуждениями, длительным бодрствованием во сне.
3. В 2 случаях наблюдалась инверсия сна и синдром “заходящего солнца”.
4. Во всех 17 случаях показатели деятельности жизненно важных органов и лабораторные показатели находились в пределах нормы (по международным стандартам лечения ОНМК).
5. САС ни в одном случае не наблюдался.
С целью коррекции нарушений сна были использованы следующие медикаменты:
1. Имован (таб.7.5 мг №5 AVENTIS / RHONEPOULENC).
2. Ивадал (таб. 10 мг №20 SYNTHELABO GROUPE).
3. Терален (алимемазин) (таб. 5 мг №50 THERAPLIX RHONE-POULENC RORER).
В результате динамического наблюдения за пациентами и анализа клинических и параклинических данных было выявлено, что больным с ОНМК с нарушениями сна без синдрома апноэ во сне и без сопутствующей инверсии сна была эффективна монотерапия — как ивадалом, так и имованом в дозе 1 таб. на ночь (особенно стоит обратить внимание на то, что эти средства не вызывают негативного влияния на функцию дыхания во сне, возможную у больных мозговым инсультом). При выраженных нарушениях сна с его инверсией и синдромом “заходящего солнца” (2 пациента) эффективной для нормализации сна была комбинация имована (ивадала) в дозе 1 таблетка на ночь и тералена в дозе 2.5мг – 5 мг однократно на ночь, что позволило удлинить время сна, уменьшить время бодрствования во сне. В процессе лечения все больные становились более контактными, спокойными, восстановительный период протекал более гладко и быстро. Переносимость всех препаратов в указанных дозировках была хорошей, побочных эффектов не наблюдалось.
Заключение
Применение современных снотворных средств последнего поколения (циклопирролоновых и имидазопиридиновых производных) у больных ОНМК средней степени тяжести, является необходимым компонентом стандарта лечения этих больных (как с ишемическим так и с геморрагическим характером заболевания) для ускорения процессов восстановления нарушенных функций и для профилактики более тяжелых расстройств психической деятельности.
Влияние нарушений сна на эффективность восстановительного лечения больных, перенесших инсульт
Маркин С.П.
Инсульт (в переводе с латинского «удар») – одна из наиболее тяжелых форм сосудистых поражений головного мозга. По данным Национальной ассоциации по борьбе с инсультом. в России ежегодно регистрируется 450000 инсультов (или 2,5–3 случая на 1000 населения в год). В большинстве случаев больные. перенесшие инсульт. имеют определенную степень восстановления нарушенных функций. Так, в нашей стране инвалидизация вследствие инсульта (3,2 на 10.000 населения в год) занимает первое место (40–50%) среди патологий, являющихся причиной инвалидности. На данный момент в Российской Федерации насчитывается около 1 млн. инвалидов вследствие инсульта. При этом потери государства от одного больного. получившего инвалидность, составляют 1,247 млн. рублей в год [6].
Заболеваемость (инвалидность) изменяет «качество жизни» больного и выдвигает перед ним новые проблемы (приспособление к дефекту, изменение профессии, поведение в семье и другие). Так, согласно данным Б.С. Виленского, на момент выписки из стационара больные. перенесшие инсульт. в 34% случаев выразили опасение быть обузой в семье, а 12% «не представляли, что будет дальше» [4].
Оценка «качества жизни», выполненная самим пациентом, является ценным показателем его состояния и в сочетании с врачебным заключением позволяет составить объективную картину течения заболевания. В связи с этим появилась необходимость количественной оценки «качества жизни», для которой используются временные характеристики (годы качественной жизни – QALY; годы возвращенной трудоспособности – DALY; эквивалентные годы здоровья – HYE), а также выраженные в баллах показатели различных шкал.
Так, с целью оценки «качества жизни» нами обследовано 40 больных (в возрасте 47,4±4,5 лет), перенесших ишемический инсульт, с помощью индекса общего психологического благополучия [1]. Как показали результаты исследования, индекс составил лишь 43,5±4,0 балла (при максимальном значении 110 баллов), что составляет 39,6% от нормы.
Наиболее частым последствием инсульта, влияющим на «качество жизни» больных, являются нарушения двигательных функций, которые к концу острого периода (3 недели от начала инсульта) наблюдаются у 81,2% из 100 выживших больных. Однако ОНМК нередко приводит к развитию депрессии, нарушению когнитивных функций, а также расстройствам сна. которые находятся в «тени» основного (двигательного) дефекта, но иногда в большей степени влияют на «качество жизни» постинсультных больных. При этом они также оказывают существенное влияние на ход восстановительного лечения и могут являться «негативными предикторами» эффективности восстановительных мероприятий. Вследствие этого состояние данных функций может служить прогностическим критерием восстановления больных.
До недавнего времени считалось, что ткань головного мозга имеет незначительные возможности для адаптивного ответа на повреждение, в частности ишемию вследствие инсульта. Однако исследования последних лет свидетельствуют о способности мозга к ре-генерации за счет процесса пластичности. Пластичность представляет собой совокупность ряда механизмов при самом активном участии АМРА– и NMDA–глутаматных рецепторов, а также Са2+ и Na+–каналов [5]:
– функционирование ранее неактивных путей;
– спруттинг волокон сохранившихся клеток с формированием новых синапсов;
– реорганизация нейрональных цепей – формирование многих цепей, обеспечивающих близкие функции.
Основными задачами восстановительного лечения больных, перенесших инсульт, являются:
– восстановление нарушенных функций;
– лечение вторичных патологических синдромов;
– профилактика повторных инсультов.
При этом наиболее полное восстановление отмечается в раннем восстановительном периоде (до 6 месяцев от начала инсульта). В последующем способность головного мозга к регенерации значительно снижается. Среди факторов, влияющих на восстановительные способности мозга, прежде всего следует выделить возраст пациента, длительность воздействия повреждающего агента, локализацию повреждения мозга и объем его поражения.
Само по себе острое поражение головного мозга является мощным фактором, активизирующим процессы пластичности. Однако при развитии обширного инсульта наблюдается ограниченность регенерации мозга, что требует дополнительного использования различных методов восстановительного лечения. положительно влияющих на пластичность ЦНС. Среди медикаментозных препаратов внимание заслуживает церебролизин – единственный ноотропный препарат с доказанной нейротрофической активностью, аналогичной действию естественных факторов роста нейронов. Кроме того, показана терапевтическая эффективность транскраниальной электростимуляции (ТЭС), которая нейтрализует негативные эффекты стресс–реакции, обусловленные инсультом, и усиливает адаптационную готовность организма путем нормализации работы нейроэндокринных центров [2].
Говоря о способности головного мозга к восстановлению, необходимо отметить важную роль в этом процессе сна. Так, по данным Я.И. Левина, изменения структуры сна в острейшем периоде инсульта имеют важное прогностическое значение. Если в течение 7–10 дней после ОНМК не происходит восстановления нормальной картины сна. то прогноз считается неблагоприятным [7]. Вследствие этого при восстановительном лечении больных, перенесших инсульт, необходимо большое внимание обратить именно на нарушение сна .
Потребность во сне взрослого человека в среднем составляет 7–8 часов в сутки. По данным ряда исследователей, спать меньше нормы, например, всего 4–5 часов, не только вредно для здоровья, но и опасно для жизни. Сон является неоднородным процессом. Он представляет собой последовательность функциональных состояний головного мозга – 1, 2, 3 и 4 стадии фазы медленного сна (ФМС) и фазы быстрого сна (ФБС). Нормальный 8–часовой сон состоит из 4–6 волнообразных циклов, каждый из которых длится около 90–110 минут. При этом в целом за ночь ФМС занимает 75–85% от всего времени сна, а ФБС – лишь 15–25%. Традиционно считают, что для восстановительных целей служит не весь сон, а только его часть – ФМС [3].
Нарушения сна при мозговом инсульте, по данным полисомнографического исследования, достигают 100% случаев и проявляются в виде инсомнии, нарушения цикла «сон–бодрствование» и расстройства дыхания во сне по типу синдрома «апноэ во сне».
Инсомния – расстройство, связанное с трудностями инициации и/или поддержания сна. В зависимости от длительности нарушений сна выделяют острые (длительностью менее 3 недель) и хронические (более 3 недель) инсомнии. Среди факторов, влияющих на длительность инсомнии, в первую очередь выделяют депрессию, а также использование «долгоживущих» бензодиазепинов.
В клинической картине инсомнии выделяют пресомнические, интрасомнические и постсомнические расстройства. Пресомнические расстройства – трудности начала сна. В норме процесс засыпания составляет в среднем 10 минут. Однако при развитии инсомнии данный процесс может затягиваться до 2 часов и более. Интрасомнические расстройства проявляются в виде частых ночных пробуждений, после которых пациент долго не может вновь заснуть. Постсомнические расстройства – расстройства, возникающие в ближайшее время после пробуждения. При этом наиболее часто больные жалуются на чувство «разбитости» [10].
Инсомнии у больных, перенесших инсульт, характеризуются изменением продолжительности сна, частыми ночными пробуждениями, отсутствием удовлетворенности ночным сном, а также появлением «тяжести» в голове. Данная клиническая картина подтверждается результатами полисомнографического исследования, при котором отмечается увеличение 1 и 2 стадий, уменьшение 3 и 4 стадий ФМС и нередко уменьшение ФБС.
При лечении инсомнии достаточно часто назначают бензодиазепины (например, феназепам), которые негативно влияют на процессы пластичности нервной системы, что значительно снижает эффективность восстановительного лечения. Наиболее физиологическое действие на организм больного, перенесшего инсульт, оказывает синтетический препарат с выраженным снотворным эффектом, производное этаноламина – Донормил (блокатор гистаминовых Н1–рецепторов).
Целью настоящего исследования было изучение нарушений сна у постинсультных больных и возможности их коррекции с помощью Донормила. Всего обследовано 60 пациентов (27 мужчин и 33 женщины) в возрасте 54,7±4,9 лет, перенесших ишемический инсульт давностью 2–3 недели. Различные нарушения сна отмечались в 100% случаев от 4 до 7 раз в неделю. Количественная оценка сна проводилась с использованием стандартной анкеты субъективной оценки сна, разработанной в сомнологическом центре МЗ РФ. Максимальная суммарная оценка по всем показателям составляет 30 баллов. Сумма 22 балла и более – сон не нарушен, 19–21 балл – пограничные состояния функции сна и 0–18 баллов – сон нарушен.
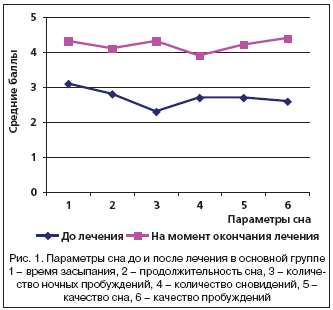
Согласно проведенному анкетированию, до лечения нарушения сна (11,9±0,18 балла) выявлены у 34 человек (56,7%) и пограничные значения функции сна (19,9±0,17 балла) – у 26 человек (43,3%). В среднем суммарная балльная оценка составила 16,2±0,15 балла. При этом время засыпания было оценено в 3,1±0,14 балла, продолжительность сна – 2,8±0,11 балла, ночные пробуждения – 2,3±0,16 балла, сновидения – 2,7±0,14 балла, качество сна – 2,7±0,17 балла и качество пробуждения – 2,6±0,18 балла. В дальнейшем все пациенты были разделены на основную (37 человек) и контрольную (23 человека) группы. Пациенты основной группы принимали Донормил в дозе 15 мг (1 таблетка) за 15–30 минут до сна на протяжении 14 дней. Больные же контрольной группы получали лишь плацебо.
Как показали результаты исследования, применение Донормила способствовало достоверному улучшению сна (включая сон по всем его характеристикам) у пациентов основной группы (рис. 1).
Так, время засыпания составило 4,3±0,17 балла, продолжительность сна – 4,1±0,14 балла, ночные пробуждения – 4,3±0,15 балла, сновидения – 3,9±0,11 балла, качество сна – 4,2±0,13 балла, качество пробуждения – 4,4±0,16 балла и суммарная оценка качества сна – 25,2±0,14 балла (р0,05) (табл. 1).
Кроме того, Донормил не давал побочных эффектов и хорошо переносился больными. Таким образом, применение Донормила при лечении инсомнии у больных, перенесших инсульт, способствует не только нормализации сна, но и предупреждению осложнений, связанных с приемом бензодиазепинов (депрессия, снижение когнитивных функций и др.).
Инверсия цикла «сон–бодрствование» – засыпание в дневное и бодрствование в ночное время. По данным наших наблюдений, нарушение цикла «сон–бодрствование» встречается у 29% постинсультных больных. Основным механизмом, ответственным за поддержание сна, является циркадианный биоритм, в котором ключевую роль отводят гормону мелатонину. Поэтому в настоящее время для нормализации цикла «сон–бодрствование» предложен препарат агомелатин, являющийся агонистом мелатонина и антагонистом 5–НТ2с–рецепторов.
Синдром «апноэ во сне» (САС) – периодически возникающее во время сна кратковременное прекращение дыхания (10 секунд и более) и повторяющееся больше 5–6 раз на протяжении одного часа сна. Для того чтобы предположить наличие сонных апноэ, достаточно сочетание сильного храпа во сне, инсомнических проявлений с частыми эпизодами пробуждений и дневной сонливостью. Сомнологическим центром Минздрава РФ предложена анкета для скриннинга синдрома «апноэ во сне». В соответствии с данной анкетой при наличии 4 и более баллов синдром апноэ во сне вероятен. Однако окончательный диагноз устанавливают по данным полисомнографии. Для оценки степени САС предложен индекс сонных апноэ (количество остановок дыхания в течение 1 часа сна), которое в норме не превышает 5. Так, легкая форма соответствует 5–9 баллам, умеренно тяжелая форма – 10–19 и тяжелая форма – 20 и более баллам [10].
В настоящее время выделяют 2 вида САС: синдром обструктивных апноэ во сне (СОАС) и синдром центральных апноэ во сне (СЦАС). Одной из причин СОАС является анатомическое сужение верхних дыхательных путей с их окклюзией. СЦАС развивается в результате органического поражения ствола головного мозга, в том числе вследствие инсульта.
САС повышает риск развития мозгового инсульта в 2–8 раз по сравнению со здоровыми людьми. При этом наличие расстройств дыхания во сне до возникновения ОНМК значительно ухудшает течение заболевания, появление же САС после развития инсульта является прогностически неблагоприятным фактором. Достаточно часто САС является причиной нарушения когнитивных функций у больных, перенесших инсульт.
Нами обследовано 79 больных (45 мужчин и 34 женщины) в возрасте 64,4±3,7 лет, перенесших ишемический инсульт давностью 2–3 недели. Нарушение дыхания во сне исследовали с помощью анкеты для скрининга синдрома «апноэ во сне», состояние когнитивных функций – по данным теста «5 слов», пробы Шульте и теста «рисования часов». Как показали результаты исследования, 32 пациента страдали САС (результаты анкеты составили более 4 баллов). Нарушение когнитивных функций различной степени выраженности выявлены у 57 больных. Данную группу составили 32 пациента с расстройствами дыхания во сне и 25, не страдавших САС. Результаты исследования приведены в таблице 2.
Как видно из таблицы, у больных с САС значительно выражены когнитивные расстройства. Ниже в качестве примера приведены результаты выполнения теста «рисования часов» больных с САС (рис. 2, 3).
При невозможности использования полисомнографии для диагностики САС постинсультным больным, страдающим храпом, нельзя назначать миорелаксанты и бензодиазепины, которые могут ухудшить течение заболевания, а иногда явиться причиной смерти во сне. Наиболее эффективным методом лечения САС является использование постоянного положительного давления воздуха (СРАР–терапия).
Депрессия и расстройства сна. Развитие депрессии после инсульта встречается в 35–72% случаев. При этом количество больных с постинсультной депрессией возрастает по мере осознания пациентом потери своего социального статуса [9]. Так, многие больные желают «инсультообразного», т.е. быстрого восстановления нарушенных функций. Однако процесс восстановления может затягиваться на длительное время, вследствие этого возможности восстановительного лечения представляются больными бесперспективными. Депрессия может быть прямым следствием инсульта, психологической реакцией на болезнь, а также следствием побочных эффектов терапии, проводимой в связи с основным заболеванием. При этом нарушение сна является наиболее частым симптомом депрессии постинсультных больных [8].
Нами обследовано 129 больных, перенесших инсульт (в возрасте 54,8±2,7 лет) давностью 2–3 недели, с помощью шкалы Center Epidemiological studies of USA (CES–D). Из них выявлено 40 пациентов (32%) с депрессией:
– 14 пациентов (35%) с легкими депрессивными расстройствами (19–25 баллов);
– 26 человек (65%) с выраженными депрессивными расстройствами (более 26 баллов).
Помимо подавленного настроения у всех пациентов с депрессией отмечались нарушения сна различной степени выраженности. Так, согласно анкете субъективной характеристики сна, при умеренных депрессивных расстройствах отмечались пограничные значения нарушений сна (18,9±0,9 балла), а при тяжелых депрессивных расстройствах – выраженные нарушения сна (14,8±0,5 балла). Инсомния при депрессии имеет свои особенности: ранние утренние пробуждения и короткий латентный период ФБС. Свое состояние пациенты после сна оценивают как «словно в тумане». Столь частое сочетание депрессии и нарушений сна объясняется наличием единых патогенетических (серотонинергических) механизмов:
– развитие депрессии связывают с нарушением обмена моноаминов (серотонина);
– серотонин участвует в формировании цикла «сон–бодрствование».
Терапия нарушений сна при депрессии предусматривает лечение основного заболевания (т.е. депрессии). Лечение депрессий производится только единственным классом препаратов – антидепрессантами (это, в частности, селективные ингибиторы обратного захвата серотонина). Эффективность терапии повышается при сочетании антидепрессантов с ТЭС. Нами обследовано 67 больных (в возрасте от 41 до 57 лет) спустя 3 недели после ишемического инсульта. В качестве скрининга для оценки степени тяжести депрессии использовалась шкала CES–D, выраженность нарушений сна оценивалась по анкете балльной оценки субъективных характеристик сна.
Согласно проведенному тестированию, выявлено 46 пациентов (68,6%) с легкими депрессивными расстройствами (21,5±0,4 балла) и 21 пациент (31,4%) с выраженной депрессией (35,0±2,0 балла) (в среднем 28,3±1,2 балла). При этом в 100% случаев депрессия сочеталась с инсомнией (суммарная оценка качества сна составила 15,9±0,15 балла). Все пациенты с депрессией были разделены на основную (37 человек) и контрольную (30 человек) группы. При этом больные основной группы получали ТЭС (от аппарата «Трансаир–01») по 10 минут через день в сочетании с флувоксамином в дозе 50 мг (однократно на ночь) на протяжении 24 дней. Пациенты же контрольной группы получали лишь флувоксамин в дозе 100 мг в сутки.
После проведенного лечения в основной группе на фоне применения ТЭС в сочетании с флувоксамином отмечалось более выраженное снижение депрессии (на 33,6% (р
Выводы
1. При лечении инсомнии у больных, перенесших инсульт, наиболее физиологическое действие на организм оказывает Донормил, который не влияет на процессы пластичности.
2. При инверсии цикла «сон–бодрствование» препаратом выбора является агонист мелатонина и 5–НТ2с–рецепторов агомелатин, способствующий нормализации циркадианного ритма.
3. Наиболее эффективным методом лечения САС является СРАР–терапия.
4. Комплексное применение антидепрессантов (на примере флувоксамина) с ТЭС способствует нормализации сна у больных с постинсультной депрессией.
Литература
1. Белова А.Н. Щепетова О.Н. Шкалы, тесты и опросники в медицинской реабилитации. М. Антидор, 2002. – 440 с.
2. Борисов В.А. С.П. Маркин. Реабилитация постинсультных больных //Журнал теоретической и практической медицины. М. 2005 – №1 – С. 21.
3. Вейн А.М. Стресс и сон у человека. – М. Изд–во «Нейромедиа», 2004 – 96 с.
4. Виленский Б.С. Инсульт: профилактика, диагностика и лечение. СПб: Изд–во «Фолиант» – 120 с.
5. Гехт А.Б. Качество жизни и лечение больных, перенесших инсульт. М. Издательско–полиграфическая фирма «Эхо», 2002 – 45 с.
6. Гусев Е.И. Скворцова В.И. Проблема инсульта в Российской Федерации //Качество жизни. Медицина. М. 2006 – №2 – С. 10.
7. Левин Я.И. Инсомния: современные и диагностические подходы. М. Медпрактика, 2005. – 115 с.
8. Маркин С.П. Маркина В.А. Депрессия и инсомния у больных, перенесших инсульт //Актуальные проблемы сомнологии. Тезисы докладов V Всероссийской конференции. – М. 2006 – С. 69.
9. Смулевич А.Б. Депрессии при соматических заболеваниях –М. Медицинское информационное агентство, 2003. – 432 с.
10. Цыган В.Н. Богословский М.М. Апчел В.Я. Князькин И.В. Физиология и патология сна. СПб. Изд–во СпецЛит, 2006 – 157 с.

Здравствуйте! Я пишу бакалаварскую работу про нарушения сна после инсульта. Я бы хотела бы у Вас попросить анкету по которой Вы вели опрос пациентов и разрешения на её использование. Спасибо жду Вашего ответа