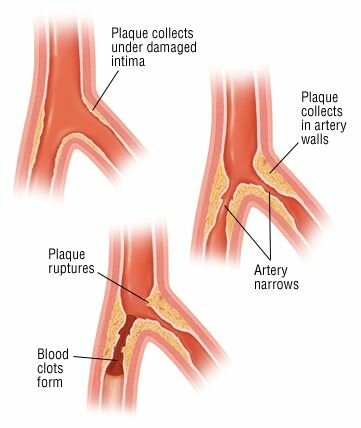
Стеноз почечной артерии (РАС) определяется как сужение одной или обеих почечных артерий или их ветвей (как правило, более чем на 70-80%, чтобы быть функционально значимым) .8 Это может быть вызвано любой деформацией почечных артерий, Наиболее распространенным типом является фибромышечная дисплазия или атеросклеротическое заболевание.
Родственные термины:
Скачать в формате PDF
Об этой странице
Узнайте больше о стеноз почечной артерии
Животные модели заболеваний почек
Стеноз почечной артерии
Стеноз почечной артерии — это сужение артерий, транспортирующих кровь к почкам. Это в первую очередь вызвано атеросклерозом у людей и увеличивает риск развития гипертонии, ХБП, а также сердечной заболеваемости и смертности (Al-Suraih and Grande, 2014). Большая часть повреждения тканей, вызванного стенозом почечных артерий, связана с ишемией, поскольку узкие артерии вызывают гипоперфузию почек. Факторы риска развития стеноза почечной артерии включают возраст; быть женщиной; иметь гипертонию или другие сосудистые заболевания, ХБП или диабет; курение; и высокий уровень холестерина. Животные модели стеноза почечной артерии развивают признаки, обнаруживаемые при стенозе почечной артерии человека, такие как реноваскулярная гипертензия, уменьшение объема коры и всей почки, уменьшение кортикального и целостного кровотока в почках и нарушение функции почек. Снижение объема почек и кровотока коррелирует с тяжестью стеноза, аналогично заболеванию человека (Lerman et al., 1999). Односторонний стеноз почечной артерии вызывает значительную разницу между размерами к> (Lerman et al., 1999). У животных с атеросклерозом, а также со стенозом почечной артерии развивается более тяжелое заболевание. У них снижена внутрипочечная микрососудистая плотность, а также повышенный фиброз, повреждение канальцев, АФК и отношение микрососудистых сред почек к просвету (Sun et al., 2016). Гистологически, на животных моделях также развивается вакуолизация тубулярных эпителиальных клеток, серповидных структур (в основном состоящих из подоцитов) в клубочках и дополнительное подоцитарное повреждение; кроме того, в небольших почечных артериях развивается концентрическая гиперплазия интимы.
Свинные модели стеноза почечной артерии обычно используются из-за сопоставимой анатомии и физиологии почек у свиней и людей. В связи с этим патофизиология, возникающая в результате искусственно вызванного стеноза почечной артерии, сходна с естественным стенозом почечной артерии у человека. Например, внутрисосудистая модель медного стента включает развитие сосудистого поражения (Lerman et al., 1999). Эта модель также неинвазивна, что снижает нагрузку на животных. Это включает в себя чрескожное использование баллона для встраивания медной проволоки в почечную артерию, что вызывает стеноз. Инвазивные модели стеноза почечной артерии включают модель с двумя почками / двумя зажимами, модель с двумя почками / одним зажимом и модель с одной почкой / одним зажимом и могут быть выполнены на мышах, крысах, собаках и свиньи (Al-Suraih и Grande, 2014). Эти модели сравнимы с моделями IRI (двусторонние, односторонние и односторонние с UNX), хотя с уменьшенным почечным кровотоком вместо отсутствующего почечного кровотока. Эти модели чувствительны к антагонистам системы ренин-ангиотензин (Ang), а также к изменениям в потреблении натрия (Grossman, 2010). Животных обычно умерщвляют через 4–12 недель после запуска модели.
Ограниченные исследования были проведены с целью изучения механизмов и роли ER стресса, апоптоза и воспаления при стенозе почечных артерий. Поскольку большая часть повреждений в моделях стеноза почечной артерии вызвана сниженным, но не отсутствующим, кровотоком к почке (почкам), вполне вероятно, что большая часть обнаруженного повреждения вызвана механизмами, подобными тем, которые обнаружены в моделях IRI. ER стресс усиливается в этой модели, и, следовательно, он может играть роль в развитии повреждения почек, а также индукции апоптоза и воспаления (Yang et al., 2014). Было обнаружено, что маркеры стресса ER, такие как CHOP и GRP94, активируются в эндотелиальных и проксимальных канальцевых клетках почек, которые проходят эту модель, но не в дистальных канальцевых клетках (Zhu et al., 2013).
Как уже упоминалось, было проведено небольшое исследование для углубленного изучения апоптоза; исследователи склонны просто отмечать наличие или отсутствие апоптоза (окрашивание TUNEL) (Chade et al., 2003; Favreau et al., 2010; Zhu et al., 2013), но не изучают механизм (механизмы), из которого он развивается , Повышенные уровни проапоптотического белка, CHOP, могут играть роль в повышенном апоптозе, обнаруженном в этой модели стеноза почечной артерии (Zhu et al., 2013); однако также было высказано предположение, что апоптоз индуцируется АФК (Lerman et al., 2009). Апоптотические маркеры, такие как увеличение расщепленной каспазы-3 и снижение Bcl-2, обнаруживаются в почках этой модели. Интересно, что мезенхимальные стволовые клетки, которые обладают способностями к восстановлению сосудов, уменьшают как стресс ER, так и апоптоз в этой модели (Zhu et al., 2013).
В модели с медным стентом инфильтрация воспалительных клеток происходит в почечной артерии вблизи места расположения стента; это прежде всего состоит из нейтрофилов, которые ограничены лимфоцитами и макрофагами. Случайные мононуклеарные клетки могут быть обнаружены в интерстиции почки этой модели (Lerman et al., 1999). Маркеры воспаления TNF-α и IL-1β также повышены в модели одностороннего стеноза почечной артерии; их экспрессия была снижена путем инфузии мезенхимальных стволовых клеток (Zhu et al., 2013). Было обнаружено, что NF-κB, который участвует в провоспалительном сигнальном пути, а также в фиброзном пути, значительно повышен в модели атеросклеротического стеноза почечной артерии, но не в модели без атеросклероза (Sun et al., 2016). Как уже упоминалось, ингибирование апоптоза может предотвратить воспаление в почках ИРИ (Daemen et al., 1999). Хотя этот механизм не изучен при стенозе почечных артерий, возможно, что существует аналогичная система, в результате которой апоптоз приводит к воспалению.
Стеноз почечной артерии вызывает почечный фиброз, который усугубляется атеросклерозом (Sun et al., 2016) или гиперхолестеринемией (Chade et al., 2003), симулятор атеросклероза. Как уже упоминалось, NF-κB, который активирует профибротические цитокины, увеличивается в тубулярных, интерстициальных и клубочковых клетках. TGF-β также повышен в почечных канальцах и клубочках. Гиперхолестеринемия увеличивала уровни фиброза, NF-κB, но не TGF-β в этой модели (Chade et al., 2003). Когда Smad3, который находится ниже TGF-β, генетически выбит из мыши, животное почти полностью защищено от стеноза почечной артерии. В почках развивается менее тубулярная атрофия, интерстициальное воспаление и интерстициальный фиброз (Warner et al., 2012).
Сосудистые заболевания почек
Томас Д. Дубоз-младший, Ренато М. Сантос, в «Сесильской медицине Голдмана» (двадцать четвертое издание), 2012
Стеноз почечной артерии
Определение
Стеноз почечной артерии, который представляет собой сужение почечных артерий, приводит к гипоперфузии одной или обеих почек. Двумя наиболее распространенными формами стеноза почечной артерии являются атеросклеротическая болезнь и фибромышечная дисплазия. Они различаются по распространенности, патофизиологии, клинической картине, прогнозу и ведению.
Ep> Атеросклеротическое заболевание, которое встречается гораздо чаще, чем фибромышечная дисплазия, составляет 90% стеноза почечной артерии. Распространенность стеноза почечной артерии в популяции Medicare составляет всего 0,5%, но у 2–4% у пациентов с артериальной гипертензией (глава 67) и около 5,5% у пациентов с хроническим заболеванием почек. Атеросклеротическое заболевание также чаще встречается у пожилых людей и у пациентов с типичными сердечно-сосудистыми факторами риска, такими как ишемическая болезнь сердца, сердечная недостаточность, заболевание сонных или периферических сосудов и дислипидемия. У пациентов с установленным заболеванием коронарной артерии или заболеванием периферических сосудов и артериальной гипертензией распространенность некоторой степени стеноза почечной артерии может достигать 20-40%.
Фибромышечная дисплазия встречается у женщин в 2-10 раз чаще, чем у мужчин. Это важная причина излечимой гипертонии у молодых пациентов без сердечно-сосудистых факторов риска, и она патологически и ангиографически отличается от атеросклеротической болезни. Хотя причина неизвестна, существует генетическая предрасположенность к фибромышечной дисплазии. Другие возможные патогенетические факторы включают гормональные влияния (большинство пациентов — женщины детородного возраста), механические факторы и ишемию стенки сосуда.
патобиологии
Патобиология атеросклеротического стеноза почечной артерии идентична таковой атеросклеротического заболевания в других артериальных ложах (Глава 70). Фибромышечная дисплазия включает четыре различных гистопатологических типа: медиальная фиброплазия, которая является наиболее распространенным типом и составляет от 75 до 80% случаев; перимедиальная фиброплазия с нерегулярным утолщением носителя; медиальная гиперплазия с гиперплазией гладких мышц без фиброза; и фиброплазия интимы. В отличие от атеросклеротического заболевания, которое локализуется в осевых и проксимальных сегментах почечных артерий, фибромышечная дисплазия чаще поражает средние и дистальные сегменты артерий.
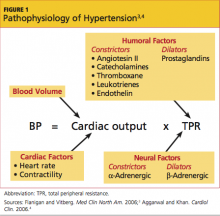
Модели реноваскулярной гипертензии с использованием зажимов почечной артерии у животных элегантно продемонстрировали, что активация системы ренин-ангиотензин-альдостерон при почечной гипоперфузии вызывает повышение системного артериального давления. Этот механизм дополнительно подтверждается способностью ингибиторов ангиотензинпревращающего фермента (АПФ) и блокаторов рецепторов ангиотензина (БРА) контролировать результирующую гипертензию у животных и у пациентов с фибромышечной дисплазией. Механизм развития гипертонии со стенозом почечной артерии, однако, представляется более сложным. Хотя атеросклеротическая почечная активация системы ренин-ангиотензин-альдостерон посредством почечной гипоперфузии имеет важное значение для инициации реакции прессора, она временная. Со временем патобиология переходит к прессорным механизмам, независимым от ангиотензина II, включая вазоконстрикцию из-за окислительного стресса, эндотелиальной дисфункции, высвобождения эндотелина и симпатической активации. Сопутствующие риски, включая курение, преклонный возраст, дислипидемию, диабет и саму гипертонию, которые могут способствовать повреждению сосудов. Неопределенная причинно-следственная связь этих сопутствующих рисков может объяснить непоследовательную реакцию артериального давления на реваскуляризацию почек при атеросклеротическом стенозе почечной артерии по сравнению с фибромышечной дисплазией.
Стеноз почечной артерии приводит к ишемической нефропатии, определяемой как нарушение функции почек за пределами окклюзионного заболевания в основных почечных артериях. Однако патофизиологическая основа повреждения почек, вероятно, является многофакторной. В отличие от сердечной или мозговой ткани, перфузия почек определяется ультрафильтрацией клубочков и ауторегуляцией СКФ и почечного кровотока, а не метаболическими потребностями. Менее 10% почечного кровотока требуется для удовлетворения потребности почек в кислороде. Следовательно, серьезное снижение перфузии всей почечной паренхимы необходимо для существенного влияния на функцию почек. Эта взаимосвязь подтверждается наблюдением, что гемодинамически значимые поражения фибромышечной дисплазии редко связаны с почечной дисфункцией. И наоборот, снижение функции почек характерно для атеросклеротического стеноза почечной артерии. Атерогенные раздражители, такие как гиперхолестеринемия, могут усиливать окислительный стресс и активировать провоспалительные и профиброгенные пути. Повторные приступы гипоперфузии при атеросклеротическом заболевании могут привести к повреждению почечных канальцев и, со временем, могут привести к тубулоинтерстициальному фиброзу. Таким образом, сочетание повторяющихся перфузионных нарушений, наложенных на атерогенные факторы риска, способствует дисфункции почек.
Клинические проявления
Клинические особенности стеноза почечной артерии связаны, прежде всего, с реноваскулярной гипертензией и ишемической нефропатией (Таблица 127-1). Значительный процент пациентов имеет резистентную гипертонию, которая не реагирует на высокие дозы нескольких гипотензивных препаратов. Злокачественная фаза гипертонии, хотя редко встречается с современными антигипертензивными препаратами, все еще встречается.
ТАБЛИЦА 127-1. Клинические особенности стеноза почечной артерии
Начало гипертонии до 30 или после 50 лет
Отсутствие семейной истории гипертонии
Короткая продолжительность или недавнее ухудшение гипертонии
По материалам сайта: www.sciencedirect.com