ГЛОМЕРУЛОНЕФРИТ ПРИ БЕРЕМЕННОСТИ
Частота гломерулонефрита среди беременных женщин составляет 0,1—0,2 %. Для данного заболевания характерно преимущественное поражение клубочков почек, но вовлекающее и канальцы, и интерстициальную ткань. Характерным возбудителем гломерулонефрита является 12 или 49 типы гемолитического стрептококка группы А. Источниками заболевания могут служить: хронический тонзиллит, перенесенная ангина, пиодермия, рожа, скарлатина. Очень редко возбудителями заболевания могут быть стафилококк, пневмококк, дифтерийная палочка, зеленящий стрептококк, менингококк, вирус гепатита В, сальмонелла, вирусы острых респираторных заболеваний и пр.
Возбудитель вызывает иммуноаллергическую реакцию организма к инфекции. К развитию заболевания предрасполагает переохлаждение организма, достаточно резкого однократного охлаждения.
Клиника
Клинически гломерулонефрит проявляется появлением отеков, патогенез которых сложен, многокомпонентен. К основным причинам, приводящим к появлению отеков, являются:
1) снижение глубочковой фильтрации (у беременных женщин снижается на 40 %), в первом триместре она составляет 81,4 мл/мин, во втором — 68,8, в конце беременности — 61,1 мл/мин; при гломерулонефрите клубочковая фильтрация снижается еще больше, что приводит к задержке натрия и воды. Стоит заметить о снижении экскреции альдостерона при гломерулонефрите, что нарушает регуляцию канальцевой реабсорбции;
2) увеличение проницаемости капилляров для жидкости и белка, вызванное повышением активности гиалуронидазы, исследование отечной жидкости в этой ситуации дает возможность судить о порозности сосудистой стенки — при нефритах в ней содержится до 1 % белка (при сердечных отеках до 0,3—0,5 % белка);
3) накопление воды в тканях способствует увеличению в их составе осмотически активных веществ (соли, мочевина и др.). Это обусловлено изменениями обмена веществ в тканях и понижением фильтрационной способности почек. При остром нефрите происхождение отеков связано с гиперволемией; при хроническом нефрите гиперволемия отсутствует, и большое значение приобретает гиподиспротеинемия.
В патогенезе нефротических отеков начальным звеном является поражение базальной мембраны и эпителиального слоя канальцев почечных клубочков, что приводит к массивной протеинурии, а в дальнейшем к гипопротеинемии и снижению коллоидно-осмотического давления, откуда и возникают отеки. Ко всему вышесказанному, отекам способствует активация гиалуронидазы и гипокальциемии, вызванной гиперкальциурией. Следует отметить, что у больных гломерулонефритом во время беременности отеки появляются чаще, чем вне беременности, причем это не связано с обострением заболевания.
Еще одним симптомом для гломерулонефрита является артериальная гипертензия, которая встречается у 35 % беременных, больных гломерулонефритом. Артериальная гипертензия, связанная с увеличением объема циркулирующей крови вследствие уменьшения глубочковой фильтрации и ретенции натрия и воды. Отсюда увеличивается приток крови к сердцу, возрастает минутный объем крови, при этом периферическое сопротивление кровотоку снижается.
Механизм гипертензии при хроническом гломерулонефрите отличается, развивается эукинетический (с нормальным сердечным выбросом) или гипокинетический (с уменьшенным минутным объемом крови) тип кровообращения, к тому же периферическое сопротивление кровотоку увеличивается.
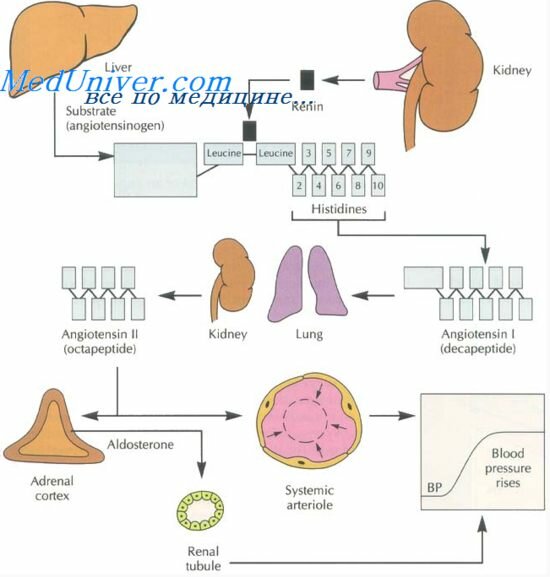
В процессе регуляции артериального давления огромное значение имеет адекватное функционирование системы ренин-ангиотензин-альдестерон и ретенции натрия, именно нарушения в этой системе приводят к развитию гипертензии при гломерулонефрите. Во время беременности почечный кровоток у больных гломерулонефритом уменьшен. При гипертонической и смешанной формах гломерулонефрита он составляет в первом триместре 820 мл/мин, во втором — 780 мл/мин, в третьем — 720 мл/мин, в то время как у здоровых беременных этот показатель равен соответственно 1460, 1150 и 1045 мл/мин (Шехтман М.М. и соавторы, 1982).
При столь значительных изменениях стоило бы ожидать резкого увеличения секреции и активации ренина и альдостерона, но у беременных, больных гломерулонефритом, наблюдается снижение активности ренина, т.е. при беременности происходят изменения, противоположные тем, которые характерны для гипертензии вне беременности. Объяснением этому может служить то, что ренин во время беременности секретируется не только юкстагломерулярным аппаратом почек, но и плацентой. Следует отметить, что такого понятия, как “относительный гиперальдостеронизм”, обусловленного дефицитом прогестерона — антагониста альдостерона по влиянию на экскрецию натрия почечными канальцами, также не существует во время беременности, что объясняется увеличением прогестерона в крови во время беременности у больных гломерулонефритом в 10 раз (у здоровых беременных увеличивается в 9,3 раза), в то время как экскреция альдостерона отстает. Имеются данные о роли депрессорных веществ в генезе артериальной гипертензии у беременных, в частности о значении дефицита кининов и простогландинов А и Е, но эти данные мало изучены.
Протеинурия при гломерулонефрите возникает в результате поражения подоцитов эпителиальных клеток клубочковых капилляров, и в зависимости от степени их поражения количество выделяемого с мочой белка разное. Протеинурия такого происхождения обратима и может исчезнуть под влиянием лечения. Поражение эндотелия и базальной мембраны наблюдается при длительном течении заболевания, что приводит к протеинурии, которая не исчезает после лечения.
У беременных, больных гломерулонефритом, протеинурия составляет от 0,033 г/л до 30 г/л; наиболее высока она при нефротической форме хронического гломерулонефрита. Некоторые авторы отмечают усиление протеинурии во время беременности, порою она становится массивной, после родов протеинурия обычно снижается до исходной. Наиболее вероятной причиной является присоединение гестоза, что подтверждается появлением других признаков этого осложнения беременности и быстрой ликвидацией протеинурии после родов.
Еще одним немаловажным симптомом патологии почек может служить малокровие. Нарушение функциональной активности костного мозга отмечается уже на ранних стадиях заболевания. Изменения в крови связаны со снижением эритропоэтина, стимулирующий дифференциацию гемоцитобластов костного мозга в сторону эритробластов, он же повышает синтез гемоглобина. Для заболеваний почек характерна нормохромная, реже гипохромная анемия. Формируется так называемый порочный круг: нарушение эритропоэтической функции почек ведет к развитию анемии, а почки очень чувствительны к гипоксии; снижение количества гемоглобина сопровождается нарушением деятельности канальцев, что усугубляет течение основного заболевания.
Одним из факторов развития анемии при остром гломерулонефрите является также разведение крови вследствие гиперволемии и прежде всего гидремии.
По клиническому течению различают острый и хронический гломерулонефрит.
Острый гломерулонефрит чаще принимает циклическую форму, реже встречается ациклическая форма.
Для циклической формы гломерулонефрита характерно появление симптомов заболевания через 10 дней (от 1 до 3 недель) после стрептококкового заболевания или вакцинации. Появляются головная боль, боли в пояснице, одышка, отеки на лице, часто олигурия; повышается давление; у 1/3 беременных лихорадка. В анализах мочи с самого начала заболевания выраженные изменения: у многих больных легко заметен ее буро-красный цвет, характерный для макрогематурии. Микрогематурия выявляется почти у всех женщин, также как протеинурия и цилиндрурия. Именно наличие в осадке мочи эритроцитов и кровяных цилиндров подтверждает диагноз острого гломерулонефрита. Также определяется лейкоцитурия, но при количественном исследовании осадка мочи в ней преобладают эритроциты. Нередко наблюдается умеренная азотемия. Симптоматика заболевания сохраняется от нескольких дней до 2—3 недель, однако изменения мочи сохраняются долго (гематурия и протеинурия сохраняются в течение нескольких месяцев).
Ациклическая форма острого гломерулонефрита начинается постепенно, проявляется маловыраженными отеками на ногах, слабостью, небольшой отдышкой и случайно обнаруживаемыми изменениями в моче: протеинурией или гематурией. Эта форма чаще приобретает хроническое течение. Для беременности острый гломерулонефрит является нечастым заболеванием, оно более характерно для детского и юношеского возраста. Плюс ко всему во время беременности отмечается гиперпродукция глюкокортикоидов, препятствующая развитию острого гломерулонефрита.
У больных острым гломерулонефритом беременность редко завершается благополучно, в основном плод погибает внутриутробно или заболевание приводит к преждевременному прерыванию беременности. Более благоприятен прогноз при остром гломерулонефрите без гипертензии и азотемии.
Во второй половине беременности острый гломерулонефрит может быть принят за гестоз.
В пользу гломерулонефрита будут изменения анализа мочи (гематурия, кровяные цилиндры) и высокий титр анти-О-стрептолизина.
Острый гломерулонефрит, не вылеченный в течение года, считают перешедшим в хронический нефрит.
Хронический гломерулонефрит. Во время беременности обострение хронического гломерулонефрита происходит очень редко. У большинства женщин симптоматика обострения хронического гломерулонефрита такая же, как и до беременности (гипертензия, отеки, протеинурия в зависимости от формы гломерулонефрита).
Редко во время беременности возникает такая форма заболевания, как очаговый гломерулонефрит, которая развивается непосредственно во время инфекционного заболевания. При этом в результате прямого токсическо-бактериального воздействия поражается только часть нефронов. Отмечаются изменения в моче: гематурия, небольшая протеинурия, изредка цилиндрурия. Симптоматика выражена незначительно, основные жалобы на течение самого инфекционного процесса (грипп, ангина, пневмония, аппендицит и др.).
Гломерулонефрит оказывает неблагоприятное влияние на течение беременности и особенно на состояние плода. У таких женщин чаще развивается гестоз, раньше обычных сроков (28 недель). Гестоз так же, как и другие осложнения (преждевременные роды, незрелость плода), зависит от того, протекает ли гломерулонефрит с повышенным или нормальным артериальным давлением. Наиболее тяжелые осложнения отмечаются во время беременности у женщин с гипертензивной формой хронического гломерулонефрита и нарушением функции почек. Известны данные течения беременности при гломерулонефрите: гестоз отмечается у 35 % женщин, нефропатия у 27 %, преэклампсия у 8 %, преждевременная отслойка нормально расположенной плаценты наблюдалась у 2 % женщин. К тому же известно, что задержка роста плода составляет 10 % у женщин с заболеванием почек с нормальным артериальным давлением и 35 % у беременных с хроническим заболеванием почек и гипертензией. Имеется и патология у детей, рожденных женщинами, болеющими гломерулонефритом – у них часто находят патологию почек.
Для удобства врачей акушеров-гинекологов выделено 3 степени риска, определяющие частоту неблагополучного исхода беременности и родов.
1 степень риска — минимальная, осложнения возникают не более чем у 20 % женщин.
2 степень риска — выраженная, экстрагенитальные заболевания часто вызывают осложнения беременности гестозом, самопроизвольным абортом, преждевременными родами; часто отмечается гипотрофия плода; увеличена перинатальная смертность — от 20 % до 50 %.
3 степень риска — максимальная, более 50 % — беременность представляет опасность для здоровья и жизни женщины, редко рождаются доношенные дети в удовлетворительном состоянии, высокая перитониальная смертность. У беременных, больных хроническим гломерулонефритом, степень риска зависит от формы заболевания.
1 степень риска — латентная форма и очаговый гломерулонефрит.
2 степень риска — нефротическая форма.
3 степень риска — гипертоническая и смешанная формы, азотемия при любой форме нефрита, а также острый гломерулонефрит и обострение хронического.
Женщины с хроническим гломерулонефритом должны быть обследованы в первые 12 недель беременности для уточнения формы заболевания вопроса о сохранении беременности.
Лечение
Беременные, больные гломерулонефритом, должны соблюдать режим, который позволял бы проводить дневной отдых в постели. Большая роль в лечении гломерулонефрита отводится диете. Основное требование заключается в ограничении поваренной соли и жидкости (при остром нефрите до 3 г соли в сутки; по мере ликвидации отеков потребление соли можно несколько увеличить). Количество выпитой жидкости, вводимое парентерально, должно соответствовать диурезу, выделенному накануне, плюс 700 мл жидкости, теряемой внепочечным путем. Во время беременности не рекомендуется ограничивать потребление белка, что советуют больным гломерулонефритом. Для нормального развития плода оправдана диета, содержащая повышенное количество белка (120—160 г в сутки). При беременности применяется только симптоматическое лечение, в этиологической терапии нет необходимости, поскольку острый гломерулонефрит возникает редко. А если течение гломерулонефрита легкое, латентные беременные вообще не нуждаются в лекарственной терапии.
Лекарственное лечение почечной симптоматической гипертензии производится прежде всего антагонистами кальция, бета-адреноблокаторами, диуретиками, альфа-адреноблокаторами. У беременных женщин с этой же целью возможно применять физиотерапию: гальванизацию зоны “воротника” (у больных с эмоциональной неустойчивостью, повышенной раздражительностью, невротическими реакциями) или эндоназальный электрофорез. Ультразвук на область почек в импульсном режиме излучения обладает выраженным вазотропным влиянием (расширяет сосуды) и оказывает противовоспалительное, десенсибилизирующее действие. Эти методы позволяют снизить дозы гипотензивных средств, что немаловажно во время беременности. У беременных с гломерулонефритом, несмотря на протеинурию, гиповолемии обычно нет. Для лечения отеков у беременных могут быть использованы диуретические препараты. В лечении гипопротеинемии используется сухая плазма (в разведении бидистилированной водой в отношении 1. 3 вводят по 200—300 мл внутривенно капельно 2—3 раза в неделю) или раствор альбумина и протеин по 200—300 мл.
Непременно следует уделять внимание лечению анемии у беременных, больных гломерулонефритом, назначаются препараты железа, витамины группы В, фолиевая кислота, хотя данная терапия не всегда эффективна, более надежно переливание эритроцитной массы.
При лечении хронического гломерулонефрита также используются антиагреганты: теоникол по 0,15 г 3 раза в сутки, трентал по 0,1 г 3 раза в сутки, курантил по 0,05 г 4 раза в сутки или никошпан по 1 таблетке 3 раза в день. Может применяться гепарин по 20 000 ЕД в сутки подкожно. Назначая терапию, нужно помнить, что непрямые антикоагулянты противопоказаны беременным и родильницам, поскольку могут вызвать у плода и новорожденного геморрагический синдром, снижение уровня протромбина и смерть.
Имеются данные о хороших результатах в лечении хронического гломерулонефрита у беременных фитотерапии (череда, тысячелистник, фиалка трехцветная, смородина черная, толокнянка, земляника).
Лечение очагового нефрита предусматривает в первую очередь терапию основного заболевания антибиотиками, диету с ограничением поваренной соли (до 5 г в сутки) и назначение легкоусвояемых углеводов, а также витаминов С и Р.
Основное, о чем помнят врачи акушеры-гинекологи о развитии у беременных с гломерулонефритом осложнений беременности, чаще всего нарушения маточно-плацентарной гемодинамики. В связи с этим патогенетически обосновано применение препаратов, нормализующих тромбоцитарно-эндотелиальное взаимодействие и улучшающих как маточно-плацентарный, так и почечный кровоток. В качестве такого препарата используется аспирин в дозе 45 мг/кг при сроке с 28 по 38 неделю, с 12—19 неделю. Совместно с аспирином рекомендуют применение курантила, способного повышать выработку простациклина, уменьшающего коагуляционную способность крови.
Хронический гломерулонефрит — Острый гломерулонефрит
Страница 4 из 7
Хронический гломерулонефрит — воспалительное заболевание почек иммунного генеза с первичным и преимущественным поражением клубочков, канальцев и интерстиция обеих почек и прогрессирующем течением, в результате чего развивается нефросклероз и ХПН.
Эпидимиология. заболеваемость первичным хроническим гломерулонефритом составляет 13-50 случаев на 10 000 населения; для вторичного хронического гломерулонефрита заболеваемость зависит от распространённости основного заболевания. По сравнению с острым — встречается в 2-4 раза чаще. Основная масса больных (88 %) находится в возрастном диапазоне 16-50 лет. Первичный гломерулонефрит наблюдается в два раза чаще у мужчин, чем у женщин.
Этиология: наиболее часто хронический гломерулонефрит является следствием перенесенного ( ОГН Г в анамнезе у 1/3 больных ХГ)
Признается развитие первично – хронического гломерулонефрита. Большое значение придается генетической предрасположенности к развитию хронического гломерулонефрита. Развитие заболевания связывают с наличием длительно существующих очагов инфекции, однако часто причину заболевания выяснить не удается.
Патогенез: механизмы развития хронического гломерулонефрита, в целом аналогичен патогенезу острого гломерулонефрита. т.е в основе лежит иммунный воспалительный процесс, в развитии, которого принимают участие отложение антител и фрагментов комплимента, формирование комплиментмембраноповреждающего комплекса, коагуляционные факторы крови, лейкотриены, цитокины, нейтрофилы, тромбоциты, макрофаги, Т- лимфоциты.
Наряду с иммунными реакциями большое значение имеют и неиммунные механизмы прогрессирования, к которым относят: развитие прогрессирующего почечного фиброза; гемодинамические факторы; метаболические механизмы; коагуляционные механизмы; тубулоинтерстициальный склероз.
Иммуновоспалительный процесс сопровождается репаративными изменениями, исходы которых различны: возможно, полное восстановление структуры клубочков или при неблагоприятном течении – развитие прогрессирующего фиброза, который является основой хронической почечной недостаточности. Прогрессирующий почечный фиброз обусловлен гиперфункционированием гломерулярных клеток и клеток крови, инфильтрирующих клубочки почек, что сопровождается избыточным накоплением соединительнотканного матрикса и одновременно недостаточной его утилизацией.
Ведущую роль в прогрессирование гломерулосклероза играют мезангиальные клетки. При хроническом гломерулонефрите имеет место пролиферация мезангиоцитов. повышенный синтез ими компонентов мезангиального матрикса, расширение и склероз матрикса. При хроническом гломерулонефрит установлено снижение активности протеолитических ферментов. Это нарушает резорбцию отложившегося матрикса, и, следовательно способствует дальнейшему накоплению его в клубочках почек.
Важную роль в развитие прогрессирующего почечного фиброза играет ангиотензин 2. он не только обуславливает внутриклубочковую гипертензию, но стимулирует пролиферацию мезангиальных клеток почечных клубочков.
Гемодинамические нарушения (артериальная гипертензия)
Ведущую роль в прогрессировании нефритов играет артериальная гипертензия. Патогенез почечной артериальной гипертензии сложен, среди механизмов ее развития наиболее важными признаны следующие
— задержка натрия и воды с увеличением объема циркулирующей крови, сердечного выброса и накопления натрия в сосудистой стенке с ее отеком
— повышение чувствительности сосудистой стенки к прессорным агентам, что создает основу для увеличения общего периферического сосудистого сопротивления
— активация прессорных систем организма – ренин- ангиотензиновой системы и тесно связанной с ней альдестероновой, вазопрессина, системы катехоламинов
— недостаточность почечных депрессорных систем – простагландинов, кининов.
Возникновение артериальной гипертензии резко ухудшает прогноз болезни и ускоряет прогрессирование почечной недостаточности.
Во-первых, АГ приводит к снижению кровоснабжению почек и развитию ишемии;
Во-вторых — системная артериальная гипертензия вызывает нарушение внутрипочечной гемодинамики – внутриклубочковую гипертонию и гиперфильтрацию. Последние два фактора считаются ведущими причинами неиммунного (гемодинамического) прогрессирования почечной недостаточности
Метаболические нарушения.
Важнейшее значение среди метаболических нарушений в прогрессировании хронического гломерулонефрита имеют липидные сдвиги. Они наиболее часто встречаются у лиц с нефротическим синдромом, но развиваются также и при гломерулонефрите без нефротического синдрома. Изменения липидного обмена чаще всего заключается в повышении содержание в крови холестерина, триглециридов, липопротеинов низкой плотности. Нарушение липидного обмена сопровождается нефротоксическим действием. Нарушения липидного обмена при хроническом гломерулонефрите сопровождаются активацией перекисного окисления липидов с образованием свободных радикалов и перекисных соединений, оказывающих повреждающее действие на почки и способствующих развитию фиброза.
Коагуляционные механизмы
Следующим механизмом прогрессирования хронического гломерулонефрита является локальная внутрисосудистая коагуляция крови с образованием микротромбов в капиллярах клубочков и отложению в них фибрина. Ведущую роль в развитие внутрисосудистой гемокоагуляции в почках играет повреждение эндотелия иммунными комплексами, цитокинами медиаторами воспаления.
Классификация хронического гломерулонефрита
Современная классификация хронического гломерулонефрита базируется на результатах исследования биоптатов почек с помощью световой, электронной и иммунофлюресцентной микроскопии. Однако выполнение биопсии почек возможно только в специализированном нефрологическом отделении. Поэтому наряду с морфологической классификацией существует и клиническая классификация хронического гломерулонефрита
Классификация ХГ по И. Е.Тареевой ( 1995)
- нефротический ХГ
- латентный или ХГ с изолированным мочевым синдромом
- гематурическая форма
- гипертоническая форма
- смешенная форма хронического гломерулонефрита
- терминальный ХГ ( конечная стадия гломерулонефрита любого типа).
В течении хронического гломерулонефрита различают
— фазу ремиссии, при которой наблюдается небольшая гематурия, умеренная диспротеинемия и стабилизация артериального давления, и
— фазу обострения с тремя степенями активности.
В 1978 году (Лондон) экспертами ВОЗ разработана морфологическая классификация гломерулонефрита.
- Минимальные изменения (липоидный нефроз).Основной и характерный признак – деструкция малых отростков подоцитов на фоне очагового набухания, разрыхления и утолщения базальных мембран и пролиферации эндотелия лишь в отдельных петлях клубочковых капилляров. Клинически проявляется нефротическим синдромом. Диагностируется только при электронной микроскопии.
- Мембранозный-гломерулонефрит. Резкое диффузное утолщение, набухание и расщепление базальных мембран клубочков капилляров в нескольких (очаговый) либо всех (диффузный) капиллярных петлях клубочка.
- Мембранозно-пролиферативный (мезангиокапилярный). Идет сочетание мембранозных и пролиферативных изменений в клубочках, которые носят диффузный характер. Клинически проявляется латентной формой нефрита.
- Пролиферативный-интракапиллярный. Характеризуется выраженной пролиферацией клеток эндотелия и мезангия при сравнительно незначительных изменениях базальной мембраны клубочков.
- Пролиферативный-экстракапиллярный. Характеризуется наличием полулуний, образующихся вследствие пролиферации клеток эпителия капсулы клубочка, которые, заполняя просвет капсулы, образуют полулуния, сдавливают капиллярные петли клубочка и нарушают в них кровообращение. Одновременно отмечается экссудация и выпадение фибрина в полость капсулы клубочка. Экстракапиллярный нефрит составляет основу злокачественного (подострого) гломерулонефрита.
- Фибропластический (склерозирующий). Представляет собой собирательную эволютивную форму мембранозно-пролиферативного и пролиферативного нефрита с минимальными изменениями.
- Диффузный мезангиопролиферативный гломерулонефрит
Нефритический синдром
Нефритический синдром ( НС )– это проявление острого воспаления клубочков.
В тяжелых случаях он развивается быстро (от нескольких суток до 1 – 2 недель и сопровождается ОПН и олигоурией (диурез менее 400 млсутки ). Почечный кровоток и СКФ снижаются из-за обструкции клубочковых капилляров лейкоцитами и пролиферирующими клетками клубочка, эти нарушения усугубляются из-за спазма артериол и сокращения мезангиальных клеток.
Из за снижения СКФ и усиления канальцевой реабсорбции натрия и воды увеличивается объем внеклеточной жидкости и развиваются отеки и артериальная гипертония.
Проявляется активным мочевым осадком, содержащим эритроцитарные цилиндры, измененные эритроциты (возможно макрогематурия) и лейкоциты, а также протеинурией (обычно менее 3,5 г/ сутки). Возникает вследствие повреждения стенок клубочковых капилляров.
Типичная морфологическая картина при нефритическом синдроме — это пролиферативный гломерулонефрит. В начале число клеток в клубочке увеличивается за счет инфильтрации нейтрофилами и макрофагами, а позже начинают пролиферировать эндотелиальные и мезангиальные клетки клубочка (эндокапиллярная пролиферация).
В тяжелых случаях поражено более 50% клубочка (диффузный пролиферативный гломерулонефрит).
В более легких — менее 50% (очаговый пролиферативный нефрит).
В наиболее легких случаях пролиферация ограничивается мезангием (мезангиопролиферативный гломерулонефрит).
Нефротический синдром
Нефротический синдром имеет множество проявлений. Это в первую очередь:
- высокая протеинурия (более 3,5 гр в сутки ),
- гипо и диспротеинемия (гипоальбуминемия),
- гиперлипидемия (гиперхолестеринемия),
- отеки,
- и повышение свертываемости крови.
Важно отметить, что первичное нарушение — это протеинурия, которая возникает из-за повышенной проницаемости клубочкового фильтра при повреждении клубочковой базальной мембраны и фильтрационных щелей между ножками подоцитов. Все остальные проявления нефротического синдрома — это следствие протеинурии
Гипоальбуминемия – прямое следствие протеинурии; уровень белка те ниже чем, чем выше его экскреция с мочой. Другие причины гипоальбуминемии — распад реабсорбированного белка в проксимальных канальцах и недостаточный синтез альбуминов печенью.
Отеки — существует две теории образование отеков при нефротическом синдроме наиболее распространенная «гиповолемическая » теория описывающая этот процесс так. при гипоальбуминемии снижается онкотическое давление плазмы, что приводит к выходу воды из сосудов в интерстиций. В ответ на уменьшение ОЦК активируется ренин –ангиотензиновая система, повышается симпатический тонус, секреция АДГ растет, а секреция предсердного натрийуретического гормона падает. Все это приводит к задержке натрия и воды. Однако, существует второй механизм образование отеков (гиперволемический вариант ) в этом случае ОЦК повышен. а ренин –ангеотензиновая система подавлена. Вероятно в таких случаях образование отеков обусловлено задержкой натрия и воды.
Гиперлипидемия — развивается из-за того, что печень усиливает выработку липопротеидов в ответ на снижение онкотического давление плазмы, а так же из-за потери с мочой белков, регулирующих обмен липопротеидов. Уровни ЛПНП и холестерина повышены у большинства больных, а ЛПОНП и триглицеридов – в наиболее тяжелых случаях.
Повышение свертывание крови — имеет несколько причин: потеря с мочой антитромбина 3, усиленный синтез фибриногена печени, ослабление фибринолиза и повышенная агрегация тромбоцитов. Клинически это проявляется ТЭЛА и тромбозами периферических сосудов.
Группа воспалительных (нефритических) поражений клубочка:
- очаговый пролиферативный гломерулонефрит (если пролиферируют в основном клетки мезангия, он называется мезангиопролиферативным ),
- диффузный пролиферативный
- экстракапилярный гломерулонефрит..
Группа заболеваний с поражением подоцитов и базальной мембраны, т.е. тех слоев клубочкового фильтра, которые образуют основной барьер для белка:
- мембранозная нефропатия,
- болезнь минимальных изменений
- фокально-сегментарный гломерулосклероз
Эти заболевания проявляются высокой (свыше 3 гсутки ) протеинурией и скудным мочевым осадком (единичные эритроциты, лейкоциты и клеточные цилиндры). Высокая протеинурия ведет к гипоальбуминемии, отекам и гиперхолестеринемии, те есть к развитию нефротического синдрома.
Группа заболеваний с объединенными чертами двух выше описанных групп.
- Мезангиокапилярный гломерулонефрит объединяет черты двух описанных выше групп. Морфологически он характеризуется поражением базальных мембран в сочетании с пролиферацией клеток клубочка (от сюда и другое название болезни — мембраннопролиферативный гломерулонефрит), а клинически — сочетанием нефротического и нефритического синдромов.
Основные симптомы при остром гломерулонефрите
Отёки — одно из основных проявлений ОНС — возникают у 60—80% больных. Степень выраженности может варьироваться в широких пределах: от отёков век по утрам до выраженной отёчности лица, голеней, передней брюшной стенки. Очень редко, но могут развиваться полостные отёки: гидроторакс, гидроперикард, асцит. За период нарастания отёков больные могут прибавить в весе 2—5 кг. Появление отёков происходит постепенно. Они плотные, малоподвижные.
Механизм формирования отёков:
• увеличение объёма циркулирующей крови в результате снижения клубочковой фильтрации — гиперволемия;
• задержка натрия и воды (гиперальдостеронизм, повышение секреции АДГ);
• повышенная сосудистая проницаемость в результате гиалурони- дазной активности стрептококка, выброса гистамина и активации калликреин-кининовой системы.
Образование периферических отёков можно рассматривать как компенсаторный механизм, так как часть жидкости из сосудистого русла перемещается в ткани, уменьшая гиперволемию, и это препятствует развитию осложнений. С депонированием жидкости может быть также связано увеличение печени и селезёнки. Отёки обычно легко купировать назначением бессолевой диеты и диуретических препаратов. Длительность отёков составляет 5—14 дней.
Артериальная гипертензия
Артериальная гипертензия — один из грозных симптомов острого гломерулонефрита (ОГН) — возникает у 60—70% больных. Больные жалуются на головную боль, тошноту, рвоту. Развитие артериальной гипертензии происходит быстро. С ней чаще всего связаны осложнения: эклампсия и острая сердечная недостаточность. Артериальная гипертензия носит систоло-диастолический характер, но с большим подъёмом систолического давления. Механизм артериальной гипертензии при ОНС:
• гиперволемия, т.е. увеличение объёма циркулирующей крови (ОЦК), происходит в связи с падением клубочковой фильтрации, задержкой воды и натрия;
• гораздо меньшую роль играет активация ренин-ангиотензин- альдостероновой системы.
В силу того, что основным механизмом развития артериальной гипертензии служит гиперволемия, она легко поддаётся лечению (бессолевая диета, диуретики), реже возникает необходимость в назначении антигипертензивных препаратов. Нельзя вводить препараты, увеличивающие ОЦК. Длительность гипертензионного синдрома — 7—14 дней.
Мочевой синдром
Олигурия — уменьшение нормального диуреза на 20—50% нормы. Возникает олигурия в связи с падением клубочковой фильтрации и повышенной реабсорбцией воды и натрия, развитием «антидиуреза» и повышением секреции АДГ. Относительная плотность мочи высокая. Олигурия возникает в первые дни заболевания и длится 3—7 дней.
Гематурия — одно из главных проявлений мочевого синдрома — возникает у 100% больных. Макрогематурию обнаруживают в начале заболевания у 60—80% больных, её выраженность постепенно уменьшается к 3—4-й неделе. У основной массы больных гематурия полностью прекращается к 8—10-й неделе, однако у некоторых микрогематурия остаётся в течение 6—12 мес.
Гематурия связана с повышенной проницаемостью БМ, её разрывами. В моче появляются дисморфичные эритроциты (изменённые, неправильной формы), что обусловлено их гломерулярным происхождением. Могут встречаться также эритроцитарные цилиндры.
Протеинурия — один из ведущих признаков поражения почек, во всех случаях необходимо установить суточную потерю белка. В норме она составляет 100—200 мг/сут. При ОНС суточная протеинурия колеблется в пределах от 1 до 2,5 г/сут. Белок, теряемый с мочой, плазменного происхождения и содержит мелкие и крупные белки, т.е. протеинурия неселективная. Ведущим механизмом протеинурии служат структурные изменения базальной мембраны (увеличение размеров пор, трещины) и функциональные изменения (потеря отрицательного заряда). Протеинурия постепенно уменьшается к 2—3-й неделе заболевания. Длительная протеинурия до 1,5—2 г/сут — плохой прогностический признак.
Лейкоцитурия при ОНС может возникать в первую неделю заболевания и имеет абактериальную природу. Она объясняется активным иммунным воспалением с привлечением на 1—2-й неделе в очаг воспаления нейтрофилов, лимфоцитов, моноцитов.
Цилиндрурия может присутствовать (30—60%) в начальном периоде. По своей структуре цилиндры — это тубулярный белок (уропротеин Тамма—Хорсфалла) с включением форменных элементов, эпителиальных клеток, детрита. При ОГН могут появляться эритроцитарные, зернистые цилиндры.
Для постановки диагноза, кроме клинической картины, большое значение имеет лабораторная диагностика.
В общем анализе крови в первые дни заболевания может быть диагностирована анемия, связанная с гиперволемией, т.е. анемия относительная. Могут быть обнаружены небольшой лейкоцитоз и увеличение СОЭ.
Этиологическую роль стрептококка подтверждает повышение концентрации АСЛ-О, а также высев из зева и носа гемолитического стрептококка.
Повышение содержания ЦРБ и серомукоида свидетельствует о воспалении, а увеличение количества ЦИК, иммуноглобулинов (G, М), снижение концентрации СЗ-компонента комплемента свидетельствуют об иммунном его характере. Содержание общего белка и альбуминов может быть несколько снижено, а холестерина — повышено.
В начальный период при олигурии возможно повышение концентрации мочевины и креатинина при высоком удельном весе мочи, что расценивают как почечную недостаточность острого периода.
При ультразвуковой диагностике отмечают увеличение размеров почек и нарушение дифференцировки структур.
Клиническая картина
Течение ОНС, как правило, циклическое, с постепенным уменьшением клинических и лабораторных показателей.
Прежде всего, происходит исчезновение клинических симптомов, в первую неделю заболевания нормализуются диурез, АД, исчезают отёки, снижается концентрация мочевины и креатинина. Нормализация количества комплемента происходит к 6—8-й неделе, исчезновение изменений осадка мочи происходит медленнее. Макрогематурия проходит через 2—3 нед, протеинурия — в течение 3—6 мес, исчезновение микрогематурии происходит в течение года.
Прогноз благоприятный. Выздоровление наблюдают в 85—90% случаев. Летальный исход бывает редко (менее 1%).
Дальнейшее ведение
Диспансерное наблюдение обязательно в течение 5 лет.
Осложнения при остром нефритическом синдроме
Осложнения при ОНС диагностируют у детей нечасто. В патогенезе всех осложнений ОНС лежат гиперволемия и электролитные нарушения.
Почечная эклампсия (5%), или ангиоспастическая энцефалопатия, может развиваться в первые дни ОНС. В клинической картине доминирует быстро нарастающая артериальная гипертензия при отсутствии или незначительных отёках и азотемии. Состояние больного быстро ухудшается, появляются сильная головная боль, тошнота, рвота, нарушение зрения, мелькание «мушек» перед глазами, в тяжёлых случаях — обратимая потеря зрения, судороги. Возникает тахикардия, превалирует повышение систолического давления. При спинномозговой пункции жидкость вытекает под давлением. Состояние, как правило, обратимое, но необходимо проведение немедленных лечебных мероприятий.
Отёк лёгкого развивается при бурном нарастании отёчного синдрома. Повышенная транссудация жидкости и отёк интерстиция лёгочной ткани происходят вследствие повышенной сосудистой проницаемости на фоне увеличения ОЦК и электролитных нарушений.
Клиническая картина: одышка, вынужденное сидячее положение, кашель, цианоз носогубного треугольника. В тяжёлом случае появляется розовая пенистая мокрота. В лёгких — жесткое дыхание и влажные мелкопузырчатые хрипы в задненижних отделах. Тоны сердца приглушены, тахикардия. При рентгенологическом исследовании грудной клетки: симметричные облаковидные тени, сливающиеся с корнем лёгкого. Нередко такие больные поступают с подозрением на пневмонию, однако обнаружение отёков и изменений в моче помогает правильно поставить диагноз.
Острая почечная недостаточность (ОПН) возникает в 2% случаев. Она характеризуется острым нарушением функции почек. В основе ОПН лежит внутри сосуд и стая блокада почечного кровотока в результате локального внутрисосудистого тромбоза. Нарастают олигурия при низком удельном весе мочи, азотемическая интоксикация, гиперкалиемия, ацидоз. Появляются выраженная головная боль, сонливость, тошнота, рвота, неврологические расстройства, парестезии. При высокой гиперкалиемии могут наступать тяжёлые нарушения сердечной деятельности.
Отсутствие эффекта от консервативной терапии в течение 3—5 дней или анурия 24 ч, повышение концентрации мочевины более 20—24 ммоль/л, гиперкалиемия более 7,5 ммоль/л, прибавка в весе более 5—7% в сутки служат показанием к гемодиализу.
Дифференциальная диагностика острого нефритического синдрома
Дифференциальную диагностику ОНС проводят с вторичными гломерулонефритами (системной красной волчанкой, узелковым полиартериитом) при которых, помимо поражения почек, существуют и другие симптомы: сыпи, артрит, лихорадка, нарастающая почечная недостаточность, злокачественная артериальная гипертензия. При выраженном отёчном синдроме проводят дифференциальную диагностику с отёками другого происхождения (сердечная недостаточность, аллергические отёки).
Если заболевание начинается с макрогематурии, то следует исключать опухоль почки, мочекаменную болезнь, геморрагический цистит, травму почки. Присутствие отёков и гипертензионного синдрома даёт основание исключить данные заболевания.
В редких случаях артериальная гипертензия выступает на первый план. Тогда следует исключать заболевания, характеризующиеся артериальной гипертензией (врождённые почечные аномалии, узелковый полиартериит, опухоль почки).
Иногда больные поступают уже с осложнениями ОНС в виде отёка лёгкого; нередко одышка и изменения в лёгких позволяют заподозрить пневмонию. Однако при отёке лёгких нет лихорадки, инфекционного токсикоза, процесс носит двусторонний характер.
Анализ мочи, как правило, даёт основание поставить правильный диагноз.
Острый гломерулонефрит с изолированным мочевым синдромом
ОГН с изолированным мочевым синдромом начинается постепенно, с симптомов интоксикации через 1—3 нед после перенесённой инфекции. Характеризуется только изменениями в моче в виде микро- или макрогематурии и протеинурии менее 2 г/сут. Отёки и артериальная гипертензия отсутствуют.
Лабораторная активность не выражена, функции почек не нарушены. В постановке диагноза может помочь снижение количества СЗ-компонента комплемента и небольшое повышение концентрации у-глобулина, повышение титра АСЛ-О, серомукоида.
Этот вариант ОГН очень труден для диагностики, достоверно подтвердить диагноз может только биопсия почек, однако её практически никогда не проводят. При морфологическом исследовании обнаруживают небольшую пролиферацию мезангиальных клеток и отложения И К, СЗ-компонента комплемента в мезангии. При наиболее распространённой форме (болезни Берже) находят отложение IgA и IgG.
Дифференциальную диагностику проводят:
• с наследственным нефритом (семейный анамнез, тугоухость);
• мочекаменной болезнью (почечная колика, транзиторная гематурия, камень на УЗИ или обзорном снимке брюшной полости);
• циститом (дизурические явления, выраженная бактериальная лейкоцитурия и транзиторная гематурия);
• опухолью почки (гематурия и пальпируемое образование в брюшной полости).
Течение заболевания ациклическое, нередко происходит переход в хронический процесс. Гематурия длится долго — до 6—12 мес.
Нефротический синдром при остром гломерулонефрите
Нефротический синдром — клинико-лабораторный симпто- мокомплекс, характеризующийся протеинурией [более 3 г/сут или 50 мгДкгхсут)], гипоальбуминемией (менее 30 г/л), гиперлипидемией и отёками, вплоть до анасарки. Данный вариант ОГН возникает с наибольшей частотой у детей раннего и дошкольного возраста (с 1 года до 7 лет). На этот возрастной период приходится 93% больных с НС, пик заболеваемости — на третьем году жизни. Чаще болеют мальчики.
Факторы, предшествующие заболеванию, в 30—40% случаев определить не удаётся; в 60—70% отмечают ОРВИ, детские инфекции, атопию. У детей с наибольшей частотой обнаруживают характерные морфологические изменения, называемые минимальными, или болезнью «малых ножек подоцитов». В литературе такая форма нефротического синдрома именуется НС с минимальными изменениями (НСМИ).
Клиническая картина НСМИ характеризуется быстрым появлением отёков, реже отёки развиваются постепенно. При этом общее состояние остаётся относительно удовлетворительным. Появление отёков нередко расценивают как прибавку веса. При небольших отёках видны следы от перетягивающей одежды, трусов, носков, обуви. В тяжёлых случаях появляется отёк лица, голеней, передней брюшной стенки, мошонки, полостные отёки (гидроторакс, гидроперикард, асцит), вплоть до развития анасарки.
В формировании отёков первостепенную роль играет выраженная протеинурия, приводящая к гипопротеинемии, гипоальбуминемии. Поскольку альбумин служит основным белком, удерживающим воду в сосудистом русле (одна молекула альбумина удерживает 7 молекул воды), то его снижение способствует уменьшению онкотического давления и перемещению жидкости в ткани и развитию гиповолемии.
Низкий ОЦК, возбуждая рецепторы сосудистой стенки, включает компенсаторные механизмы поддержания внутрисосудистого объёма — гормональную регуляцию. Происходит повышенное выделение натрийзадерживающего гормона — альдостерона и АДГ. Однако задержанная жидкость вновь поступает в ткани. Нефротические отёки — мягкие, легко смещаемые, подвижные, так как они безбелковые.
Артериальная гипертопия для НСМИ не характерна, хотя в 4—10% возможно кратковременное повышение АД, что объясняют централизацией кровообращения. Возможно появление жидкого стула как результат отёка слизистой оболочки кишечника.
Подтверждением нефротического синдрома служит протеинурия более 3 г/сут или 50 мг/(кгхсут). Протеинурия селективная, так как через потерявшие отрицательный заряд БМ проходят белки низкомолекулярных фракций (в основном альбумины). Гематурия и лейкоцитурия не характерны. Относительная плотность мочи высокая (1026—1030).
В анализе крови возможно повышение количества эритроцитов (гиповолемия) и увеличение СОЭ до 50—70 мм/ч. Концентрация сывороточного белка снижена в результате уменьшения содержания альбуминов. По степени снижения концентрации альбуминов определяют тяжесть течения НС:
• средняя тяжесть — гипоальбуминемия от 30 до 20 г/л;
• тяжёлое течение — гипоальбуминемия менее 20 г/л;
• крайне тяжёлое — гипоальбуминемия менее 10 г/л. Диспротеинемия характеризуется относительным повышением концентрации а2- и р-глобулинов, так как они относятся к крупнодисперсным фракциям и не проходят через БМ.
Высокая гиперлипидемия обусловлена нарушением образования, транспорта и расщепления липидов. В крови повышена концентрация холестерина, триглицеридов и липопротеинов высокой плотности. Повышение содержания липидов коррелируется со снижением концентрации альбуминов.
Часто отмечают гиперфибриногенемию, снижение AT III и фибринолитической активности, что может быть причиной тромбозов.
Функция почек даже в острый период нарушается крайне редко.