Ишемическая болезнь сердца (ИБС)
Ишемическая болезнь сердца (ИБС) — это несоответствие коронарного кровотока потребностям миокарда в кислороде, приводящее к ишемии сердечной мышцы и развитию кардиосклероза. ИБС может протекать в виде двух основных форм: стенокардии и инфаркта миокарда.
Этиология
Основным этиологическим фактором ИБС является атеросклероз коронарных сосудов.
Факторами риска развития ИБС являются гиперлипидемия, артериальная гипертензия, курение, гиподинамия, избыточная масса тела, обменные нарушения (сахарный диабет), генетическая предрасположенность.
Стенокардия
— это клинический синдром, проявляющийся чувством стеснения или болью в грудной клетке сжимающего или давящего характера, которая локализуется чаще всего за грудиной и может иррадиировать в левую руку, шею, нижнюю челюсть. Стенокардия может возникать не только как проявление ИБС, но и при аортальном стенозе. гипертрофической кардиомиопатии. тяжелой артериальной гипертензии с выраженной гипертрофией левого желудочка
Классификация
Формы стенокардии:
1) впервые возникшая стенокардия — длительностью менее 1 месяца. Характерна полиморфность течения. Впервые возникшая стенокардия может исчезнуть, перейти в стабильную стенокардию или быстро прогрессировать;
2) стабильная стенокардия — давность заболевания более 1 месяца. Характеризуется возникновением типичных ангинозных приступов.
Выделяют 4 функциональных класса стабильной стенокардии.
Функциональный класс I: обычная физическая нагрузка не вызывает ангинозных приступов. Они возникают лишь при чрезмерных нагрузках, выполняемых длительно и в быстром темпе (латентная стенокардия). При обследовании определяется высокая толерантность к стандартизованной велоэргометрической пробе.
Функциональный класс II: небольшое ограничение обычной физической активности. Приступы стенокардии возникают при среднем темпе ходьбы ( 80—100 шагов в 1 минуту) по ровному месту на расстояние свыше 500 м, при подъеме по лестнице выше одного этажа
Функциональный класс III: выраженное ограничение обычной физической активности. Приступы возникают при ходьбе в среднем темпе по ровному месту на расстояние 100—500 м, при подъеме вверх по лестнице на один этаж.
Функциональный класс IV: ограничение физической активности резко выражено. Стенокардия возникает при ходьбе по ровному месту на расстояние менее 100 м и в случаях минимальных бытовых и эмоциональных нагрузок. Возникают приступы стенокардии в покое.
Клиника
Основным симптомом стенокардии является типичный болевой приступ, связанный с повышением потребности миокарда в кислороде на фоне низкой возможности его доставки. Чаще всего доставка ограничивается из-за сужения просвета коронарных артерий атеросклеротическими бляшками или длительным спазмом артерий. При стенокардии возникают сжимающие, давящие или жгучие боли за грудиной или в области сердца слева от грудины, возникающие при физической нагрузке или эмоциональном напряжении, длящиеся от 2—3 до 10—15 мин и исчезающие с уменьшением нагрузки или ее прекращением. Часто эти боли иррадиируют в левую руку к мизинцу, левую лопатку, нижнюю челюсть слева или левую половину шеи. После приема нитроглицерина боль купируется.
Прием нитроглицерина эффективен и для профилактики ангинозного приступа. После его приема толерантность к физической нагрузке увеличивается на 20—30 мин.
Возникновение приступа стенокардии зависит также от метеорологических условий и времени суток. Стенокардические боли чаще возникают при физической нагрузке (ходьбе) в утренние часы и в холодную ветреную погоду.
При атипичном течении больной может жаловаться на одышку или удушье, изжогу или приступы слабости в левой руке, которые при условии эффективности нитроглицерина следует расценивать как эквивалент стенокардических проявлений.
Прогрессирующая (нестабильная) стенокардия формируется чаще на фоне стабильной. Она проявляется нарастающими по частоте, продолжительности и интенсивности типичными болевыми приступами с выраженным снижением толерантности к физическим нагрузкам, а также с увеличением площади локализации болей, путей их иррадиации, снижением эффекта от приема нитроглицерина Причиной прогрессировать, как правило, является быстро-нарастающее сужение просвета сосуда из-за повреждения бляшки или развития тромбоза.
Спонтанная стенокардия (стенокардия Принцметала) проявляется приступами ангинозных болей, возникающих без видимой связи с провоцирующими факторами, приводящих к повышению потребности миокарда в кислороде.
У большинства больных этой формы приступы стенокардии возникают в строго определенное время суток, чаще ночью или в момент пробуждения. Такой болевой приступ состоит из серии болевых эпизодов ( 3—5 ), чередующихся с безболевыми промежутками. Причиной развития стенокардии Принцметала является спазм крупных, чаще субэпикардиальных, артерий. Часто эта форма стенокардии сопровождается различными нарушениями сердечного ритма.
Осложнения
При типичном течении стенокардии осложнений нет.
Диагностика
Ведущим методом диагностики стенокардии является ЭКГ. Однако для ИБС не существует патогномоничных изменений ЭКГ, и подтвердить ее наличие могут выявление характерных ЭКГ-признаков (депрессии сегмента SТ, свидетельствующей об ишемии миокарда, возможно, в сочетании с коронарным зубцом Т) во время приступа и их быстрое исчезновение.
Для выявления признаков стенокардии применяют пробы с физической нагрузкой, в первую очередь велоэргометрию. Показаниями к проведению велоэргометрии являются:
1) атипичный болевой синдром;
2) отсутствие изменений на ЭКГ при подозрении на ИБС;
3) не свойственные ишемии миокарда изменения на ЭКГ у лиц среднего и пожилого возраста, а также у молодых мужчин с предварительным диагнозом ИБС.
Проведение проб с физической нагрузкой противопоказано при:
1) остром инфаркте миокарда;
2) частых приступах стенокардии напряжения и покоя;
4) прогностически неблагоприятных нарушениях ритма и проводимости;
6) тяжелых формах артериальной гипертензии;
7) острых инфекционных заболеваниях.
Проба считается положительной, если в момент нагрузки отмечают:
1) возникновение приступа стенокардии;
2) появление выраженной одышки, удушья;
3) снижение артериального давления;
4) снижение сегмента SТ на 1 мм и более;
5) подъем сегмента SТ на 1 мм и более.
Кроме того, для диагностики ИБС проводят различные медикаментозные пробы с дипиридамолом, эргометрином и др.
При рентгеноскопии можно выявить признаки атеросклероза аорты .
При биохимическом исследовании можно выявить гиперлипидемию как фактор риска развития заболевания. Изменения не являются специфическими и не связаны с основным заболеванием.
Лечение
Лечение стенокардии необходимо начинать с низкой разовой дозы таблетированных форм нитратов (для тринитратов с 5,6—6,4 мг, для динитратов — с 10—20. для мононитратов — с 10—30 мг) с дальнейшим постепенным ее повышением до достижения клинического эффекта.
Прием нитратов может приводить к появлению побочных эффектов: распирающей головной боли, головокружения, ортостатического коллапса. Побочные эффекты пролонгированных нитратов можно уменьшить путем одновременного приема аспирина или парацетамола.
Нитраты, являющиеся периферическими вазодилататорами, способствуют депонированию крови в венозной системе, снижают венозный возврат к сердцу (преднагрузку на миокард), следовательно, снижают постнагрузку, предупреждают и снимают спазм в нормальных и пораженных атеросклеротическим процессом артериях.
Для лечения больных стенокардией широко применяются неселективные β-адреноблокаторы (пропранолол, окспренолол).
Пропранолол применяют внутривенно взрослым по 5—10 мл 0,1%-ного раствора внутрь 1—3 раза в сутки, начальная доза — 20 мг, разовая — 40—80 мг, максимальная суточная — 320 мг. Кратность применения — 2—3 раза в сутки.
Окспренолол применяют внутрь при стенокардии напряжения по 20 мг 3 раза в день (до 80 мг 2 раза в день), максимальная суточная доза — 160 мг.
При применении β-адреноблокаторов начинать лечение необходимо с небольших доз, а при хорошей переносимости препаратов их дозу постепенно повышают. Отмена препарата должна проводиться постепенно на протяжении 7—10 дней с целью профилактики возникновения синдрома отмены.
β-адреноблокаторы противопоказаны при гиперчувствительности, декомпенсированной сердечной недостаточности. нарушении атриовентрикулярной проводимости, бронхиальной астме. выраженной брадикардии, кардиогенном шоке. хронической обструктивной болезни легких. сахарном диабете. нарушении функций печени и почек, облитерирующих заболеваниях сосудов, беременности.
Также при стенокардии применяют антагонисты кальция (блокаторы кальциевых каналов), которые уменьшают потребность миокарда в кислороде из-за снижения его сократимости, а также снижения постнагрузки вследствие дилатации артерий и снижения артериального давления. Кроме того, антагонисты кальция вызывают расширение коронарных сосудов и являются препаратами выбора при спазме коронарных артерий. В эту группу входят различные препараты.
Препараты верапамила обладают способностью тормозить проводящую систему миокарда и его сократимость и оказывать отрицательный хронотропный эффект, поэтому применяются у больных стенокардией со склонностью к различным нарушениям ритма и гипертензии.
Верапамил назначают внутрь во время или после еды, запивая небольшим количеством воды 40—120 мг в день в 3 приема
Препараты нифедипина действуют преимущественно на тонус сосудов, поэтому применяются в основном у больных стенокардией в сочетании с артериальной гипертензией. Все антагонисты кальция являются препаратами выбора при стенокардии вследствие длительного спазма сосудов. Препараты нифедипина можно принимать сублингвально.
Нифедипин применяют внутрь с небольшим количеством воды, по 1—2 таблетки 3 раза в день. При стенокардии Принцметала: по 2 таблетки 4—6 раз в день с интервалом не менее 2 ч, обычная суточная доза — 80 мг, максимальная — 120 мг.
Больные со стенокардией при отсутствии противопоказаний должны ежедневно получать аспирин по 1/4 таблетки (0,125 мг в сутки).
При выраженном нарушении липидного обмена применяют антиоксиданты (токоферола ацетат, аевит и др.), статины.
Принципы лечения стенокардии в зависимости от функционального класса:
При ФК I медикаментозное лечение обычно не проводится, назначают рациональное питание, нормализуют режим дня, при необходимости назначают низкокалорийную диету для снижения избыточного веса, по возможности исключают действие факторов риска. С целью профилактики принимают небольшие дозы аспирина ( 80—100 мг в сутки). Редкие приступы стенокардии купируют приемом нитроглицерина под язык либо применением нитратов в виде спрея.
При ФК II больным назначают дополнительное лечение нитратами продленного действия, β-адреноблокаторами или антагонистами кальция .
При ФК III добавляется один из неприменявшихся антиангинальных препаратов. Например, проводится лечение препаратом из группы нитратов в сочетании с β-адреноблокатором или антагонистом кальция .
У больных с ФК IV обычно используются 3 препарата нитрат-пролонг, β-адреноблокатор и блокатор кальциевых каналов. При неэффективности медикаментозной терапии решается вопрос о хирургическом лечении. Возможно проведение реваскуляризации миокарда путем аортокоронарного шунтирования либо чрезкожной внутрисосудистой коронарной ангиопластикой.
Показаниями к реваскуляризации являются:
1) наличие клинических симптомов заболевания, неприемлемых для данного пациента в связи с необходимостью ограничения физической активности и изменения образа жизни или в связи с ограничениями в приеме медикаментозных препаратов или их побочными эффектами;
2) высокая вероятность улучшения прогноза у данного пациента в случае выполнения реваскуляризации по данным коронарографии.
Профилактика
Профилактика заключается в первую очередь в борьбе с имеющимися факторами риска. Кроме того она включает в себя отказ от курения, лечение артериальной гипертензии. Необходима коррекция избыточного веса, обменных нарушений, гиперлипидемии, рекомендуются активный образ жизни, ежедневная гимнастика и посильные физические нагрузки.
Инфаркт миокарда
— это острый некроз сердечной мышцы, обусловленный острым нарушением коронарного кровообращения преимущественно вследствие тромбоза одной из коронарных артерий.
Этиология
Основной причиной развития инфаркта миокарда является, как правило, атеросклероз коронарных артерий. осложненный тромбозом или кровоизлиянием в атеросклеротическую бляшку. Инфаркт миокарда также может возникать вследствие длительного спазма коронарных артерий, при эмболиях и тромбозах, вызванных воспалительными процессами в сосудах, сдавлении коронарной артерии извне опухолью или аневризмой аорты.
Факторы, способствующие развитию инфаркта миокарда:
1) аномалии развития коронарных артерий;
3) нарушение реологических свойств крови ;
4) резкое повышение потребности миокарда в кислороде;
5) нарушение в миокарде процессов микроциркуляции.
Патогенез
Основное звено патогенеза инфаркта миокарда — прекращение притока крови к участку сердечной мышцы. Это вызывает развитие его некроза, который сопровождается резорбционно-некротическим синдромом. Некроз участка сердечной мышцы способствует снижению ударного и минутного объема сердца и приводит к развитию острой левожелудочковой недостаточности в виде отека .
Классификация
1. Клинические варианты начала острого инфаркта миокарда:
1) ангинозный вариант — типичный и чаще встречающийся, характеризующийся интенсивной жгучей или сжимающей болью за грудиной, длится более 20 мин, с частой иррадиацией в левую руку, ключицу, шею, нижнюю челюсть, левую лопатку или межлопаточное пространство, которая сопровождается психоэмоциональным возбуждением, чувством страха смерти и не купируется нитроглицерином;
2) астматический вариант, характеризующий одышкой или удушьем; чаще наблюдается у больных с повторным инфарктом миокарда, гипертонической болезнью тяжелого течения;
3) гастралгический (абдоминальный) вариант. Заболевания чаще возникает при локализации очага некроза на нижней поверхности, характеризуется болью в эпигастральной области, тошнотой. рвотой. вздутием живота, напряжением мышц брюшной стенки;
4) аритмический вариант инфаркта миокарда, проявляющийся пароксизмальными нарушениями ритма, чаще желудочковой тахикардией, фибрилляцией желудочков, полной атриовентрикулярной блокадой;
5) церебральный вариант, проявляющийся неврологическими нарушениями, напоминающими клинику инсульта (головной болью, головокружением, двигательными и чувствительными нарушениями);
6) бессимптомный вариант, проявляющийся общей слабостью, недомоганием, адинамией. Чаще встречается у пожилых, диагностируется только на основании данных ЭКГ.
2. Классификация по размерам зоны ишемии:
1) мелкоочаговый;
2) крупноочаговый;
3) трансмуральный;
4) нетрансмуральный.
3. По наличию осложнений:
Ишемическая болезнь сердца — Инфаркт миокарда
Инфаркт миокарда — острая и длительная ишемия миокарда с развитием участка некроза. Как правило, инфаркт миокарда является следствием коронарного атеросклероза. Обычно он возникает в результате внезапного тромбоза атеросклеротически измененной коронарной артерии. Инфаркту способствует повреждение бляшки (изъязвление, разрыв) и локальное увеличение коагуляции. Чем проксимальнее тромбоз, тем распространеннее инфаркт. Инфаркт миокарда называют трансмуральным, если он охватывает всю толщу стенки сердца, и субэндокардиальным, или интрамуральным, если он охватывает лишь участок субэндокардиального слоя. Инфаркт почти всегда возникает в стенке левого желудочка и иногда распространяется на правый желудочек и предсердия. При большом инфаркте может развиться острая сердечная недостаточность, обычно левожелудочковая, что еще более ухудшает коронарный кровоток. Инфаркт миокарда провоцируется теми же воздействиями, что и стенокардия, главным образом физическими и эмоциональными нагрузками. Чрезвычайно редко (несколько чаще у молодых) инфаркт возникает вне связи с коронаросклерозом — вследствие коронарита, эмболии коронарной артерии или, возможно, коронароспазма.
Симптоматика. У многих больных инфаркту предшествуют повторные приступы стенокардии, особенно часто нестабильная стенокардия. У отдельных больных инфаркт может быть первым клиническим проявлением ИБС.
Давящие боли возникают за грудиной, иррадиируют в левую руку, шею, эпигастральную область или, усиливаясь, могут иррадиировать более широко. В отличие от стенокардии боли сильнее и приступ продолжительнее (более получаса). Нитроглицерин не дает стойкого обезболивания. Больные тяжело переносят боли из-за большой их силы и чувства тревоги. У части больных боли могут быть слабыми, или они локализуются только в местах характерной иррадиации, или вовсе отсутствуют. Иногда уже в начале приступа на первый план в клинической картине выступают осложнения — аритмии, сердечная недостаточность, у пожилых это может быть и нарушение сознания.
Больной обычно бледен, встревожен, обильно потеет. Обнаруживается тахикардия. АД может быть повышено во время болевого приступа, но в дальнейшем характерно его снижение по сравнению с обычным для данного больного. У части больных появляются и нарастают признаки левожелудочковой недостаточности. Возможен шум трения перикарда.
Из лабораторных данных для подтверждения диагноза наибольшее значение имеет преходящее увеличение активности некоторых ферментов крови (КФК, ACT, ЛДГ, тропонин), которое может стать заметным через 4—10 ч после начала приступа. Более информативно определение кардиоспецифических изоферменгов. Характерны также небольшое повышение температуры в ближайшие 2—3 дня после приступа, лейкоцитоз со сдвигом влево и эозинопенией, а позже — увеличение СОЭ.
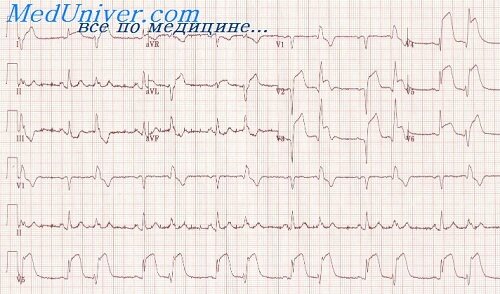
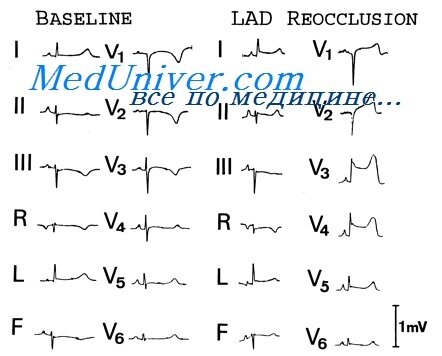
ЭКГ в типичных случаях может изменяться уже во время болевого приступа. Самым ранним признаком обычно является смещение сегмента ST вверх с выпуклостью в ту же сторону. Позже увеличивается зубец Q, зубец R снижается или исчезает. Через несколько дней сегмент 5Тснижается и начинает формироваться отрицательный зубец Т. В дальнейшем в течение нескольких недель или месяцев признаки инфаркта подвергаются обратному развитию, причем позже других исчезает увеличенный зубец Q, который нередко (но необязательно) остается пожизненным признаком перенесенного трансмурального инфаркта миокарда.
ЭКГ позволяет судить о локализации и распространении инфаркта. Характерные изменения возникают в отведениях, в которых активный электрод обращен к участку некроза. Наиболее часты инфаркты следующих локализаций: обширный передний (Vb6, aVL, I, И), передне перегородочный (V,_4), боковой (V5.8, aVL), заднедиафрагмальный (задний, нижний, диафрагмальный — aVF, HI, И). При более обширных инфарктах изменения обнаруживаются в большем числе отведений.
У части больных изменения ЭКГ нехарактерны, выявляются позже или отсутствуют. ЭКГ имеет ограниченное диагностическое значение при повторных инфарктах, которые лишь в четверти случаев сопровождаются типичными изменениями; у некоторых из этих больных возможно ложное улучшение ЭКГ. При блокаде левой ножки пучка Гиса возникновение инфаркта может не сопровождаться новыми изменениями ЭКГ или приводит к нехарактерным или мало заметным изменениям — уменьшению величины комплекса QRS, повороту электрической оси, небольшой деформации сегмента ST. Оценить размеры и локализацию инфаркта по ЭКГ при этом трудно. Во всех случаях важно сопоставление повторно снятых ЭКГ.
Эхокардиограмма иногда позволяет выявить локальные особенности движения стенок сердца, оценить функцию левого желудочка, диагностировать некоторые осложнения — внутренние разрывы, выпот в перикарде, аневризму, пристеночный тромб.
Субэндокардиальный (мелкоочаговый) инфаркт миокарда часто протекает атипично. Боли и лабораторные сдвиги выражены меньше. Изменения ЭКГ касаются только конечной части желудочкового комплекса, могут быть нехарактерными или вообще не регистрируются. Улучшение и стабилизация ЭКГ в общем происходят быстрее, чем при трансмуральном инфаркте. Хотя клиническое течение в целом более благоприятно, возможны различные осложнения и смертельный исход. Клинические критерии отличия субэндокардиального инфаркта от трансмурального в общем достаточно условны.
Многочисленные осложнения утяжеляют течение инфаркта. Аритмии наблюдаются у большинства больных, особенно в первые трое суток болезни. Наиболее опасны мерцание желудочков и полная атриовентрикулярная блокада дистального типа с остановкой сердца — главные причины смерти в первые сутки. Мерцанию желудочков иногда предшествуют желудочковые тахикардия и экстрасистолия. Перед полной блокадой может быть замечено нарастающее нарушение проводимости дистального типа, обычно при переднем инфаркте. Стойкие или преходящие нарушения внутри-желудочковой проводимости, возникшие одновременно с болевым приступом, иногда сами по себе свидетельствуют об инфаркте миокарда, хотя собственно инфарктные изменения на ЭКГ при этом могут быть затушеваны.
Наджелудочковые аритмии в общем менее характерны. Они могут быть связаны с подавлением функции синусового узла, распространением инфаркта на предсердия. Примерно у 10% больных регистрируется мерцательная аритмия, обычно преходящая. Дисфункция синусового узла и нарушения атриовентрикулярной проводимости проксимального типа чаще наблюдаются при заднедиафрагмальном инфаркте. Аритмии и нарушения проводимости при инфаркте частично могут быть следствием противоаритмического лечения.
Сердечная недостаточность, почти всегда левожелудочковая, возникает нередко в остром периоде заболевания, проявляется одышкой, застойными хрипами, сердечной астмой или отеком легких, тахикардией с трехчленным ритмом. В дальнейшем могут присоединиться и признаки правожелудочковой недостаточности. Сердечная недостаточность чаще возникает при больших инфарктах или если сердце уже было ослаблено до инфаркта. Ранними признаками ослабления левого желудочка является увеличение диастолического объема и снижение фракции выброса (по Эхо КГ). Треть больных инфарктом миокарда, осложненным отеком легких, погибают.
Кардиогенный шок — наиболее тяжелая, чаще смертельная, форма сердечной недостаточности при обширном инфаркте. Он обусловлен уменьшением сердечного выброса (менее 2 л/мин), проявляется падением систолического АД (ниже 80—90 мм рт. ст.), тахикардией и признаками нарушения периферического кровообращения — холодная бледная кожа, цианоз, нарушение сознания, падение диуреза (менее 20 мл/ч). В редких, прогностически сравнительно более благоприятных случаях кардиогенный шок связан не столько с поражением сократительного миокарда, сколько с тахиаритмией, гиповолемией.
Реже инфаркт осложняется эмболией в системе легочной артерии или в большом круге кровообращения, наружным разрывом сердца, разрывом межжелудочковой перегородки, острой митральной недостаточностью, острой аневризмой левого желудочка, через одну или несколько недель — постинфарктным синдромом.
Лечение. Больных немедленно госпитализируют, по возможности в кардиологический блок интенсивной терапии. Транспортируют с использованием носилок, в сопровождении врача. Лечение начинают на догоспитальном этапе и продолжают в стационаре.
Для снятия боли внутривенно вводят морфин (1 — 2 мл 1% раствора) с атропином (0,5 мл 0,1% раствора). Применяют фентанил (1—2 мл 0,005% раствора) с дро-перидолом (2 мл 0,25% раствора). Используют ингаляции закиси азота с кислородом. При наличии частых желудочковых экстрасистол и пароксизмах желудочковой тахикардии вводят внутривенно лидокаин по 50— 100 мг с возможным повторением этой дозы через 5 мин. При возникновении мерцания желудочков немедленно проводят электроимпульсную терапию. Если боль рецидивирует, вводят нитроглицерин внутривенно или дают нитраты продленного действия, назначают Р-адреноблокаторы с учетом противопоказаний (в частности, систолическое АД должно быть не ниже 100 мм рт. ст.). Избегают каких-либо внутримышечных инъекций, учитывая опасность гематом при последующем антикоагулянтном лечении.
С первого дня, при условии исключения противопоказаний, назначают гепарин в количестве 15 000 ЕД внутривенно и далее по 5 000 ЕД внутривенно или подкожно каждые 4—6 ч, контролируя время свертывания крови. Примерно с 5-го дня переходят на антикоагулянты непрямого действия, поддерживая протромбиновый индекс на уровне 40—60%. Лечение антикоагулянтами заканчивают, как правило, при выписке из стационара, снижая дозу в течение нескольких дней. Лечение антикоагулянтами противопоказано при признаках перикардита, тяжелых заболеваниях печени, геморрагическом синдроме и заболеваниях со склонностью к кровотечениям (например, при обострении язвенной болезни).
В хорошо оснащенных блоках интенсивной терапии, при наличии соответствующего опыта и если больной, поступает со смешением сегмента ST в сроки до 6 ч после начала болей, проводят системную тромболити-ческую терапию (например, стрептокиназой) или внутрикоронарный тромболизис (в процессе селективной коронароангиографии). Основные опасности тромболитической терапии — геморрагический инсульт и реперфузионные желудочковые аритмии. В зависимости от результатов коронароангиографии иногда вместо тромболизиса тут же выполняется чрескожная транслюминальная коронарная ангиопластика с возможной установкой стента.
Лечение осложнений проводится специалистами в условиях постоянного клинического и кардиомониторного наблюдения. После 2—3 дней строгого постельного режима его постепенно расширяют. В случае осложнений и при рецидивах стенокардии режим расширяют позже и медленнее. После выписки из стационара и лечения в кардиологическом санатории больные, как правило, нуждаются в диспансерном наблюдении. Обычно полезен длительный прием аспирина, Р-адреноблокатора и ингибитора АПФ в малых дозах.
Ишемическая болезнь сердца. Инфаркт миокарда.
Терминология
Термин “инфаркт миокарда” (ИМ) следует использовать в тех случаях, когда имеет место доказанный некроз миокарда вследствие длительно острой ишемии миокарда.
Патогенез
ИМ это процесс гибели клеток сердечной мышцы вследствие длительной ишемии. Гибель миокардиоцитов происходит не одномоментно, а, как показано в эксперименте, по прошествии 20 минут, или менее того, у некоторых лабораторных животных. С момента образования некротической ткани до возможности ее макро- или микроскопического патологоанатомического определения проходит несколько часов. Длительность ишемии, способной привести к некрозу составляет 2–4 часа, этот зависит от наличия коллатералей в ишемизированной зоне, стойкой или интермиттирующей окклюзии коронарной артерии, чувствительности клеток миокарда к ишемии, феномена ишемического прекондиционирования, индивидуальной потребности в кислороде и нутриентах. Патофизиологический процесс рубцевания обычно занимает 5–6 недель. Реперфузия может оказать значительное влияние на макро- и микроскопическую картину.
Клиническая картина
Развитие ишемии миокарда это первый этап развитии ИМ и результат дисбаланса между доставкой кислорода и потребностью в нем сердечной мышцы. Ишемия миокарда это клиническое состояние, которое обычно диагностируется посредством сбора анамнеза и анализа электрокардиограммы. Наиболее распространенные симптомы могут появляться как при нагрузке, так и в покое, включают в себя: дискомфорт в груди с иррадиацией в руку или челюсть, дискомфорт в эпигастральной области или эквиваленты стенокардии – одышку и слабость. Дискомфорт, свидетельствующий о развитии инфаркта миокарда, продолжается в среднем 20 минут. Болевые ощущения часто диффузные, не имеют четкой локализации и связи с физическим усилием и могут сопровождаться повышенным потоотделением, тошнотой и синкопальным состоянием. Однако вышеописанные симптомы не являются высокоспецифичными для ишемии сердечной мышцы. Соответственно, их могут ошибочно трактовать как проявления патологии желудочно-кишечного тракта, нервной, бронхолегочной или костно-мышечной системы. Иногда ИМ может проявляться атипичными симптомами – такими как стать различные нарушения ритма, вплоть до остановки сердца или вообще быть бессимптомным; например у женщин, пожилых пациентов, лиц, страдающих сахарным диабетом, в раннем послеоперационном периоде или находящихся в критическом состоянии. Во всех подобных ситуациях рекомендуется проводить более тщательный осмотр, особенно при определении повышенного уровня тропонинов.