Инфаркт миокарда: классификация, клиническая картина, диагностика, лечение.
Прочитайте:
ИМ — ишемический некроз миокарда, который возникает при остром несоответствии потребности миокарда в кислороде и неспособностью удовлетворить эту потребность.
Этиология: 1. Тромбоз коронарной артерии с полной окклюзией на фоне атеросклеротической бляшки или изъязвления атеросклеротической бляшки. 2. Спазм коронарной артерии 3. Острый дисбаланс между потребностью миокарда и доставкой. 4. Реже: — ТЭ коронарной артерии при инфекционном эндокардите коронарных клапанов — коронариты при системных васкулитах — врожденные аномалии — фиброзные бляшки.
Патогенез. Тромбоз коронарной артерии = ишемия миокарда => ч/з 20 мин в центре зоны ишемии — зона повреждения (обратимые стадии). Через 1 час в центре зоны повреждения формируется очаг некроза (необратимая стадия). Участок некроза — зона некроза, окруженная зоной повреждения и кнаружи зоной ишемии. Сила сокращающегося миокарда снижается => ОСН в виде отека легких или еще тяжелее — кардиогенного шока. Если участок некроза располагается в межжелудочковой перегородке, где проводящаях система => блокада левой дуги пучка Гисса. Если тромбоз коронарной артерии, которая питает АВ-узел => АВ-блокада. Миомаляция на 2-3 сутки течения ИМ. Миомаляция опасна осложнением: разрыв миокарда. Некротизированная ткань замещается соединительной тканью (рубцевание). Через 1 месяц — постинфарктный кардиосклероз. Если ИМ был обширный, участок кардиосклероза тоже обширный => ХСН.
Клиническая картина. Типичный вариант. Ангинальный синдром:боль интенсивная, давящая, сжимающая, жгучая; загрудинная, реже в области сердца, не купируется нитроглицерином, а только наркотическими анальгетиками и то не всегда, иррадиирует в левую руку, лопатку, челюсть и длится 20мин. Похожа на стенокардитическую боль. Атипичный вариант. Абдоминальный вариант -б Боль в эпигастрии, сопровождается диспепсическими явлениями (при заднедиафрагмальном и заднебазальном ИМ). Астматический вариант — одышка до степени удушья, влажные хрипы в нижних отделах легких. Отсутствие боли. Появление острой ЛЖН. Церебральный вариант — н арушение сознание, заторможенность, вялость => церебральная ишемия развивается при снижении сердечного выброса. Клиника напоминает ИИ, у лиц с атеросклерозом (возрастная группа). Аритмический вариант — аритмии и нарушения проводимости (суправентрикулярная тахикардия желудочков, АВ-блокада, фибрилляция желудочков). Атипическая локализация боли — боль не загрудинная, локализация в тех местах, где типичная иррадиация (левое плечо, спина). Бессимптомный вариант -немотивитованная слабость, могут быть бледными с диффузным гипергидрозом (холодный пот), возбужден, страх смерти. Если развивается отек легких => влажные хрипы в нижних отделах. Сердце: границы в норме, 1 тон приглушен, у 1/3 больных 3-х членный ритм галопа. Если развился инфаркт сосочковой мышцы => дисфункция митрального клапана по типу недостаточности => систолический шум.
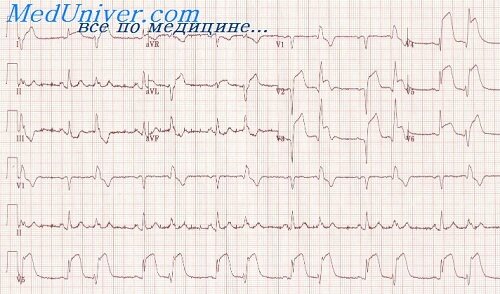
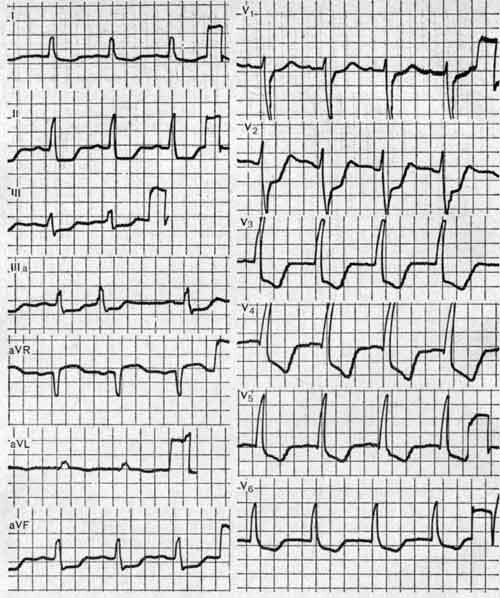
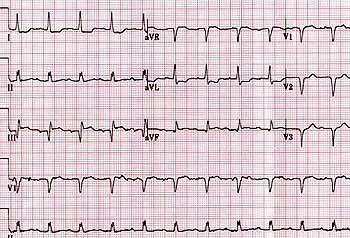
Дополнительные методы. 1. ЭКГ: — верификация ИМ, определение глубины и обширности. 1) ИМ с формированием зубца Q — это крупноочаговый и трансмуральный ИМ. 2) ИМ без формирования зубца Q — это мелкоочаговый ИМ. ИМ с формированием зубца Q. — подъем ST выше изолинии более чем на 2 мм. Сегмент ST сливается с сегментом Т — монофазная кривая. Ч/з 1 час некроз, появляется зубец Q на ЭКГ, который отражает некроз (по глубине в норме не превышает ¼ зубца R). В отведениях V1 -V3 (грудные отведения) в норме зубца Q вообще нет. Продолжительность патологического зубца Q более 0,04с. Реципрокные изменения (снижение сегмента STниже изолинии + отрицательный зубец Т) – на стенке противоположной ИМ. ИМ – трансмуральный (некроз во всей толще) при этом зубец R исчезает →QS. Передняя стенка – I отвед, AVL, V2. V3 Верхушка — I отвед, AVL, V4 Боковая стенка — I отвед, AVL, V5 -V6 Задняя стенка – II, III отвед, AVF Базальные отделы – V7. V8 ,V9. Дальше начинается организация и поэтому сегмент ST начинает спускаться к изолинии, а зубец Т становится отрицательным. К концу 3 недели сегмент ST должен вернуться на изолинию при нормальном течении ИМ. Если к концу 3 недели сегмент ST не возвращается, называется застывшей кардиограммой — формируется аневризма сердца. ИМ без формирования зубца Q. Подъем ST выше изолинии, зубец Q не появится. Монофазная кривая. Со временем сегмент ST может спускаться. Субэндокардиальный ИМ: депрессия сегмента ST. Ниже изолинии более 1мм + отрицательный зубец Т → держится от 3 до 5 дней. Потом постепенно сегмент ST возвращается на изолинию. Проводить тромболизис нельзя. 2. Обнаружение в крови маркеров некроза миокарда — мембраны миокардиальных клеток разрушаются и ферменты (органоспецифические) попадают в кровь: тропонин И и Т; КФК + кардиоспецифический изофермент NV; миоглобин. Начинают подниматься ч/з 2-4 часа, тропонин держится в течение 10 суток, КФК и миоглобин – 3 дня. ОАК – развитие резорбционного некроза: лейкоцитоз, который к 3-4 дню уходит, анэозинофилия 3. ЭхоКГ — зоны гипокинеза и акинеза, снижение сердечного выброса, при развитии инфаркта сосочковой мышцы – митральная недостаточность. 4. Сцинтиграфия очага некроза. Используют пирофосфат меченный технецием — 9, который способен накапливаться в очаге некроза (выглядит как горячий очаг). Перфузионная сцинтиграфия миокарда с использованием талия → проходит через здоровые коронарные артерии и поглощается здоровым миокардом. Через тромбированные коронарные артерии талий не проходит → холодный очаг, не накопивший радиоизотоп. 5. Селективная коронарография. Тромбоз коронарных артерий.
Лечение. Цель: — восстановление проходимости коронарных артерий — ограничение некроза — предупреждение развития осложнений. Лечение ИМ в ранние сроки. Всех больных после оказания 1-й помощи госпитализируют в реанимационное отделение. Режим – полный покой. Медикаментозная терапия: купирование болевого синдрома с помощью наркотических анальгетиков: морфин, фентонил + нейролептики: дроперидол или галоперидол. Можно добавить транквилизатор – диазепам. Тромболитическая терапия. Проводится в случае крупноочагового ИМ с наилучшим эффектом его проведения в течение 1 часа, когда некроза нет. Это «золотой час». Допускается и в течение 6 часов: стрептокиназа, урокиназа, аутоплаза, ретоплаза. Альтернатива тромболитической терапии чрескожное коронарное вмешательство т.е. баллонная ангиопластика и сцинтирование коронарной артерии. Антиагрегантная терапия . аспирин (кардиомагнил, тромбо-АСС), диклопедин. Антикоагулянты: гепарин, фроксипарин. Терапия, напрвленная на ограничение некроза . Β-адреноблокаторы – уряжают ЧСС, ↓АД →снижается потребность миокарда в кислороде. Уряжаем до 50-60/мин: бисопролол, метопролол, атенолол, пропранолол, карведиол. Назначать во всех случаях. когда нет противопоказаний: — ЧСС < 50/мин, — АД<90 мм.рт.ст. — острая левожелудочковая недостаточность, — АВ-блокада, — бронхиальная обструкция. Ингибиторы АПФ. Снижают постнагрузку: каптоприл, эналоприл, резиноприл, раниприл. Показания: большие размеры ИМ. Противопоказания: АД ниже 100 мм.рт.ст, тяжелая ХПН, стеноз почечной артерии. Нитраты. Ограничитьб зону некроза: нитроглицерин в/в кап. Прказания: стойкая, повторяющаяся ишемия миокарда; стойкое повышение АД. Лечение ИМ в поздние сроки: β-адреноблокаторы, ингибиторы АПФ, антиагреганты. Принимают длительное время.
Осложнения инфаркта миокарда: кардиогенный шок (рефлекторный, истинный, аритмический), отек легких, разрывы миокарда (наружный, внутренние), хроническая аневризма левого желудочка, постинфарктный синдром Дресслера.
Ранние: — ОСН, — нарушение ритма и проводимости; Промежуточные: — тромбэндокардит, -разрывы миокарда, -эпистенокардит, перикардит; Поздние: — аневризма левого желудочка, — постинфарктный синдром Дресслера.
1) Отек легких встречается у 10-15% больных ИМ, вследствии некроза части миокарда снижается сократительная способность, т.е. ни вся кровь в систолу выбрасывается в аорту → повышается конечное диастолическое давление → повышается давление в левом предсердии →в капиллярах МКК →пропотевание жидкой части в альвеолы. Сначала в интерстиций (интерстициальная форма отека), затем в альвеолы (альвеолярная форма). Пропотевание жидкости + воздуха →пена, которая забивает дыхательные пути и ухудшает оксигенацию. Клиника: одышка, доходящая до удушья, тахипноэ, ортопноэ, пенистая мокрота, иногда с кровью. Аускультация: в легких ослабленное дыхание, в нижних отделах появляются влажные хрипы. Альвеолярная форма – наличие пенистой мокроты и влажных хрипов по обоим легочным полям. Аускультация сердца: тоны приглушены, на верхушке – ритм галопа, тахикардия. На рентгенограмме – затемнение в области корней легких в виде крыла летучей мыши. Лечение: — оксигенотерапия, — пеногасители, кислород увлажненный спиртом или антифомсилоном, — приподнимаем головной конец и опускаем ножной конец, — сильный диуретик в/в струйно (лазикс), который снижает ОЦК →снижается давление вМКК, — нитроглицерин в/в капельно (периферический вазодилятатор – расширяет периферические венулы, депонируется кровь → снижается венозный возврат к сердцу) разгружает МКК, — наркотический анальгетик, морфин →подавляет дыхательный центр, кроме этого успокаивает, — тромболизис (после 6ч ИМ)- стрептокиназа.
2) Кардиогенный шок. Снижение АД ниже 990 мм.рт.ст, сопровождается признаками периферической гипоперфузии тканей. Бывает 3-х видов: — рефлекторный – аритмический — истинный. Клиника одинаковая: Систолическое давление ниже 90 мм.рт.ст. Диастолическое давление ниже 50 мм.рт.ст. Среднее давление ниже 60 мм.рт.ст. Пульсовое давление меньше 30 мм.рт.ст. Признаки гипоперфузии: больной бледный, активируется симпато-адреналовая система →спазм сосудов. Со стороны ЦНС снижение АД проявляется заторможенностью, иногда возбуждением, в тяжелых случаях – сопор, кома. Со стороны органов дыхания – тахипноэ. Со стороны почек – олигоанурия, менее 30 мл мочи в час. Рефлекторный кардиогенный шок – это есть снижение АД в ответ на интенсивный болевой синдром. Лечение: наркотические анальгетики – морфин, фентомин в сочетании с дроперидолом, галоперидолом. Если АД не нормализуется, то применяют адреналин, добутамин, допамин: ГКС-дексаметазон. Аритмический кардиогенный шок – развивается при тяжелых нарушениях ритма и проводимости, при таких как желудочковая тахикардия, пароксизмальные и мерцательные аритмии, при АВ-бдокадах 1,2 степени. При этом отсутствует синхронизация между предсердием и желудочком + укорачивается диастола →желудочки не успевают заполниться кровью → АД снижается. Лечение: 1. Восстановление синусового ритма: антиаритмические препараты, такие как лидокаин, новокаинамид, кордарон; или с помощью электрической кардиоверсии. 2. При АВ-блокаде – атропин, кардиостимуляция. Истинный кардиогенный шок – самый тяжелый, в основе – обширный некроз. При некрозе 40% массы левого желудочка → истинный кардиогенный шок. Выделяют клинические формы: 1. Больные без предшествующей ИБС, у которых впервые развился ИМ большого размера 2. больные, которые перенесли ИМ и повторный ИМ даже небольших размеров может спровоцировать развитие истинного кардиогенного шока. 3. больные, у которых кардиогенный шок развился на фоне ИМ на 3-4 сутки → развиваются механические осложнения: разрывы миокарда, острая аневризма. Патогенез истинного кардиогенного шока. 1.Большой инфаркт и снижение сократительной способности миокарда →↓сердечного выброса→ ↓ коронарная перфузия →расширение зоны некроза →еще больше ↓АД 2. при снижении сердечного выброса повышается давление в левом желудочке, в левом предсердии → в МКК →гипоксия, еще больше ↓ сократительная способность миокарда. При ↓ сократительной способности миокарда активируется симпатоадреналовая система→ спазм периферических сосудов →↓оксигенация тканей →развитие метаболического ацидоза → оказывает кардиодепрессивное действие. Спазм периферических сосудов →жидкость из сосудов уходит в ткани →↑ вязкость крови → сладж форменных элементов →микротромбоз→еще больше усугубляется микроциркуляторное нарушение. Чаще кардиогенный шок развивается при переднем ИМ. Лечение: Восстановление гемодинамики и кровотока, — оксигенотерапия, -плазмозаменители (физ р-р), -условия для начала диффузионной терапии: отсутствие влажных хрипов. Струйно 200-250 мл замещающего р-ра. Если АД↑, то дальше капельная инфузия. Если на быстрое введение АД не реагирует, прекращаем введение плазмозаменителя и вводим симпатомиметики: добутамин и допамин; и ГКС. — внутриаортальная баллонная контропульсация. В аорту на уровне брюшной аорты вводится катетер, на котором имеется баллончик, который может раздуваться, совпадает с сокращением сердца. В диастолу баллончик раздувается →нагнетается кровь в коронарную артерию, в конце диастолы баллончик спадает → ↓ постнагрузку. — можно привести тромболитическую терапию – стрептокиназа, ретаплаза,аутоплаза или проведение чрескожнокоронарного вмешательства, т.е. баллонная ангиопластика и сцинтирование или же аортокоронарное шунтирование.
3) Разрывы миокарда. Встречается в 5% случаев, и делятся на внешние и внутренние. Обстоятельства, способствующие: СД, ГБ, женский пол, возраст. Разрывы встречаются в период миомаляции с 1-6 день. Внешний разрыв. При быстро развивающемся внешнем разрыве боль не успевает развиться →тампонада сердца→летальный исход. Если разрыв более медленный – боль интенсивная →АД↓→рефлекторный кардиогенный шок. Феномен: на ЭКГ сердце сокращается, но тонов нет. Внутренний разрыв: 1. Разрыв межжелудочковой перегородки. Условия: трансмуральный инфаркт, локализующийся в перегородке. Происходит сброс крови из ЛЖ в правый →перегрузка ПЖ →правожелудочковая недостаточность. Клиника: систолический шум с эпицентром в 3-4 межреберье и нарастают явления застоя в БКК → отеки, гепатомегалия, набухание шейных вен. 2.Отрыв сосочковой мышцы. Дисфункция митрального клапана по типу митральной недостаточности, систолический шум на верхушке, ритм галопа. Нарастают явления ОСН →отек легких и кардиогенный шок. Диагностика. ЭхоКГ выявляет и наружные и внутренние разрывы миокарда. Лечение. Поддержание гемодинамики, купирование отека легких, ↑АД + хирургическая коррекция.
4) Постинфарктный синдром Дресслера. У 3-6% перенесших ИМ. Патогенез. Некротизированные массы миокарда начинают восприниматься организмом как чужеродные. В ответ на них вырабатываются аутоантитела, которые соединяются с аутоАГ →комплексы, которые могут оседать на перикарде – перикардиты, на плевре — плевриты, на легких — пневмониты, на суставах – артриты. Клиника. Развитие через 2 недели (до 6 недель) после перенесенного ИМ. Субфебрильная лихорадка и симптоматика, связанная с поражением органов. Триада Дресслера . перикардит, плеврит, плечевой артрит. Не обязательно присутствие 3-х признаков у одного больного. Шум трения перикарда при экссудативном перикардите – приглушение тонов, при плеврите – ослабленное везикулярное дыхание на стороне поражения, при пневмоните – хрипы. Дополнительные методы исследования. ЭхоКГ. Рентгенологический – пневмонит, плеврит ОАК — эозинофилия и у всех СОЭ↑, циркулирующие иммунные комплексы ↑. Лечение: 1.НПВС – диклофенак, мелоксиком 2.ГКС-преднизолон.
5) Хроническая аневризма левого желудочка. Развивается почти у 1/3 больных, перенесших ИМ. При этом у 85% — с передней локализацией ИМ вследствие трансмурального ИМ. Делятся на . анатомические, функциональные, ложные. Анатомическая – это есть участок истонченной рубцовой ткани, выпячивающийся. Анатомическая аневризма: диффузная, малиновая, грибовидная. Функциональная аневризма – это зона постинфарктного кардиосклероза, которая выбухает в систолу т.е. движется дискинетически. Ложная аневризма формируется после разрывов миокарда с истечением крови в перикард с формированием полости. Ограниченной сращениями миокарда. Клиника: складывается из симптомов собственно самой аневризмы, ОСН, аритмии. Симптомы собственной аневризмы: -прекардиальный пульс, — систолический шум над аневризмой, -симптом коромысла. Со временем отеки, гепатомегалия, в стадии аневризмы воспалительные изменения →пристеночный тромбоз →тромбоэндокардит. У 70% имеются тромбы →источники ТЭ сосудов БКК, в органы БКК + разные формы аритмии. Диагностика: 1. ЭКГ – застывший ЭКГ, т.е. через 3 недели после ИМ сегмент ST не спускается. Есть признаки трансмурального поражения→отсутствие зубца R. Передняя локализация — I отвед, AVL, V1 -V6 2. ЭхоКГ – наличие участка дискинеза (несинхронного сокращения). — пристеночные тромбы — дилятация левого желудочка — ↓сердечного выброса. 3. Рентгеноскопия сердца . пульсация аневризмы. Лечение 1. Профилактика и лечение ХСН — и-АПФ, -β-адреноблокаторы. Если развилась ХСН к ним + диуретики, антогонисты альдостерона. 2.Антиагреганты – аспирин, тиклопидин. Хирургическое лечение.
Клиническая картина инфаркта миокарда
В качестве факторов, провоцирующих его развитие, часто выступают психоэмоциональное или физическое напряжение, гипертонический криз. В результате появляется участок некроза (омертвения) сердечной мышцы, возникающий вследствие прекращения притока крови или поступления ее в количестве, недостаточном для покрытия потребности миокарда в кислороде.
Развитие инфаркта в большинстве. случаев обусловлено закупоркой атеросклеротически измененной артерии. Так, при крупноочаговых инфарктах миокарда закрытие магистральных артерий сердца тромбом происходит в 90—97% случаев. Некроз (омертвление ткани) развивается, если ишемия миокарда продолжается в течение 20—25 минут. В зависимости от размеров участка некроза различают мелкоочаговый и крупноочаговый инфаркт. Если на каком-то участке не-кротизируется вся толща миокарда, то говорят о трансмуральном инфаркте.
Клиническая картина инфаркта миокарда отличается многообразием, что затрудняет постановку правильного диагноза в максимально короткий срок. Типичным считается наиболее часто встречающийся ангинозный вариант, характеризующийся внезапными интенсивными болями в области сердца, за грудиной, нередко типа кинжальной или сдавливающей боли. В отличие от боли при стенокардии она продолжительнее, носит волнообразный характер, не снимается нитроглицерином. Больные, стараясь облегчить боль, мечутся по комнате, меняют положение в постели.
Однако далеко не всегда в начале болезни бывает такой болевой синдром. Больной может ощущать лишь дискомфорт в груди. В ряде случаев боль отсутствует или оказывается не такой интенсивности и локализации.
Из нетипичных форм наиболее часто наблюдается астматический вариант инфаркта миокарда, проявляющийся приступом удушья. У больного возникает ощущение острой нехватки воздуха, которое затем может перейти в тягостное удущье. У него возникает беспокойство и чувство страха, он не может лежать, стремится сесть.
Гастралгический, или абдоминальный, вариант инфаркта начинается с болей в верхней половине живота, тошноты, рвоты, вздутия живота. Такое начало очень напоминает острое заболевание органов брюшной полости и нередко приводит к ошибочным действиям как самого больного, так и медицинских работников.
Церебральный вариант встречается редко, преимущественно у людей преклонного возраста с выраженным атеросклерозом мозговых сосудов. Инфаркт начинается с обморока или как острое нарушение мозгового кровообращения.
Аритмический вариант инфаркта миокарда характеризуется остро возникшим тяжелым нарушением сердечного ритма. Известны и малосимптомные формы, проявляющиеся лишь ухудшением самочувствия больного, немотивированной общей слабостью, ухудшением настроения.
Диагностика инфаркта миокарда основывается на клинической картине болезни и данных лабораторного и инструментального обследования. Основным методом диагностики является, безусловно, ЭКГ, позволяющая судить о локализации инфаркта миокарда, его обширности, давности. Однако этот метод имеет определенные ограничения, так как не всегда инфаркт (особенно повторный) вызывает изменения ЭКГ в первые минуты и часы своего развития.
Кроме этого, распознаванию болезни помогает ряд признаков, обусловленных распадом мышечных волокон сердца и, всасыванием в кровь продуктов распада. К лабораторным показателям, облегчающим распознавание этого заболевания в остром периоде, относятся увеличение количества лейкоцитов и СОЭ, изменение активности ряда ферментов крови.
Особенно важным для диагноза является неоднократное исследование ферментативной активности крови. При инфаркте миокарда характерна определенная их динамика в зависимости от давности некроза сердечной мышцы.
Сочетание электрокардиографии с лабораторными данными в большинстве случаев позволяет правильно распознать инфаркт миокарда. В сомнительных случаях врачи используют дополнительные исследования, например радиоизотопные методы выявления очага некроза миокарда.
* * *
Течение инфаркта миокарда циклично. В его развитии выделяют острый, подострый и послеинфарктный периоды, пишут В.Панченко и В. Свистухин.
Острый период длится от 2 до 10 дней и соответствует времени окончательного формирования очага некроза. В этом периоде высока вероятность развития различных осложнений и смерти. Поэтому больные в это время помещаются в отделение интенсивного наблюдения.
Подострый период, продолжительностью 4—8 недель, прогностически более благоприятен, так как наиболее опасные осложнения заболевания уже позади. В это время происходит рассасывание некротического, участка, и на его месте начинается образование рубца.
Послеинфарктный период — время полного рубцевания очага некроза и консолидации рубца. В этот период (2^6 месяцев) происходит адаптация сердечно-сосудистой системы к новым условиям функционирования, что характеризуется выключением из сократительной функции определенного участка миокарда.
Выделяют еще предынфарктный период — время, предшествующее его развитию.
В этот период при своевременной госпитализации больных, в ряде случаев удается предотвратить развитие инфаркта миокарда. К сожалению, какой-либо типичной только для этого периода симптоматики нет, и наблюдается он далеко не у всех больных. При ретроспективном анализе самочувствия больных лишь у 30—60% пациентов выявляются признаки уси-ления коронарной недостаточности в течение 3—4 недель до развития инфаркта.
Особого внимания заслуживает впервые возникшая стенокардия у молодых людей, нередко начинающаяся нетипично.
Вскоре после выписки из больницы у многих больных отмечается субъективное ухудшение. Оно выражается прежде всего в появлении болей в области сердца. Болевому синдрому следует уделять серьезное внимание, вместе с врачом установить истинное происхождение болей.
Не все боли в области сердца следует расценивать как стенокардию и угрозу повторного инфаркта. Нередко в этом периоде наблюдаются боли невротического характера. При расширении режима физической активности у части больных, перенесших инфаркт миокарда, могут выявиться признаки сердечной недостаточности. Тогда ведущими симптомами становятся одышка во время физической нагрузки и сердцебиение.
Сердечная недостаточность может выразиться в появлении потребности спать на высоких подушках, в возникновении ночного кашля, учащении мочеиспускания. Нередко в этот период наблюдаются различные аритмии, чаще всего экстрасистолия.
Помимо указанных симптомов, связанных непосредственно с перенесенным инфарктом, чаще крупноочаговым, могут быть признаки общей де-тренированности (общая слабость, быстрая утомляемость, неустойчивость настроения и т.д.). Считают, что субъективное ухудшение после выписки из стационара вызывается в основном увеличением физической нагрузки.
Так, например, возобновление стенокардии не всегда является следствием истинного ухудшения кровоснабжения миокарда, а может лишь отражать несоответствие резерва коронарного кровотока быстро возрастающим физическим нагрузкам. Большинство симптомов, характерных для восстановительного периода, через 1—1,5 месяца исчезает.
Возможен и постинфарктный кардиосклероз. Врачи ставят такой диагноз не ранее чем через 2 месяца с момента возникновения инфаркта миокарда. За этот срок на месте некротического участка в миокарде образуется очаг склероза.
Так как клинические проявления кардиосклероза могут быть «весьма скудными, немало людей, перенесших инфаркт, долгое время ничего об этом осложнении не знают (тем болеег
ес=-ли в этот период у них не снималась ЭКГ). Только появление признаков сердечной» недостаточности и нарушений сердечного ритма, характерных для кардиосклероза, заставляют больного обратиться к врачу.
К осложнениям трансмурального инфаркта миокарда относят аневризмы левого желудочка, расположенные чаще всего в его переднебоковой стенке.
Аневризма представляет собой ограниченное выбухание стенки сердца (размером от 1 до 10 сантиметров). Чаще она образуется в остром периоде инфаркта миокарда, когда омертвевший участок мышцы, потерявший способность сокращаться, начинает растягиваться, истончается и выпячивается под влиянием внутрижелудочкового давления крови. В дальнейшем этот участок рубцуется, аневризма же становится хронической.
Способствуют возникновению аневризмы несоблюдение больным режима физической активности в ранние сроки болезни, наличие у больного артериальной гипертонии. Лечат аневризму левого желудочка только путем хирургического вмешательства.
Клиническая картина инфаркта миокарда
По объему поражения инфаркт миокарда делится на крупноочаговый (трансмуральный) и мелкоочаговый; по клиническому течению — на 5 периодов: предынфарктный, острейший, острый, подострый и постинфарктный.
Предынфарктный период клинически соответствует течению нестабильной, прогрессирующей стенокардии и острой коронарной недостаточности. Продолжительность от нескольких часов до 1,5 месяцев.
Острейший период инфаркта миокарда начиная с момента развития острой ишемии миокарда длится от 30 мин до 2 ч и завершается формированием его некроза. Клинически проявляется болевым синдромом чрезвычайной интенсивности (чем обширнее зона некроза, тем сильнее боль), сжимающего, давящего, распирающего или острого, — кинжального- характера, с иррадиацией в левую руку, лопатку, нижнюю челюсть, ухо, зубы, иногда в надчревную область. Боль обычно то несколько ослабевает, то усиливается вновь, продолжается несколько часов (более 30 мин) и даже суток, не снимается приемом нитроглицерина (за исключением случаев атипичного течения).
Объективно: кожные покровы и видимые слизистые бледные, возможен акроцианоз. Артериальное давление при болевом синдроме повышено, затем постепенно снижается. При развитии осложнений (сердечной недостаточности, кардиогенного шока) давление значительно снижено. Перкуторно: левая граница сердца расширена. Аускультативно: ослаблен I или оба тона, слабый систолический шум на верхушке и над аортой, в 25- 30% случаев возникает ритм галопа. Первоначально может отмечаться брадикардия, которая затем сменяется нормо- или тахикардией; иногда сразу возникает тахикардия, возможны различные нарушения ритма и проводимости.
В остром периоде инфаркта миокарда (заключительный этап образования некроза) боль исчезает (сохранение последней говорит либо о глубокой ишемии миокарда вокруг зоны инфаркта либо о развитии перикардита). При крупноочаговом инфаркте в остром периоде типично появление сердечной недостаточности (если она не возникла раньше), артериальной гипотонии. В остальном клиника соответствует таковой в острейшем периоде. Острый период длится от 2 до 14 дней.
Подострый период инфаркта миокарда (до 4-8 недель от начала заболевания) характеризует начальные этапы организации рубца. Болевой синдром отсутствует, явления острой сердечной недостаточности постепенно купируются, в некоторых случаях может развиться хроническая сердечная недостаточность. Сохраняются нарушения ритма (35- 40% случаев). Частота сердечных сокращений возвращается к норме, систолический шум исчезает, атриовентрикулярная проводимость (в случаях ее нарушения) восстанавливается. Нормализуется активность ферментов крови.
Постинфарктный период (до 3-6 месяцев от момента развития инфаркта) отражает повышение плотности рубца, адаптация миокарда к создавшимся условиям работы достигает максимума. При благоприятном течении объективное исследование практически не выявляет отклонений в состоянии сердечно-сосудистой системы. В иных случаях возможно развитие возвратной стенокардии напряжения, повторного инфаркта миокарда, формирование хронической сердечной недостаточности.
При мелкоочаговом инфаркте болевой синдром менее выражен, чем при крупноочаговом. Интенсивность боли несколько превосходит приступ стенокардии, длительность ее меньше, чем при крупноочаговом инфаркте. Протекает более благоприятно, обычно без развития сердечной недостаточности, часто сопровождается различными аритмиями. В первые двое суток отмечается субфебрилитет.
И.A. Бepeжнoва E.А. Poмaновa