ТАКТИКА АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ
Выбор антибиотиков при инфекционном эндокардите — сложная задача, Трудности прежде всего связаны с широким распространением нетипичных возбудителей заболевания и высокой резистентностью многих микроорганизмов к существующим антибактериальным средствам. Имеет значение и то, что антибиотики плохо проникают в клапаны сердца и миокард. Во многих случаях (например, на фоне искусственных клапанов сердца, шунтов, кардиостимуляторов) течение эндокардита приобретает не всегда прогнозируемые особенности. И, может быть, главная трудность связана с тем, что даже в условиях хорошо оснащенных клиник далеко не всегда удается идентифицировать возбудителя инфекции.
Между тем процесс диссеминирует быстро, и промедление недопустимо. Антибактериальное лечение необходимо начинать как можно раньше, не дожидаясь идентификации возбудителя патологического процесса.
Практический опыт, к счастью, подсказывает достаточно перспективные пути такого эмпирического «слепого» лечения.
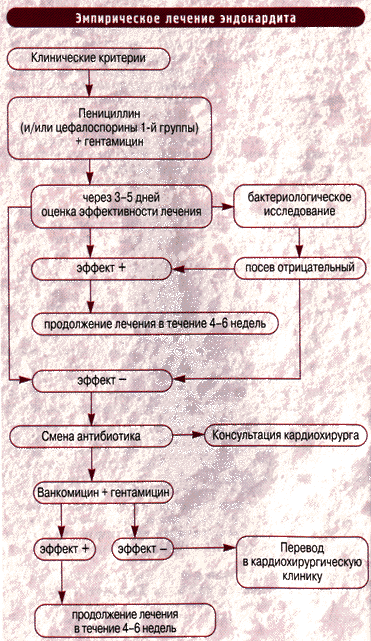
Целесообразно применять комбинацию двух антибиотиков. Пенициллин вводят в/м 6 раз в день в суточной дозе 12-20млн ЕД. Возможно и в/в введение натриевой соли пенициллина, а также его сочетание с гентамицином -160-240 мг в день в 2-3 приема.
При отсутствии данных о возбудителе и эффекта от терапии пенициллином и аминогликозидом в течение 3-5 дней (сохранение лихорадки и других симптомов) суточную дозу пенициллина увеличивают до 40 мл ЕД. вводя его через каждые 4 часа. Можно также заменить пенициллин ампициллином (или оксациллином), вводя его в/м 4 раза в день в суточной дозе 6-10 г. Если эффект отсутствует и от такого лечения. допустимо к двум антибиотикам присоединить третий, например цефазолин (суточная доза — 4-6 г). Подобная комбинация часто дает осложнения, поэтому применяют ее лишь в крайних случаях.
При аллергии к пенициллинам лечение следует начинать с в/в введения клиндамицина 2,4-3,6 г в день или ванкомицина -2г в день.
Отсутствие эффекта и отрицательные результаты бактериологического исследования позволяют предположить наличие стафилококкового эндокардита, который вероятнее всего обусловлен пенициллин- или метициллинрезистентными стафилококками. В данной ситуации необходимы смена антибиотика и в/в введение ванкомицина или тейкопланина в виде монотерапии либо в комбинации с гентамицином (или амикацином).
Терапию бета-лактамными антибиотиками и гликопептидами можно усилить добавлением рифампицина в/в (суточная доза — 600-900 мг). Монотерапия эндокардита рифампицином нецелесообразна.
Нередко эмпирическое лечение начинают с комбинированных препаратов, содержащих ампициллин и сулбактам, пиперациллин и тазобактам. Перечисленные комбинированные препараты так же эффективны, как цефалоспорины 1-й группы (цефазолин, цефрадин).
По-видимому, клапанный аппарат сердца наиболее часто страдает от стафилококкового эндокардита. Это очень серьезная клиническая проблема. Распространенность, а возможно, и рост в будущем эндокардита обусловлены преобладанием пенициллин-и метициллинрези-стентных штаммов бактерий, увеличением частоты в/в инфузий и числа больных с имплантированным искусственным клапаном сердца и шунтами, применением длительной катетеризации (катетер Хикмана), ростом иммунодефицитных состояний (в том числе и СПИДа).
Эндокардит, вызванный золотистым стафилококком, нередко сочетается с септицемией (в 10% случаев), летальность при нем достигает 49-60%. Для предотвращения неблагоприятного исхода требуется длительная — в течение 4-6 недель антибактериальная парентеральная терапия. Общая летальность при инфекционном поражении искусственного клапана сердца достигает 30%, причем в 1/3 случаев выделяют эпидермальный и золотистый стафилококки.
При подозрении на стафилококковый эндокардит рекомендуется на чать лечение с в/в введения бета-лактамных антибиотиков (пенициллины и цефалоспорины) в максимально переносимой дозе.
Применение пенициллина, а также ампициллина или пиперациллина в виде монотерапии нецелесообразно, так как эти антибиотики разрушаются бета-лактамазами, продуцируемыми стафилококками.
Эффективна комбинация пенициллинов с ингибиторами бета-ла-ктамаз: ампициллин + сулбактам, амоксициллин + клавулановая кислота, пиперациллин + тазобактам. По действию на бета-лактамаз-продуцирующие бактерии эти комбинации приближают пенициллины к оксациллину или цефапоспоринам 1-й группы (например, цефазолину).
Экспериментально установлено, что эндокардит, вызванный метициллинрезистентным золотистым или эпидермальным стафилококком, резистентен ко всем бета-лактамным антибиотикам.
В эксперименте комбинация амоксициллина с клавулановой кислотой также эффективна, как ванкомицин.
Внегоспитальные штаммы золотистого стафилококка, резистентные, как правило, к пенициллину, сохраняют постоянную чувствительность к полусинтетическим пенициллинам, оксациллину, клоксациллину, диклоксациллину, флуклоксациллину, которые не изменяются под влиянием стафилококковых (амбулаторных) штаммов бета-лактамаз. Эти препараты сравнимы по эффективности, переносимости и фармакокинетическим данным. Они не эффективны при эндокардите, вызванном метициллинрезистентными штаммами, выделяемыми обычно при внутригоспитальной инфекции. Как выяснилось, метициллин, ранее использовавшийся для лечения стафилококковой инфекции, очень часто вызывает лейкопению, интерстициальный гломерулонефрит и реакцию гиперчувствительности, и поэтому его сейчас не рекомендуют применять в клинике.
Большинство цефалоспоринов достаточно устойчивы к действию бета-лактамаз, продуцируемых стафилококками, исключение составляют метициллинрезистентные штаммы.
При стафилококковом эндокардите наиболее эффективны цефазолин, цефрадин.
Примерно такой же эффективностью обладают цефамандол и цефуроксим. Антистафилококковая активность цефотаксима, цефодизима и цефтриаксона ниже.
Цефепим и цефпиром отличаются высокой противостафилококковой активностью.
Синергизм в действии антибиотиков наблюдается при сочетании бета-лактамных препаратов (пенициллины и цефалоспорины) с аминогликозидами. Такие комбинации применяются часто. Однако нельзя упускать из вида, что аминогликозидам свойственны ототоксичность, нефротоксичность и поражение вестибулярного аппарата. Предупре
дить потенциальные органотоксические эффекты можно, осуществляя терапевтический мониторинг препарата в процессе лечения, корригируя его дозу в соответствии с возрастом больного и функциональным состоянием почек.
Метициллинрезистентные стафилококки наиболее чувствительны к амикацину и нетилмицину.
Линкомицин и клиндамицин применяют при стафилококковом эндокардите в случаях аллергии к бета-лактамам, но необходимо учитывать, что метициллинрезистентные штаммы могут быть устойчивы к этим препаратам. Наиболее высокий эффект они дают при стрептококковом эндокардите. Большое преимущество имеет в/в введение клиндамицина, так как при этом достигаются высокие концентрации препарата в тканях сердца.
Гликопептиды — ванкомицин и тейкопланин активно действуют на грамположительные кокки, включая стафилококки и энтерококки. Эти антибиотики активны в отношении метициллинрезистентных стафилококков, однако ванкомицин, как и аминогликозиды, обладает нефротоксичностью. Для предотвращения этого побочного эффекта следует коррелировать дозу препарата с возрастом больного и функцией почек и (или) определять концентрацию антибиотика в крови. Комбинация ванкомицина с аминогликозидами высокоэффективна при лечении стафилококкового эндокардита, хотя риск токсического поражения почек при таком сочетании увеличивается.
Эффективность ванкомицина повышается при его комбинации с рифампицином. Действие ванкомицина при лечении эндокардита, вызванного метициллинрезистентными и метициллинчувствительными штаммами стафилококка, примерно одинаково. По-видимому, тейкопланин более активен и безопасен, однако на коагулазонегативные стафилококки он действует слабее, чем на золотистый.
Тейкопланин имеет большой период полуэлиминации и поэтому вводится в/в раз в день. Существуют 2 схемы его применения для борьбы со стафилококковой инфекцией. Ранее вводили 400мг препарата и по достижении клинического эффекта дозу снижали. Теперь назначают по 10-20 мг/кг в день в течение 2-4 дней, а затем дозу снижают до 8-10 мг/кг.
При эндокардите, вызванном грамположительными бактериями, включая стафилококки и стрептококки, с помощью тейкопланина удается добиться выздоровления и эррадикации бактерий в 90% случаев. Причем отмечена примерно одинаковая эффективность при нативном эндокардите и поражении искусственных клапанов сердца,
Тейкопланин назначают для лечения тяжелой инфекции, связанной с катетеризацией крупных вен. Введение этого препарата при инвазии эпидермальным стафилококком в 90% случаев приводит к успеху. Примерно такая же эффективность наблюдалась при инфекции, вызванной другими грамположительными бактериями. Результаты лечения при наличии катетера были такие же, как и при его отсутствии.
Особую форму представляет инфекционный эндокардит у больных с искусственными клапанами сердца и водителем ритма, а также у находящихся на гемодиализе. При искусственном клапане сердца возможен ранний эндокардит, возникающий в течение 2 месяцев после протезирования, и поздний, который проявляется позже.
При раннем эндокардите высевают золотистый или эпидермальный стафилококки (50%), грамотрицательную микрофлору (21%), грибы (10%) и другие возбудители. С учетом такой флоры для лечения можно использовать комбинацию цефалоспоринов (цефазолин, цефрадин) с гентамицином (до 240 мг в день), эффективен также ванкомицин.
При отрицательном результате бактериологического исследования рекомендуется в/в введение ванкомицина по 500 мг каждые 6 часов и гентамицина по 80 мг 3 раза в день с обязательным контролем функции почек.
Возбудителями позднего эндокардита становятся эпидермальный стафилококк и стрептококки (50% случаев), золотистый стафилококк (16%), энтерококки (11%), грамотрицательная микрофлора (11%). У 7% больных получают отрицательный результат посева крови.
Если эндокардит вызван эпидермальным стафилококком, целесообразно назначить ванкомицин вместе с рифампицином (по 300 мг и вдень внутрь в течение 6 недель) и гентамицин в дозе 1 мг/кг 3 часов в течение 7-10 дней.
Против других возбудителей применяют те же препараты, что и при типичном инфекционном эндокардите.
В случае отрицательного результата посева крови наилучшая комбинация цефалоспоринов (или ванкомицина) с аминогликозидами, поскольку эти препараты воздействуют на наиболее часто встречающуюся микрофлору.
У больных, находящихся на гемодиализе, эндокардит обычно вызывают золотистый стафилококк, зеленящий стрептококк, энтерококк, синегнойная палочка. В лечении можно использовать те же антибактериальные средства, которые чаще всего применяют при инфекционном эндокардите, но с учетом изменения их фармакокинетики из-за хронической почечной недостаточности и гемодиализа.
Возбудителями эндокардита у больных с искусственным водителем ритма бывают золотистый или эпидермальный стафилококки, грамотрицательная микрофлора, стрептококки, грибы. Эффекта можно добиться в/в введением тех же антибиотиков, что и при обычном инфекционном эндокардите, но в больших дозах. При угрозе эндокардита удаляют электроды и генератор.
Возврат на главную страницу.
Возврат в КУНСТКАМЕРУ.
Лечение
Терапия инфекционного эндокардита базируется на нескольких принципах:
1. Терапия должна быть по возможности этиотропной, то есть направленной на эрадикацию конкретного возбудителя.
2. Необходимо применять комбинацию нескольких антибактериальных препаратов для достижения высоких бактерицидных концентраций и предупреждения развития резистентности.
3. Терапия должна быть продолжительной: при заболевании стрептококковой этиологии — не менее 4 нед, стафилококковой — 6 нед, при заболевании, вызванном грамотрицательными возбудителями, — не менее 8 нед.
4. При нарастании признаков иммунного конфликта в форме гломерулонефрита, васкулита, миокардита и др. а также проявлений инфекционно-токсического шока рассматривают вопрос о назначении ГКС.
5. При острых формах инфекционного эндокардита, вызванного преимущественно стафилококками и грамотрицательными микроорганизмами, целесообразно проведение иммунотерапии (антистафилококковая плазма, антистафилококковый у-глобулин) и дезинтоксикации.
6. При отсутствии эффекта в течение 2 нед после применения адекватной антибиотикотерапии необходима консультация кардиохирурга. Хирургическое лечение следует проводить по строгим показаниям и своевременно.
В соответствии с приказом МЗ Украины № 436 от 03.07.2006 г. «Стандарти надання допомоги кардіологічним хворим» программа лечения инфекционного эндокардита предусматривает следующий перечень медицинских услуг:
Обязательный ассортимент
• оперативное лечение;
• этиотропная терапия: антибиотикотерапия под контролем чувствительности возбудителя, применение ГКС и др.
• симптоматическое лечение СН и осложнений.
Дополнительный ассортимент
• применение амиодарона у больных с симптомными или тяжелыми желудочковыми аритмиями;
• внутривенное введение симпатомиметических средств (допамина и/или добутамина);
• непрямые антикоагулянты у больных с постоянной формой фибрилляции предсердий, наличием тромбов в полостях сердца, тромбоэмболий в анамнезе.
При выборе антибиотика следует учитывать результаты микробиологического исследования, чувствительность выделенного возбудителя.
Трудности лечения прежде всего обусловлены широким распространением нетипичных возбудителей заболевания с высокой резистентностью многих микроорганизмов к существующим антибиотикам. Немаловажное значение имеет и тот факт, что антибиотики плохо проникают в клапаны сердца и миокард и во многих случаях (например при наличии искусственных клапанов сердца, шунтов, кардиостимуляторов) течение эндокардита не всегда прогнозируемо. При выявлении инфекционного эндокардита антибактериальное лечение необходимо начинать как можно раньше, не дожидаясь идентификации возбудителя, поскольку процесс быстро диссеминирует. В случаях с неустановленным возбудителем инфекционного эндокардита рекомендуют начинать терапию бета-лактамными антибиотиками и аминогликозидами (схема 7.1). Отсутствие эффекта через 3—5 дней и отрицательные результаты бактериологического исследования позволяют предположить наличие стафилококкового эндокардита, который вероятнее всего обусловлен пенициллино- и метициллинорезистентными стафилококками, что требует замены антибиотика.
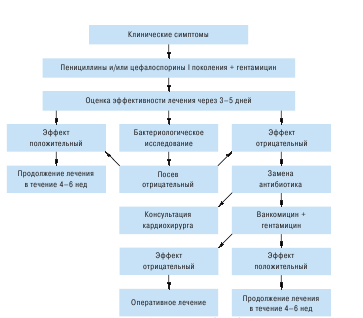
Схема 7.1.
Алгоритм эмпирического лечения инфекционного эндокардита
Наиболее эффективными считаются бензилпенициллин, цефалоспорины и аминогликозиды. Антибиотиком выбора для начальной терапии, как правило, является бензилпенициллин в суточной дозе 12—24 млн ЕД. Выбор этого антибиотика (при соблюдении рекомендуемой дозы) объясняется его доступностью, выраженным бактерицидным действием на многие микроорганизмы и широким терапевтическим диапазоном.
Современная этиотропная химиотерапия инфекционного эндокардита у больных с нормальной функцией почек представлена в табл. 7.2.
Таблица 7.2
Этиотропная химиотерапия инфекционного эндокардита
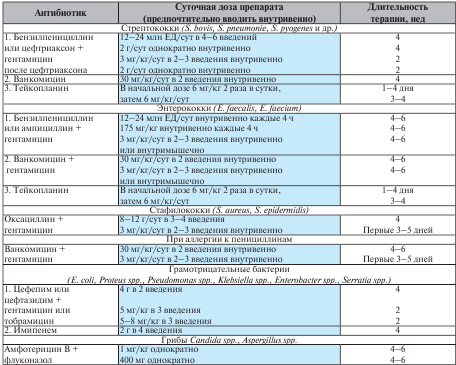
Для лечения инфекционного эндокардита, вызванного стрептококком, назначают бензилпенициллин в течение 4 нед или бензилпенициллин в комбинации с аминогликозидом (гентамицин, тобрамицин в течение 2 нед). Эти режимы требуют длительной госпитализации пациентов и использования внутривенных катетеров, что часто приводит к развитию флебитов. AHA опубликовала результаты двух исследований по лечению цефтриаксоном пациентов со стрептококковым эндокардитом. Высокая степень излечения (98%) после 4-недельной терапии препаратом оправдывает применение цефтриаксона с учетом спектра активности и фармакокинетических особенностей, позволяющих назначать его 1 раз в сутки и использовать для амбулаторного лечения неосложненного инфекционного эндокардита.
При аллергических реакциях на пенициллины и цефалоспорины рекомендованы гликопептидные антибиотики.
Современная антибиотикотерапия энтерококкового эндокардита с учетом того, что энтерококки значительно менее чувствительны к бензилпенициллину и гентамицину, включает комбинацию антибиотиков, обладающих синергическим действием: аминопенициллин (ампициллин) или гликопептидный антибиотик (ванкомицин, тейкопланин) с аминогликозидами (гентамицин, стрептомицин). Серьезную проблему представляют инфекционный эндокардит, вызванный энтерококками с высоким уровнем резистентности к аминогликозидам. В этих случаях назначают длительную (8-12 нед) терапию бензилпенициллином или ампициллином в высоких дозах. При аллергии к бета-лактамным антибиотикам следует назначать ванкомицин в комбинации с аминогликозидами внутривенно, тейкопланин. Частота рецидивов при этом составляет 50%. При рецидиве показано кардиохирургическое лечение с имплантацией клапана. Если энтерококки резистентны к пенициллинам, аминогликозидам и ванкомицину, эффективной антибактериальной терапии нет. Возможно применение линезолида в дозе 600 мг каждые 12 ч.
Цефалоспорины не следует применять для лечения энтерококкового эндокардита из-за первичной резистентности к ним этих микроорганизмов.
При стафилококковом эндокардите доказано, что бактерицидный эффект, стерилизация клапанов и профилактика их тяжелых повреждений обеспечиваются быстрее при использовании комбинации пенициллинов или цефалоспоринов, устойчивых к действию беталактамаз, и аминогликозидов. При неэффективности терапии, выделении пенициллино- и метициллинорезистентных штаммов золотистого или эпидермального стафилококка или при аллергии к бета-лактамным антибиотикам применяют гликопептиды (ванкомицин, тейкопланин) в сочетании с аминогликозидами. В случаях аллергии к бета-лактамным антибиотикам при стафилококковом эндокардите применяют также линкозамиды (линкомицин, клиндамицин). Высокой противостафилококковой активностью отличается цефепим.
Эндокардиты, вызванные грамотрицательными микроорганизмами, почти всегда развиваются в результате внутригоспитального инфицирования и лечить их сложно из-за наличия у возбудителей различных механизмов резистентности. Современная антибиотикотерапия предполагает применение аминогликозидов (тобрамицин, нетилмицин, амикацин) в сочетании с цефалоспоринами Ш—1У поколения (цефтриаксон, цефепим) или карбапенемов (имипенем, меропенем) в течение 4—6 нед.
При грибковых эндокардитах проводят комбинированную химиотерапию амфотерицином В и флуконазолом в сочетании с хирургическим лечением. Даже при оптимальном лечении отмечают высокую смертность и поздние рецидивы заболевания (через 2 года и более).
Для лечения пациентов с эндокардитом протезированных клапанов можно использовать комбинацию цефалоспоринов с гентамицином или тобрамицином, эффективен ванкомицин. При заболевании, вызванном эпидермальным стафилококком, чаще применяют ванкомицин/ тейкопланин с рифампицином и гентамицин. Монотерапия рифампицином нецелесобразна.
При длительном проведении антибактериальной терапии внутривенно рекомендуют добавлять гепарин из расчета 1 ЕД/мл раствора антибиотика для предотвращения образования тромбов и 1 раз в неделю вводить амфотерицин В (50 000 ЕД 990 внутривенно капельно) для предупреждения грибковой инфекции. Противогрибковые препараты целесообразно применять приблизительно с середины курса антибиотикотерапии, когда можно ожидать развития грибковой инфекции. Для диагностики последней и оценки эффективности терапии необходимо проводить посевы соскобов с корня языка и посевы мочи для выявления грибковой флоры.
Дискуссионным остается вопрос о применении ГКС, многие исследователи обращались к этой проблеме, но она до сих пор не решена. В настоящее время можно утверждать, что применение ГКС не предотвращает разрушения клапанного аппарата: подавляя воспалительную реакцию вокруг очага инфекции, они, наоборот, обусловливают более быстрое разрушение клапана. Гормональная терапия ведет к угнетению клеточного и гуморального иммунитета, необходимого для борьбы с инфекцией, вызывает снижение фагоцитарной активности лейкоцитов и уровня образования антител, которые могут способствовать генерализации септического процесса. Назначение ГКС нежелательно до достижения надежного подавления возбудителя антибиотиками (нормализации температуры тела, тенденции к снижению СОЭ). ГКС опасно применять в случаях заболевания с отрицательной гемокультурой, когда врачи вынуждены проводить эмпирическую антибактериальную терапию, а гормоны, устраняя лихорадку, анемию и замедляя СОЭ, лишают их критериев оценки эффективности этой терапии.
Недопустимо применение ГКС при рецидивах заболевания, особенно ранних (в течение первых 2-3 мес), когда нет возможности провести полную эрадикацию возбудителя. В случаях заболевания с установленным возбудителем и известной его чувствительностью к антибиотикам в применении гормонов, как правило, нет необходимости.
Таким образом, ГКС не являются препаратами первого ряда, они противопоказаны при остром септическом эндокардите, наличии септического синдрома при подостром септическом эндокардите, неустановленном возбудителе, отсутствии эрадикации возбудителя, при рецидивирующем инфекционном эндокардите. Неблагоприятное влияние ГСК на течение инфекционного эндокардита, особенно в дозе >30 мг/сут, делают их применение нежелательным.
Показанием к назначению ГКС является инфекционно-токсический шок, при котором кратковременное применение ГКС в высоких дозах (>100-200 мг в пересчете на преднизолон) жизненно необходимо. Несомненным показанием к их назначению является медикаментозная аллергия. Относительным показанием к их применению является тяжелое иммуновоспалительное поражение почек (протеинурия >1 г/л) и миокарда.
При инфекционном эндокардите, особенно остром, проводят пассивную иммунизацию готовыми антитоксическими сыворотками с целью нейтрализации циркулирующих в крови микробных токсинов. Наиболее эффективна гипериммунная плазма (в зависимости от вида возбудителя — антистафилококковая, антисинегнойная и др.). Антистафилококковую плазму вводят внутривенно капельно по 125-250 мл ежедневно или через день (4—6 вливаний на курс). Антисинегнойную плазму вводят внутривенно из расчета 4—6 мл/кг (в среднем 250 мл) с интервалами между вливаниями 1—3 дня (4—6 вливаний на курс). Антистафилококковый гаммаглобулин не только является источником антител, но стимулирует также факторы неспецифического иммунитета, применяется в виде внутримышечных инъекций по 5—10 мл ежедневно в течение 10 дней. Иммуноглобулин человека вводят внутривенно по 50 мл со скоростью 20—40 капель/мин ежедневно в течение 3—5 дней.
Оперативное лечение проводится как в ранние сроки заболевания при сохраняющихся лихорадке и бактериемии, так и по завершении как минимум 4—6-недельного курса антибактериальной терапии. В хирургическом лечении нуждаются около 20% больных инфекционным эндокардитом.
Показаниями к оперативному вмешательству на нативных клапанах являются:
• СН вследствие остро возникшей недостаточности аортального или митрального клапана;
• персистирующая лихорадка и бактериемия более 8 дней, несмотря на антибактериальную терапию;
• абсцессы, псевдоаневризмы, нарушения проводимости, миокардит;
• выявление возбудителей, часто не поддающихся антибактериальной терапии (грибы, Brucella, Coxiella);
• выявление микроорганизмов c высоким потенциалом к быстрой деструкции структур сердца (S. Iugdunensis);
• поражения миокарда и фиброзного кольца.
К относительным показаниям к хирургическому лечению инфекционного эндокардита нативных клапанов относят наличие массивных вегетаций на внутрисердечных структурах (по данным эхоКГ), эмболии периферических сосудов, выделение в гемокультуре грамотрицательной палочки или стафилококка.
Хирургический метод заключается в удалении пораженных клапанных структур с вегетациями и имплантации вместо него искусственного механического или биологического протеза. Имеются сообщения о новых подходах: иссечении вегетаций, ушивании перфорации створки клапана, изолированном протезировании одной из створок митрального или аортального клапана ксеноперикардом и санации камер сердца, закрытии полости абсцесса. Общая 5-летняя выживаемость с учетом госпитальной летальности составляет 70—75%.
Показаниями для проведения неотложного хирургического вмешательства при инфекционном эндокардите протезированных клапанов сердца являются установление грибковой этиологии инфекционного эндокардита, появление симптомов СН, признаков нарушения функции протеза, внутрисердечных абсцессов, прогрессирование нарушений проводимости сердца, рецидивирующие эмболические осложнения. Хирургическое лечение инфекционного эндокардита протезированных клапанов сопровождается высоким операционным риском. Операция может потребоваться также для лечения пациентов с тяжелыми системными эмболическими осложнениями, для иссечения абсцесса селезенки или лечения микотических аневризм.
АНТИБАКТЕРИАЛЬНАЯ ТЕРАПИЯ ЭНДОКАРДИТА
Антибактериальное лечение инфекционного эндокардита нужно начинать как можно раньше. В большинстве случаев лечение приходится начинать еще в тот период, когда возбудитель не идентифицирован. Целесообразно применять комбинацию двух антибиотиков. Вводят пенициллин 4-6 раз в сутки в суточной дозе 12-20 млн ЕД внутримышечно. Возможно и внутривенное введение натриевой соли пенициллина. Его сочетают с гентамицин ом 160-240 мг в сутки в 2-3 приема (табл. 14.37 ).
При отсутствии данных о возбудителе, эффекта от проводимой терапии пенициллином и амин огликозидом в течение 3-5 дней (сохранение лихорадки и т.д.) дозу пенициллина следует увеличить до 40 млн; вводят его через каждые 4 ч. Можно также заменить пенициллин ампициллин ом (или оксациллин ом) в дозе 6-10 г в сутки, вводя его внутримышечно 4 раза в сутки. Если отсутствует эффект и от такого лечения, можно присоединить к 2 антибиотикам цефалоспорины, например, цефазолин (4-6 г). Такая комбинация антибиотиков часто дает осложнения, поэтому должна применяться лишь в крайних случаях.
S.viridans. Лечение проводят одним пенициллином (9-20 млн ЕД/сут в индивидуальной дозировке через каждые 4 ч) или пенициллином в комбинации с амин огликозидами (стрептомицин — 0,5 г каждые 12 ч). При этом амин огликозиды используют только первые 2 нед. В последующие 2 недели вводят один пенициллин. Таким образом, общий курс терапии составляет 4 недели.
Стафилококковый эндокардит является, по-видимому, наиболее частым видом поражения клапанного аппарата сердца (в 16-25% нативного первичного эндокардита). Причем стафилококковый эндокардит представляет собой очень серьезную клиническую проблему, что обусловлено преобладанием пенициллин- и метициллинрезистентных штаммов, увеличением числа внутривенных инфузий лекарств, больных с имплантированными искусственными клапанами сердца и шунтами, длительной катетеризацией (катетер Хикмана), повышением количества больных с иммунодефицинтыми состояниями (в том числе и СПИД).
Эндокардит, вызванный S.aureus, нередко сочетается с септицемией (в 10%) и отличается высокой летальностью (40-60%) и требует длительной в течение 4-6 недель антибактериальной парентеральной терапии.
Общая летальность при эндокардите искусственного клапана сердца достигает 30%, причем в трети случаев выделяют S.epidermidis и в 14% S.aureus.
При подозрении на стафилококковый эндокардит наиболее часто используют бета-лактамные антибиотики (пенициллины и цефалоспорины) в максимальной переносимой дозе и внутривенно.
Применение пенициллина, а также ампициллин а или пиперациллин а в виде монотерапии нецелесообразно, так как эти антибиотики разрушаются бета-лактамазами, продуцируемыми стафилококками. Наиболее часто для лечения стафилококковой инфекции рекомендуют комбинацию пенициллинов с ингибиторами бета-лактамаз: ампициллин +сулбактам, амоксициллин +клавулановая кислота, пиперациллин +тазобактам. Эти комбинации делают пенициллин таким же эффективным против бета-лактамаз- продуцирующих бактерий, как оксациллин или цефалоспорины 1 группы (например, цефазолин ). Комбинация амоксициллин а с клавулановой кислотой была так же эффективна, как ванкомицин.
Внегоспитальные штаммы S.aureus, как правило, резистентные к пенициллину, сохраняют постоянную чувствительность к изоксазолиловым производным пенициллина: нафциллин, оксациллин. клоксациллин. дикло ксациллин. флуклоксациллин. которые не деградируют под влиянием стафилококковых (амбулаторных) штаммов бета-лактамаз. Препараты сравнимы по эффективности, переносимости и фармакокинетическим данным, хотя метициллин очень часто вызывает лейкопению, интерстициальный гломерулонефрит и реакции гиперчувствительности. Однако эти антибиотики не эффективны в случаях эндокардита, вызванного метициллинрезистентными штаммами, как правило, выделяемыми при внутригоспитальной инфекции.
Большинство цефалоспоринов достаточно устойчивы к действию бета-лактамаз, продуцируемых стафилококками, однако исключение составляет метициллинрезистентные штаммы S.aureus и S.epidermidis.
При стафилококковом эндокардите наиболее эффективны следующие цефалоспорины:цефазолин, цефапирин. цефалотин. цефрадин. Цефалоридин из-за своей нефротоксичности не может длительно применяться у больных эндокардитом.
Примерно одинаковой эффективностью по сравнению с перечисленными препаратами обладает цефамандол. цефуроксим. цефотиам.
Более низкой антистафилококковой активностью по сравнению с вышеперечисленным обладают цефатоксим, цефозидим, цефтриаксон ; in vitro хорошей антибактериальной активностью отличается цефпиром и цефиксим. однако клинического опыта и крупномасштабной оценки эффективности этих антибиотиков при стафилококковом эндокардите не накоплено.
Эндокардит, вызванный метициллинрезистентными стафилококками, плохо лечится цефалоспориновыми антибиотиками.
Синергизм в действии антибиотиков наблюдается при сочетании бета-лактамных антибиотиков (пенициллинов и цефалоспоринов) с амин огликозидами. Поэтому эта комбинация антибиотиков наиболее распространена при лечении эндокардита. В то же время ототоксичность, нефротоксичность и поражение вестибулярного аппарата, свойственные амин огликозидам, ограничивают возможности их применения в клинике. Предупредить потенциальные и довольно частые органотоксические эффекты можно осуществляяя терапевтический мониторинг антибиотика в процессе лечения, корригируя дозу препарата в соответствии с возрастом больного и функцией почек. Для метициллинрезистентных стафилококков наибольшая активность наблюдается in vitro для нетилмицин а.
Линкомицин и клиндамицин следует применять при стафилококковом эндокардите в случаях аллергии к бета-лактамам. Однако следует учитывать, что метициллинрезистентные штаммы могут быть устойчивы к клиндамицин у и линкомицин у. Хотя клинические данные подчеркивают достаточно высокую эффективность препарата, по-видимому, за счет большей эффективности при стрептококковом эндокардите. Следует учесть высокие концентрации клиндамицин а при внутривенном введении в тканях сердца: до 16 мкг/мг в ткани правого предсердия.
Гликопептиды – ванкомицин и тейкопланин являются активными агентами против грамположительных кокков, включая стафилококки и энтерококки. Ванкомицин и тейкопланин активны против метициллинрезистентных стафилококков, однако следует отметить нефротоксичность ванкомицин а, которую можно сравнить с амин огликозидами. Для предотвращения нефротоксического эффекта следует кореллировать дозу препарата с возрастом, функцией почек и (или) определять концентрацию препарата в крови с последующей коррекцией дозы препарата.
Комбинация ванкомицин а с амин огликозидами является высокоэффективной при лечении стафилококкового эндокардита, хотя риск токсического поражения почек увеличивается. Эффективность ванкомицин а повышается при комбинации препарата с рифампицин ом.
При этом клиническая эффективность при лечении ванкомицин ом эндокардита, вызванного метициллинрезистентными и метициллинчувствительными штаммами стафилококка, примерно одинакова.
Тейкопланин. по-видимому, более активен и безопасен, чем ванкомицин при эндокардите, вызванном чувствительными и резистентными к ванкомицин у штаммами стафилококков. Однако следует подчеркнуть, что на коагулазонегативные стафилококки тейкопланин действует слабее, чем на S.aureus.
Тейкопланин имеет большой период полуэлиминации и поэтому вводится один раз в сутки. Для лечения стафилококковой инфекции используют два подхода к применению тейкопланин а. В ранних работах вводили 400 мг препарата один раз в сутки и по достижении клинического эффекта дозу снижали. В более поздних исследованиях применяли тейкопланин по 10-20мг/кг.сут 2-4 дня, а затем дозу снижали до 8-10 мг/кг.сут, что позволяло достичь достаточно безопасной концентрации в крови 15-25 мг/л.
При эндокардите, вызванном грамположительными бактериями, включая S.aureus, E.faecalis, S.viridaus, тейкопланин вызывал в 90% случаев выздоровление и эрадикацию бактерий. Причем отмечена примерно одинаковая эффективность при нативном эндокардите и поражении искусственных клапанов сердца. Сообщают об итогах лечения тяжелой инфекции, связанной с катетеризацией крупных вен: в 81 случае выделен S.epidermidis (в 44% резистентный к метициллину), в 25 % изолятов – S.aureus, в 10 – зеленящий стрептококк, в 7 – энтерококк и в двух – Corynebacterium. В 90% случаев был достигнут успех при введении тейкопланин а при инвазии эпидермальным стафилококком, примерно такая же эффективность наблюдалась при инфекции, вызванной другими грамположительными бактериями. Обращает на себя внимание поразительно одинаковая эффективность при лечении тейкопланин ом при наличии катетера и при его удалении.
При изучении сравнительной эффективности была обнаружена примерно одинаковая результативность при лечении тейкопланин ом и комбинацией флуклоксациллин а с фузидиевой кислотой. По-видимому, различий в клинической эффективности тейкопланин а с ванкомицин ом нет, однако переносимость первого гораздо лучше. При применении тейкопланин а и бета-лактамов число побочных эффектов при лечении пенициллинами и цефалоспоринами было больше.
Обсуждается вопрос о применении при стафилококковой инфекции фторхинолонов (ципрофлоксацин) в комбинации с рифампицин ом или фузидиевой кислотой. Применение фузидиевой кислоты ограничено в связи с большим числом желудочно-кишечных расстройств, в частности гипербилирубинемией, наблюдаемой у половины больных в процессе лечения. В некоторых странах получило распространение лечение эндокардита фосфомицин ом в дозе до 8 г/сут.
Пневмококки, гонококки и менингококки. В случае переносимости пенициллина и чувствительности к нему микрофлоры этот препарат является лекарством выбора в дозировке 10-20 млн ЕД/сут внутримышечно в течение 4 нед.
H. parainfluenzae. Данный вид эндокардита лечат комбинацией амин огликозидов (гентамицин — 4,5-5,0 мг/кг массы тела в сутки в индвидуальной дозировке через каждые 8 ч) с ампициллин ом (200-300 мг/кг массы тела в сутки). Продолжительность лечения составляет 6-8 нед.
Энтеробактерии. При лечении эндокардита данной этиол огии обычно используют комбинацию карбенициллин а (340 г в сутки) с амин огликозидами (гентамицин — 4,5-5,0 мг/кг массы тела в сутки) в течение 6 нед или цефалоспорины II группы.
При всех случаях отрицательного результата бактериологического анализа необходимо помнить, что наиболее частая причина бактериального эндокардита — стафилококковая микрофлора, поэтому лечение рекомендуется начинать с комбинации полусинтетических пенициллинов (оксациллин — 2 г каждые 4 ч) и амин огликозидов (гентамицин — 1 мг/кг массы тела каждые 8 ч).
Следует корригировать дозу антибиотиков в соответствии с тяжестью поражения почек. К неспецифическим методам лекарственной терапии относятся стероидные и нестероидные противовоспалительные средства, иммуномодуляторы и антикоагулянты.
Особую форму эндокардита представляет инфекционный эндокардит у больных с искусственными клапанами сердца и водителем ритма и у лиц, находящихся на гемодиализе.
У больных с искусственным клапаном сердца различают ранний эндокардит, возникающий в течение 2 мес после протезирования, и поздний, который определяется спустя 2 мес после операции. В 50% случаев раннего эндокардита высевают золотистый и эпидермальный стафилококки, грамотрицательную микрофлору (21%), грибы (10%) и другие возбудители. В этой связи для лечения можно использовать комбинацию цефалоспоринов с гентамицин ом (или тобрамицин ом). Успешно применяют также ванкомицин. При отрицательном бактериологическом исследовании рекомендуется введение ванкомицин а по 500 мг внутривенно каждые 6 ч и гентамицин а (или тобрамицин а) с обязательным контролем функции почек.
Возбудителями позднего эндокардита у лиц с протезированными клапанами сердца являются в 50% случаев эпидермальный стафилококк и стрептококки, золотистый стафилококк (16%), энтерококки (11%), грамотрицательная микрофлора (12%). Отрицательный результат посева крови получают у 7% больных. Если инфекционный эндокардит вызван эпидермальным стафилококком, для лечения применяют ванкомицин вместе с рифампицин ом (по 300 мг 2-3 раза в сутки внутрь в течение 6 нед) и гентамицин в дозе 1 мг/кг массы тела каждые 8 ч в течение 7-10 дней. Против других возбудителей применяют те же препараты, что и при обычном инфекционном эндокардите.
При отрицательном результате посева крови наилучшей является комбинация цефалоспоринов (или ванкомицин а) с амин огликозидами, что оправдано с точки зрения их воздействия на наиболее часто встречающуюся микрофлору.
У больных, находящихся на гемодиализе, эндокардит вызывают золотистый стафилококк, зеленящий стрептококк, энтерококк, синегнойная палочка.
При этом используют те же антибактериальные средства, что и при обычном инфекционном эндокардите, с учетом изменения фармакокинетики лекарств из-за хронической почечной недостаточности и гемодиализа.
Причинами эндокардита у больных с искусственным водителем ритма являются золотистый и эпидермальный стафилококки, грамотрицательная микрофлора, стрептококки, грибы. Применяют те же антибиотики, что и при обычном инфекционном эндокардите, но в больших дозах внутривенно. В этом случае удаляют электроды и генератор.
Эндокардит у наркоманов с поражением чаще всего трехстворчатого клапана обусловлен в первую очередь золотистым стафилококком (50%), стрептококком (20%), грамотрицательной микрофлорой, включая синегнойную палочку (15-20%), и грибами (10%). Антибактериальная терапия неэффективна и требуется замена клапана.




