Новые рекомендации ESH/ESC 2013 г. по лечению артериальной гипертонии: основные изменения
Карпов Ю.А. Старостин И.В.
Введение
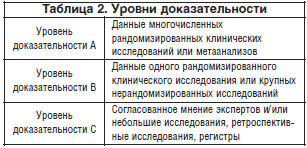
В июне 2013 г. на Ежегодной европейской конференции по артериальной гипертонии (АГ) были представлены новые рекомендации по ее лечению. созданные Европейским обществом по гипертонии (ЕОГ, ESH) и Европейским обществом кардиологов (ЕОК, ESC). Они являются продолжением рекомендаций от 2003 и 2007 гг. обновленных и дополне нных в 2009 г. [1–3]. Эти рекомендации сохраняют преемственность и приверженность основным принципам: основаны на правильно выполненных исследованиях, найденных при всестороннем анализе литературы, учитывают приоритет рандомизированных контролируемых исследований (РКИ) и метаанализов данных исследований, а также результаты обсервационных и других исследований должного качества, класс рекомендаций (табл. 1) и уровень доказательности (табл. 2). Рекомендации вырабатывались на протяжении 18 мес. и перед изданием были дважды рассмотрены 42 европейскими специалистами (по 21 от каждого Общества).
В настоящее время Российское медицинское общество по артериальной гипертонии (РМОАГ), аффилированное с Европейским обществом по АГ, осуществляет подготовку к изданию отечественной версии данных рекомендаций.
Новые аспекты
В новых рекомендациях по лечению артериальной гипертонии. выпущенных ЕОГ/ЕКО в 2013 г. перечислены 18 наиболее важных отличий от предыдущих рекомендаций:
1. Новые эпидемиологические данные по АГ и ее контролю в странах Европы.
2. Признание большего прогностического значения домашнего мониторирования артериального давления (ДМАД) и его роли в диагностике и лечении АГ.
3. Новые данные о влиянии на прогноз значений ночного АД, «гипертонии белого халата» и маскированной гипертонии .
4. Оценка общего сердечно-сосудистого риска – больший акцент на величину АД, сердечно-сосудистые факторы риска, бессимптомное поражение органов-мишеней и клинические осложнения.
5. Новые данные о влиянии бессимптомного поражения органов-мишеней, включая сердце, сосуды, почки, глаза и головной мозг, на прогноз.
6. Уточнение риска, связанного с избыточной массой тела, и целевого значения индекса массы тела (ИМТ) при АГ.
7. АГ у пациентов молодого возраста.
8. Начало антигипертензивной терапии. Повышение доказательности критериев и воздержание от медикаментозной терапии при высоком нормальном АД.
9. Целевые значения для терапии АД. Унифицированные целевые значения систолического артериального давления (САД) (<140 мм рт.ст.) у пациентов из группы как с высоким, так и с низким сердечно-сосудистым риском.
10. Свободный подход к начальной монотерапии, без какого-либо ранжирования препаратов.
11. Измененная схема предпочтительных комбинаций из двух препаратов.
12. Новые алгоритмы терапии для достижения целевого АД.
13. Дополненный раздел по тактике лечения в особых ситуациях.
14. Изменения в рекомендациях по лечению гипертонии у больных пожилого и старческого возраста.
15. Медикаментозная терапия у лиц старше 80 лет.
16. Особое внимание к резистентной АГ, новые подходы к ее лечению.
17. Усиление внимания к терапии с учетом поражения органов-мишеней.
18. Новые подходы к длительной (хронической) терапии АГ.
Далее в статье будут отражены наиболее важные, с нашей точки зрения, изменения по сравнению с предыдущими рекомендациями, что может быть интересно широкому кругу врачей и научных работников и послужит некоей «дорожной картой» для более детального изучения полной версии рекомендаций. С полной версией рекомендаций Вы можете ознакомиться на официальном сайте Российского медицинского общества по АГ – www.gipertonik.ru.
Новые эпидемиологические данные по АГ
Одним из лучших суррогатных показателей, отражающих ситуацию с АГ, является инсульт и смертность от него [4, 5]. В странах западной Европы отмечается снижение частоты инсультов и смертности от них, в то время как в восточно-европейских странах, в т.ч. в России (данные ВОЗ с 1990 по 2006 гг.), смертность от инсульта до последнего времени увеличивалась [6] и только в последние 3 года стала снижаться.
Внеофисное мониторирование АД
Под внеофисным мониторированием АД понимают суточное мониторирование АД (СМАД), осуществляемое с помощью непрерывно носимого в течение суток аппарата, и домашнее мониторирование АД (ДМАД), при котором обученный технике измерения АД больной самостоятельно производит измерения. Внеофисное измерение АД имеет ряд преимуществ, что нашло отражение в новых рекомендациях по АГ от 2013 г. Основное из них – большее число измерений, что лучше отражает реальную ситуацию с АД, чем измерения у врача. Кроме того, амбулаторное изменение АД лучше, чем офисное коррелирует с такими маркерами поражения органов-мишеней у больных АГ, как гипертрофия левого желудочка (ГЛЖ), толщина комплекса интима-медия сонной артерии и др. [7, 8], а СМАД лучше коррелирует с заболеваемостью и смертностью, чем офисное [9–12]. Интересно, что преимущество внеофисного мониторирования АД выявлено как в общей популяции, так и в отдельных подгруппах: у больных молодого и пожилого возраста, у лиц обоих полов, как находящихся на медикаментозном лечении, так и без него, а также у лиц высокого риска, у лиц с сердечно-сосудистыми заболеваниями и заболеваниями почек [13–17]. Также установлено, что ночное АД является более сильным предиктором, чем дневное [14, 18]. В новых рекомендациях подчеркивается, что клиническое значение типа изменения ночного АД (т.н. «диппинг») на настоящий момент до конца не определено, т.к. данные по изменению сердечно-сосудистого риска у лиц с выраженным «диппингом» неоднородны [13, 19].
В настоящее время существуют рекомендации, которых следует придерживаться при ДМАД [20, 21]. Оставив в стороне методологические вопросы проведения ДМАД, следует отметить, что в обиход входят телемониторинг и приложения для ДМАД к смартфонам [22, 23], причем интерпретация результатов и коррекция лечения должны, безусловно, проводиться под руководством врача. В отличие от СМАД ДМАД позволяет оценить изменение АД за длительное время и связано с существенно меньшими затратами [24], однако не позволяет оценить ночные значения АД, различия в ночном и дневном АД, а также изменение АД через короткие промежутки времени [25]. Следует отметить, что ДМАД не хуже, чем СМАД, коррелирует с поражением органов-мишеней и имеет такую же прогностическую значимость [7, 26, 27].
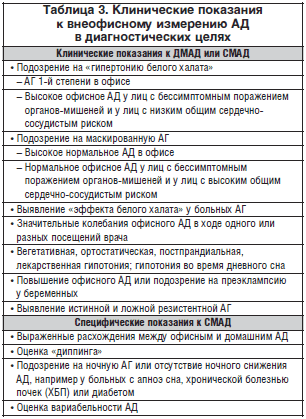
Выбор методики измерения АД вне офиса (СМАД или ДМАД) зависит от конкретной ситуации. Так, при поликлиническом наблюдении логичным будет использование ДМАД, в то время как СМАД при этом может использоваться при пограничных или патологических результатах ДМАД [28]. В рамках специализированной помощи логичнее выглядит использование СМАД. В обоих случаях длительный контроль эффективности лечения невозможен без ДМАД. Клинические показания к внеофисному измерению АД представлены в таблице 3.
Изолированная офисная АГ
(или «гипертония белого халата»)
и маскированная АГ
(или изолированная амбулаторная АГ)
СМАД и ДМАД являются стандартными методами выявления данных нозологических форм. В связи с присущими этим методам измерения АД различиями определения «гипертония белого халата» и «маскированная гипертония» ;, диагностированные методом СМАД и ДМАД, совпадают не полностью [25]. Предметом дебатов остается вопрос, можно ли отнести лиц с «гипертонией белого халата» к истинным нормотоникам. В некоторых исследованиях у лиц с данным состоянием показан промежуточный между стойкой АГ и истинной нормотонией отдаленный сердечно-сосудистый риск [27]. При этом, по данным метаанализов, учитывающих пол, возраст и другие вмешивающиеся факторы, сердечно-сосудистый риск при «гипертонии белого халата» существенно не отличался от такового при истинной нормотонии [29–31]; впрочем, это может быть связано с лечением, которое получает часть этих больных. Диагноз «гипертония белого халата» рекомендуется подтверждать не позднее чем через 3–6 мес. а также тщательно обследовать и наблюдать данных пациентов.
По данным популяционных исследований, распространенность маскированной гипертонии достигает 13% (диапазон от 10 до 17%) [29]. Метаанализы проспективных исследований свидетельствуют о двукратном, в сравнении с нормотонией, росте сердечно-сосудистой заболеваемости при данном заболевании, что соответствует стойкой АГ [29–32]. Возможным объяснением данного феномена является плохая диагностируемость этого состояния и, соответственно, отсутствие лечения у данных больных.
Начало антигипертензивной терапии
и целевые значения
Согласно рекомендациям ESH/ESC 2007 г. [2], антигипертензивную терапию следовало назначать даже больным с АГ 1-й степени без других факторов риска или поражения органов-мишеней, если медикаментозная терапия оказалась безуспешной. Кроме того, больным с диабетом, сердечно-сосудистыми заболеваниями и ХБП антигипертензивную терапию рекомендовалось назначать, даже если их АД находится в высоком нормальном диапазоне (130–139/85–89 мм рт.ст.).
В настоящее время доказательств в пользу антигипертензивного лечения больных с АГ 1-й степени низкого и среднего риска крайне мало – ни одно исследование не было специально посвящено этим больным. Однако в недавно опубликованном Кохрановском метаанализе (2012-CD006742) выявлена тенденция к снижению частоты инсульта на фоне лечения больных с АГ 1-й степени, однако в связи с небольшим числом больных статистическая значимость не была достигнута. В то же время, существует ряд аргументов в пользу лечения АГ 1-й степени даже при низком и среднем уровне риска, а именно: повышение риска при выжидательной тактике, неполная эффективность терапии в отношении снижения сердечно-сосудистого риска, большое число безопасных препаратов, наличие дженериков, что сопровождается хорошим соотношением «стоимость – польза».
Повышение систолического АД выше 140 мм рт.ст. при сохранении нормального диастолического АД (<90 мм рт.ст.) у молодых здоровых мужчин не всегда сопровождается повышением центрального АД [33]. Известно, что изолированная систолическая гипертония у молодых не всегда переходит в систолическую/диастолическую АГ [33], а доказательств, что антигипертензивная терапия принесет пользу, не существует. Таким образом, этих больных следует тщательно наблюдать и рекомендовать изменение образа жизни.
Также изменилось и отношение к назначению антигипертензивной терапии больным высокого и очень высокого сердечно-сосудистого риска, связанного с диабетом, сопутствующими сердечно-сосудистыми или почечными заболеваниями, при высоких нормальных значениях АД (130–139/85–89 мм рт.ст.). Cкудные доказательства целесообразности столь раннего медикаментозного вмешательства не позволяют рекомендовать таким больным начало антигипертензивной терапии [33, 34].
Целевые значения АД для большинства групп больных составляют менее 140 мм рт.ст. для систолического АД [3, 34–43] и менее 90 мм рт.ст. – для диастолического [44]. В то же время, больным АГ пожилого и старческого возраста моложе 80 лет с исходным уровнем САД ≥160 мм рт.ст. рекомендовано снижение САД до 140–150 мм рт.ст. [34]. При этом удовлетворительное общее состояние здоровья этой группы больных делает потенциально целесообразным снижение САД <140 мм рт.ст. а у пациентов с ослабленным состоянием здоровья следует выбирать целевые значения САД в зависимости от переносимости. У больных старше 80 лет с исходным САД ≥160 мм рт.ст. рекомендовано его снижение до 140–150 мм рт.ст. при условии, что они находятся в удовлетворительном физическом и психическом состоянии [45]. Больным диабетом рекомендуется снижение ДАД до значений менее 85 мм рт.ст. [44].
На настоящий момент не существует рандомизированных исследований с клиническими конечными точками, которые позволили бы определить целевые значения АД при проведении его домашнего и амбулаторного мониторирования [46]. Тем не менее, по некоторым данным, эффективное снижение офисного АД сопровождается не слишком большими отличиями внеофисных показателей [47]. Другими словами, в данном исследовании показано, что чем более выражено снижение АД (по данным измерений в больнице) на фоне антигипертензивной терапии, тем ближе эти значения к величинам, полученным в ходе амбулаторного мониторирования, причем максимальное сходство результатов достигается при офисном АД <120 мм рт.ст.
Выбор антигипертензивной терапии
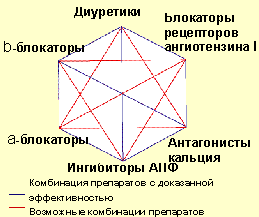
Как и в рекомендациях ESH/ESC 2003 и 2007 гг. [1, 2], в новых рекомендациях сохраняется утверждение об отсутствии превосходства какого-либо класса антигипертензивных препаратов над другими, т.к. основные преимущества антигипертензивной терапии обусловлены снижением АД как таковым [48–50]. В связи с этим новые рекомендации подтверждают использование диуретиков (включая тиазидные, хлорталидон и индапамид), β-блокаторов, антагонистов кальция, ингибиторов ангиотензинпревращающего фермента (АПФ) и блокаторов рецепторов ангиотензина в качестве начальной и поддерживающей, моно- и комбинированной терапии. Таким образом, не существует какого-либо универсального ранжирования антигипертензивных препаратов в связи с отсутствием их предпочтительности.
В новых рекомендациях сохраняется утверждение о целесообразности начала лечения с комбинации двух препаратов у больных высокого риска или при очень высоком исходном АД [2]. Это связано с тем, что комбинация двух антигипертензивных препаратов из разных классов, как показал метаанализ более 40 исследований, ведет к большему снижению АД, чем увеличение дозы при монотерапии [51]. Комбинированная терапия ведет к более быстрому снижению АД у большего числа больных, что особенно актуально именно для больных высокого риска и с очень высоким АД. Кроме того, больные, получающие комбинированную терапию, отказываются от лечения реже, чем больные, получающие монотерапию [52]. Не следует забывать и о синергидности между препаратами разных классов, что может вести к меньшей выраженности побочных эффектов. В то же время, комбинированная терапия имеет недостаток, который заключается в потенциальной неэффективности одного из препаратов в комбинации, что трудно выявить.
При неэффективности монотерапии или комбинации двух препаратов рекомендуется увеличить дозу до достижения целевого АД, вплоть до полной дозы. Если применение комбинации двух препаратов в полных дозах не сопровождается достижением целевого АД, можно добавить третий препарат или перевести больного на другую комбинированную терапию. Следует помнить, что при резистентной к лечению АГ добавление каждого препарата должно происходить с отслеживанием эффекта, при отсутствии которого препарат следует отменять.
Существует значительное число рандомизированных клинических исследований, посвященных антигипертензивной терапии с использованием комбинаций антигипертензивных препаратов, однако лишь в трех из них постоянно применялась конкретная комбинация двух антигипертензивных препаратов. В исследовании ADVANCE комбинацию ингибитора АПФ с диуретиком или плацебо добавляли к уже проводимой антигипертензивной терапии [39]. В исследовании FEVER проведено сравнение комбинированной терапии антагонистом кальция и диуретиком с монотерапией диуретиком плюс плацебо [36]. В исследовании ACCOMPLISH проведено сравнение комбинации ингибитора АПФ и диуретика с тем же ингибитором АПФ и антагонистом кальция [53]. Во всех остальных исследованиях лечение во всех группах начиналось с монотерапии, и лишь затем часть больных получали дополнительный препарат, причем не всегда только один. А в исследовании антигипертензивной и гиполипидемической терапии ALLHAT исследователь самостоятельно выбирал второй препарат среди тех из них, которые не использовались в другой терапевтической группе [54].
Тем не менее, почти все антигипертензивные комбинации применялись как минимум в одной группе лечения в плацебо-контролируемых исследованиях, за исключением блокаторов рецепторов ангиотензина и антагониста кальция. Во всех случаях выявлены существенные преимущества в группах активной терапии [36, 39, 40, 45, 55–60]. Кроме того, при сравнении разных режимов комбинированной терапии существенных различий выявлено не было [54, 61–68]. В виде исключения в двух исследованиях комбинация блокатора рецепторов ангиотензина и диуретика, а также комбинация антагониста кальция и ингибитора АПФ превзошли комбинацию β-блокатора и диуретика по снижению числа сердечно-сосудистых событий [69, 70]. В то же время, в ряде других исследований комбинация β-блокатора с диуретиком была столь же эффективна, как и другие комбинации [54, 63, 67, 68]. В исследовании ACCOMPLISH с прямым сравнением двух комбинаций выявлено значимое превосходство ингибитора АПФ в комбинации с антагонистом кальция перед ингибитором АПФ в сравнении с диуретиком, хотя уровни АД были идентичными [53]. Возможно, это связано с более эффективным действием антагониста кальция и ингибитора РААС на центральное давление [71]. По данным исследований ONTARGET [47] и ALTITUDE [72], комбинирование двух разных блокаторов РААС не рекомендуется.
В новых рекомендациях поощряется применение комбинаций из фиксированных доз двух и даже трех антигипертензивных препаратов в одной таблетке, т.к. это ведет к улучшению приверженности больного к лечению, а значит, улучшает контроль АД [73, 74]. Имевшая место ранее невозможность изменения дозы одного из компонентов независимо от другого постепенно уходит в прошлое, т.к. появляется все больше комбинаций с различными дозами компонентов.
Заключение
В настоящей статье мы остановились лишь на небольшой части тех изменений, которые претерпели рекомендации по АГ. Тем не менее, прочтение данной статьи поможет сформировать первое впечатление о новых рекомендациях и несколько упростить знакомство с полной версией, что необходимо, безусловно, всем специалистам, связанным с проблемой АГ.

Литература
1. European Society of Hypertension-European Society of Cardiology Guidelines Committee. 2003 European Society of Hypertension-European Society of Cardiology guidelines for the management of arterial hypertension // J. Hypertens. 2003. Vol. 21. P. 1011–1053.
2. Mancia G. De Backer G. Dominiczak A. et al. 2007 Guidelines for the management of arterial hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC).
3. Mancia G. Laurent S. Agabiti-Rosei E. et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document // Blood Pressure. 2009. Vol. 18(6). P. 308–347.
4. Cooper R.S. Using public health indicators to measure the success of hypertension control // Hypertension. 2007. Vol. 49. P. 773–774.
5. Wolf-Maier K. Cooper R.S. Banegas J.R. et al. Hypertension prevalence and blood pressure levels in 6 European countries, Canada and the United States // JAMA. 2003. Vol.289. P. p. 2363–2369.
6. Redon J. Olsen M.H. Cooper R.S. et al. Stroke mortality trends from 1990 to 2006 in 39 countries from Europe and Central Asia: implications for control of high blood pressure // Eur. Heart J. 2011. Vol. 32. P. 1424–1431.
7. Gaborieau V. Delarche N. Gosse P. Ambulatory blood pressure monitoring vs. self-measurement of blood pressure at home: correlation with target organ damage // J. Hypertens. 2008. Vol. 26. P. 1919–1927.
8. Bliziotis I.A. Destounis A. Stergiou G.S. Home vs. ambulatory and office blood pressure in predicting target organ damage in hypertension: a systematic review and meta-analysis // J. Hypertens. 2012. Vol. 30. P. 1289–1299.
9. Staessen J.A. TLFROECDdLPea. Predicting cardiovascular risk using conventional vs ambulatory blood pressure in older patients with systolic hypertension. Systolic Hypertension in Europe Trial Investigators // JAMA. 1999. Vol. 282. P. 539–546.
10. Clement D.L. De Buyzere M.L. De Bacquer D.A. et al. Office vs. Ambulatory Pressure Study Investigators. Prognostic value of ambulatory blood-pressure recordings in patients with treated hypertension. // N. Engl. J. Med. 2003. Vol. 348. P. 2407–2415.
11. Dolan E. Stanton A. Thijs L. et al. Superiority of ambulatory over clinic blood pressure measurement in predicting mortality: the Dublin outcome study // Hypertension. 2005. Vol. 46. P. p. 156–161.
12. Sega R. Facchetti R. Bombelli M. et al. Prognostic value of ambulatory and home blood pressures compared with office blood pressure in the general population: follow-up results from the Pressioni Arteriose Monitorate e Loro Associazioni (PAMELA) study. Circulation. 2005. Vol.111. P. 1777–1783.
13. Boggia J. Li Y. Thijs L. et al. Prognostic accuracy of day vs. night ambulatory blood pressure: a cohort study // Lancet. 2007. Vol. 370. P. 1219–1229.
14. Fagard R.H. Celis H. Thijs L. et al. Daytime and night-time blood pressure as predictors of death and cause-specific cardiovascular events in hypertension // Hypertension. 2008. Vol. 51). P. 55–61.
15. Fagard R.H. Thijs L. Staessen J.A. et al. Prognostic significance of ambulatory blood pressure in hypertensive patients with history of cardiovascular disease // Blood Press. Monit. 2008. Vol. 13. P. 325–332.
16. Minutolo R. Agarwal R. Borrelli S. et al. Prognostic role of ambulatory blood pressure measurement in patients with nondialysis chronic kidney disease // Arch. Intern. Med. 2011. Vol. 171. P. 1090–1098.
17. de la Sierra A. Banegas J.R. Segura J. et al. Ambulatory blood pressure monitoring and development of cardiovascular events in high-risk patients included in the Spanish ABPM registry: the CARDIORISC Event study // J. Hypertens. 2012. Vol. 30. P. 713–719.
18. Hansen T.W. Li Y. Boggia J. et al. Predictive role of the night-time blood pressure // Hypertension. 2011. Vol. 57. P. 3–10.
19. Fagard R.H. Thijs L. Staessen J.A. et al. Night-day blood pressure ratio and dipping pattern as predictors of death and cardiovascular events in hypertension // J. Hum. Hypertens. 2009. Vol. 23. P. 645–653.
20. Parati G. Stergiou G.S. Asmar R. et al. European Society of Hypertension practice guidelines for home blood pressure monitoring // J. Hum. Hypertens. 2010. Vol. 24. P. 779–785. J Hum Hypertens. 2010. Vol. 24. P. 779–785.
21. Parati G. Stergiou G.S. Asmar R. et al. European Societyof Hypertension Working Groupon Blood Pressure Monitoring. European Society of Hypertension guidelines for blood pressure monitoring at home: a summary report of the Second International Consensus Conference on Home Blood Pressure Monitoring // J. Hypertens. 2008. Vol. 26. P. 1505–1526.
22. Parati G. Omboni S. Role of home blood pressure telemonitoring in hypertension management: an update // Blood Press. Monit. 2010. Vol. 15. P. 285–295.
23. Stergiou G.S. Nasothimiou E.G. Hypertension: Does home telemonitoring improve hypertension management? // Nature Rev. Nephrol. 2011. Vol. 7. P. 493–495.
24. Kikuya M. Ohkubo T. Metoki H. et al. Day-by-day variability of blood pressure and heart rate at home as a novel predictor of prognosis: the Ohasama study // Hypertension. 2008. Vol. 52. P. 1045–1050.
25. Stergiou G.S. Bliziotis .IA. Home blood pressure monitoring in the diagnosis and treatment of hypertension: a systematic review // Am. J. Hypertens. 2011. Vol. 24. P. 123–134.
26. Fagard R.H. Van Den Broeke C. De Cort P. Prognostic significance of blood pressure measured in the office, at home and during ambulatory monitoring in older patients in general practice // J. Hum. Hypertens. 2005. Vol. 19. P. 801–807.
27. Mancia G. Facchetti R. Bombelli M. et al. Long-term risk of mortality associated with selective and combined elevation in office, home and ambulatory blood pressure // Hypertension. 2006. Vol. 47. P. 846–853.
28. Hodgkinson J. Mant J. Martin U. et al. Relative effectiveness of clinic and home blood pressure monitoring compared with ambulatory blood pressure monitoring in diagnosis of hypertension: systematic review // BMJ. 2011. Vol. 342. P.d3621.
29. Fagard R.H. Cornelissen V.A. Incidence of cardiovascular events in white-coat, masked and sustained hypertension vs. true normotension: a meta-analysis // J. Hypertens. 2007. Vol 25.P. 2193–2198.
30. Pierdomenico S.D. Cuccurullo F. Prognostic value of white-coat and masked hypertension diagnosed by ambulatory monitoring in initially untreated subjects: an updated meta analysis // Am. Hypertens. 2011. Vol. 24. P. 52–58.
31. Franklin S.S. Thijs L. Hansen T.W. et al. Significance of white-coat hypertension in older persons with isolated systolic hypertension: a meta-analysis using the International Database on Ambulatory Blood Pressure Monitoring in Relation to Cardiovascular Outcomes population // Hypertension. 2012. Vol. 59. P. 564–571.
32. Bobrie G. Clerson P. Menard J. et al. Masked hypertension: a systematic review // J. Hypertens. 2008. Vol. 26. P.1715–1725.
33. O’Rourke M.F. Adji A. Guidelines on guidelines: focus on isolated systolic hyprtension in youth // J. Hypertens. 2013. Vol. 31. P. 649–654.
34. Zanchetti A. Grassi G. Mancia G. When should antihypertensive drug treatment be initiated and to what levels should systolic blood pressure be lowered? A critical re-appraisal // J. Hypertens. 2009. Vol. 27. P. 923–934.
35. Medical Research Council Working Party. MRC trial on treatment of mild hypertension: principal results // Br. Med. J. 1985. Vol. 291. P. 97–104.
36. Liu L. Zhang Y. Liu G. et al. The Felodipine Event Reduction (FEVER) Study: a randomized long-term placebocontrolled trial in Chinese hypertensive patients // J. Hypertens. 2005. Vol. 23. P. 2157–2172.
37. Zhang Y, Zhang X, Liu L, Zanchetti A. Is a systolic blood pressure target >
38. Heart Outcomes Prevention Evaluation Study Investigators. Effects of ramipril on cardiovascular and microvascular outcomes in people with diabetes mellitus: results of the HOPE study and MICRO-HOPE sub-study // Lancet. 2000. Vol. 355. P. 253–259.
39. ADVANCE Collaborative Group. Effects of a fixed combination of perindopriland indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial // Lancet. 2007. Vol. 370. P. 829–840.
40. PROGRESS Collaborative Group. Randomised trial of a perindopril based blood-pressure-lowering regimen among 6105 individuals with previous stroke or transient ischaemic attack // Lancet. 2001. Vol. 358. P. 1033–1041.
41. Yusuf S. Diener H.C. Sacco R.L. et al. Telmisartan to prevent recurrent stroke and cardiovascular events // N. Eng. J. Med. 2008. Vol. 359. P. 1225–1237.
42. Arguedas J.A. Perez M.I. Wright J.M. Treatment blood pressure targets for hypertension // Cochrane Database Syst. Rev. 2009. CD004349.
43. Upadhyay A. Earley A. Haynes S.M. Uhlig K. Systematic review: blood pressure target in chronic kidney disease and proteinuria as an effect modifier // Ann. Intern. Med. 2011. Vol.154. P. 541–548.
44. UK Prospective Diabetes Study Group. Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38 // Br. Med. J. 1998. Vol. 317. P. 703–713.
45. Beckett N.S. Peters R. Fletcher A.E. et al. Treatment of hypertension in patients 80 years of age or older // N. Eng. J. Med. 2008. Vol. 358. P. 1887–1898.
46. Zanchetti A. Mancia G. Longing for clinical excellence: a critical outlook into the NICE recommendations on hypertension management: is nice always good? // J. Hypertens. 2012. Vol. 30).P. 660–668.
47. Mancia G. Parati G. Bilo G. et al. Ambulatory Blood Pressure Values in the Ongoing Telmisartan Alone and in Combination with Ramipril Global Endpoint Trial (ONTARGET) // Hypertension. 2012. Vol. 60. P. 1400–1406.
48. Law M.R. Morris J.K. Wald N.J. Use of blood pressure lowering drugs in the prevention of cardiovascular disease: meta-analysis of 147 randomised trials in the context of expectations from prospective epidemiological studies // BMJ. 2009. Vol. 338. P. b1665.
49. Blood Pressure Lowering Treatment Trialists’ Collaboration. Effects of different blood pressure-lowering regimens on major cardiovascular events in individuals with and without diabetes mellitus: results of prospectively designed overviews of randomized trials // Arch. Intern. Med. 2005. Vol. 165. P. 1410–1419.
50. Blood Pressure Lowering Treatment Trialists’ Collaboration. Effects of different blood-pressure-lowering regimens on major cardiovascular events: results of prospectively- designed overviews ofrandomised trials // Lancet. 2003. Vol. 362. P. 1527–1535.
51. Wald D.S. Law M. Morris J.K. et al. Combination therapy vs. monotherapy in reducing blood pressure: meta-analysis on 11 000 participants from 42 trials // Am. J. Med. 2009. Vol. 122. P. 290–300.
52. Corrao G. Parodi A. Zambon A. et al. Reduced discontinuation of antihypertensive treatment by two-drug combination as first step. Evidence from daily life practice // J. Hypertens. 2010. Vol. 28. P. 1584–1590.
53. Jamerson K. Weber M.A. Bakris G.L. et al. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high-risk patients // N. Eng. J. Med. 2008. Vol. 359. P. 2417–2428.
54. ALLHAT officers and co-ordinators for the ALLHAT Collaborative Research Group. Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT) // JAMA. 2002. Vol. 288. P. 2981–2997.
55. SHEP Co-operative Research Group. Prevention of stroke by antihypertensive drug treatment in older persons with isolated systolic hypertension. Final results of the Systolic Hypertension in the Elderly Program (SHEP) // JAMA. 1991. Vol. 265. P. 3255–2364.
56. Lithell H. Hansson L. Skoog I. et al. The Study on Cognition and Prognosis in the Elderly (SCOPE): principal results of a randomized double-blind intervention trial // J. Hypertens. 2003. Vol. 21. P. 875–886.
57. Staessen J.A. Fagard R. Thijs L. et al. Randomised double-blind comparison of placebo and active treatment for older patients with isolated systolic hypertension. The Systolic Hypertension in Europe (Syst-Eur) Trial Investigators // Lancet. 1997. Vol. 350. P. 757–764.
58. Liu L. Wang J.G. Gong L. et al. Comparison of active treatment and placebo in older Chinese patients with isolated systolic hypertension. Systolic Hypertension in China (Syst-China) Collaborative Group // J. Hypertens. 1998. Vol. 16. P. 1823–1829.
59. Coope J. Warrender T.S. Randomised trial of treatment of hypertension in elderly patients in primary care // BMJ. 1986. Vol. 293. P. 1145–1151.
60. Dahlof B. Lindholm L.H. Hansson L. et al. Morbidity and mortality in the Swedish Trial in Old Patients with Hypertension (STOP-Hypertension) // Lancet. 1991. Vol. 338. P. 1281–1285.
61. Zanchetti A. Bond M.G. Hennig M. et al. Calcium antagonist lacidipine slows down progression of asymptomatic carotid atherosclerosis: principal results of the European Lacidipine Study on Atherosclerosis (ELSA), a randomized, double-blind, long-term trial // Circulation. 2002. Vol. 106. P. 2422–2427.
62. Blood Pressure Lowering Treatment Trialists’ Collaboration. Do men and women respond differently to blood pressure-lowering treatment? Results of prospectively designed overviews of randomized trials // Eur. Heart J. 2008. Vol. 29. P. 2669–2680.
63. Hansson L. Lindholm L.H. Niskanen L. et al. Effect of angiotensin-converting-enzyme inhibition compared with conventional therapy on cardiovascular morbidity and mortality in hypertension: the Captopril Prevention Project (CAPPP) randomized trial // Lancet. 1999. Vol. 353. P. 611–616.
64. Julius S. Kjeldsen S.E. Weber M. et al. VALUE trial group. Outcomes inhypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial // Lancet. 2004. Vol. 363. P. 2022–2031.
65. Black H.R. Elliott W.J. Grandits G. et al. CONVINCE Trial group. Principal results of the Controlled Onset Verapamil Investigation of Cardiovascular End Points (CONVINCE) trial // JAMA. 2003. Vol. 289. P. 2073–2082.
66. Pepine C.J. Handberg E.M. Cooper-De Hoff R.M. et al. INVEST investigators. A calcium antagonist vs a noncalcium antagonist hypertension treatment strategy for patients with coronary artery disease. The International Verapamil-Trandolapril Study (INVEST): a randomized controlled trial // JAMA. 2003. Vol. 290. P. 2805–2816.
67. Hansson L. Lindholm L.H. Ekbom T. et al. Randomised trial of old and new antihypertensive drugs in elderly patients: cardiovascular mortality and morbidity the Swedish Trial in Old Patients with Hypertension-2 study // Lancet. 1999. Vol. 354. P. 1751–1756.
68. Hansson L. Hedner T. Lund-Johansen P. et al. Randomised trial of effects of calcium antagonists compared with diuretics and beta-blockers on cardiovascular morbidity and mortality in hypertension: the Nordic Diltiazem (NORDIL) study // Lancet. 2000. Vol. 356. P. 359–365.
69. Dalhof B. Sever P.S. Poulter N.R. et al. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindoprilas required vs. atenolol adding bendroflumethiazide as required in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA) // Lancet. 2005. Vol. 366. P. 895–906.
70. Dahlof B. Devereux R.B. Kjeldsen S.E. et al. LIFE Study Group. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomised trial against atenolol // Lancet. 2002. Vol. 359. P. 995–1003.
71. Williams B. Lacy P.S. Thom S.M. et al. Differential impact of blood pressure-lowering drugs on central aortic pressure and clinical outcomes: principal results of the Conduit Artery Function Evaluation (CAFE) study // Circulation. 2006. Vol. 113. P. 1213–1225.
72. Parving H.H. Brenner B.M. McMurray J.J.V. et al. Cardiorenal endpoints in a trial of aliskiren for type 2 diabetes // N. Eng. J. Med. 2012. Vol. 367. P. 2204–2213.
73. Gupta A.K. Arshad S. Poulter N.R. Compliance, safety and effectiveness of fixed-dose combinations of antihypertensive agents: a metaanalysis // Hypertension. 2010. Vol. 55. P. 399–407.
74. Claxton A.J. Cramer J. Pierce C. A systematic review of the association between dose regimens and medication compliance // Clin. Ther. 2001. Vol. 23. P. 1296–1310.
Новые рекомендации по артериальной гипертензии РМОАГ/ВНОК 2010 г. вопросы комбинированной терапии
Карпов Ю.А.
Артериальная гипертония (АГ), будучи одним из основных независимых факторов риска развития инсульта и ишемической болезни сердца (ИБС), а также сердечно–сосудистых осложнений – инфаркта миокарда (ИМ) и сердечной недостаточности, – относится к чрезвычайно важным проблемам здравоохранения большинства стран мира. Для успешной борьбы с таким распространенным и опасным заболеванием необходима хорошо продуманная и организованная программа по выявлению и лечению. Такой программой безусловно стали рекомендации по АГ, которые регулярно, по мере появления новых данных, пересматриваются [1–3]. Со времени выхода в 2008 г. третьей версии Российских рекомендаций по профилактике, диагностике и лечению АГ были получены новые данные, требующие пересмотра этого документа [1]. В связи с этим по инициативе Российского медицинского общества по АГ (РМОАГ) и Всероссийского научного общества кардиологов (ВНОК) недавно была разработана новая. четвертая версия этого важнейшего документа, которая прошла детальное обсуждение и в сентябре 2010 г. представлена на ежегодном Конгрессе ВНОК [4].
В основу настоящего документа легли рекомендации по лечению АГ Европейского общества по артериальной гипертонии (ЕОГ) и Европейского общества кардиологов (ЕОК) 2007 и 2009 гг. [2,3] и результаты крупных Российских исследований по проблеме АГ. Так же как и в предшествующих версиях рекомендаций. величина АД рассматривается как один из элементов системы стратификации общего (суммарного) сердечно–сосудистого риска. При оценке общего сердечно–сосудистого риска учитывается большое количество переменных, но величина АД является определяющей в силу своей высокой прогностической значимости. При этом уровень АД является наиболее регулируемой переменной в системе стратификации. Как показывает опыт, эффективность действий врача при лечении каждого конкретного пациента и достижение успехов по контролю АД среди населения страны в целом в значительной степени зависят от согласованности действий и терапевтов. и кардиологов, что обеспечивается единым диагностическим и лечебным подходом. Именно эта задача рассматривалась в качестве основной при подготовке рекомендаций .
Целевой уровень АД
Интенсивность лечения больного АГ во многом определяется поставленной целью в плане снижения и достижения определенного уровня АД. При лечении больных АГ величина АД должна быть менее 140/90 мм рт.ст. что является ее целевым уровнем. При хорошей переносимости назначенной терапии целесообразно снижение АД до более низких значений. У пациентов с высоким и очень высоким риском сердечно–сосудистых осложнений необходимо снизить АД до 140/90 мм рт.ст. и менее в течение 4 нед. В дальнейшем, при условии хорошей переносимости рекомендуется снижение АД до 130–139/80–89 мм рт.ст. При проведении антигипертензивной терапии следует иметь в виду, что бывает трудно достичь уровня систолического АД менее 140 мм рт.ст. у пациентов, больных сахарным диабетом, поражением органов–мишеней, у пожилых больных и уже имеющих сердечно–сосудистые осложнения. Достижение более низкого целевого уровня АД возможно только при хорошей переносимости и может занимать больше времени, чем его снижение до величины менее 140/90 мм рт.ст. При плохой переносимости снижения АД рекомендуется его снижение в несколько этапов. На каждой ступени АД снижается на 10–15% от исходного уровня за 2–4 нед. с последующим перерывом для адаптации пациента к более низким величинам АД. Следующий этап снижения АД и, соответственно, усиление антигипертензивной терапии в виде увеличения доз или количества принимаемых препаратов возможно только при условии хорошей переносимости уже достигнутых величин АД. Если переход на следующий этап вызывает ухудшение состояния пациента, целесообразно вернуться на предыдущий уровень еще на некоторое время. Таким образом, снижение АД до целевого уровня происходит в несколько этапов, число которых индивидуально и зависит как от исходного уровня АД, так и от переносимости антигипертензивной терапии. Использование этапной схемы снижения АД с учетом индивидуальной переносимости, особенно у пациентов с высоким и очень высоким риском осложнений, позволяет достичь целевого уровня АД и избежать эпизодов гипотонии, с которыми связано увеличение риска развития ИМ и мозгового инсульта. При достижении целевого уровня АД необходимо учитывать нижнюю границу снижения систолического АД до 110–115 мм рт.ст. и диастолического АД до 70–75 мм рт.ст. а также следить за тем, чтобы в процессе лечения не происходило увеличения пульсового АД у пожилых пациентов, что возникает главным образом за счет снижения диастолического АД.
Эксперты все классы антигипертензивных препаратов разделили на основные и дополнительные (табл. 1). В рекомендациях отмечается, что все основные классы антигипертензивных препаратов (ингибиторы АПФ, блокаторы ангиотензиновых рецепторов, диуретики, антагонисты кальция, b–блокаторы) одинаково снижают АД; у каждого препарата есть доказанные эффекты и свои противопоказания в определенных клинических ситуациях; у большинства пациентов с АГ эффективный контроль АД может быть достигнут только при комбинированной терапии, а у 15–20% больных контроль АД не может быть достигнут двухкомпонентной комбинацией; предпочтительны к назначению фиксированные комбинации антигипертензивных препаратов.
Недостатки ведения больных АГ обычно ассоциируются с недостаточным лечением из–за неправильного выбора препарата или дозы, отсутствия синергизма действия при использовании комбинации препаратов и проблем, связанных с приверженностью лечению. Показано, что комбинации препаратов всегда имеют преимущества в сравнении с монотерапией в снижении АД.
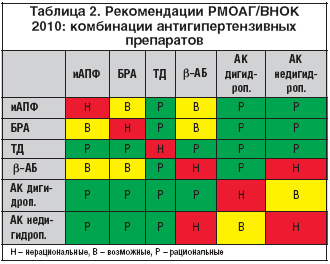
Назначение комбинаций антигипертензивных препаратов может решить все эти проблемы, и поэтому их применение рекомендуется авторитетными экспертами в плане оптимизации лечения АГ. В последнее время было показано, что некоторые комбинации препаратов не только имеют преимущества в осуществлении контроля за уровнем АД, но и улучшают прогноз у лиц с установленной АГ, которая сочетается с другими заболеваниями или нет. Поскольку у врача имеется огромный выбор различных антигипертензивных комбинаций (табл. 2.), то основная проблема состоит в выборе наилучшей комбинации с наибольшими доказательствами для оптимального лечения больных АГ.
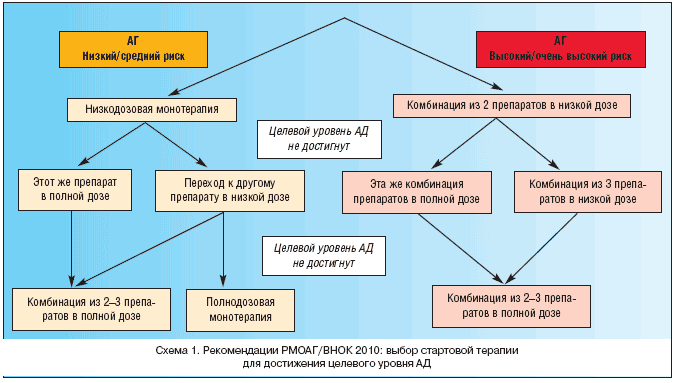
В разделе «Медикаментозная терапия» подчеркивается, что у всех больных АГ необходимо добиваться постепенного снижения АД до целевых уровней. Особенно осторожно следует снижать АД у пожилых и у больных, перенесших ИМ и мозговой инсульт. Количество назначаемых препаратов зависит от исходного уровня АД и сопутствующих заболеваний. Например, при АГ 1–й степени и отсутствии высокого риска осложнений возможно достижение целевого АД на фоне монотерапии примерно у 50% больных. При АГ 2–й и 3–й степени и наличии факторов высокого риска в большинстве случаев может потребоваться комбинация из двух или трех препаратов. В настоящее время возможно использование двух стратегий стартовой терапии АГ: монотерапии и низкодозовой комбинированной терапии с последующим увеличением количества и/или доз лекарственного средства при необходимости (схема 1). Монотерапия на старте лечения может быть выбрана для пациентов с низким или средним риском. Комбинация двух препаратов в низких дозах должна быть предпочтительна у больных с высоким или очень высоким риском осложнений. Монотерапия базируется на поиске оптимального для больного препарата; переход на комбинированную терапию целесообразен только в случае отсутствия эффекта последней. Низкодозовая комбинированная терапия на старте лечения предусматривает подбор эффективной комбинации препаратов с различными механизмами действия.
Каждый из этих подходов имеет свои преимущества и недостатки. Преимущество низкодозовой монотерапии состоит в том, что в случае удачного подбора лекарства больной не будет принимать еще один препарат. Однако стратегия монотерапии требует от врача кропотливого поиска оптимального для больного антигипертензивного средства с частой сменой лекарств и их дозировок, что лишает врача и больного уверенности в успехе и в конечном счете ведет к снижению приверженности пациентов к лечению. Это особенно актуально для больных АГ 1–й и 2–й степени, большинство из которых не испытывают дискомфорта от повышения АД и не мотивированы к лечению.
При комбинированной терапии в большинстве случаев назначение препаратов с различными механизмами действия позволяет, с одной стороны, добиться целевого АД, а с другой – минимизировать количество побочных эффектов. Комбинированная терапия позволяет также подавить контррегуляторные механизмы повышения АД. Применение фиксированных комбинаций антигипертензивных препаратов в одной таблетке повышает приверженность больных к лечению. Пациентам с АД ≥ 160/100 мм рт.ст. имеющим высокий и очень высокий риск, полнодозовая комбинированная терапия может быть назначена на старте лечения. У 15–20% пациентов контроль АД не может быть достигнут при использовании двух препаратов. В этом случае используется комбинация из трех и более лекарственных средств.
Как уже отмечалось ранее, наряду с монотерапией для контроля АД используются комбинации из двух, трех и более антигипертензивных препаратов. Комбинированная терапия имеет много преимуществ: усиление антигипертензивного эффекта за счет разнонаправленного действия препаратов на патогенетические механизмы развития АГ, что увеличивает число пациентов со стабильным снижением АД; уменьшение частоты возникновения побочных эффектов, как за счет меньших доз комбинируемых антигипертензивных препаратов, так и за счет взаимной нейтрализации этих эффектов; обеспечение наиболее эффективной органопротекции и уменьшение риска и числа сердечно–сосудистых осложнений. Однако необходимо помнить, что комбинированная терапия – это прием как минимум двух лекарственных препаратов, кратность назначения которых может быть различной. Следовательно, применение препаратов в виде комбинированной терапии должно отвечать следующим условиям: препараты должны иметь взаимодополняющее действие; должно достигаться улучшение результата при их совместном применении; препараты должны иметь близкие фармакодинамические и фармакокинетические показатели, что особенно важно для фиксированных комбинаций.
Приоритет рациональных комбинаций антигипертензивных препаратов
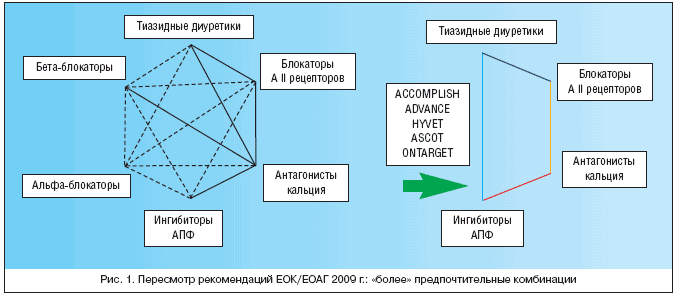
Эксперты РМОАГ предлагают разделить комбинации двух антигипертензивных препаратов на рациональные (эффективные), возможные и нерациональные. Американские эксперты, которые в 2010 г. представили новый алгоритм комбинированной антигипертензивной терапии (табл. 3), занимают в этом вопросе практически такие же позиции [5]. Эта позиция полностью совпадает с мнением европейских экспертов по АГ, высказанным в ноябре 2009 г. по вопросам комбинированной терапии [3] и представленным на рисунке 1.
В Российских рекомендациях подчеркивается, что в полной мере преимущества комбинированной терапии присущи только рациональным комбинациям антигипертензивных препаратов (табл. 2). Среди многих рациональных комбинаций заслуживают особого внимания некоторые, имеющие преимущества не только с теоретических позиций основного механизма действия, но и практически доказанной высокой антигипертензивной эффективности. В первую очередь эта комбинация ингибитора АПФ с диуретиком, при которой усиливаются преимущества и нивелируются недостатки. Данная комбинация является наиболее популярной в терапии АГ благодаря высокой гипотензивной эффективности, защите органов–мишеней, хорошей безопасности и переносимости. В опубликованных рекомендациях Американского общества АГ (ASH) по комбинированной терапии АГ (табл. 3) также приоритет (более предпочтительные) отдается комбинации препаратов, блокирующих активность ренин–ангиотензиновой системы (блокаторы ангиотензиновых рецепторов или ингибиторы АПФ) с диуретиками или с антагонистами кальция [5].
Препараты потенцируют действие друг друга за счет взаимодополняющего влияния на основные звенья регуляции АД и блокады контррегуляторных механизмов. Снижение объема циркулирующей жидкости вследствие салуретического действия диуретиков приводит к стимуляции ренин–ангиотензиновой системы (РАС), чему противодействует ингибитор АПФ. У пациентов с низкой активностью ренина плазмы ингибиторы АПФ обычно недостаточно эффективны, и добавление диуретика, приводящего к повышению активности РАС, позволяет ингибитору АПФ реализовать свое действие. Это расширяет круг больных, отвечающих на терапию, и целевые уровни АД достигаются более чем у 80% пациентов. Ингибиторы АПФ предотвращают гипокалиемию и уменьшают негативное влияние диуретиков на углеводный, липидный и пуриновый обмен.
Ингибиторы АПФ широко используются в лечении больных АГ, острых форм ИБС, хронической сердечной недостаточности. Один из представителей большой группы ингибиторов АПФ – лизиноприл. Препарат был детально изучен в нескольких крупномасштабных клинических исследованиях. Лизиноприл продемонстрировал профилактическую и терапевтическую эффективность при сердечной недостаточности, в том числе после острого ИМ, и при сопутствующем сахарном диабете (исследования GISSI 3, ATLAS, CALM, IMPRESS). В самом крупном клиническом исследовании по лечению АГ различными классами препаратов ALLHAT среди принимавших лизиноприл достоверно снизилась заболеваемость СД 2–го типа [6].
В российском фармакоэпидемиологическом исследовании ПИФАГОР III [7] изучались предпочтения практических врачей в выборе антигипертензивной терапии. Результаты были сопоставлены с предшествующим этапом исследования ПИФАГОР I в 2002 г. [8]. По данным этого опроса врачей, структура антигипертензивных препаратов, которые назначаются пациентам с АГ в реальной практике, представлена пятью основными классами: ингибиторами АПФ (25%), β –адреноблокаторами (23%), диуретиками (22%), антагонистами кальция (18%) и блокаторами ангиотензиновых рецепторов. В сравнении с результатами исследования ПИФАГОР I наблюдается уменьшение доли ингибиторов АПФ на 22% и β –блокаторов на 16%, увеличение доли антагонистов кальция на 20% и почти 5–кратное увеличение доли блокаторов рецепторов ангиотензина II.
В структуре препаратов класса ингибиторов АПФ наибольшие доли имеют эналаприл (21%), лизиноприл (19%), периндоприл (17%), фозиноприл (15%) и рамиприл (10%). Вместе с тем в последние годы наблюдается тенденция к повышению значимости и частоты применения комбинированной антигипертензивной терапии для достижения целевого уровня у пациентов с АГ. По данным исследования ПИФАГОР III в сравнении с 2002 г. подавляющее большинство (около 70%) врачей предпочитают использовать комбинированную терапию в виде свободных (69%), фиксированных (43%) и низкодозовых комбинаций (29%) и только 28% продолжают применять тактику монотерапии. Среди комбинаций антигипертензивных препаратов 90% врачей предпочитают назначение ингибиторов АПФ с диуретиком, 52% – β –блокаторов с диуретиком, 50% врачей назначают не содержащие диуретики комбинации (антагонисты кальция с ингибиторами АПФ или β –блокаторами).
Одной из наиболее оптимальных комбинаций ингибитора АПФ и диуретика является препарат «Ко–Диротон»® (Gedeon Richter) – комбинация лизиноприла (10 и 20 мг) и гидрохлоротиазида (12,5 мг), составные части которого имеют хорошую доказательную базу. «Ко–Диротон» может использоваться при наличии у больного АГ хронической сердечной недостаточности, выраженной гипертрофии левого желудочка, метаболического синдрома, избыточной массы тела, сахарного диабета. Оправданно применение «Ко–Диротона» при рефрактерной гипертонии, а также при тенденции к увеличению числа сердечных сокращений.
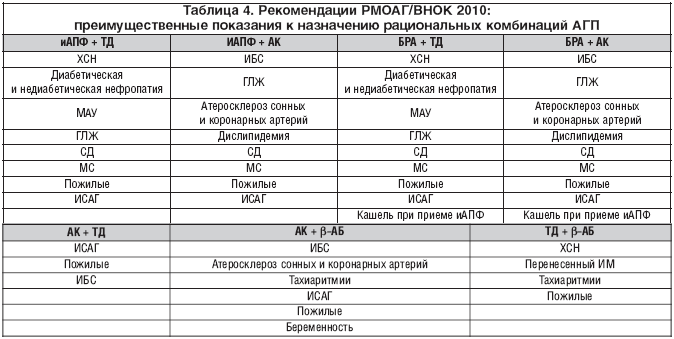
С учетом растущего интереса врачей к применению комбинированной терапии эксперты РМОАГ впервые представили таблицу, в которой указаны преимущественные показания к назначению рациональных комбинаций (табл. 4).
Новый лидер
комбинированной терапии
Комбинация антагониста кальция и ингибитора АПФ в последние годы приобретает все большую популярность, увеличивается число клинических испытаний и появление новых комбинированных лекарственных форм. Антагонист кальция амлодипин был изучен во многих клинических проектах. Препарат эффективно контролирует АД и относится к числу наиболее изученных антагонистов кальция в различных клинических ситуациях. Наряду с оценкой АД–снижающих эффектов активно изучались сосудопротективные и антиатеросклеротические свойства этого антагониста кальция. Были проведены два исследования PREVENT [9] и CAMELOT [10] с применением методов, визуализирующих сосудистую стенку, у больных ИБС, в которых оценивалось влияние амлодипина на развитие атеросклероза. По результатам этих и других контролируемых исследований эксперты Европейского общества АГ/Европейского общества кардиологов внесли в рекомендации наличие атеросклероза сонных и коронарных артерий у больных с АГ в качестве одного из показаний для первоочередного назначения антагонистов кальция [2]. Доказанные антиишемические и антиатеросклеротические свойства амлодипина позволяют его рекомендовать для контроля за АД у больных АГ в сочетании с ИБС.
С точки зрения снижения риска развития сердечно–сосудистых осложнений и улучшения прогноза при АГ (основная цель в лечении этого заболевания) этот препарат продемонстрировал большой протективный потенциал в таких сравнительных исследованиях, как ALLHAT, VALUE, ASCOT, ACCOMPLISH [6,11–13].
Клиническая практика и результаты нескольких клинических исследований дают веские аргументы в пользу такой комбинации. Наиболее важными в этом плане стали данные таких исследований, как ASCOT [12], в котором большинство больных получали свободную комбинацию антагониста кальция и ингибитора АПФ; недавний post–hoc–анализ исследования EUROPA [14]; новый анализ исследования ACTION [15] и особенно исследование ACCOMPLISH [13]. В этом проекте сравнивалось влияние двух режимов исходно комбинированной терапии на частоту сердечно–сосудистых осложнений у 10 700 больных с АГ высокого риска (у 60% больных имеется сахарный диабет, у 46% – ИБС, у 13% – инсульт в анамнезе, средний возраст 68 лет, среднее значение индекса массы тела 31 кг/м2) – ингибитора АПФ беназеприла с амлодипином либо с тиазидным диуретиком гидрохлоротиазидом.
Вначале было показано, что при переводе больных на фиксированную комбинацию лекарственных препаратов существенно улучшился контроль АД, а через три года это исследование было прекращено досрочно, поскольку были получены четкие доказательства более высокой эффективности комбинации антагониста кальция с ингибитором АПФ [13]. При одинаковом контроле за АД в этой группе было достоверное снижение риска развития сердечно–сосудистых осложнений (первичная конечная точка) по сравнению с группой, получавших комбинацию ингибитора АПФ с диуретиком – на 20%. Результаты этого исследования свидетельствуют о том, что комбинация антагонистов кальция с ингибиторами АПФ имеет хорошие перспективы более широкого применения в клинической практике. Можно предполагать, что такая комбинация может быть особенно востребованной в лечении больных АГ в сочетании с ИБС.
Усиление АД–снижающего действия при использовании комбинации антагонистов кальция и ингибиторов АПФ сопровождается уменьшением частоты возникновения нежелательных реакций, в частности отеков голеней, характерных для дигидропиридиновых антагонистов кальция. Имеются данные о том, что кашель, ассоциированный с приемом ингибиторов АПФ, также ослабляется антагонистами кальция, включая амлодипин.
Фиксированные комбинации:
больше преимуществ
Для комбинированной терапии АГ могут использоваться как свободные, так и фиксированные комбинации препаратов. Эксперты РМОАГ рекомендуют практическим врачам в большинстве случаев отдавать предпочтение фиксированным комбинациям антигипертензивных препаратов, содержащим два лекарства в одной таблетке. Отказаться от назначения фиксированной комбинации АД–снижающих средств можно только при абсолютной невозможности ее использования в случае наличия противопоказаний к одному из компонентов. В документе отмечается, что фиксированная комбинация: всегда будет рациональной; является самой эффективной стратегией достижения и поддержания целевого уровня АД; обеспечивает лучшее органопротективное действие и уменьшение риска осложнений; позволяет сократить количество принимаемых таблеток, что существенно повышает приверженность пациентов лечению.
В уже упоминавшемся ранее исследовании ACCOMPLISH было впервые проведено сравнительное изучение эффективности фиксированных комбинаций [13]. Одна из первых фиксированных комбинаций в нашей стране – это препарат «Экватор» (в составе антагонист кальция амлодипин и ингибитор АПФ лизиноприл). Оба эти препарата имеют хорошую доказательную базу, включающую крупномасштабные клинические исследования. Клинические исследования продемонстрировали высокую антигипертензивную эффективность препарата «Экватор». Среди фиксированных комбинированных препаратов в исследовании ПИФАГОР III врачи назвали 32 торговых наименования, среди которых чаще всего отмечали комбинированные препараты ингибиторов АПФ и диуретиков, а также «Экватор» в 17% [7].
Эксперты считают, что назначение фиксированной комбинации двух антигипертензивных препаратов может быть первым шагом лечения пациентов с высоким сердечно–сосудистым риском или следовать сразу за монотерапией.
Роль других комбинаций
в лечении АГ
К возможным комбинациям антигипертензивных препаратов относятся сочетание дигидропиридинового и недигидропиридинового АК, ингибиторов АПФ + β –блокаторов, БРА + β –блокаторов, ингибиторов АПФ + БРА, прямого ингибитора ренина или α –адреноблокатора со всеми основными классами антигипертензивных препаратов. Применение этих комбинаций в виде двухкомпонентной антигипертензивной терапии в настоящее время не является абсолютно рекомендованным, но и не запрещено. Однако сделать выбор в пользу такого сочетания лекарственных средств допустимо только при полной уверенности в невозможности использования рациональных комбинаций. На практике больным АГ, имеющим ИБС и/или хроническую сердечную недостаточность, одновременно назначаются ингибиторы АПФ и β –блокаторы. Однако, как правило, в таких ситуациях назначение β –блокаторов происходит главным образом из–за наличия ИБС или сердечной недостаточности, т.е. по самостоятельному показанию (табл. 5).
К комбинациям нерациональным, при использовании которых не происходит потенцирования антигипертензивного эффекта препаратов и/или усиливаются побочные эффекты при их совместном применении, относятся: сочетания разных лекарственных средств, относящихся к одному классу антигипертензивных препаратов, β –блокаторы + недигидропиридиновый антагонист кальция, ингибитор АПФ + калийсберегающий диуретик, β –блокатор + препарат центрального действия.
Вопрос комбинирования трех и более препаратов еще не достаточно изучен, поскольку нет результатов рандомизированных контролируемых клинических исследований, изучавших тройную комбинацию антигипертензивных препаратов. Таким образом, антигипертензивные препараты в данных комбинациях объединены вместе на теоретической основе. Однако у многих пациентов, в том числе у больных с рефрактерной АГ, только с помощью трех и более компонентной антигипертензивной терапии можно достичь целевого уровня АД.
Заключение
В новых рекомендациях по лечению АГ РМОАГ/ВНОК особое внимание уделяют вопросам комбинированной терапии как важнейшего компонента успеха в предотвращении сердечно–сосудистых осложнений. По-вышенный интерес к комбинированной терапии АГ, многочисленные клинические исследования, а главное – их воодушевляющие результаты все отчетливее обозначают важную тенденцию в кардиологии: акцент на разработку многокомпонентных лекарственных форм. Среди фиксированных лекарственных форм эксперты выделяют комбинации препаратов, блокирующих активность РААС (ингибиторы АПФ и др.), с антагонистами кальция или диуретиками.



Литература
1. Российское медицинское общество по артериальной гипертонии (РМОАГ), Всероссийское научное общество кардиологов (ВНОК). Диагностика и лечение артериальной гипертензии. Российские рекомендации (третий пересмотр). Кардиоваскулярная терапия и профилактика 2008; № 6, приложение 2.
2. The Task Force for the management of arterial hypertension of the European Society of Hypertension and of the European Society of Cardiology. 2007 Guidelines for the management of arterial hypertension. J Hypertens 2007, 25: 1105–1187.
3. Российское медицинское общество по артериальной гипертонии (РМОАГ), Всероссийское научное общество кардиологов (ВНОК). Диагностика и лечение артериальной гипертензии. Российские рекомендации (четвертый пересмотр), 2010.
4. Mancia G. Laurent S. Agabiti–Rosei E. et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document. J Hypertension 2009; 27: 2121–2158.
5. Gradman A.H. Basile J.N. Carter B.L. et al. Combination therapy in hypertension. J Am Soc Hypertens 2010; 4: 42–50.
6. The ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. Major outcomes in high–risk hypertensive patients randomized to angiotensin–converting enzyme inhibitor or calcium channel blocker vs. diuretic: the Antihypertensive and Lipid Lowering treatment to prevent Heart Attack Trial (ALLHAT). JAMA, 2002; 288: 2981–97.
7. Леонова М.В. Белоусов Д.Ю. Штейнберг Л.Л. аналитическая группа исследования ПИФАГОР. Анализ врачебной практики проведения антигипертензивной терапии в России (по данным исследования ПИФАГОР III). Фарматека 2009, № 12: 98–103.
8. Леонова М.В. Белоусов Д.Ю. аналитическая группа исследования ПИФАГОР. Первое Российское фармакоэпидемиологическое исследование артериальной гипертонии. Качественная клиническая практика, 2002. № 3: 47–53.
9. Pitt B. Byington R.P. Furberg C.D. et al. Effect of amlodipine on the progression of atherosclerosis and the occurrence of clinical events. PREVENT Investigators. Circulation 2000, 102: 1503–1510.
10. Nissen S.E. Tuzcu E.M. Libby P. et al. Effect of antihypertensive agents on cardiovascular events in patients with coronary disease and normal blood pressure: the CAMELOT study: a randomized controlled trial. JAMA, 2004; 292: 2217–2225.
11. Julius S. Kjeldsen S.E. Weber M. et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipin: the VALUE randomised trial. Lancet, 2004; 363: 2021–2031.
12. Dahlof B. Sever P.S. Poulter N.R. et al. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo–Scandinavian Cardiac Outcomes Trial–Blood Pressure Lowering Arm (ASCOT–BPLA): a multicentre randomised controlled trial. Lancet 2005, 366: 895–906.
13. Jamerson K.A. Weber M.A. Bakris G.L. et al. on behalf of the ACCOMPLISH investigators. Benazepril plus amlodipine or hydrochlorotiazide for hypertension in high–risk patients. N Engl J Med, 2008; 359: 2417–2428.
14. Bertrand M.E. Ferrari R. Remme W.J. et al. Clinical synergy of perindopril and calcium–channel blocker in the prevention of cardiac events and mortality in patients with coronary artery disease. Post hoc analysis of the EUROPA study. Am Heart J, 2010; 159: 795–802.
15. Elliott H.L. Meredith P.A. Preferential benefits of nifedipine GITS in systolic hypertension and in combination with RAS blockade: further analysis of the `ACTION` database in patients with angina. J Human Hypertension, 25 Feb. 2010; doi:10.1038 / jhh.2010.19.
Novel Russian Recommendations on Arterial Hypertension – Priority for Combination Therapy (Russian Medical Society on Arterial Hypertension, Section of Evidence Based Hypertensiology)
С момента выхода в 2008 г. третьей версии Российских рекомендаций по артериальной гипертонии (АГ) были получены новые данные, обусловливающие необходимость пересмотра этого основного документа [1]. По инициативе Российского медицинского общества по АГ (РМОАГ) и Всероссийского научного общества кардиологов (ВНОК) были разработаны рекомендации, в основу которых легли положения, предложенные экспертами Европейского общества по артериальной гипертонии (ЕОАГ) и Европейского общества кардиологов (ЕОК) в 2009 г. а также результаты крупных российских исследований по проблеме АГ [2—4].
Как и ранее, основная цель лечения больных АГ заключается в максимальном снижении риска развития сердечно-сосудистых осложнений (ССО) и смерти от них. Для достижения этой цели требуются не только снижение АД до целевого уровня, но и коррекция всех модифицируемых факторов риска, предупреждение и замедление темпа прогрессирования и/или уменьшение поражения органов-мишеней, а также лечение ассоциированных и сопутствующих заболеваний — ишемической болезни сердца, сахарного диабета (СД) и т.д. При лечении больных АГ АД должно быть менее 140/90 мм рт.ст. что является его целевым уровнем.
Помимо монотерапии при лечении АГ используются комбинации из 2, 3 и более антигипертензивных препаратов. В последние годы в соответствии с международными и отечественными рекомендациями по лечению АГ наблюдается тенденция к повышению значимости и частоты применения комбинированной антигипертензивной терапии для достижения целевого уровня АД [2—4]. Комбинированная терапия имеет много преимуществ: усиление антигипертензивного эффекта за счет разнонаправленного действия препаратов на патогенетические звенья АГ, что увеличивает число пациентов со стабильным снижением АД. При комбинированной терапии в большинстве случаев назначение препаратов с различными механизмами действия позволяет, с одной стороны, добиться целевого уровня АД, а с другой, минимизировать число побочных эффектов. Комбинированная терапия позволяет также подавить контррегуляторные механизмы повышения АД. Применение фиксированных комбинаций антигипертензивных препаратов в одной таблетке повышает приверженность больных к лечению.
Комбинации 2 антигипертензивных препаратов делят на рациональные (эффективные), возможные и нерациональные. Все преимущества комбинированной терапии присущи только рациональным комбинациям антигипертензивных препаратов. К ним относятся ингибитор ангиотензинпревращающего фермента (АПФ) + диуретик; блокатор рецепторов ангиотензина II (БРА) + диуретик; ингибитор АПФ + антагонист кальция; БРА + АК; дигидропиридиновый антагонист кальция + β-адреноблокатор; антагонист кальция + диуретик; β-адреноблокатор + диуретик.
Одной из наиболее эффективных считается комбинация ингибиторов АПФ и диуретиков. Показания к применению этой комбинации — диабетическая и недиабетическая нефропатия; микроальбуминурия (МАУ); гипертрофия левого желудочка; СД; метаболический синдром (МС); пожилой возраст; изолированная систолическая АГ. Комбинация антигипертензивных препаратов этих классов является одной из наиболее часто назначаемых, одна из них — фиксированная комбинация периндоприла с индапамидом (нолипрел А и нолипрел А форте) по данным исследования ПИФАГОР — самая популярная среди врачей [5].
Новости комбинированной терапии АГ (фиксированные комбинации)
Ранее сообщалось о появлении новой соли периндоприла аргинина, получившей название «престариум А», вместо тертбутиламиновой соли [6]. Затем был предложен новый нолипрел А, в котором аргининовая соль периндоприла в дозе 2,5 и 5 мг представлена в комбинации с индапамидом 0,625 (нолипрел А) и 1,25 мг (нолипрел А форте) соответственно [7].
Эффективность нолипрела была изучена во многих международных и российских клинических исследованиях. Одно из них — российская программа СТРАТЕГИЯ (СравниТельная пРогрАмма по оценке эффекТивности нолипрЕла у пациентов с артериальной ГИпертензией с недостаточным контролем артериального давлениЯ). В этом исследовании изучалась эффективность фиксированной комбинации периндоприл/индапамид (нолипрела и нолипрела форте) у 1726 больных АГ с недостаточным контролем АД [8].
В ходе исследования OPTIMAX II изучалось влияние МС по критериям NCEP ATPIII на контроль АД у больных АГ, получающих нолипрел [9]. В это проспективное наблюдение длительностью 6 мес были включены 24 069 больных (56% мужчин, средний возраст 62 года, у 18% имелся СД, среднее АД при включении 162/93 мм рт.ст. МС у 30,4%). Частота нормализации АД составила от 64 до 70% в зависимости от режима назначения нолипрела форте — как начальная терапия, замена или дополнительная терапия, и не зависела от наличия МС.
Адекватный контроль за уровнем АД с помощью комбинированного препарата нолипрел А форте обеспечивает органопротекцию. В исследовании PICXEL было показано, что применение фиксированной комбинации нолипрела форте более эффективно уменьшает гипертрофию левого желудочка, чем монотерапия высокими дозами ингибитора АПФ эналаприла, и обеспечивает лучший контроль АД [10]. Это было первое исследование, в котором изучалось влияние на гипертрофированный миокард комбинированного препарата в качестве стартовой терапии.
По данным исследования PREMIER (Preterax in Albuminuria Regression), нолипрел форте в большей степени, чем эналаприл в высокой дозе 40 мг, уменьшал выраженность альбуминурии у больных СД 2-го типа и АГ, причем независимо от влияния на уровень АД [11]. В этом контролируемом исследовании принял участие 481 больной с СД 2-го типа, АГ и МАУ. Больные были рандомизированы в 2 группы, получавших либо комбинацию периндоприл 2 мг/индапамид 0,625 мг (увеличение до 8 мг и 2,5 мг соответственно), либо эналаприл 10 мг (увеличение до 40 мг при необходимости) в течение 12 мес.
Применение фиксированной комбинации нолипрел форте у больных СД 2-го типа в исследовании ADVANCE (Action in Diabetes and VAscular disease — preterax and Diamicron MR Controlled Evaluation) значительно снизило риск развития основных ССО, включая смерть [12]. В исследование были включены 11 140 больных с СД 2-го типа и высоким риском развития осложнений. В ходе длительного наблюдения (в среднем 4,3 года) относительный риск развития основных макро- и микрососудистых осложнений (первичная конечная точка) достоверно снизился на 9% (р=0,04). Лечение нолипрелом у больных СД 2-го типа привело к достоверному снижению риска смерти от всех причин на 14% (р=0,03) и от сердечно-сосудистых причин на 18% (р=0,03). В группе активного лечения был достоверно ниже риск развития коронарных осложнений на 14% (р=0,02) и почечных осложнений на 21% (р 140 мм рт.ст. и/или диастолическое АД (ДАД) >95 мм рт.ст. Антигипертензивнная терапия при включении в программу была представлена β-адреноблокаторами, АК, ингибиторами АПФ (кроме престариума А), диуретиками (кроме арифона, арифона ретард), препаратами центрального действия, БРА в виде монотерапии или свободных комбинаций. К предшествующей антигипертензивной терапии всем включенным в исследование больным была назначена комбинация периндоприла аргинин/индапамид (нолипрел А форте 1 таблетка в сутки). Больным, ранее получавшим ингибиторы АПФ или диуретики с антигипертензивной целью, эти препараты заменяли нолипрелом А форте со следующего дня терапии. В дальнейшем через 4 нед терапии при уровне САД ≥130 мм рт.ст. и/или ДАД ≥80 мм рт.ст. дозу нолипрела А форте удваивали (2 таблетки в сутки).
Двенадцатинедельный период активного наблюдения завершили 2296 больных АГ с высоким и очень высоким риском развития ССО (31% мужчин и 69% женщин) в возрасте 57,1 года. Исходное клиническое АД составило 159,6/95,5 мм рт.ст. Через 4 нед отмечалось достоверное и клинически значимое снижение САД до 135 мм рт.ст. (р
HTML-код для размещения ссылки на сайте или в блоге: