Алгоритм лечения больных с ОКС

Этиология, патогенез, диагностические критерии острого им
Инфаркт миокарда- это некроз (гибель) сердечной мышцы, обусловленный острым нарушением коронарного кровообращения в результате несоответствия между потребностью сердечной мышцы в кислороде и его доставкой к сердцу. Остр им длится от 2 часов до 10 дней
Этиология
Инфаркт миокарда развивается в результате обтурации просвета сосуда кровоснабжающего миокард (коронарная артерия). Причинами могут стать (по частоте встречаемости):
Атеросклероз коронарных артерий (тромбоз, обтурация бляшкой) 93-98 %
Хирургическая обтурация (перевязка артерии или диссекция при ангиопластике)
Эмболизация коронарной артерии (тромбоз при коагулопатии, жировая эмболия т. д.)
Спазм коронарных артерий
Отдельно выделяют инфаркт при пороках сердца (аномальное отхождение коронарных артерий от легочного ствола) Обычно при инфаркте миокарда выявляются следующие признаки:
длительная интенсивная сжимающе-давящая боль за грудиной в области сердца, может отдавать в руку, шею, спину или область лопаток;
боль не проходит после приема нитроглицерина;
бледность кожи, холодный пот;
обморочное состояние
. В остром периоде инфаркта миокарда наблюдаются артериальная гипертензия (часто значительная), исчезающая после стихания боли и не требующая применения гипотензивных препаратов; учащение пульса (не всегда); повышение температуры тела (со 2—3-х суток); гиперлейкоцитоз, сменяющийся стойким повышением СОЭ.
Диагноз устанавливается по наличию трех критериев:
типичный болевой синдром
изменения на электрокардиограмме
изменения показателей биохимического анализа крови, говорящие о повреждении клеток мышцы сердца.
Патогенез: 4стадии:
Ишемии
Повреждения (некробиоза)
Некроза
Рубцевания
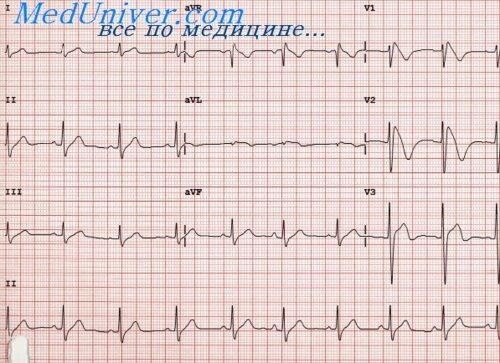
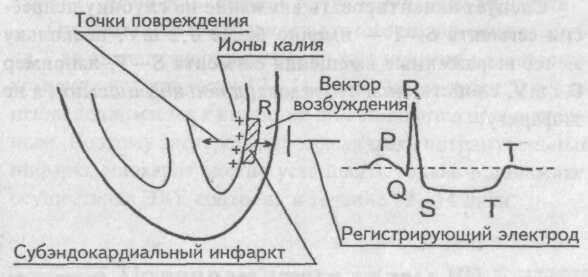
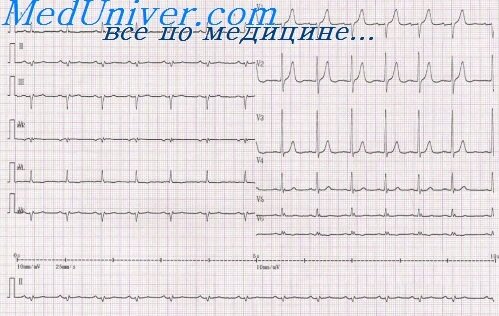
Острая стадия инфаркта миокарда (2-3 недели) в центре поврежденной зоны, формируется очаг некроза. Отличается появлением патологического зубца Q, глубина которого превышает четверть зубца R, ширина больше 0,03 с; снижением (комплекс QRS) или полным отсутствием (комплекс QS) зубца R при трансмуральном инфаркте; куполообразным смещением сегмента ST выше изолинии, отрицательным зубцом Т.
6.Этиология, патогенез, диагностические критерии острого им осложненного левожелудочковой недостаточностью.
Вследствие наличия зоны некроза и выключения части миокарда из процесса сокращения, а также в связи с нарушением функционального состояния периинфарктной зоны и нередко интактного миокарда развиваются систолическая дисфункция (снижение сократительной способности) и диастолическая дисфункция (уменьшение податливости) миокарда левого желудочка. Вследствие падения сократительной функции миокарда левого желудочка и увеличения его конечного диастолического давления происходит последовательное повышение давления крови в левом предсердии, в легочных венах, капиллярах и артериях малого круга. Развитию гипертензии в малом круге кровообращения способствует также рефлекс Китаева — сужение (спазмирование) легочных артериол в ответ на рост давления в левом предсердии и легочных венах. Рефлекс Китаева играет двойственную роль: вначале в определенной мере предохраняет переполнение кровью малого круга кровообращения, а в последующем способствует развитию легочной гипертензии и снижению сократительной способности миокарда правого желудочка. В развитии рефлекса Китаева имеет значение активация системы ренин-ангиотензин II и симпатоадреналовой системы. Результатом повышения давления в левом предсердии и легочных венах является увеличение объема крови в легких, что в свою очередь вызывает уменьшение эластичности и растяжимости легких, глубины дыхания и оксигенации крови. Наблюдается также прогрессирующий рост гидростатического давления в легочных капиллярах и, наконец, наступает момент, когда гидростатическое давление начинает значительно превышать коллоидно-осмотическое, в результате чего происходит пропотевание плазмы и скопление жидкости вначале в интерстиции легких, а затем и в альвеолах, т.е. развивается альвеолярный отек легких. Это в свою очередь вызывает резкое нарушение диффузии кислорода из альвеол в кровь, развитие системной гипоксии и гипоксемии и резкое повышение проницаемости альвеолярно-капиллярных мембран, что еще больше усугубляет отек легких. Повышению проницаемости альвеолярно-капиллярных мембран способствует высвобождение в условиях гипоксемии и метаболического ацидоза биологически активных веществ гистамина, серотонина, кининов..
У больных инфарктом миокарда нередко развиваются тахи- и брадиаритмии, которые также способствуют развитию сердечной недостаточности, уменьшая сердечный выброс.
Диагностика. Наиболее характерным симптомом является появление нарастающей одышки, переходящей в удушье. Болевой синдром для данного состояния не характерен. Если сердечная астма возникла на фоне постинфарктного кардиосклероза, то данный вариант приступа может протекать в безболевой форме, либо боли в области сердца будут носить «ишемический» характер. Типично занимаемое больным вынужденное положение: полусидячее, с опущенными ногами. Отмечаются беспокойство, возбуждение; кожные покровы бледные, акроцианоз. Тоны сердца, как правило, приглушены и плохо прослушиваются из-за большого количества влажных хрипов в легких. Возможно появление акцента II тона над легочной артерией. АД на первоначальных этапах заболевания повышено (влияние симпато-адреналовой реакции), в последующем снижается. Отмечается тахикардия, возможны нарушения ритма сердечной деятельности. Затруднен вдох. В легких определяются влажные хрипы. Динамика их появления начинается с задненижних отделов легких, симметрично с двух сторон. Количество и характер влажных хрипов зависит от выраженности сердечной недостаточности. В наиболее тяжелых случаях у больного из дыхательных путей появляется пена, иногда имеющая розовый оттенок. методы исследования:
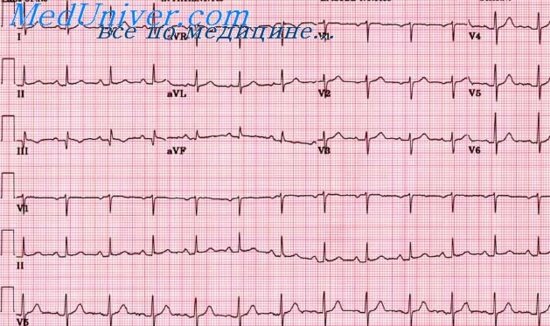
ЭКГ-признаки левожелудочковой острой сердечной недостаточности: раздвоение и увеличение амплитуды зубца Р в отведениях I, II, aVL, V5-6;увеличение амплитуды и продолжительности второй отрицательной фазы зубца РилиформированиеотрицательногозубцаРвотведенияхV1;трицательный или двухфазный зубец РIII;увеличение ширины зубца Р – более 0.1 с
Острая стадия инфаркта миокарда (2-3 недели) в центре поврежденной зоны, формируется очаг некроза. Отличается появлением патологического зубца Q, глубина которого превышает четверть зубца R, ширина больше 0,03 с; снижением (комплекс QRS) или полным отсутствием (комплекс QS) зубца R при трансмуральном инфаркте; куполообразным смещением сегмента ST выше изолинии, отрицательным зубцом Т.
7. Кардиогенный шок – это острое нарушение перфузии тканей организма, вызванное значительным повреждением миокарда и нарушением его сократительной функции. Обычно кардиогенный шок развивается в первые часы после появления первых симптомов ИМ и значительно реже – в более поздний период. Риск развития этого грозного осложнения и его тяжесть во многом определяются обширностью инфаркта – размерами пострадавшего от ишемии и некроза миокарда. Поэтому чаще всего кардиогенный шок развивается при ИМ передней стенки левого желудочка, верхушки сердца и передней части межжелудочковой перегородки, то есть при окклюзии левой коронарной артерии, которая обеспечивает кровью большую часть массы миокарда, а также при поражении всех трех основных венечных артерий (что обусловливает вовлечение в зону инфаркта более 40% массы миокарда левого желудочка). Кардиогенный шок при ИМ правого желудочка бывает значительно реже Самой большой проблемой при кардиогенном шоке является следующий порочный круг: выраженное угнетение систолической функции и снижение артериального давления (АД) обусловливают неэффективность коронарной перфузии, в результате коронарный кровоток еще больше ухудшается, а ишемия и некроз миокарда прогрессивно усугубляются, что дополнительно ухудшает насосную функцию левого желудочка. По классификации T. Killip, состоянию кардиогенного шока соответствует снижение АД <90 мм рт. ст. и наличие признаков периферической вазоконстрикции (олигурия, цианоз, потливость); по классификации J.S. Forrester – признаки сниженной перфузии тканей организма в сочетании с высоким давлением «заклинивания» в легочной артерии.
В обновленном в конце 2008 г. руководстве ESC по ведению больных ИМ с подъемом ST [1], кардиогенный шок определяется снижением систолического АД <90 мм рт. ст. повышением давления наполнения желудочков сердца (и, соответственно, давления «заклинивания» легочной артерии) >20 мм рт. ст. уменьшением сердечного индекса <1,8 л/мин/м 2
Кардиогенный шок при инфаркте миокарда обычно развивается при тяжелом трехсосудистом поражении со значительным поражением передней нисходящей артерии. По данным аутопсии, при кардиогенном шоке обычно поражается не менее 40% миокарда левого желудочка. У 40% больных имеются инфаркты миокарда в анамнезе. При большом инфаркте в анамнезе даже небольшой повторный инфаркт может вызвать кардиогенный шок.
АЛГОРИТМ ЛЕЧЕНИЯ ОТЕКА ЛЕГКИХ, КАРДИОГЕННОГО ШОКА У БОЛЬНЫХ С ОСТРЫМ ИНФАРКТОМ МИОКАРДА Текст научной статьи по специальности « Медицина и здравоохранение »
Новости науки
Мягкость стейка научились определять при помощи рентгена
Ученые из норвежской частной исследовательской организации SINTEF создали технологию для проверки качества сырого мяса при помощи слабого рентгеновского излучения. Пресс-релиз новой методики опубликован на сайте gemini.no.
Читать полностью
-
Создан подвесной авиационный контейнер с открытой архитектурой
Американская компания Northrop Grumman представила новый авиационный подвесной контейнер OpenPod для различных сенсоров, созданный с открытой архитектурой. Масса контейнера составляет 226 килограммов. Благодаря открытой архитектуре другие производители смогут выпускать собственные системы для OpenPod. Контейнер может быть установлен на истребители F-15 Eagle и F/A-18E/F Super Hornet, штурмовики A-10 Thunderbolt II, транспортные самолеты C-130J Super Hercules, а также различные типы вертолетов.
Компания Magic Leap официально объявила о создании платформы для разработчиков дополненной реальности. Оставить контакты можно в соответствующем разделе на сайте компании. Об этом представители компании сообщили в рамках конференции EmTech Digital.
Читать полностью
Алгоритм лечения острого коронарного синдрома с подъемом сегмента st (инфаркт миокарда с подъемом сегмента st, инфаркт миокарда с зубцом Q)
Утвержден
протоколом Экспертного Совета МЗ РК
от 17 апреля 2012 г. № 8
Алгоритм лечения
острого коронарного синдрома с подъемом сегмента ST (инфаркт миокарда с подъемом сегмента ST, инфаркт миокарда с зубцом Q)
Цель лечения в данном случае заключается в достижении быстрой, полной и стойкой реперфузии посредством первичной ангиопластики или фибринолитической терапии. На уровне каждого региона должна быть создана система неотложной медицинской помощи (I А), которая будет контролировать сеть больниц с различными уровнями оказания помощи, и связывать их между собой эффективными путями транспортировки пациентов. Необходимо постоянно информировать население о признаках острого сердечного приступа и необходимости своевременного обращения за медицинской помощью.
^ Догоспитальный этап
Чрезвычайно необходимо сократить все задержки времени, особенно в первые 2 ч с момента появления симптомов заболевания. Организация догоспитальной помощи при остановке сердца должна способствовать качественному проведению сердечно-легочной реанимации, ранней дефибрилляции (при необходимости) и эффективной поддержки жизненных функций. Первичная диагностика и оценка риска состояния пациента должна быть выполнена в пределах 10 мин от момента прибытия скорой помощи. Пять критериев с 90% достоверностью определяют смертность в первые 30 суток – возраст, уровень систолического АД, класс cердечной недостаточности по Кillip, увеличенная ЧСС, передняя локализация инфаркта. Любая бригада СМП, поставив диагноз ОКС сп ST (мониторинг ЭКГ для определения жизнеугрожаемых аритмий (ЖТ/ФЖ), должна экстренно доставить пациента в специализированную клинику для выполнения первичного ЧКВ или в другое лечебное учреждение для лечения таких пациентов.
Кислород — подача 4-8 л/мин, если насыщение кислородом 75 лет. При фибринолизисе – 300 мг. При планировании ЧКВ — 600 мг для более быстрого начала действия (I С).
При появлении гипотонии и брадикардии необходимо ввести атропин (0,5-1 мг внутривенно, общая доза не должна превышать 2 мг).
При отсутствии противопоказаний и невозможности проведения первичного ЧКВ необходимо начать проведение фибринолитической терапии на догоспитальном этапе (II а А). особенно если транспортировка в стационар займет более 30 мин, при следующих условиях:
Если время от начала ангинозного приступа 4 — 6 ч, по крайней мере не превышает 12 ч;
На ЭКГ отмечается подъем сегмента ST > 0,l mV, как минимум в 2-х последовательных грудных отведениях или в 2-х отведениях от конечностей или появляется новая блокада левой ножки пучка Гиса (БЛНПГ).
Введение тромболитиков оправдано в те же сроки при ЭКГ признаках истинного заднего ИМ (высокие зубцы R в правых прекардиальных отведениях V1 -V2 и депрессия сегмента ST в отведениях V1 -V4 с направленным вверх зубцом Т).
Альтеплаза – вводится в/в (предварительно препарат растворяют в 100-200 мл дистиллированной воды или 0,9 % раствора хлорида натрия) по схеме «болюс + инфузия». Доза препарата 1 мг/кг массы тела (но не более 100 мг): болюсно вводится 15 мг; последующая инфузия 0,75 мг/кг массы тела за 30 мин (но не более 50 мг), затем 0,5 мг/кг (но не более 35 мг) за 60 мин (общая продолжительность инфузии — 1,5 ч). Или
Тенектеплаза – внутривенно 30 мг при массе тела 90 кг, требуемая доза вводится в виде болюса, в течение 5 — 10 сек. Учитывая более длительный период полувыведения из организма препарат используется в виде однократного болюса, что особенно удобно при догоспитальном тромболизисе. Или
Стрептокиназа – вводится в/в в дозе 1500000 ME за 30-60 мин в небольшом количестве 0,9 % раствора хлорида натрия. Часто отмечается развитие гипотензии, острых аллергических реакций. Нельзя вводить повторно (уточнить анамнез).
^ Абсолютные противопоказания к фибринолитической терапии:
Ранее перенесенный геморрагический инсульт или нарушение мозгового кровообращения неизвестного происхождения.
Ишемический инсульт перенесенный в течение последних 6-ти месяцев, за исключением ишемического инсульта, происшедшего в пределах 3 ч, который может быть пролечен тромболитиками.
Недавняя обширная травма/операция/ повреждение головы (последние 3 месяцев).
Изменение структуры мозговых сосудов, наличие артерио-венозной мальформации, артериальные аневризмы.
Заболевание печени в прогрессирующей стадии.
Обострение язвенной болезни желудка или 12-ти перстной кишки.
Инфекционный эндокардит.
Неэффективность реанимационных мероприятий. Травматичная или длительная (> 10 мин) сердечно-легочная реанимация.
Для стрептокиназы – предшествующее применение (> 5 дней назад и до одного года и более) или аллергическая реакция на нее.
Во избежание каких-либо задержек и промедлений в оказании помощи рекомендуется всех пациентов, у которых был проведен догоспитальный фибринолизис, транспортировать в лечебное учреждение, в котором имеются условия для выполнения ЧКВ.
^ Антикоагулянтная терапия без реперфузионной терапии (при противопоказаниях к фибринолитической терапии и в отсутствии возможности проведения ЧКВ)
Фондапаринукс — 2,5 мг п/к, затем 2,5 мг 1 раз в сутки. Или
Эноксапарин — в/в болюсно по 30 мг; затем через 15 минут п/к в дозе 1 мг/кг каждые 12 часов. Для больных старше > 75 лет не применяется в/в болюсное введение, п/к доза уменьшается до 0,75 мг/кг каждые 12 ч; первые дозы не должны превышать 75 мг. Или
^ Отделение/Блок реанимации и интенсивной терапии
(при отсутствии – палата интенсивной терапии)
Обеспечить постельный режим, мониторинг жизненно-важных функций и многоканальный мониторинг ЭКГ.
Кислород – через носовые катетеры с подачей 4-8 л/мин, если насыщение кислородом 75 лет. При фибринолизисе – 300мг. При ЧКВ как можно быстро 600 мг (I С).
Нитраты – нитроглицерин в/в 10-20 мкг/мин с увеличением дозы до 200 мкг/мин или изосорбид динитрат 1-10 мг/ч с осторожностью, тщательно титруя дозу до исчезновения симптомов (ишемии и/или отдышки) при отсутствии побочных эффектов (головная боль или гипотензия). Стандартное введение нитратов в острой фазе ИМ сп ST не рекомендуется.
Бета-блокатор — метопролол тартрат в/в по 5 мг 2-3 раза с интервалом как минимум 2 мин до общей дозы 15 мг, под контролем АД и ЧСС. Раннее внутривенное введение β-блокаторов противопоказано пациентам с клиническими признаками гипотонии или сердечной недостаточности.
^ Фибринолитическая терапия на госпитальном этапе — при отсутствии возможности первичного ЧКВ, отсутствии противопоказаний и если не выполнена на догоспитальном этапе. Критерии успешного фибринолизиса (исчезновение боли в грудной клетке, возникновение реперфузионных аритмий — пробежки идиовентрикулярного ритма, уменьшение подъема сегмента ST на ЭКГ более чем на 70% в течение 60-90 мин) должны быть документированы в истории болезни.