Инфекционный Эндокардит
Отмечен случай, когда ИЭ трикуспидального клапана развился в результате лазерного облучения крови с использованием специального внутривенного катетера. При бактериологическом исследовании повторно был высеян золотистый стафилококк. Приведенный случай демонстрирует типичное развитие ИЭ после внутрисосудистых манипуляций.
К группе нозокомиальных эндокардитов относится эндокардит при хроническом гемодиализе. Наблюдалось 5 подобных больных, у 3 – ИЭ развился на трикуспидальном, у 1- на митральном и у 1 – на трикуспидальном и митральном клапанах. ИЭ при хроническом гемодиализе склонны к рецидивирующему течению и, в итоге, к неблагоприятному исходу, хотя при активной терапии удается добиться длительной ремиссии (у одного из наблюдаемых больных – до 1,5 года). По всей вероятности, для рецидивирующего течения ИЭ у больных с ХПН могут иметь значение не только постоянное существование артериовенозной фистулы, но и глубокие нарушения иммунологической реактивности.
К описанной группе близко примыкает ИЭ наркоманов. Число таких пациентов в последние годы значительно возросло; наблюдались 18 больных. Как правило, это так же не стрептококковые эндокардиты, поражающие в первую очередь трехстворчатый клапан и имеющие рецидивирующее течение. Так, описан больной с так называемым героиновым эндокардитом, у которого в течение 3 лет наблюдались 8 рецидивов ИЭ, во время одного из них ему было проведено протезирование митрального клапана.
Эндокардит искусственных клапанов также можно отнести к нозокомиальным. Он встречается у 1-4% больных после протезирования. Раннюю инфекцию (в течение 2 месяцев после операции) обычно вызывают Staph. aureus, Staph. epidermidis, грамотрицательные палочки, Candida spp. и другие условно-патогенные микроорганизмы. Диагностика данного осложнения затрудняется тем, что преходящая бактериемия и лихорадка в послеоперационном периоде отмечается у многих больных. Однако, возможность его развития необходимо рассматривать всегда, когда после протезирования клапанов бактериемия длительно сохраняется. Поздний эндокардит искусственных клапанов (2 месяца после операции и позже) обычно вызывают те же микроорганизмы, что и подострый бактериальный эндокардит естественных клапанов.
К относительно новым ИЭ, которые могут представлять значительные трудности для диагностики, относятся эндокардиты при застойной и гипертрофической кардиомиопатии, а также пристеночный эндокардит, сопровождаемый абсцессами миокарда и эндокардит при пролабировании митрального клапана.
Следует особо подчеркнуть, что в настоящее время у больных ИЭ весьма редко и только при отсутствии адекватного лечения развивается генерализованный сепсис. В начальный же период заболевание начинается с небактериального тромбоэндокардита, чаще всего на аортальном клапане, после чего при наличии достаточно длительной и массивной бактериемии патогенными микроорганизмами, стресса, или (и) стойкого иммунологического неблагополучия инфекция оседает на уже измененном тромбоэндокардитом клапане. В этом случае инфекционный процесс длительно развивается в сердце, поражая клапаны миокарда, и, значительно реже, перикард; и только при поздней диагностике и длительном отсутствии адекватной терапии выявляется клиническая картина генерализованного сепсиса.
Чрезвычайно важным методом диагностики ИЭ является эхокардиография, которая позволяет обнаружить вегетации на клапанах и признаки формирования клапанного порока – основные симптомы ИЭ. Современная аппаратура дает возможность выявить вегетации у 80 – 83% больных ИЭ при трансторакальной эхокардиографии и у 95% — при применении чреспищеводного датчика. При использовании высококачественной аппаратуры достаточно часто диагностируют абсцессы клапанов, разрывы хорд, подвижные вегетации с угрозой эмболии. В то же время нет единой точки зрения о поведении вегетаций после излечения эндокардита (часть авторов считает, что этот симптом сохраняется в неизмененном виде в течение, по крайней мере, 3 лет после клинического излечения).
Кроме того, плохо видны вегетации размером менее 3 мм, плоские вегетации; у больных пожилого и старческого возраста весьма трудна дифференциальная диагностика с сигналами, зависящими от отложения извести на клапанах, и вегетациями.
Значительные трудности представляет диагностическая оценка результатов посева крови, так как некоторые микроорганизмы плохо культивируются, а также возможно загрязнение сред, посевов персоналом и т.д. Наиболее достоверным может считаться выделенный возбудитель, когда он высевается повторно или в нескольких посевах, особенно на высоте лихорадки.
По данным Вашингтонского медицинского университета в посевах крови рост микроорганизмов выявляется более чем у 90% больных эндокардитом. При подостром бактериальном эндокардите наиболее информативен посев крови (трижды на протяжении 24 ч.). Однако, после 1-2 недельной антимикробной терапии выявить возбудитель удается значительно реже. Острый бактериальный эндокардит требует неотложного лечения, поэтому все 3 забора крови необходимо сделать из разных вен в течение 1 часа перед началом эмпирической терапии. При подозрении на трудно культивируемый возбудитель культуру следует инкубировать в течение 4-х недель.
Особенностью ИЭ последнего десятилетия является увеличение количества больных пожилого и старческого возраста. Диагностика у них представляет значительные трудности, т.к. в этой возрастной группе чаще наблюдается «лихорадка неясного генеза», менее достоверны данные эхокардиографии из-за меньшей акустической доступности и часто встречающихся отложений кальция на клапанном аппарате.
В этой возрастной группе приходится проводить дифференциальную диагностику со злокачественными новообразованиями, сопровождающимися высокой лихорадкой.
Довольно часто «маской» ИЭ, особенно у пожилых, является пиелонефрит. В этом случае мочевая инфекция может явиться этиологическим фактором развития эндокардита или причиной ошибочного диагноза этого заболевания при наличии у больного ревматического или атеросклеротического порока сердца.
Лечение эндокардита.
Терапия ИЭ представляет сложную задачу, прежде всего из-за постоянно меняющихся возбудителей болезни, появления новых штаммов внутри одного вида микроорганизмов, продолжающегося широкого раннего и нерационального использования высокоактивных антимикробных средств при еще неустановленном диагнозе, преобладания во многих случаях ИЭ не столько септических проявлений, сколько иммунокомплексных процессов.
При проведении лечения ИЭ необходимо руководствоваться рядом основополагающих принципов:
1) Терапия ИЭ должна быть по возможности этиотропной, т.е. направленной на конкретного возбудителя.
2) Терапия ИЭ должна быть продолжительной: при стрептококковой этиологии не менее 4 нед, при стафилококковой – 6 нед, при грамотрицательных возбудителях – не менее 8 нед.
3) При нарастании признаков иммунного конфликта в форме гломерулонефрита, васкулита, миокардита и др. а также проявлений бактериального шока возможно использование глюкокортикоидов.
Инфекционный эндокардит с поражением трех клапанов в практике лечения хроническим гемодиализом
Республиканская больница МЗ РК, г. Петрозаводск
Адрес для переписки: 185035, Карелия, г. Петрозаводск, ул. Ленина, д. 9, кв. 34
Телефон: 76-42-85. Михеева Юлия Сергеевна
Ключевые слова: инфекционный эндокардит, гемодиализ, сердечные клапаны, эхокардиография
Проблема инфекционного эндокардита (ИЭ) остается актуальной и требует постоянного внимания в связи с сохраняющейся высокой летальностью и увеличением частоты [1-7].
ИЭ у диализных пациентов встречается относительно нечасто в структуре сердечно-сосудистых осложнений, но характеризуется высокой летальностью [6,7]. Выживаемость диализных больных с ИЭ через 30 дней от начала заболевания достигает 71%, через 60 дней — 53% и через 1 год — 35% [6]. Наиболее частыми возбудителями являются Staphylococcus aureus (40-75%), Enterococcus (20%), Streptococcus viridans (15%), Staphylococcus epidermidis (10%) [3,4,6-9]. Особенно неблагоприятна энтерококковая инфекция, которая часто сопровождается высокой резистентностью к антибактериальным препаратам и сопутствующими неврологическими осложнениями [6,8,10]. Предрасполагают к развитию ИЭ у диализных пациентов наличие сосудистого доступа, повторные пункции, снижение иммунитета и дегенеративные изменения клапанов, прежде всего их кальцификация [11]. Использование постоянных и временных диализных катетеров, артериовенозных протезов сопровождается более высокой частотой развития ИЭ по сравнению с обычной артериовенозной фистулой в качестве сосудистого доступа для проведения гемодиализа [6,9]. Митральный клапан поражается в 41-45%, аортальный — в 25-33% [6,7], тогда как у недиализных пациентов отмечается преобладающее поражение аортального клапана (до 62-65,6%) [3,4].Частота вовлечения трикуспидального клапана и клапана легочной артерии не превышает частоты в общей популяции и составляет около 5%, однако приводит к более тяжелому и торпидному течению заболевания [3-6,12]. Крайне редко встречаются случаи поражения нескольких клапанов [1,3,4]. Эхокардиографическое исследование остается «золотым» стандартом диагностики ИЭ, причем использование трансэзофагеального способа предпочтительнее из-за более высокой чувствительности и специфичности [3,4,6]. Вовлечение правых отделов сердца, размер вегетации более 2 см3, наличие сахарного диабета и исходный уровень лейкоцитов крови более 12,5 тыс. являются плохими прогностическим признаками [6]. Основными причинами смерти являются эмболические, неврологические осложнения и сердечная недостаточность [1,10]. Показания для протезирования клапанов те же, что и у недиализных пациентов. Средняя выживаемость после протезирования низкая: через 12 месяцев после протезирования — 60±12%, через 60 месяцев — 42±14% [13].
Таким образом, частота ИЭ у диализных больных, несмотря на наличие сосудистого доступа в качестве постоянного источника инфицирования, сниженного иммунитета, частых сопутствующих изменений клапанов сердца в виде кальциноза и фиброза, не превышает таковую в общей популяции. Однако он значительно ухудшает прогноз, сопровождается высокой смертностью, в том числе после протезирования поврежденных клапанов. Поражение трикуспидального клапана и энтерококковая инфекция, также как и в общей популяции, встречаются реже, но служат неблагоприятным и факторами.
Мы представляем историю заболевания больной Б. 33 лет, получающей лечение хроническим гемодиализом с 29.11.2000 г. по поводу терминальной ХПН вследствие хронического гломерулонефрита. 13.02.2001 г. выполнено оперативное вмешательство в связи с развившейся аневризмой артериовенозной фистулы, удалены некротические ткани. Отмечался воспалительный процесс в области раны, в связи с чем проводилась антибактериальная терапия ципрофлоксацином. Наблюдалась положительная динамика, заживление раны. Однако на 13-е сутки после операции появилась фебрильная лихорадка до 38-39,5оС с ознобами. Отмечено нарастание сердечной недостаточности в виде одышки в покое, венозного застоя и двухстороннего гидроторакса при рентгенологическом исследовании, выраженных отеков на ногах, асцита, увеличения печени до 5 см ниже реберной дуги. При аускультации сердца отмечался систолодиастолический шум над всей областью. Учитывая фебрильную лихорадку, оперативное вмешательство на артериовенозной фистуле, быстрое прогрессирование сердечной недостаточности, заподозрен ИЭ, в связи с чем выполнено ЭхоКГ-исследование (на 3-й день лихорадки), при котором обнаружены вегетации на трикуспидальном клапане с трикуспидальной регургитацией II степени. Значительная дилатация правого предсердия (5,2см), умеренная — правого желудочка (4,2см) и левого предсердия (4,4 см).
При лабораторном исследовании однократно регистрировался лейкоцитоз — 12,2 тыс. в дальнейшем уровень лейкоцитов от 5,75 до 8,2 тыс. палочкоядерного сдвига не было, СОЭ от 21 до 51 мм/ч. Быстрое нарастание анемии (гемоглобин от 50 до 82 г/л) требовало частых повторных гемотрансфузий. Объем гемотрансфузий составил 2030 мл. Уровень иммуноглобулинов: IgA — 1,5; IgM — 3,0; IgG — 17,6 г/л. С-реактивный белок — 2, формоловая проба — 0, сиаловые кислоты — 280 ед. фибриноген — 2,2. Общий белок — 5б,8, альбумины — 50,1%, альфа-1-глобулины — 6,5, альфа-2 — 10,3, бета -10,6, гамма- 22,2 отн.%. Циркулирующие иммунные комплексы — 0,105.
При посеве крови обнаружен Streptococcus faecalis.
Антибактериальная терапия (до результатов посева крови) цефалоспоринами III поколения (цефтазидим, цефоперазон, цефотаксим), макропеном, амикацином неэффективна. После результата посева начата терапия тиенамом, ципрофлокацином, метроджилом с отчетливым положительным эффектом, нормализовалась температура тела, улучшилось общее состояние. Уменьшились проявления сердечной недостаточности, исчезли отеки, уменьшились размеры печени, явления венозного застоя в легких. Диализное лечение проводилось с форсированной ультрафильтрацией.
При динамическом ЭхоКГ-исследовании кроме вегетаций на трикуспидальном клапане обнаружена вегетация на передней створке митрального клапана, пролабирующая в полость левого предсердия, размером 2,1 см3, митральная регургитация II степени и более рыхлые мелкие вегетации на створках аортального клапана с аортальной регургитацией I степени (рис.1). Через 60 дней вегетации на клапанах уплотнились и несколько уменьшились в размерах, размеры полостей на прежнем уровне, сократительная способность миокарда не нарушена.
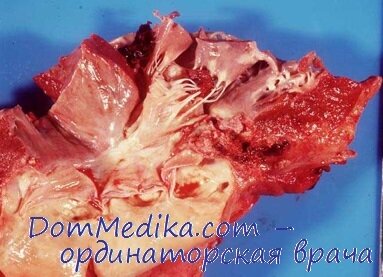
Рис. 1. Инфекционный эндокардит: вегетации на створках трикуспидального, митрального и аортального клапанов. Преимущественная дилатация правых отделов сердца и левого предсердия
%img src=»http://nefro.ru/magazine/image.php?id=10791%3E%3C/p%3E%0D%0A%0D%0A%3Cp%3E%D0%92″ /%
Через 12 месяцев от начала заболевания больная продолжает получать адекватное заместительное лечение программным ГД (индекс KT/V 1,37). Сердечная недостаточность не прогрессирует, застойных явлений в легких, отеков и гепатомегалии нет. При ЭхоКГ через 1 год отмечался фиброз створок митрального, аортального и трикуспидального клапанов. По краю передней створки трикуспидального клапана старая кальцинированная вегетация 0,4 см. Дилатация правых отделов сердца (правый желудочек — 4,0 см, правое предсердие — 4,5 см). Трикуспидальная регургитация III, митральная и аортальная — I степени. Сократительная способность миокарда не нарушена, фракции выброса 80%.
Таким образом, у данной больной, получающей лечение хроническим ГД, имел место ИЭ с поражением трикуспидального, митрального и аортального клапанов сердца. Вовлечение трех клапанов встречается достаточно редко и в значительной степени ухудшает прогноз. Источником инфицирования явилась артериовенозная фистула. Инфекция, вызнанная Streptococcus faecalis, хотя и уступает по частоте стафилококковой, однако отличается тяжелым течением и резистентностью ко многим группам антибиотиков, прежде всего цефалоспоринам III поколения. Ведущей в клинической картине была сердечная недостаточность по смешанному типу. Поражение трикуспидального клапана, большой размер вегетаций, лейкоцитоз в дебюте заболевания служили неблагоприятными прогностическими признаками, позволяющими предполагать серьезный отдаленный прогноз.
Список литературы:
- Брусина Е.В. Коломыщев А.В. Барбараш О.Л. Бурматов Н.П. Инфекционный эндокардит — эволюция болезни. Тер. арх. 2000; 9: 47-50.
- Буклевич О.М. Виноградоаа Т.Л. Некоторые вопросы современной терапии инфекционного эндокардита, Теp. арх. 2000; 9: 54-57.
- Тазина C.Я. Гypевич M.A. Современный инфекционный эндокардит. Часть I. Клин. мед. 1999; 12: 19-23.
- Тазина C.Я. Гypевич M.A. Современный инфекционный эндокардит. Часть II. Клин. мед. 2000; 1: 15-20.
- Ferrer C. Jakob E. Pastorino G. Juncos L.I. Right-sided bacterial endocaiditis due to Flavobacterium odoratum in a patient on chronic hemodialysis. Am. J. Nephrol. 1995; 15(1): 82-84.
- McCarthy J.T. Steckelberg J.M. Infective endocarditis in patients receiving long-term hemodialysis Mayo Clin. Proc. 2000; 75(10): 1008-1014.
- Takahashi C. Warrak E.A. Ruzany F. Infectious endocarditis in patients on periodic hemodialysis AMB Rev. Assac Med Bгаs. 1991; 37(3): 119-126.
- Lin D.P. Wada S. Jimenez-LuchoV.E. Enterococcus faecalis endocarditis presenting аs meningitis. Infection. 1998; 26(5): 304-305.
- Rocha J.L. Gonzalez-Roncero F. Lopez-Hidalgo R. et al. Inverse paradoxical embolism in a patient on chronic hemodialysis with aortic bacterial endocarditis. Am. J. Kidney Dis. 1999; 34(2): 338-340.
- Vijayvargiya R. Veis J.H. Antibiotic-resistant endocarditis in a hemodialysis patient. J. Am. Soc. Nephrol. 1996; 7(4): 536-542.
- Kopal V. Svejda J. Svobodowa. Is antibiotic prophylaxis necessary in patients on chronic dialysis and with recurrent endocarditis? Vnitr. Lek. 1996; 42(3): 150-152.
- Kamaraju S. Nelson K. Williams D.N. et al. Staphylococcus lugdunensis pulmonary valve endocarditis in a patient on chronic hemodialysis. Am. J. Nephrol. 1999; 19(5): 605-608.
- Lucke J.C. Samy R.N. Atkins B.Z. et al. Results of valve replacement with mechanical and biological protheses in chronic renal dialysis patients. Ann. Thorac. Surg. 1997; 64(1): 129-132.
Инфекционный эндокардит: современная клиническая картина (обзор литературы)
Инфекционный эндокардит: современная клиническая картина (обзор литературы)
Николаевский Е.Н.
Ремедиум-Поволжье — Кардиология (Журнал для практикующих врачей) — 2004;10:23-7
Николаевский Евгений Николаевич — доктор медицинских наук, Самарский военно-медицинский институт МО РФ (443099, Самара, ул. Пионерская, дом 22), электронная почта: [email protected]
За последние десятилетия клиническая картина инфекционного эндокардита (ИЭ) существенно изменилась. Перестали быть редкостью острые формы ИЭ, протекающие с гектической лихорадкой и быстрым формированием порока сердца. Увеличилось количество больных со стертой картиной болезни, характеризующейся затяжным малосимптомным течением с длительно сохраняющейся субфебрильной лихорадкой (Голочевская В.С. 1991; Шевченко Ю.Л. Шихвердиев Н.Н. 1993). Появились особые клинические формы болезни: ИЭ у наркоманов (с преимущественным поражением правых камер сердца), ИЭ протеза клапана (ИЭПК), нозокомиальный инфекционный эндокардит, ИЭ у лиц с имплантированным электрокардиостимулятором и лиц, находящихся на программном гемодиализе, эндокардит у реципиентов трансплантированного органа (Гуревич М.А. 1997, 1999; Симоненко В.Б. Колесников С.А. 1999; Тазина С.Я. Гуревич М.А. 1999; Иванов А. С. и др. 2001; Мишаевский А.Л. 2001; Мазуров В.И. Уланова В.И. 2001; Тюрин В.П. 2001). Клиническая картина современного ИЭ отличается значительным многообразием симптомов, что предопределяет трудности диагностики болезни. В целом, клиническая картина современного ИЭ складывается из проявлений инфекционно-септической интоксикации, нарушений гемодинамики вследствие поражения клапанов и миокарда, специфических осложнений (Шевченко Ю.Л. 1995).
Наиболее частым и ранним симптомом болезни является лихорадка, встречающаяся у 90-95% больных (Шевченко Ю.Л. 1995; Пшоник С.С. и соавт. 1996; Хубулава Г.Г. 1996). Характер температурной реакции самый разнообразный: от периодического субфебрилитета до постоянной гектической лихорадки. В начале заболевания субфебрильная температура может быть волнообразной. Иногда возникают ознобы с повышением температуры до 38-39С, что характерно для ИЭ стрептококковой этиологии. Для стафилококкового ИЭ характерно внезапное начало заболевания с озноба и повышения температуры тела до 39-40С, которая держится неделями, напоминая гектическую. При этом потливость достигает иногда степени профузного пота. Озноб — важный, хотя и непостоянный симптом. Он может варьировать от лёгкого познабливания до потрясающего озноба с резким повышением температуры тела.
При осмотре больных кожные покровы и видимые слизистые бледные или с желтоватым, иктеричным оттенком, приблизительно у одной трети больных наблюдаются петехии, геморрагическая сыпь, как следствие аутоиммунного васкулита и поражения мелких сосудов циркулирующими иммунными комплексами (Дёмин А.А. Дёмин Ал.А. 1978; Спасокукоцкий А.Ю. Валько А.С. 1993). Утолщение концевых фаланг пальцев в виде «барабанных палочек» и изменения ногтей в виде «часовых стекол» можно наблюдать у 12-10% больных ИЭ. У 5-6% больных отмечаются признаки воспаления суставов в виде моно- или олигоартритов крупных суставов верхних и нижних конечностей (Гогин Е.Е. Тюрин В.П. 1996).
Патогномоничным и частым симптомом является формирование порока сердца в результате разрушения клапанного аппарата сердца. Наиболее часто поражается аортальный клапан, что характеризуется развитием симптоматики его недостаточности (Яковлев Г.М. и соавт. 1990). Характерны сердцебиение, слабость, ощущение пульсации в различных частях тела, шум в ушах, головная боль пульсирующего характера, расстройство зрения, боли в области сердца стенокардитического характера, головокружение, склонность к обморокам.
При объективном исследовании определяются бледность кожных покровов, усиленная пульсация артерий, капиллярный пульс (симптом Квинке), ритмичное расширение и сужение зрачков (симптом Ландольфи), загрудинная пульсация (пульсация дуги аорты), скорый, высокий, частый пульс, умеренное повышение максимального артериального давления, снижение минимального, увеличение пульсового давления, усиление верхушечного толчка, смещение его вниз и влево; смещение границ относительной сердечной тупости влево и вниз, аортальная конфигурация сердца; ослабление 1 тона на верхушке, ослабление или отсутствие 2 тона на аорте, диастолический (протодиастолический) шум на аорте, мягкий, дующий, убывающий к концу диастолы, проводящийся вдоль левого края грудины к верхушке сердца, с максимумом звучания в точке Боткина — Эрлиха, лучше выслушивающийся в положении больного сидя с наклоном вперёд при задержке дыхания на вдохе; систолический шум относительного стеноза устья аорты во втором межреберье справа от грудины; систолический шум на верхушке сердца вследствие относительной недостаточности митрального клапана («митрализация» порока); пресистолический шум относительного стеноза левого венозного устья (шум Флинта), выслушивающийся на верхушке сердца; двойной тон Траубе и двойной шум Дюрозье на периферических сосудах.
При поражении митрального клапана характерны сердцебиение, одышка при физической нагрузке, в последующем — в покое, приступы сердечной астмы, кашель сухой или с небольшим количеством мокроты, кровохарканье; различные по характеру и интенсивности боли в области сердца. При осмотре определяются: цианоз губ, акроцианоз в поздних стадиях заболевания, «facies mitralis» у больных молодого возраста со значительной регургитацией; тахикардия, мерцательная аритмия, разлитой верхушечный толчок, смещённый влево и вниз; сердечный толчок; эпигастральная пульсация; набухание шейных вен, отёки, увеличение печени; смещение границ относительной сердечной тупости влево и вверх и вправо (в поздних стадиях заболевания); ослабление звучности 1 тона у верхушки сердца; акцент и расщепление 2 тона над лёгочной артерией; 3 тон у верхушки сердца, протодиастолический ритм галопа; систолический шум у верхушки сердца, начинающийся с 1 тоном, убывающий, различной продолжительности и громкости, проводящийся в подмышечную область или к основанию сердца.
При сочетании митральной и аортальной недостаточности характерны относительно длительная компенсация порока. Если преобладает аортальная недостаточность, то характерны головные боли, головокружение, обмороки, пульсация периферических сосудов, снижение диастолического давления, диастолический шум во 2-3 межреберье слева от груди, ослабление 2 тона на аорте. Если преобладает митральная недостаточность, то характерны: одышка, акроцианоз, мерцательная аритмия, увеличение левого предсердия наряду с гипертрофией левого желудочка, ослабление 1 тона и систолический шум на верхушке сердца с иррадиацией в левую подмышечную область, наличие 3 тона.
При поражении трёхстворчатого клапана больных беспокоит общая слабость, сердцебиения, перебои и неопределённого характера боли в области сердца при физической нагрузке; умеренная одышка, обычно не соответствующая тяжести состояния, тяжесть и ноющие боли в области правого подреберья, связанные с увеличением печени, диспептические расстройства; боли распирающего характера по всему животу при развитии асцита, отёки. При объективном исследовании определяется цианоз кожи, акроцианоз, субъэктеричность кожи и склер; асцит, умеренные периферические отёки; набухание шейных вен, усиливающееся при горизонтальном положении больного, систолическая пульсация шейных вен и экстенсивная пульсация печени; увеличение печени вследствие застоя, развитие «сердечного цирроза», экстенсивная пульсация печени, малый, частый, пульс; снижение артериального давления, значительное увеличение венозного давления (в 2-3 раза выше нормы); перкуторно определяемое смещение границ сердца вправо; ослабление 1 тона у мечевидного отростка, ослабление звучности 2 тона над лёгочной артерией; негромкий, продолжительный, мягкого тембра «дующий» систолический шум у основания мечевидного отростка, проводящийся вдоль правого края грудины к правой ключице, а так же в правую подмышечную область, усиливающийся при задержке дыхания на высоте глубокого вдоха (симптом Риверо-Корвальо).
Клапан лёгочной артерии поражается ИЭ исключительно редко. Клинические симптомы, патогномоничные только для этого порока, выделить трудно, так как в изолированном виде встречается редко. Наиболее характерны одышка, сердцебиения, цианоз кожных покровов, расширение ногтевых фаланг по типу «барабанных палочек», отёки, застойное увеличение печени, гидроторакс, асцит; систолическая пульсация во 2 и 3 межреберье слева от грудины вследствие расширения лёгочной артерии; эпигастральная пульсация, обусловленная гипертрофией правого желудочка; положительный сердечный толчок; перкуторно определяемое расширение сердца вверх и вправо; ослабление 1 тона над лёгочной артерией, диастолический шум во 2 и 3 межреберьях слева от грудины, нежный, «дующий», усиливающийся в вертикальном положении больного, проводящийся вверх или вправо (шум Грехема-Стилла).
Клиническая картина ИЭПКС весьма неспецифична (Голочевская В.С.,1991). Характерна полиморфность клинических проявлений (Дёмин А.А. Дробышева В.П. 1991), что способствует ошибкам в диагностике и позднему выявлению этой нозологической формы. Проявления заболевания, его течение и исход зависят от возбудителя, возраста больного, формы ИЭ, предшествующего применения АБ, наличия осложнений и других причин.
Картина болезни под влиянием современной антибиотикотерапии нередко бывает стёртой, с уменьшением инфекционно-токсических проявлений и более выраженным проявлением иммунновоспалительных проявлений (Дёмин А.А. Дробышева В.П. 1988; Козлова В.М. 1996). Наиболее характерным началом для ИЭПКС являются множественные лёгочные инфекционные очаги, иногда септические легочные эмболии вызывают двусторонний пневмоторакс и этим синдромом манифестирует заболевание (Agаado J.M. et. al.,1990). Типична манифестация с так называемой «лихорадки неясного генеза», которая является одной из самых частых и важных симптомов и встречается у 90-95% больных (Барт Б.Я. 1989, 1992; Remetz M.S. et. al. 1992). Озноб так же один из наиболее частых симптомов ИЭПКС. Причиной его развития является массивное поступление в сосудистое русло микроорганизмов и продуктов их жизнедеятельности (Малиновский Н.Н. 1992; Светухин А.М. и соавт. 1992; Bann N.I. et al. 1995). В последующем он сопровождается обильным потоотделением. Характерным является отсутствие улучшения после потоотделения (Барт Б.Я. и др.,1987; Симоненко В.Б.,1992).
При осмотре больных обращает внимание бледность кожных покровов, часто связанная с септической анемией. Желтушность кожных покровов обусловлена, как правило, инфекционно-токсическим гепатитом или вирусным поражением печени, что характерно для наркоманов. Приблизительно у одной трети больных наблюдаются петехии и геморрагическая сыпь. Отёки нижних конечностей обусловлены развитием сердечной недостаточности, которая при ИЭПКС развивается на поздних стадиях болезни (Gahl-K. 1987; Baldi N. 1990). Это объясняется тем фактом, что гемодинамические проявления при разрушении структур правых камер сердца менее выражены, чем при левосторонних поражениях.
У 10-15% больных ИЭПКС сердечных шумов может и не быть (Барт Б.Я. Пашкова Т.Л. и соавт. 1987). У 50-60% пациентов ИЭПКС шум не выслушивается или определяется только у 20% больных (Petitalot J.P. et al. 1995). Недостаточно активная антибактериальная терапия способствует прогрессированию сепсиса, формированию септического миокардита. Для диффузного миокардита характерны сердцебиения, тахикардия, реже — брадикардия, ослабление тонов, нарушения сердечного ритма и проводимости. Экстрасистолии на ЭКГ встречаются у одной трети пациентов. У 20-30% отмечаются различные нарушения ритма и проводимости сердца (Палеев Н.Р. и соавт. 1992; Матвеев С.А. 1994).
Поражения лёгких при ИЭПКС являются его характерной особенностью, с которой он часто и манифестирует (Шевченко Ю.Л. 1992; Левина Л.И. и соавт. 1993; Arvay A. et al. 1995). Как правило, это множественные легочные септические эмболии (Голочевская В.С.,1991; Gonzales-Cocina E. et. al. 1991) c клинической картиной тромбоэмболии лёгочной артерии (ТЭЛА). Они могут осложняться инфаркт-пневмониями, абсцессами лёгких (Сумароков А.В. 1992; Титков Ю.С. 1995; Gray L.E. et. al. 1991). ТЭЛА при ИЭПКС может манифестировать двусторонним пневмотораксом (Agaado J.M.,1990).
В клинической картине ИЭПКС поражение почек занимает значительное место. Как правило это диффузный гломерулонефрит, обусловленный поражением ЦИК. При подостром ИЭ диффузный гломерулонефрит встречается примерно у 8% пациентов (Савичевский М.С. и соавт.,1988). У 10% при ДГ с почечной недостаточностью он протекает с нормальной температурой тела (Демидова А.В. Новичкова Ю.Н. 1991). Поражение селезёнки встречается у 25-30% больных ИЭ и выражается её увеличением. Поражение печени происходит при декомпенсации сердечной недостаточности и вследствие формирования инфекционно-токсического гепатита (Белокриницкая О.А. Таранова Н.В. 1995; Жибурт Е.Б. 1995). Выраженная печёночная недостаточность тем не менее бывает редко (Дмитриев А.Е. и соат. 1992).
Отдельного рассмотрения требует одна из современных форм заболевания — ИЭ протеза клапана (ИЭПК). Инфекционный эндокардит протеза клапана — наиболее тяжёлое осложнение в кардиохирургии (Нарсия Б.Е. 1998; Цукерман Г.И. Скопин И.И. 1997; Шевченко Ю.Л. 1995, 1997; Cowgill L. et al. 1999). По мнению Черепанина И.М. (1999) термин ИЭПК характеризует генерализованную реакцию организма (сепсис) и подразумевает воспалительные изменения в эндокарде. При ИЭПК поражаются парапротезные ткани с частым формированием абсцессов.
По времени возникновения (Колесникова Н.И. 1991, 1995; Aranki S.F. et al. 1994; Chastre J. Trouillet J.L. 1995; Horstkotte D. et al. 1995) различают ранний (возникающий в течение первых 60 дней после протезирования клапанов) и поздний (развивающийся позднее 60 дней) ИЭПК. Деление на ранний и поздний ИЭПК вызвано особенностями микробиологических, клинических и диагностических данных, течением и прогнозом болезни (De Castro S. et al. 1997; Chastre J. 1998).
Клиническое течение болезни может быть различным. Оно зависит от многих факторов: срока возникновения (ранний, поздний), вида возбудителя, возраста больного, ранее применяемой антибактериальной терапии (Черепанин И.М. 1999). При высоковирулентном возбудителе (золотистый стафилококк, грамотрицательная флора) преобладает острое течение с ранним развитием полиорганной недостаточности (Gahl K. 1994). При маловирулентном возбудителе разворачивается классическая картина sepsis lent, что более характерно для позднего ИЭПК.
Наиболее частым симптомом при раннем и позднем ИЭПК является лихорадка, встречающаяся у 95-97% больных (Черепанин И.М. 1999; Muehrcke D.D. 1995; Harken D.E. 1997). Характер её разнообразный: от периодического субфебрилитета до постоянной гектической. На фоне субфебрилитета или нормальной температуры тела могут быть подъёмы температуры в необычное для её измерения время («свечи»).
Озноб — важный, но не непостоянный, симптом болезни. Он может варьировать от лёгкого познабливания до потрясающего озноба с резким повышением температуры тела и последующим профузным потоотделением, которое не облегчает состояния больного. На фоне повышения температуры тела у 20% больных бывают полиартромиалгии (Черепанин И.М. 1999).
Сердечная недостаточность развивается вследствие параклапанной недостаточности, обструкции, септического миокардита. Она наблюдается у 56-100% больных при раннем и у 30% — при позднем ИЭПК (Черепанин И.М. 1998). Септический шок встречается у 33% больных с ранним и у 10% — с поздним ИЭПК (Черепанин И.М. 1997). В 15-20% случаев раннего и в 5-10% позднего ИЭПК наблюдаются нарушения атриовентрикулярной проводимости (Черепанин И.М. 1997). По данным того же автора спленомегалия отмечена у 26,8% пациентов с ранним ИЭ протезированного клапана и у 44% — с поздним. Петехии, пятна Рота, узелки Ослера нередко отсутствуют. Их сочетание со спленомегалией связывают с вовлечением аутоиммунных механизмов (Chastre J. Trouillet J.L. 1995).
Частота развития эмболий составляет 10-32% (Chastre J. Trouillet J.L. 1995; Gnecco G. et al. 1998). Наиболее характерны эмболии, вызванные грибковой микрофлорой (Cowgill L.D. et al. 1999). При раннем ИЭПК частота эмболий составляет 10-11%, а при позднем — 23-28% (Chastre J. Trouillet J.L. 1995). По мнению Millaire A. и соавт. (1997) при позднем ИЭПК чаще встречаются экстрацеребральные эмболии (25-35,6%).
Ранняя форма ИЭПК характеризуется выраженными клиническими проявлениями. В большинстве случаев лихорадочное состояние сопровождается ознобом, который, завершается обильным потоотделением, не облегчавшим состояния пациентов. Больные предъявляют жалобы на одышку, приступы удушья, кардиалгии, сердцебиение, перебои в работе сердца, артромиалгии, отсутствие аппетита. При осмотре выявляются бледность и желтушность кожи, иктеричность склер (вследствие инфекционно-токсического гепатита), признаки аутоиммунного васкулита (петехии, геморрагическая сыпь), симптомы декомпенсации сердечной недостаточности (отёки нижних конечностей, асцит, набухание шейных вен и др.).
Для всех больных ранним ИЭПК характерно тяжёлое и крайне тяжёлое общее состояние. При объективном обследовании классическим признаком болезни является изменение аускультативной картины сердца. Более чем у 2/3 больных выслушиваются новые шумы, происходит изменение ранее существовавших шумов сердца. Для лиц с протезом аортального клапана характерно появление диастолического шума параклапанной недостаточности. У пациентов с протезами митрального и трикуспидального клапанов выслушиваются систолический шум параклапанной недостаточности. Значительно реже определяется шум, вызванный обструкцией искусственного клапана тромботическими массами и крупными микробными вегетациями. Частым клиническим признаком раннего ИЭПК является спленомегалия (68%). У 38% больных определяются эмболии артерий верхних и нижних конечностей, сосудов почек, лёгких и головного мозга. Довольно часто (80-90%) эмболии вызывают формирование метастатических абсцессов в сердце, печени, селезёнке, почках, лёгких и головном мозге.
Клиническое течение позднего ИЭПК носит подострый характер, что значительно затрудняет своевременную диагностику болезни. Симптомы сепсиса мало выражены у 56% больных (Черепанин И.М. 1999). В 21% случаев наблюдается безлихорадочное течение, у 42% лиц происходит повышение температуры тела до субфебрильных цифр. У 37,5% лихорадка имеет классическую картину: подъём температуры в виде «свечи», сопровождающийся потрясающим ознобом и проливным потом. В отличии от раннего при позднем ИЭПК менее выражены одышка, сердцебиение, общая слабость, артромиалгии. Проявления иммунновоспалительных реакций в виде системного васкулита (20%), спленомегалии (66%) и гломерулонефрита (41%) по сравнению с предыдущей группой выявляются чаще. Артериальные эмболии (25%) и абсцессы органов (50%) встречаются несколько реже. Появление шумов сердца, изменение их характеристик выявляется у 63% больных.
Особенности клиники ИЭ протеза клапана обусловлены преобладанием в видовом составе микрофлоры стафилококков и грамотрицательных бактерий, преимущественным поражением протеза аортального клапана, формированием парапротезных фистул и отрывов клапанов, поздней диагностикой, развитием тяжёлых осложнений на фоне малоэффективной антибактериальной терапией. На первый план выступают признаки сепсиса, дополняемые симптомами сердечной недостаточности и осложнениями.
Ранняя форма ИЭПК, вызванная высоковирулентными бактериями (стафилококки, грамотрицательные бактерии, грибы), характеризуется острым течением и яркой клинической картиной, быстрой декомпенсацией сердечной недостаточности, частым развитием фатальных осложнений (острой сердечной, полиорганной и почечной недостаточности, эмболий, септического шока). Для поздней формы ИЭПК свойственно подострое течение и стёртая клиническая картина, обусловленные превалированием в микробной пейзаже маловирулентных бактерий (streptococcus viridans, streptococcus piogenuse), наличием периодов ремиссии болезни на фоне эффективной антибактериальной терапии.
В течение последних десятилетий произошло заметное «постарение» инфекционного эндокардита (Гуревич. 1997). Больные старше 60 лет составляют более 30% от всех пациентов (Тазина С.Я. Гуревич М.А. 1999). Это связано с тем, что в этой возрастной группе чаще проводят хронический гемодиализ, внутривенные вливания, уретро- и цистоскопию, установку кардиостимуляторов и длительно действующих венозных катетеров, колоноскопию, различные хирургические операции и т.д. Клиника ИЭ у людей пожилого и старческого возраста имеет особенности: раннее развитие хронической сердечной недостаточности, обусловленное предшествующим изменением клапанов сердца и миокарда, безлихорадочное течение, частые неврологические осложнения (в результате эмболий головного мозга, разрывов микотических аневризм). Предложены критерии диагноза ИЭ у лиц пожилого и старческого возраста (Gantz N.M. 1992): лихорадка с необъяснимой сердечной недостаточностью и цереброваскулярными расстройствами, лихорадка с почечной недостаточностью, анемия неясного происхождения, вновь развившийся шум в сердце, внутрибольничная инфекция у больных с внутривенными катетерами.
Таким образом, инфекционный эндокардит является весьма трудным для диагностики заболеванием. Современное клиническое течение болезни характеризуется развитием фатальных осложнений, высокой летальностью. Вопросы ранней диагностики и эффективного лечения требуют дальнейшего изучения и разработки.
Список литературы
- Голочевская В.С. Трудности диагностики подострого инфекционного эндокардита // Клиническая медицина. — 1991. — Т.69, № 6. — С.108 — 112.
- Шевченко Ю.Л. Шихвердиев Н.Н. Ангиогенный сепсис. СПб. Наука.-1995.-125 с.
- Гуревич М.А. Тазина С.Я. Особенности современного инфекционного эндокардита // Рос. мед. журнал.-1999.- № 8. — С. 27-32.
- Гуревич М.А. Особенности современного течения инфекционного эндокардита // Клин. медицина. — 1997. — № 6. — С. 37 — 43.
- Симоненко В.Б. Колесников С.А. Инфекционный эндокардит: современное течение, диагностика, принципы лечения и профилактики // Клин. медицина.-1999.-№3.-С.44-49.
- Тазина С.Я. Гуревич М.А. Современный инфекционный эндокардит (часть 1) // Клин. медицина. — 1999. — № 12. — С. 19-23.
- Иванов А.С. Мишаевский А.Л. Погромов А.П. Особенности клиники, диагностики и лечения инфекционного эндокардита трикуспидального клапана // Клин. медицина. — 2001. — № 1 — С. 22-25.
- Мишаевский А.Л. Инфекционный эндокардит трикуспидального клапана // Клин. медицина. — 2001. — № 2. — С. 21-25.
- Мазуров В.И. Уланова В.И. Течение инфекционного эндокардита у инъекционных наркоманов и лиц с предрасполагающими заболеваниями // Клин. медицина. — 2001. — № 8.- С. 23-28.
- Тюрин В.П. Инфекционный эндокардит. — М. ГЭОТАРМЕД, 2001. — 224 с.
- Пшоник С.С. Зюзенков М.В. Баранов М.Ф. Особенности клиники и течения бактериального эндокардита // Здравоохранение Белоруссии. — 1996. — № 6. — С.33 — 34.
- Хубулава Г.Г. Инфекционный эндокардит правых камер сердца. — СПб. Наука, 1996. — 170 с.
- Шевченко Ю.Л. Хирургическое лечение инфекционного эндокардита. — СПб. Наука, 1995. — 230 с.
- Дёмин А.А. Дёмин Ал.А. Бактериальные эндокардиты. — Москва: Медицина, 1978. — 165 с.
- Спасокукоцкий А.Ю. Валько А.С. Инфекционный эндокардит. — Киев: Здоровья, 1993. — 95 с.
- Гогин Е.Е. Тюрин В.П. Инфекционные эндокардиты // Диагностика и лечение внутренних болезней. Под редакцией Ф.И. Комарова. — Москва: Медицина, 1996. — Т.1. — С.300 — 329.
- Яковлев Г.М. Куренкова И.Г. Силин В.А. Сухов Ю.Н. Шишмарёв Ю.Н. Пороки сердца (клинико-инструментальная диагностика). — Л. Печатный двор. — 1990. — 420 с.
- Дёмин А.А. Дробышева В.П. Гипердиагностика инфекционного эндокардита // Терапевтический архив. — 1991. — Т.63, №11. — С.135 — 138.
- Дёмин А.А. Дробышева В.П. Бактериальный эндокардит: современное течение и диагностика // Терапевтический архив. — 1988. — Т.60, № 11. — С.157 — 158.
- Козлова В.М. Исходы инфекционного эндокардита // Клиническая медицина. — 1996. — Т.64, № 11. — С.105 — 108.
- Agaado J.M. Arjona R. Ugarte P. Septic pulmonari emboli: A rare cause of bilateral pneumothorax in drug abusers // Chest. -1990.-Vol. 98, № 5. — P.1302 — 1304.
- Барт Б.Я. Диагностика первичного подострого инфекционного эндокардита в амбулаторно-поликлинических условиях // Кардиология.-1989.-Т.29, № 10. — С.123 — 125.
- Барт Б.Я. Диагностика первичного подострого инфекционного эндокардита // Терапевтический архив. — 1992. — Т.64, № 6. — С.116 — 118.
- Ramirez I.A. Ragт M.I. Sepsis syndrome: recognition and pathophysiology // Sepsis and organ failure.-1992.-Vol.2, № 4.- P. 38 — 45.
- Малиновский Н.Н. Решетников Е.А. Шипилов Г.Ф. Цибин В.И. Диагностика и лечение сепсиса // Хирургия. — 1992. — №7/8. — С.3 — 8.
- Светухин А.М. Карлов В.А. Жуков В.А. и др. Ключевые вопросы патогенеза сепсиса // Хирургия. — 1992. — № 7/8. — С.8 — 13.
- Bann N.I. Kish N.A. Eaugman C.A. Supena R.E Group A Streptococcal bacteremia in intravenous drugabusers //Amer. J. Med. -1995.- Vol. 78, № 4. — P. 569 — 574.
- Барт Б.Я. Пашкова Т.Л. Калманова Е.Н. Титова Е.В. Современные подходы к ранней диагностике первичного инфекционного эндокардита // Кардиология. — 1987. — Т.27, № 2. — С.63 — 66.
- Симоненко В.Б. Клинические варианты инфекционного эндокардита // Клиническая медицина. — 1992. — Т.70, № 3/4. — С.71 — 74.
- Gahl-K Infektiose endocarditis: klinik, diagnostic und therapie // Darmstadt.- 1984.-Vol. 4, № 7.-P.201.
- Balbi N. Right-sided valvulas endocarditis supported by on unexpected intracardiac for-eign body // Chest. -1990. -Vol. 97, № 6.- P. 1486 — 1488.
- Petitalot J.P. Allal J. Poupet J.Y. Rossi F. Thomas P. Becq-Giraudon B. Cardiac insuf-ficiency in infectious endocarditis // Arch. Mal. Coeur Vaiss.-1995.- Vol.78, № 4.- P.525-532.
- Палеев Н.Р. Одинокова В.А. Гуревич М.Л. Найдштут Г.М. Миокардиты. — Москва: Медицина, 1992. — 297 с.
- Матвеев С.А. Хирургическое лечение абсцессов сердца: Автореф. дис. д-ра мед наук.- СПб. 1994. — 46 с.
- Шевченко Ю.Л. Шихвердиев Н.Н. Матвеев С.А. Хубулава Г.Г. Инфекционный эндокардит правых камер сердца // Клиническая медицина. — 1992. — Т.70, № 1. — С.37 — 40.
- Левина Л.И. Щеглова Л.В. Иванов А.В. Бактериальный эндокардит правого сердца с образованием массивного тромба после гинекологического вмешательства // Санкт-Петербургские врачебные ведомости. — 1993. — №4. — С.30 — 31.
- Arvay A. Lengyel N. Рyaepxaa H. Traitment chirurgical des endocardites bacteriennes operees durgens a la phase aiqeu // Cor Vasa.-1995. -Vol. 31, № 1.- P.27 — 36.
- Gonzalez-Cocina E. Espinosa-Caliani I.S. Cabrerizo-Comitre E. et al. Endocarditis dere-cha por Fusobacterium // Rev. Esp. Cardiol.-1991.-Vol.44, № 3.-P.207 — 209.
- Сумароков А.В. Инфекционные эндокардиты. // Болезни сердца и сосудов. Под ре-дакцией Е.И. Чазова. — Москва: Медицина, 1992. — Т.2. — С.404 — 427.
- Титков Ю.С. Инфекционный эндокардит с поражением трёхстворчатого клапана // Кардиология.-1995. — Т.35, №10. — С.95 — 98.
- Gray L.E. Infective endocarditis 1937-1987 // Brit.Heart J.-1987.-Vol.57, № 3.- P.211 — 213.
- Савичевский М.С. Рождественская Е.Д. Идов Э.М. и др. Клапанный инфекционный эндокардит: клинические аспекты и тактика лечения // Грудная и сердечно-сосудистая хирургия. — 1988. — № 2. — С.35 — 39.
- Демидова А.В. Новичкова Ю.Н. Причины ошибок в диагностике инфекционного эндокардита // Клиническая медицина. — 1991. — Т.69, № 2. — С.50 — 53.
- Белокриницкая О.А. Таранова Н.В. Современные подходы к лечению и профилактике инфекционного эндокардита // Клиническая медицина. — 1995. — Т.86, № 5. — С.23 — 26.
- Жибурт Е.Б. Обеспечение иммунологической и инфекционной безопасности гемокомпонентной терапии в хирургической практике: Автореф. дис. д-ра. мед. наук. — СПб. 1995. — 43 с.
- Дмитриев А.Е. Островский В.К. Черкасский Л.А. Синдром полиорганной недоста-точности // Клиническая медицина. — 1992. — Т.69, № 3. — С.67 — 68.
- Нарсия Б.Е. Повторные операции у больных с протезами клапанов сердца // Грудная хирургия. — 1991. — № 2. — С. 45-48.
- Цукерман Г.И. Косач Г.А. Малашенков А.И. и др. Хирургическое лечение протезного эндокардита // Грудная и сердеч.-сосудистая хирургия. — 1990. — № 2. — С. 14-19.
- Шевченко Ю.Л. Черепанин И.М. Прокофьев А.В. Возможности эхокардиографии в диагностике инфекционного эндокардита клапанного протеза. // Вестн. хирургии. — 1997. — Т. 156, № 3. — С. 97-100.
- Cowgill L.G. Addonizio V.P. Hopeman A.R. Harken A.H. A practical approach to pros-thetic valve endocarditis // Ann. Thorac. Surg. — 1999. — Vol. 43, №4. — P. 450-457.
- Черепанин И.М. Инфекционный эндокардит протезированного клапана: Автореферат дис. доктора мед. наук. — СПб. 1999. — 34 с.
- Колесникова Н.И. Эндокардиты при искусственных клапанах сердца // Грудная хирургия. — 1995. — № 5. — С. 66-70.
- Колесникова Н.И. Хирургическое лечение эндокардита протезных клапанов сердца // Грудная хирургия. — 1991. — № 3. — С. 57-59.
- Aranki S.F. Santini F. Adams D.H. et al. Aortic valve endocarditis: Determinants of early survival and late morbidity // Circulation. — 1994. — Vol. 90, №5. — P. 175-182.
- Chastre J. Trouillet J.L. Early infective endocarditis on prosthetic valves // Eur. Heart J. — 1995. — Vol. 16, suppl. B. — P. 32-38.
- Horstkotte D. Bodhar E. Infective endocarditis. — London: ICR.-1990.-365 p.
- De Castro S. d’Amati G. Cartoni D. et al. Valvular perforation in leftsided infective endocarditis: a prospective echocardiographic evaluation and clinical outcome // Am. Heart J. — 1997. — Vol. 134, №4. — P. 656-664.
- Chastre J. Trouillet J.L. Early infective endocarditis on prosthetic valves // Eur. Heart J. — 1998. — Vol. 16, suppl. B. — P. 32-38.
- Gahl K. Infektive endokarditis // Darmstadt: Steinkopff-Verlag.- 1994.- 396 s.
- Muehrcke D.D. Fungal рrosthetic valve endocarditis // Semin. Thorac. Cardiovasc. Surg. — 1995. — Vol. 7, №1. — P. 20.
- Harken A.H. A practical approach to prosthetic valve endocarditis // Ann. Thorac. Surg. — 1997. — Vol. 43, № 4. — P. 450-457.
- Черепанин И.М. Инфекционный эндокардит клапанного протеза (диагностика, лечебная тактика) // Избранные лекции по клинической хирургии. — Выпуск VIII. — СПб. — 1998. — С. 20 — 47.
- Черепанин И.М. Возможности эхокардиографии в диагностике инфекционного эндокардита клапанного протеза // Вестник хирургии. — 1997. — Т. 156, № 3. — С. 97 — 100.
- Черепанин И.М. Нарушения внутрисердечной гемодинамики у больных инфекционным эндокардитом клапанного протеза и возможности их диагностики // Terra Medica. — 1997. — Приложение 1. — С. 117 — 118.
- Gnecco G. Bezante G.P. Pestell S. et al. Diagnosis of prosthetic valve endocarditis // Cardiologia. — 1998. — Vol.36, №5. — P. 373-378.
- Millaire A. Leroy O. Gaday V. et al. Incidence and prognosis of embolic events and metastatic infections in infective endocarditis // Eur. Heart J.- 1997.- Vol.18, №4.- P. 677-684.
- Gantz N.M. Infective endocarditis // Diagn. Microbiol. Infect. Dis. — 1992. — Vol. 15, №3. — P. 273-276.
Обсудить Главная страница раздела