Главное меню
Ремоделирование левого желудочка после острого инфаркта миокарда.
Раннее постинфарктное ремоделирование.
Процесс раннего ремоделирования ЛЖ после ОИМ включает нарушение топографии как пораженных, так и непораженных областей. В пораженной области распространение зоны инфаркта с региональным расширением и истончением инфарктной зоны имеет место в первые 24 часа от начала заболевания. Распространение инфаркта значительно изменяет объем и геометрию ЛЖ, подготавливает почву для формирования острой аневризмы и разрывов миокарда и является важным субстратом для расширения полости ЛЖ. Дилатация ЛЖ в остром периоде ИМ может быть отнесена к компенсаторному механизму, поддерживающему систолический объем и возникающему при поражении более 20% миокарда.
Париетальное истончение инфацируемой области ЛЖ является следствием снижения сопротивления пораженного миокарда во время систолического напряжения при каждом сокращении и осуществляется за счет нескольких механизмов, включающих растяжение миоцитов с уменьшением их диаметра и скольжение миоцитов по отношению друг к другу.
Экспансия миокарда имеет место преимущественно при широких, трансмуральных инфарктах, которые захватывают область верхушки ЛЖ. Все большее число исследователей описывают процессы ремоделирования, имеющие место в непораженном, отдаленном от зоны некроза миокарде. Отдаленный от площади инфаркта миокард подвергнут острому увеличению диастолического миокардиального стресса. Как указывалось выше, то сопровождается скольжением миоцитов по отношению друг к другу и их гипертрофией. Наблюдаемая гипертрофия миокарда демонстрирует черты комбинированной перегрузки давлением и объемом.
Высокий миокардиальный стресс в неповрежденном участке миокарда служит стимулом к развитию гипертрофии миокарда и ремоделированию камеры в хронической фазе после ИМ. Гипертрофия непораженной сердечной мышцы является ранним физиологическим ответом на повреждение миокарда, сопровождающим изменения в пораженной зоне миокарда. Положительные эффекты начинающейся ранней фазы гипертрофии желудочка включают нормализацию систолической функции поврежденной стенки и поддержание ударного объема. Вместе с тем, длительное влияние высокого миокардиального стресса способствует переходу от гипертрофии сердечной мышцы к ее недостаточности.
Ранние изменения объема и геометрии ЛЖ имеют важное прогностическое значение для пациентов, перенесших ИМ. Даже относительно небольшое увеличение конечного систолического и конечного диастолического объемов ЛЖ после ИМ в 4 — 5 раз увеличивает риск смерти. Работы, проведенные в Институте клинической кардиологии им. Мясникова, а также другие источники показывают, что конечный систолический объем ЛЖ через 1 месяц после ОИМ является самым строгим предиктором выживаемости, превышающим значение фракции выброса.
Позднее постинфарктное ремоделирование. При позднем постинфарктном ремоделировании в процесс вовлекается оставшийся неповрежденным или сократительный миокард. При мелкоочаговых и нетрансмуральных ИМ функция и геометрия могут вернутся к норме в фазу восстановления, тогда как при обширных и трансмуральных имеет место прогрессирующее ремоделирование с дополнительным увеличением объема и дальнейшим расстройством геометрии ЛЖ. В ранние сроки после ИМ имеет место деформация полости ЛЖ в виде ее сжатия в зоне перехода от рубца к оставшемуся миокарду из-за чрезмерно высокого миокардиального стресса в этой области. На поздних стадиях процесса ремоделирования происходит сглаживание переходной зоны от рубца к оставшемуся миокарду, что проявляется поздней сферификацией ЛЖ, приводящей к поздней его дилатации. При этом позднее увеличение систолического индекса сферичности превосходит увеличение диастолического индекса сферичности. Таким образом, нормальная эллиптификация от диастолы к систоле уменьшается по мере позднего постинфарктного ремоделирования. Это приводит к относительному уменьшению ударного объема, который должен быть компенсирован увеличением сократимости миоцитов или дополнительным расширением желудочка. Прогрессирующее нарушение динамического изменения конфигурации может сказаться также на диастолическом наполнении, которое становится более зависимым от растяжения и активного расслабления миоцитов. Вышеперечисленные нарушения систолической и диастолической функций, связанные с изменением формы и геометрии ЛЖ, могут способствовать появлению симптомов застойной сердечной недостаточности.
Перейти на страницу: 1 2
Узнайте немного больше
ОСТРЫЙ ИНФАРКТ МИОКАРДА
Ричард К. Пастернак, Евгений Браунвальд, Джозеф С. Алперт (Richard С. Pasternak, Eugene Braunwald, Joseph S. Alpert)
Инфаркт миокарда это одно из наиболее часто встречающихся заболеваний в странах Запада. В США ежегодно регистрируется примерно 1,5 млн человек, перенесших инфаркт миокарда. При остром инфаркте миокарда умирает примерно 35 % заболевших, причем чуть более половины из них до того, как попадают в стационар. Еще 15-20% больных, перенесших острую стадию инфаркта миокарда, умирают в течение первого года. Риск повышенной смертности среди лиц, перенесших инфаркт миокарда, даже через 10 лет в 3,5 раза выше, чем у лиц такого же возраста, но без инфаркта миокарда в анамнезе.
Клиническая картина
Чаще всего больные с острым инфарктом миокарда жалуются на боль. У некоторых больных она бывает настолько сильной, что они описывают ее как наиболее выраженную из болей, которые им когда-либо доводилось испытывать (гл. 4). Тяжела я, сжимающая, разрывающая боль обычно возникает в глубине грудной клетки и по характеру напоминает обычные приступы стенокардии, однако более интенсивная и продолжительная. В типичных случаях боль ощущается в центральной части грудной клетки и/или в области эпигастрия. Примерно у 30 % больных она иррадиирует в верхние конечности, реже в область живота, спины, захватывая нижнюю челюсть и шею. Боль может иррадиировать даже в область затылка, но никогда не иррадиирует ниже пупка. Случаи, когда боль локализуется ниже мечевидного отростка, или когда больные сами отрицают связь боли с сердечным приступом, являются причинами постановки неправильного диагноза.
Часто боли сопровождаются слабостью, потливостью, тошнотой, рвотой, головокружением, возбуждением. Неприятные ощущения появляются обычно в состоянии покоя, чаще утром. Если боль начинается во время физической нагрузки, то в отличие от приступа стенокардии, она, как правило, не исчезает после ее прекращения.
Однако присутствует боль далеко не всегда. Примерно у 15—20 %, а по-видимому, даже и у большего процента больных острый инфаркт миокарда протекает безболезненно, и такие больные могут вообще не обращаться за медицинской помощью. Чаще безболевой инфаркт миокарда регистрируют у больных сахарным диабетом, а также у лиц преклонного возраста. У пожилых больных инфаркт миокарда проявляется внезапно возникшей одышкой, которая может перейти в отек легких. В других случаях инфаркт миокарда, как болевой, так и безболевой, характеризуется внезапной потерей сознания, ощущением резкой слабости, возникновением аритмий или просто необъяснимым резким понижением артериального давления.
Физикальное обследование
Во многих случаях у больных доминирует реакция на боль в грудной клетке. Они беспокойны, возбуждены, пытаются снять боль, двигаясь в постели, корчась и вытягиваясь, пытаются вызвать одышку или даже рвоту. Иначе ведут себя больные во время приступа стенокардии. Они стремятся занять неподвижное положение из-за боязни возобновления болей. Часто наблюдаются бледность, потливость и похолодание конечностей. Загрудинные боли, продолжающиеся более 30 мин, и наблюдаемая при этом потливость свидетельствуют о высокой вероятности острого инфаркта миокарда. Несмотря на то что у многих больных пульс и артериальное давление остаются в пределах нормы, примерно у 25 % больных с передним инфарктом миокарда наблюдают проявления гиперреактивности симпатической нервной системы (тахикардия и/или гипертония), а почти у 50 % больных с нижним инфарктом миокарда наблюдают признаки повышенного тонуса симпатической нервной системы (брадикардия и/или гипотония) .
Прекардиальная область обычно не изменена. Пальпация верхушечного толчка может быть затруднена. Почти у 25 % больных с передним инфарктом миокарда в течение первых дней болезни в периапикальной области выявляется измененная систолическая пульсация, которая вскоре может исчезнуть. Другие физикальные признаки дисфункции левого желудочка, которые могут встречаться при остром инфаркте миокарда, в порядке убывания по частоте встречаемости располагаются следующим образом: IV (S4) или III (S3) сердечные тоны, приглушенность тонов сердца и, редко, парадоксальное расщепление II тона (гл. 177).
Преходящий систолический шум на верхушке сердца, возникающий преимущественно как следствие вторичной недостаточности левого предсердно-желудочкового клапана (митральной недостаточности) из-за дисфункции сосочковых мышц, имеет средне- или позднесистолический характер. При выслушивании у многих больных с трансмуральным инфарктом миокарда временами прослушивается шум трения перикарда. У больных с инфарктом правого желудочка часто возникает пульсация растянутых яремных вен, отмечается уменьшение объема пульса на каротидных артериях, несмотря на нормальный сердечный выброс. В 1-ю неделю острого инфаркта миокарда возможен .подъем температуры тела до 38 °С, но, если температура тела превышает 38 °С, следует искать другие причины ее повышения. Величина артериального давления варьирует в широких пределах. У большинства больных с трансмуральным инфарктом миокарда систолическое артериальное давление снижается на 10—15 мм рт. ст. от исходного уровня.
Лабораторные исследования
Для подтверждения диагноза инфаркта миокарда служат следующие лабораторные показатели: 1) неспецифнческие показатели тканевого некроза и воспалительной реакции; 2) данные электрокардиограммы; 3) результаты изменения уровня ферментов сыворотки крови.
Проявлением неспецифической реактивности организма в ответ на повреждение миокарда является полиморфно-клеточный лейкоцитоз, который возникает в течение нескольких часов после появления ангинозной боли, сохраняется в течение 3—7 сут и часто достигает значений 12—15•109/л. СОЭ повышается не так быстро, как число лейкоцитов в крови, достигает пика в течение 1-й недели и иногда остается повышенной 1—2 нед.
Электрокардиографические проявления острого инфаркта миокарда подробно описаны в гл. 178. Хотя не всегда имеется четкая связь между изменениями на ЭКГ и степенью повреждения миокарда, однако появление патологического зубца Q или исчезновение зубца R обычно позволяет с большой вероятностью диагностировать трансмуральный инфаркт миокарда. О наличии нетрансмурального инфаркта миокарда говорят в тех случаях, когда на ЭКГ выявляются лишь транзиторные изменения сегмента ST и стойкие изменения зубца Т. Однако эти изменения весьма вариабельны и неспецифичны и поэтому не могут служить основой для диагностики острого инфаркта миокарда. В этой связи рациональная номенклатура для диагностики острого инфаркта миокарда должна лишь разграничивать последний на трансмуральный и нетрансмуральный в зависимости от наличия изменений зубца Q или волн ST—Т.
Сывороточные ферменты
Некротизированная во время острого инфаркта миокарда сердечная мышца выделяет в кровь большое количество ферментов. Скорость выброса различных специфических ферментов неодинакова. Изменение уровня ферментов в крови во времени имеет большую диагностическую ценность. Динамика концентрации ферментов, наиболее часто используемых для диагностики острого инфаркта миокарда, показана на рис. 190-1. Уровень двух ферментов, сывороточной глутаматоксалоацетаттрансаминазы (СГОТ) и креатинфосфокиназы (КФК) возрастает и снижается очень быстро, в то время как уровень лактатдегидрогеназы (ЛДГ) нарастает медленнее и дольше остается повышенным. Недостаток определения СГОТ заключается в том, что этот фермент содержится также в скелетных мышцах, в клетках печени, эритроцитах и может высвобождаться из этих экстракардиальных источников. Поэтому в настоящее время определение СГОТ для диагностики острого инфаркта миокарда используют реже, чем раньше, вследствие неспецифичности этого фермента и того, что динамика его концентрации занимает промежуточное положение между динамикой концентрации КФК и динамикой концентрации ЛДГ, в связи с чем информация об уровне СГОТ становится в большинстве случаев излишней. Определение содержания MB изофермента КФК имеет преимущества перед определением концентрации СГОТ, поскольку этот изофермент практически не определяется в экстракардиальной ткани и поэтому более специфичен, чем СГОТ. Поскольку подъем концентрации КФК или СГОТ определяется в течение короткого времени, он может оставаться незамеченным в тех случаях, когда образцы крови берут более чем через 48 ч после развития инфаркта миокарда. Определение MB—КФК имеет практический смысл в тех случаях, когда есть подозрение на повреждение скелетных мышц или ткани мозга, поскольку в них содержатся значительные количества этого фермента, но не его изофермента. Специфичность MB-изофермента для определения повреждения миокарда зависит от используемой методики. Наиболее специфичен радиоиммуноанализ, однако на практике тем не менее чаще используют электрофорез в геле, обладающий меньшей специфичностью и поэтому чаще дающий ложноположительные результаты. При остром инфаркте миокарда уровень ЛДГ повышается в первый же день, между 3-м и 4-м днем он достигает пика и в среднем через 14 дней возвращается к норме. При проведении электрофореза в крахмальном геле можно выделить пять изоферментов ЛДГ. Разные ткани содержат различные количества этих изоферментов. Изофермент, обладающий наибольшей электрофоретической подвижностью, в основном содержится в миокарде, его обозначают как ЛДГ). Изоферменты, обладающие наименьшей электрофоретической подвижностью, содержатся преимущественно в скелетной мускулатуре и в клетках печени. При остром инфаркте миокарда уровень ЛДГ1 повышается еще до того, как повышается уровень общей ЛДГ, т. е. может наблюдаться повышение содержания ЛДГ) при нормальном содержании общей ЛДГ. Следовательно, выявление повышенного уровня ЛДГ| является более чувствительным диагностическим тестом при остром инфаркте миокарда, чем уровень общей ЛДГ, его чувствительность превышает 95 %.
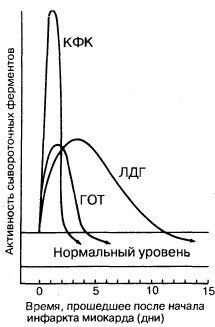
Рис. 190-1. Динамика сывороточных ферментов после типичного инфаркта миокарда.
КФК — креатинфосфокиназа; ЛДГ — лактатдегидрогеназа; ГОТ — глутаматрксалоацетаттрансаминаза.
Особую клиническую значимость представляет тот факт, что увеличенный в 2—3 раза уровень общей КФК (но не MB—КФК) может быть следствием внутримышечной инъекции. Возможны случаи парадоксальной диагностики острого инфаркта миокарда у больных, которым была сделана внутримышечная инъекция наркотика в связи с болями в грудной клетке, не связанными с патологией сердца. Кроме того, потенциальными источниками повышенного уровня КФК могут быть: 1) заболевания мышц, в том числе мышечные дистрофии, миопатии, полимиозиты; 2) электроимпульсная терапия (кардиоверсия); 3) катетеризация сердца; 4) гипотиреоидизм; 5) инсульт мозга; 6) хирургические вмешательства; 7) повреждения скелетных мышц при травмах, конвульсиях, длительной иммобилизации. Хирургические вмешательства на сердце и электроимпульсная терапия часто могут приводить к повышению уровня изофермента КФК.
Известно, что существует корреляция между количеством выброшенного в кровь фермента и размером инфаркта миокарда. Продемонстрировано, что масса миокарда, подвергшегося некрозу, может быть определена по кривой концентрация — время в том случае, если известны кинетика высвобождения фермента, его распада, распределения и пр. Анализ кривой концентрация — время для MB — КФК позволяет определить величину инфаркта миокарда в граммах. В то время как площадь под кривой изменения концентрации MB — КФК во времени отражает размеры инфаркта миокарда, абсолютные значения концентрации этого фермента и время до достижения максимума концентрации связаны с кинетикой вымывания MB — КФК из миокарда. Появление просвета в окклюзированной венечной артерии, происходящее либо спонтанно, либо под влиянием механического воздействия или фармакологических препаратов в ранние сроки острого инфаркта миокарда, вызывает быстрый рост концентрации фермента. Пик концентрации достигается через 1—3 ч после реперфузии. Общая площадь под кривой «концентрация — время» при этом может быть меньше, чем без реперфузии, что отражает меньшие размеры инфаркта миокарда.
Характерное возрастание концентрации ферментов наблюдается более чем у у 95 % больных с клинически доказанным инфарктом миокарда. При нестабильной стенокардии содержание КФК, ЛДГ, СГОТ обычно не повышается. У многих больных с подозрением на инфаркт миокарда исходный уровень ферментов в крови сохраняется в пределах нормы, при инфаркте миокарда он может повышаться в 3 раза, однако при этом он не превышает верхней границы нормы. Такую ситуацию наблюдают у больных с небольшим инфарктом миокарда. Хотя такое повышение содержания фермента нельзя рассматривать как строгий диагностический критерий острого инфаркта миокарда, оно с высокой вероятностью заставляет подозревать его. Практическую помощь в такой ситуации может оказать определение изоферментов.
Для диагностики острого инфаркта миокарда или оценки его тяжести могут оказаться полезными радионуклидные методы (гл. 179). Сцинтиграфию в острой фазе острого инфаркта миокарда (изображение «горячего пятна») выполняют с 99m’Тс-пирофосфатом, содержащим двухвалентное олово. Сканограммы обычно дают положительный результат со 2-го по 5-й день после начала инфаркта миокарда, чаще у больных с трансмуральным инфарктом миокарда. Несмотря на то что метод дает возможность определить локализацию инфаркта миокарда и его размеры (с. 887), в плане диагностики он менее точен, чем определение содержания КФК. Изображения миокарда с помощью таллия-201, который захватывается и концентрируется жизнеспособным миокардом, выявляет дефект перфузии («холодное пятно») у большинства больных в первые часы после развития трансмурального инфаркта миокарда. Эта локализованная область. сниженной радиоактивности может заполняться в течение последующих часов. Тем не менее дифференцировать острый инфаркт от старых Рубцовых изменений с помощью данного метода невозможно. Таким образом, сканирование таллием — весьма чувствительный метод для выявления инфаркта миокарда, однако оно неспецифично для острого инфаркта миокарда. Применяя радионуклидную вентрикулографию с эритроцитами, меченными 99mТе, у больных с острым инфарктом миокарда можно выявлять нарушения сократимости и снижение фракции выброса левого желудочка. Радионуклидная вентрикулография весьма ценна при оценке нарушенной гемодинамики при остром инфаркте миокарда и при необходимости установления диагноза инфаркта миокарда правого желудочка, когда снижается фракция выброса правого желудочка. Однако в целом специфичность этого метода низка, поскольку измененные радионуклидные вентрикулограммы регистрируют не только при остром инфаркте миокарда, но и при других патологических состояниях сердца.
В оценке состояния больных острым инфарктом миокарда может оказаться полезной также двухмерная эхокардиография. При этом можно легко выявить нарушения сократимости, в особенности в области перегородки и задненижней стенки. И хотя с помощью эхокардиографии нельзя дифференцировать острый инфаркт миокарда от нарушений сократимости вследствие наличия рубцов или выраженной острой ишемии миокарда, простота и безопасность этого метода позволяют рассматривать его как важный этап обследования больных с острым инфарктом миокарда. Кроме того, эхокардиография может быть весьма информативной для диагностики инфаркта миокарда правого желудочка, аневризмы левого желудочка и тромба в области левого желудочка.
Ведение больных с острым инфарктом миокарда
При остром инфаркте миокарда можно выделить два основных типа осложнений — это осложнения, обусловленные электрической нестабильностью (аритмии) и механические (насосная недостаточность). Наиболее частой причиной «аритмической» смерти при остром инфаркте миокарда служит фибрилляция желудочков. Большинство больных с фибрилляцией желудочков умирают в первые 24 ч после появления симптомов, а более половины из них — в течение первого часа. Хотя желудочковая экстрасистолия или желудочковая тахикардия нередко предшествуют фибрилляции желудочков. последняя может развиваться и без предшествующих аритмий. Это наблюдение дало повод использовать лидокаин для профилактики .спонтанной фибрилляции желудочков при остром инфаркте миокарда. Поэтому акцент лечебной тактики сместился от реанимационных мероприятий к предупреждению ситуаций, при которых возникает необходимость в подобных мероприятиях. Это привело к тому, что за последние два десятилетия частота первичной фибрилляции желудочков понизилась. Снижение смертности в больничных-условиях при остром инфаркте миокарда с 30 % до 10 % в значительной степени было результатом таких организационных мер, как быстрая доставка больных с острым инфарктом миокарда в лечебные учреждения, оборудованные устройствами для мониторирования ЭКГ и укомплектованные персоналом (не обязательно с высшим медицинским образованием), способным быстро распознать опасные для жизни желудочковые аритмии и сразу же назначить соответствующее лечение.
По мере того как уменьшилась частота внезапной смерти в стационаре вследствие адекватной профилактической антиаритмической терапии, на первый план стали выступать другие осложнения острого инфаркта миокарда, в частности недостаточность насосной функции миокарда. И, несмотря на достижения в лечении больных с острой сердечной недостаточностью, последняя в настоящее время является основной причиной смерти при остром инфаркте миокарда. Размер некротизированного вследствие ишемии участка коррелирует со степенью сердечной недостаточности и уровнем смертности, как в первые 10 дней, так и в более поздние сроки. Killip была предложена оригинальная клиническая классификация, основанная на оценке степени недостаточности функции сердца. Согласно этой классификации, больных подразделяют на четыре класса. В 1-й класс включены больные, не имеющие признаков легочного или венозного застоя; во 2-й класс — лица с умеренной сердечной недостаточностью, при которой в легких выслушиваются хрипы, в сердце—ритм галопа (Зз), имеются одышка, признаки недостаточности правых отделов сердца, включающие венозный и печеночный застой; в 3-й класс — больные с выраженной сердечной недостаточностью, сопровождающейся отеком легких; в 4-й класс — больные в состоянии шока с системным давлением ниже 90 мм рт. ст. и признаками констрикции периферических сосудов, с потливостью, периферическим цианозом, спутанностью сознания, олигурией. В некоторых исследованиях подсчитан риск госпитальной летальности для каждого из названных выше клинических классов Killip, он составляет для 1-го класса—0—5%, для 2-го—10—20%, для 3-го—35— 45 % и для 4-го — 85—90 %.
Общие соображения
Таким образом, основными принципами лечения больных с острым инфарктом миокарда является предупреждение смерти вследствие нарушений ритма и ограничение размеров инфаркта миокарда.
Нарушения ритма можно устранить при их появлении, если имеются квалифицированный медицинский персонал и соответствующее оборудование. Поскольку наибольшая смертность от аритмии наблюдается в первые несколько часов острого инфаркта миокарда, очевидно, что эффективность медицинской помощи в блоках интенсивной терапии зависит от того, как быстро больной из них доставлен. Основная задержка происходит не из-за недостатков в транспортировке больного в клинику, а вследствие того, что проходит достаточно много времени между началом болевого синдрома и принятием больным решения обратиться за медицинской помощью. Поэтому необходимо широко пропагандировать медицинские знания, разъясняя важность быстрого обращения за медицинской помощью при появлении болей в грудной клетке.
При лечении больных с острым инфарктом миокарда существует ряд общих правил, на которых следует остановиться особо. Первое и самое главное — стремиться поддерживать оптимальный баланс между снабжением миокарда кислородом и потребностью в нем с целью максимального сохранения жизнеспособности миокарда в зоне, окружающей очаг некроза. Для этого необходимо обеспечить больному покой, назначить обезболивающие средства и умеренную седативную терапию, создать спокойную атмосферу, способствующую уменьшению частоты сердечных сокращений, -основной величины, определяющей потребности миокарда в кислороде.
При выраженной синусовой брадикардии (частота сердечных сокращений менее 45 в 1 мин) следует поднять нижние конечности больного и ввести атропин, либо провести электрическую стимуляцию. Последняя предпочтительна в тех случаях, когда брадикардия сопровождается падением артериального давления или учащением желудочковых аритмий. Без выраженной брадикардии не следует -назначать больным атропин, поскольку это может привести к значительному учащению пульса. Больным с острым инфарктом миокарда с наличием тахикардии и повышенным артериальным давлением следует назначать. адреноблокаторы. Вначале внутривенно вводят 0,1 мг/кг пропранолола (анаприлин) или 15 мг метопролола, причем эту дозу делят на три равные части и вводят последовательно. Такое назначение этих препаратов безопасно, если не вызывает осложнений, таких как сердечная недостаточность, атриовентрикулярная блокада, бронхиальная астма. При всех формах тахиаритмий требуются незамедлительное и конкретное лечение. Препараты, обладающие положительным ннотропным действием, такие как сердечные гликозиды, воздействующие на сердечную мышцу симпатомиметики, следует назначать лишь при выраженной сердечной недостаточности и ни в коем случае с профилактической целью. Если имеются различные симпатомиметические амины, следует помнить, что введение изопротеренола, обладающего выраженным хронотропным и вазодилатирующим действием, наименее желательно. Добутамин, в меньшей степени влияющий на частоту сердечных сокращений и периферическое сосудистое сопротивление, предпочтителен в тех случаях, когда необходимо увеличить сердечную сократимость. Допамин оказывает положительное действие у больных с левожелудочковой недостаточностью и системной гипотонией (систолическое давление менее 90 мм рт. ст.). Диуретики показаны при сердечной недостаточности, в этих случаях их применяют до назначения кардиостимулирующих препаратов, если только нет признаков гиповолемии и гипотензии.
Всем больным нужно проводить ингаляцию воздуха, обогащенного кислородом (см. ниже). Особое внимание следует уделить сохранению адекватной оксигенации крови и у больных с гипоксемией, которая может наблюдаться в случае хронических заболеваний легких, пневмонии, недостаточности левого желудочка. При выраженной анемии, которая может способствовать расширению очага ишемии, следует осторожно вводить эритроцитную массу, иногда в комбинации с диуретиками. Сопутствующие заболевания, в частности инфекционные, сопровождающиеся тахикардией и повышенной потребностью миокарда в кислороде, также требуют немедленного внимания. Необходимо следить за тем, чтобы колебания систолического артериального давления не превышали 25 — 30 мм рт. ст. от обычного для больного уровня.
Блоки интенсивной коронарной помощи. Такие блоки предназначены для оказания помощи больным с острым инфарктом миокарда с целью уменьшить смертность среди больных и повысить знания об остром инфаркте миокарда. Блоки интенсивной терапии (БИТ) представляют собой пункты медсестринского наблюдения, укомплектованные высококвалифицированным опытным медицинским персоналом, способным оказать немедленную помощь в экстренных случаях. Такой блок должен быть оборудован системами, позволяющими осуществлять постоянное наблюдение за ЭКГ у каждого больного и мониторирование параметров гемодинамики у больных, иметь необходимое число дефибрилляторов, приборов для искусственной вентиляции легких, а также устройства для введения электролитов для кардиостимуляции и плавающие катетеры с раздувающимися баллончиками на конце. Однако наиболее важным является наличие высококвалифицированной команды среднего медицинского персонала, способной распознавать аритмии, проводить адекватное назначение антиаритмических препаратов и выполнять сердечно-сосудистую реанимацию, включая электроимпульсную терапию в тех случаях, когда она необходима. Необходимо также, чтобы всегда имелась возможность получить консультацию врача. Однако следует заметить, что средним медицинским персоналом было спасено много жизней в результате своевременной коррекции аритмий еще до прихода врача.
Наличие блоков интенсивной терапии делает возможным оказание помощи больным в максимально ранние сроки при остром инфаркте миокарда, когда медицинская помощь может быть наиболее эффективной. Для достижения этой цели следует расширять показания к госпитализации и помещать в блоки интенсивной терапии больных даже с подозрением на острый инфаркт миокарда. Проверить выполнение этой рекомендации очень легко. Для этого достаточно установить число больных с доказанным диагнозом острого инфаркта миокарда среди всех лиц, поступивших в блок интенсивной терапии. Со временем, однако, в силу ряда причин это правило было нарушено. Доступность ЭКГ-мониторирования и наличие высококвалифицированного персонала в так называемых промежуточных блоках наблюдения позволили госпитализировать в них так называемых больных невысокого риска (с отсутствием нарушений гемодинамики и без нарушений ритма). С целью экономии и оптимального использования имеющейся аппаратуры многие институты разработали методические рекомендации по оказанию помощи больным и выборе пациентов с подозрением на острый инфаркт миокарда. В США большинство таких больных госпитализируют, в других странах, например в Великобритании, больных с небольшим риском лечат на дому. Среди доставленных в стационар больных с острым инфарктом миокарда число больных, направленных в блоки интенсивной терапии, определяют как по их состоянию, так и по числу коек в блоках. В некоторых клиниках койки в блоках интенсивного наблюдения первично отводят для больных с осложненным течением заболевания, особенно для тех, кому требуется мониторирование гемодинамики. Уровень смертности в блоках интенсивного наблюдения 5—20%. Такая вариабельность отчасти объясняется различием в показаниях к госпитализации, возрастом больных, особенностями клиники, а также другими неучтенными факторами.
Реперфузия
Причиной большинства трансмуральных инфарктов миокарда является тромб, расположенный либо свободно в просвете сосуда, либо прикрепившийся к атеросклеротической бляшке. Поэтому логически обоснованным подходом к уменьшению размеров инфаркта миокарда служит достижение реперфузии с помощью быстрого растворения тромба тромболитическим препаратом. Доказано, что, для того чтобы реперфузии была эффективной, т. е. способствовала сохранению ишемизированного миокарда, ее следует проводить в короткие сроки после появления клинических симптомов, а именно в течение 4 ч, а лучше 2 ч.
Для лечения больных с острым инфарктом миокарда Управление санитарного надзора за качеством пищевых продуктов и медикаментов считает возможным введение стрептокиназы (СК) через катетер, установленный в венечной артерии. Несмотря на то, что с помощью СК удается лизировать тромб, служащий причиной инфаркта в 95 % случаев, некоторые вопросы, связанные с применением этого препарата, остаются нерешенными. В частности, неизвестно, способствует ли назначение СК уменьшению смертности. Внутривенное введение СК менее эффективно, чем внутрикоронарное, однако оно имеет большое преимущество, так как не требуется катетеризации венечных артерий. Преимущество перед СК теоретически имеет тканевый активатор плазминогена, он лизирует примерно 2/3 свежих тромбов. Вводимый внутривенно, он должен проявлять лизирующее действие в месте свежего тромбоза и в результате этого обладать менее выраженным системным тромболитическим действием. Однако даже если иметь в виду идеальный тромболитический .препарат, то неизвестно, будет ли он при рутинном назначении действительно способствовать сохранению ишемизированного миокарда, уменьшению потребности в проведении механической реваскуляризации с помощью коронарной ангиопластики и аортокоронарного шунтирования и существенному, снижению смертности больных с острым инфарктом миокарда. В настоящее время проводятся исследования, способные дать ответ на эти вопросы. В то время, когда пишутся эти строки. тканевый активатор плазминогена еще недоступен для широкого клинического применения и его назначение еще не одобрено Биологическим Бюро. Оптимальной тактикой лечения при выраженной обструкции (более 80 % просвета венечной артерии) следует считать внутривенное введение стрептокиназы в ранние сроки острого инфаркта миокарда (менее 4 ч после начала болевого синдрома) или, при возможности, внутрикоронарное введение стрептокиназы в такие же сроки, а затем проведение чрескожной транслюминальной коронарной ангиопластики (ЧТКА). Однако необходимость иметь квалифицированную ангиографическую бригаду, находящуюся в постоянной готовности, делает возможным применение такой тактики лечения лишь у небольшого числа больных с острым инфарктом миокарда. Однако если исследования, проводящиеся в настоящее время, покажут, что внутривенное введение тканевого активатора плазминогена с последующим проведением коронароангиографии (через 1 — 2 дня) и выполнением при необходимости ЧТКА позволяет существенно уменьшить повреждение миокарда у большинства больных, будет найден практический подход к лечению больных с острым инфарктом миокарда. Тогда тканевый активатор плазминогена будут вводить внутривенно сразу же после постановки диагноза острого инфаркта миокарда, причем это введение можно будет осуществлять как в блоке интенсивного наблюдения, так и в машине скорой помощи, поликлинике и даже по месту жительства или работы больного. После этого больного поместят в клинику, где в течение 2 дней ему будет проведена коронарография и при необходимости ЧТКА. При таком подходе требуется персонал не столь высокой квалификации, а также не такое сложное оборудование.
Сообщалось, что неотложная первичная ЧТКА при остром инфаркте миокарда, т. е. ЧТКА, проведенная без предшествующего тромболизиса, также может быть эффективна в плане восстановления достаточной реперфузии, однако эта процедура весьма дорогостоящая, поскольку в этом случае требуется постоянная готовность квалифицированного персонала и сложное оборудование.
Площадь миокарда, подвергающегося некрозу вторично вследствие сосудистой окклюзии, определяется не столько локализацией этой окклюзии, сколько состоянием коллатерального кровотока в ишемизированных тканях. Миокард, хорошо снабжающийся кровью коллатералями, во время ишемии способен оставаться жизнеспособным на несколько часов больше, чем миокард со слабо выраженной коллатеральной сетью. В настоящее время известно, что со временем размер инфаркта миокарда может меняться под влиянием назначаемых препаратов. Баланс между снабжением миокарда кислородом и потребностью в нем ишемизированных участков в конечном счете определяет судьбу этих участков во время острого инфаркта миокарда. Хотя в настоящее время нет общепринятого терапевтического подхода, способствующего уменьшению размеров инфаркта миокарда у всех больных, осознание того факта, что его размеры могут увеличиваться под влиянием ряда препаратов, неблагоприятно влияющих на соотношение между потребностью миокарда в кислороде и его доставкой, привело к переоценке ряда терапевтических подходов к лечению больных с острым инфарктом миокарда.
Лечение больного с неосложненным инфарктом
Аналгезия. Поскольку острый инфаркт миокарда чаще всего сопровождается сильным болевым синдромом, купирование боли — это один из важнейших приемов терапии. С этой целью чрезвычайно эффективен традиционно использующийся морфин. Однако он может снижать артериальное давление в результате уменьшения артериолярной и венозной констрикции, опосредованной через симпатическую нервную систему. Развивающееся вследствие этого депонирование крови в венах приводит к уменьшению сердечного выброса. Это следует иметь в виду, но это не обязательно свидетельствует о противопоказаниях к назначению морфина. Гипотензия, возникающая в результате депонирования крови в венах, как правило, быстро устраняется при поднятии нижних конечностей, хотя некоторым больным может потребоваться введение физиологического раствора. Больной может также ощущать потливость, тошноту, однако эти явления обычно проходят самопроизвольно.
Кроме того, благоприятный эффект от купирования болевого синдрома, как правило, превалирует над этими неприятными ощущениями. Важно отличать эти побочные действия морфина от сходных проявлений шока, чтобы не назначать без необходимости терапию вазоконстрикторами. Морфин обладает ваготоническим действием и может вызвать брадикардию или блокаду сердца высокой степени, особенно у больных с нижнезадним инфарктом миокарда. Эти побочные действия морфина можно устранить внутривенным введением атропина в дозе 0,4 мг. Морфин предпочтительно назначать небольшими (2 — 4 мг) дробными дозами каждые 5 мин внутривенно, а не в больших количествах подкожно, поскольку в последнем случае его абсорбция может привести к непредсказуемым последствиям. Вместо морфина можно с успехом использовать мепередина гидрохлорид или гидроморфона гидрохлорид.
Перед тем как начать терапию морфином, большинству больных с острым инфарктом миокарда можно назначать нитроглицерин под язык. Обычно 3 таблетки по 0,3 мг, которые назначают с 5-минутными интервалами, достаточно для развития у больного гипотензии. Такая терапия нитроглицерином, ранее считавшаяся противопоказанной при остром инфаркте миокарда, может способствовать как уменьшению потребности миокарда в кислороде (за счет уменьшения преднагрузки), так и увеличению доставки кислорода к миокарду (за счет дилатации венечных сосудов или коллатеральных сосудов в области инфаркта). Однако не следует назначать нитраты больным с низким систолическим артериальным давлением (менее 100 мм рт. ст.). Надо помнить о возможной идиосинкразии на нитраты, заключающейся во внезапном снижении давления и брадикардии. Это побочное действие нитратов, возникающее чаще всего у больных с нижним инфарктом миокарда, удается устранить внутривенным введением атропина.
Для устранения болевого синдрома при остром инфаркте миокарда можно также внутривенно вводить. адреноблокаторы. Эти препараты надежно купируют боль у некоторых больных, в основном в результате уменьшения ишемии вследствие снижения потребности миокарда в кислороде. Доказано, что при внутривенном введении. адреноблокаторов снижается внутрибольничная летальность, особенно среди больных с высокой степенью риска. Назначают р-адреноблокаторы в тех же дозах, что и при гипердинамическом состоянии (см. выше).
Кислород. Рутинное применение кислорода при остром инфаркте миокарда обосновывают тем, что артериолярное Рог снижено у многих больных, а ингаляция кислорода уменьшает по экспериментальным данным размеры ишемического повреждения. Ингаляция кислорода увеличивает артериолярное Рог и за счет этого увеличивает градиент концентрации, необходимой для диффузии кислорода в область ишемизированного миокарда из прилежащих, лучше перфузируемых зон. Хотя терапия кислородом теоретически может вызвать нежелательные эффекты, например, повышение периферического сосудистого сопротивления, и небольшое снижение сердечного выброса, практические наблюдения оправдывают его применение. Кислород назначают через свободную маску или носовой наконечник в течение одного-двух первых дней острого инфаркта миокарда.
Физическая активность. Факторы, увеличивающие работу сердца, могут способствовать увеличению размеров инфаркта миокарда. Следует избегать обстоятельств, способствующих увеличению размеров сердца, сердечного выброса, сократимости миокарда. Было показано, что для полного заживления, т. е. замещения области инфаркта миокарда рубцовой тканью, требуется 6 — 8 нед. Наиболее благоприятные условия для такого заживления обеспечивает снижение физической активности.
Большинство больных с острым инфарктом миокарда следует помещать в блоки интенсивной терапии и проводить мониторирование. Наблюдение за больными и постоянное ЭКГ-мониторирование должно продолжаться 2 — 4 дня. В периферическую вену вводят катетер и жестко закрепляют так, чтобы избежать его смещения. Через катетер следует постоянно медленно вводить изотонический раствор глюкозы либо промывать его гепарином. Такой катетер дает возможность при необходимости вводить антиаритмические или другие препараты. При отсутствии сердечной недостаточности и других осложнений в течение первых 2 — 3 дней больной должен большую часть дня находиться в постели и 1 — 2 раза присаживаться на 15—30 мин на прикроватный стул. Для дефекации используют судно. Больного следует подмывать. Принимать пищу он может самостоятельно. Использование прикроватного стульчака допускается у всех гемодинамически стабильных больных со стабильным ритмом, начиная с 1-го дня. Кровать должна быть оборудована подножкой, и больной должен жестко толкать обеими ногами эту подножку по 10 раз в час в течение дня для предупреждения венозного стаза и тромбоэмболии, а также для поддержания мышечного тонуса в ногах.
К 3—4-му дню больные с неосложненным инфарктом миокарда должны сидеть на стуле по 30—60 мин 2 раза в день. В это время им измеряют артериальное давление для выявления возможной постуральной гипотензии, которая может стать проблемой, как только больной начнет ходить. При неосложненном инфаркте миокарда вставать и постепенно начинать ходить больному разрешают между 3-м и 5-м днем. Сначала разрешают пройти до ванной комнаты, если она находится в палате больного или рядом. Время ходьбы постепенно увеличивают и в конце концов разрешают прогулки по коридору. Во многих клиниках существуют специальные программы сердечно-сосудистой реабилитации с постепенным увеличением нагрузки, начинающиеся в стационаре и продолжающиеся после выписки больного. Продолжительность госпитализации при неосложненном инфаркте миокарда составляет 7— 12 дней, однако некоторые врачи по-прежнему считают необходимым госпитализацию больных с Q-инфарктом миокарда в течение 3 нед. Больным с клиническим классом II или более может потребоваться госпитализация в течение 3 нед и более. Продолжительность лечения в стационаре зависит от того, как быстро исчезает сердечная недостаточность и какие домашние условия ожидают больного после выписки. Многие врачи считают необходимым проведение у некоторых больных теста с физической нагрузкой (ограниченного достижением определенной частоты сердечных сокращений) перед выпиской из стационара. С помощью такого теста удается выявить больных из группы высокого риска, т. е. тех, у которых во время нагрузки или сразу после нее появляется приступ стенокардии, возникают изменения сегмента ST, гипотония или желудочковая экстрасистолия высоких градаций. Этим больным требуется особое внимание. Им необходимо назначать антиаритмические препараты для борьбы с нарушениями ритма и. адреноблокаторы, нитраты пролонгированного действия или антагонисты кальция для предупреждения ишемии миокарда. Если у больных возникает ишемия ,в покое или при очень небольшой физической нагрузке или если имеется гипотония, следует проводить коронароангиографию (КАГ). Если при этом обнаруживается, что большая площадь жизнеспособного миокарда кровоснабжается артерией, имеющей критическое сужение, то может потребоваться реваскуляризация с помощью операции аортокоронарного шунтирования (АКШ) или коронарной ангиопластики. Проведение теста с физической нагрузкой помогает также разработать индивидуализированную программу физических тренировок, которая должна быть более интенсивной у больных, у которых переносимость нагрузки лучше и отсутствуют отмеченные выше неблагоприятные признаки. Проведение теста с физической нагрузкой перед выпиской из стационара помогает больному самому убедиться в своих физических возможностях. Более того, в тех случаях, когда во время теста с физической нагрузкой не возникают аритмии или не проявляются признаки ишемии миокарда, врачу легче убедить больного в отсутствии объективных признаков непосредственной опасности для жизни или здоровья.
Заключительная фаза реабилитации больного после острого инфаркта миокарда проводится в домашних условиях. С 3-й по 8-ю неделю больной должен увеличивать объем физической активности за счет прогулок по дому, в хорошую погоду выходить на улицу. Больной по-прежнему должен ночью спать не менее 8 — 10 ч. Кроме того, для некоторых больных полезны дополнительные периоды сна в утреннее и дневное время.
С 8-й недели врач должен регулировать физическую активность больного, исходя из его толерантности к физической нагрузке. Именно в этот период увеличение физической активности больного может стать причиной общей выраженной усталости. По-прежнему может сохраняться проблема постуральной гипотензии. Большинство больных способны вернуться к работе через 12 нед, а некоторые больные — и раньше. Перед тем, как больной вновь приступит к работе (через 6—8 нед), часто проводят тест с максимальной физической нагрузкой. В последнее время наметилась тенденция к более ранней активизации больных, более ранней выписке их из стационара и более быстрому восстановлению полной физической активности больных, перенесших острый инфаркт миокарда.
Диета. В течение первых 4—5 дней больным предпочтительно назначать низкокалорийную диету, пищу принимать небольшими дробными дозами, так как после приема пищи наблюдается увеличение сердечного выброса. При сердечной недостаточности необходимо ограничить потребление натрия. Поскольку больные часто страдают запорами, вполне обоснованно в рационе питания увеличить долю растительных продуктов, содержащих большое количество пищевых волокон. Кроме того, больным, получающим диуретики, следует рекомендовать продукты с высоким содержанием калия. В течение 2-й недели объем потребляемой пищи можно увеличивать. В это время больному необходимо объяснить важность ограничения калорийности диеты, содержания холестерина, насыщенных липидов. Это необходимо для того, чтобы больной сознательно соблюдал рациональный режим питания. Желания правильно питаться, бросить курить редко бывают более выраженными, чем в этот ранний период реабилитации после острого инфаркта миокарда.
Непривычное положение в постели в первые 3—5 дней болезни и действие наркотических анальгетиков, использующихся для купирования боли, часто приводят к запорам. Большинство больных с трудом могут пользоваться судном, вызывающим у них избыточное натуживание, поэтому рекомендуют использовать прикроватные стульчаки. Диета, богатая растительными продуктами, содержащими большое количество пищевых волокон, и слабительные средства, например, диоктил сульфосукцинат натрия (Dioctyl sodium sulfosuccinase) в дозе по 200 мг в день также способствуют профилактике запоров. Если, несмотря на перечисленные выше меры, запоры сохраняются, следует рекомендовать слабительные препараты. При остром инфаркте миокарда возможно провести аккуратное пальцевое массирование. прямой кишки.
Седативная терапия. Большинству больных с острым инфарктом миокарда во время госпитализации требуется назначение седативных средств, помогающих лучше перенести период вынужденного снижения активности, — диазепама по 5 мг или оксазепама по 15 — 30 мг 4 раза в день. Для обеспечения нормального сна показаны снотворные препараты. Наиболее эффективен триазолам (Triazolam) (из группы бензодиазепинов короткого действия) в дозе 0,25—0,5 мг. При необходимости обеспечить длительный снотворный эффект можно назначать темазепам (Temazepam) по 15—30 мг или флюразепам (Flurazepam) в той же дозе. Этой проблеме следует уделять особое внимание в первые несколько дней пребывания больного в БИТе, где состояние круглосуточного бодрствования может привести к нарушению сна в дальнейшем. Следует помнить, однако, что седативная терапия ни в коем случае не заменяет необходимости создания благоприятного психологического климата вокруг больного.
Антикоагулянты. Наиболее противоречивые мнения высказываются о необходимости рутинного применения антикоагулянтов при остром инфаркте миокарда (ОИМ). Однако отсутствие аргументированных статистически обоснованных подтверждений снижения летальности при применении антикоагулянтов в первые несколько недель ОИМ свидетельствует о том, что польза от этих препаратов невелика, а может быть, отсутствует вообще. Терапия антикоагулянтами для замедления процесса коронарной окклюзии в начальной фазе заболевания в настоящее время не имеет четких обоснований, однако в настоящее время она вновь привлекает интерес, т. е. признано, что тромбоз играет важную роль в патогенезе ОИМ. Признано, однако, что терапия антикоагулянтами безусловно снижает частоту тромбоэмболии как в артериях, так и в венах. Поскольку известно, что частота венозной тромбоэмболии увеличивается у больных с сердечной недостаточностью, шоком, наличием венозных тромбоэмболии в анамнезе, таким больным во время нахождения в БИТах рекомендуется рутинное, профилактическое применение антикоагулянтов. Рутинное назначение антикоагулянтов для профилактики венозной тромбоэмболии не рекомендуется больным, относящимся к I классу. У больных III и IV классов риск тромбоэмболии легочной артерии повышен, поэтому им рекомендуют проводить системную антикоагуляцию в течение первых 10—14 дней госпитализации или до выписки их из стационара. Это лучше всего достигается при постоянной внутривенной инфузии гепарина с помощью насоса. При этом необходимо измерять время свертывания и частичное тромбопластиновое время, чтобы регулировать скорость введения препарата, увеличивая или уменьшая ее. После того как больного переводят из БИТа, гепарин заменяют пероральными антикоагулянтами. Допустимо применять малые дозы гепарина в виде подкожных инъекций (5000 ЕД каждые 8—12 ч). Противоречия существуют по поводу лечения антикоагулянтами больных II класса. Им представляется целесообразным назначать антикоагулянты в тех случаях, когда застойная сердечная недостаточность существует более 3—4 дней или когда имеется обширный передний инфаркт миокарда.
Возможность артериальной эмболии тромбом, находящимся в желудочке в зоне инфаркта миокарда, хотя и невелика, но весьма определенна. Двухмерная эхокардиография (ЭХО-КГ) позволяет достаточно рано выявить тромбы в области левого желудочка примерно у 30 % больных с инфарктом передней стенки левого желудочка, однако редко бывает информативной у больных с нижним или задним инфарктом миокарда. Основным осложнением артериальной эмболии является гемипарез при вовлечении в процесс сосудов мозга и артериальная гипертензия при вовлечении в процесс сосудов почек. Невысокая частота этих осложнений контрастирует с их тяжестью, делает нецелесообразным установление жестких правил применения антикоагулянтов для профилактики артериальной эмболии при остром инфаркте миокарда. Вероятность тромбоэмболии возрастает с увеличением распространенности инфаркта миокарда, степени сопутствующих воспалительных реакций и эндокардиального стаза вследствие акинезии. Поэтому, как и в случае венозной тромбоэмболии, показания для применения антикоагулянтов для профилактики артериальной эмболии расширяются с увеличением размеров острого инфаркта миокарда. В тех случаях, когда наличие тромба четко диагностируется с помощью ЭХО-КГ или другими методами, показано проведение системной антикоагуляции (в отсутствие противопоказаний), поскольку частота тромбоэмболических осложнений при этом существенно снижается. Точная продолжительность терапии антикоагулянтами неизвестна, однако, по-видимому, она должна составлять 3 — 6 мес.
Адреноблокаторы. Внутривенное введение. адреноблокаторов (БАБ) обсуждается выше. Хорошо выполненные плацебо-контролируемые исследования подтвердили необходимость рутинного назначения БАБ внутрь по крайней мере в течение 2 лет после острого инфаркта миокарда. Снижаются общая смертность, частота внезапной смерти и в ряде случаев повторного инфаркта миокарда под влиянием БАБ. Прием БАБ обычно начинают через 5 — 28 дней после начала острого инфаркта миокарда. Обычно назначают пропранолол (анаприлин) в дозе 60 — 80 мг 3 раза в день или другие, действующие более медленно БАБ, в эквивалентных дозах. Противопоказаниями к назначению БАБ служат застойная сердечная недостаточность, брадикардия, блокада сердца, гипотония, астма и лабильный инсулинзависимый сахарный диабет.
Лечение
Аритмии (см. также гл. 183 и 184). Успехи в коррекции аритмий представляют собой наиболее значительное достижение в лечении больных с инфарктом миокарда.
Преждевременные желудочковые сокращения (желудочковые экстрасистолы). Редкие спорадические желудочковые экстрасистолы возникают у большинства больных с острым инфарктом миокарда и не требуют специального лечения. Обычно считается, что антиаритмическая терапия при желудочковой экстрасистолии должна назначаться в следующих случаях: 1) наличие более 5 одиночных желудочковых экстрасистол в 1 мин.; 2) возникновение групповых или политопных желудочковых экстрасистол; 3) возникновение желудочковых экстрасистол в фазу ранней диастолы, т. е. накладывающихся на зубец Т предыдущего комплекса (т. е. феномен R на Т).
Внутривенное введение лидокаина стало лечением выбора при желудочковой экстрасистолии и желудочковых аритмиях, так как препарат начинает действовать быстро и так же быстро исчезают побочные эффекты (в течение 15— 20 мин после прекращения введения). Для быстрого достижения терапевтической концентрации в крови лидокаин назначают в виде болюса 1 мг/кг внутривенно. Эта начальная доза может устранить эктопическую активность, а затем для поддержания эффекта проводят постоянную инфузию со скоростью 2 — 4 мг/мин. Если аритмия сохраняется, через 10 мин после введения первого болюса вводят второй в дозе 0,5 мг/кг. У больных с застойной сердечной недостаточностью, заболеваниями печени, шоком дозу лидокаина уменьшают вдвое. Как правило, желудочковая экстрасистолия исчезает спонтанно через 72—96 ч. В том случае, если значительная желудочковая аритмия сохраняется и после этого, назначают длительную антиаритмическую терапию.
Для лечения больных с постоянными желудочковыми аритмиями обычно используют новокаинамид, токайнид (Tocainide), хинидин. БАБ и дизопирамид также устраняют желудочковые нарушения ритма у больных с острым инфарктом миокарда. Больным с левожелудочковой недостаточностью дизопирамид назначают с большой осторожностью, так как он обладает существенным отрицательным инотропным действием. Если эти средства (гл. 184), используемые в виде монотерапии или в комбинациях, неэффективны в обычных дозах, следует определить их концентрацию в крови. При назначении больших доз этих препаратов необходим регулярный клинический и ЭКГ-контроль для выявления возможных признаков интоксикации.
Желудочковая тахикардия и фибрилляция желудочков. В течение первых 24 ч ОИМ желудочковая тахикардия (ЖТ) и фибрилляция желудочков (ФЖ) часто возникают без предшествующих им угрожающих нарушений ритма. Риск развития таких первичных аритмий может быть существенно уменьшен с помощью профилактического внутривенного введения лидокаина. Профилактическое назначение антиаритмических препаратов особенно показано больным, которые не могут быть помещены в клинику, или находятся в клинике, где в БИТе не обеспечено постоянное присутствие врача. При продолжительной желудочковой тахикардии в первую очередь назначают лидокаин. Если после одного-двух введений препарата в дозе 50—100 мг аритмия сохраняется, проводят электроимпульсную терапию (электрокардиоверсия) (гл. 184). Электрическую дефибрилляцию проводят сразу же при фибрилляции желудочков, а также в тех случаях, когда желудочковая тахикардия вызывает нарушения гемодинамики. Если фибрилляция желудочков продолжается несколько секунд и более, первый разряд дефибриллятора может быть безуспешным, в этих случаях перед проведением повторной кардиоверсии желательно осуществить непрямой массаж сердца, искусственную вентиляцию легких «изо рта в рот», а также внутривенно ввести бикарбонат натрия (40—90 мэкв). Улучшение оксигенации и перфузии тканей и коррекция ацидоза увеличивают вероятность успешной дефибрилляции (см. также гл. 30). При рефрактерных к терапии фибрилляции желудочков или желудочковой тахикардии может быть эффективным введение бретилия (орнид). При фибрилляции желудочков бретилий назначают в виде болюса в 5 мг/кг, затем повторяют дефибрилляцию. Если последняя не приносит результата, для облегчения дефибрилляции вводят еще один болюс бретилия (10 мг/кг). Желудочковую тахикардию можно устранить медленным введением бретилия в дозе 10 мг/кг в течение 10 мин. При рецидивах аритмий после введения первой дозы бретилия можно осуществить постоянную его инфузию в дозе 2 мг/мин. После внутривенного введения бретилия может возникнуть выраженная ортостатическая гипотензия. Поэтому во время и после введения препарата больные должны находиться в положении лежа, кроме того, следует быть готовым к внутривенному введению жидкостей.
При первичной фибрилляции желудочков длительный прогноз благоприятный. Это означает, что первичная фибрилляция желудочков является следствием острой ишемии и не связана с наличием таких предрасполагающих к ней факторов, как застойная сердечная недостаточность, блокада ножек пучка Гиса, аневризма левого желудочка. По данным одного из исследований, 87 % больных с первичной фибрилляцией желудочков остались живы и были выписаны из клиники. Прогноз у больных с вторичной фибрилляцией желудочков, развившейся вследствие недостаточной насосной функции сердца, гораздо менее благоприятный. Лишь 29 % из них остаются в живых.
В группе больных, у которых желудочковая тахикардия развивается в поздние, сроки госпитализации, смертность в течение года достигает 85%. Таким больным необходимо проведение электрофизиологического исследования (гл. 184).
Ускоренный идиовентрикулярный ритм. Ускоренный идиовентрикулярный ритм («медленная желудочковая тахикардия») — это желудочковый ритм с частотой от 60 до 100 в 1 мин. Он возникает у 25 % больных с инфарктом миокарда. Чаще всего он регистрируется у больных с нижнезадним инфарктом миокарда и, как правило, в сочетании с синусовой брадикардией. Частота сердечных сокращений при ускоренном идиовентрикулярном ритме аналогична таковой при синусовом ритме, предшествующем ему или следующем за ним. Ускоренный идиовентрикулярный ритм трудно диагностировать клинически, его выявляют лишь с помощью ЭКГ-мониторирования. Это связано с тем, что частота сокращений желудочков мало отличается от таковой при синусовом ритме, а нарушения гемодинамики минимальны. Ускоренный идиовентрикулярный ритм возникает и исчезает спонтанно по мере того, как колебания синусового ритма вызывают замедление ритма предсердий ниже ускоренного ускользающего уровня. В целом ускоренный идиовентрикулярный ритм является доброкачественным нарушением ритма и не знаменует собой начало классической желудочковой тахикардии. Однако зарегистрирован ряд случаев, когда ускоренный идиовентрикулярный ритм сочетался с более опасными формами желудочковых аритмий или трансформировался в жизненно опасные желудочковые нарушения ритма. Большинство больных с ускоренным идиовентрикулярным ритмом не требуют лечения. Достаточно тщательного мониторирования ЭКГ, поскольку ускоренный идиовентрикулярный ритм редко переходит в более серьезные нарушения ритма. Если же последнее все’ же случается, ускоренный идиовентрикулярный ритм может быть легко устранен с. помощью препаратов, уменьшающих частоту выскальзывающего желудочкового ритма, например токаинида, и/или препаратов, учащающих синусовый ритм (атропин).
Суправентрикулярная аритмия. В этой группе больных чаще всего возникают такие суправентрикулярные аритмии, как узловой ритм и узловая тахикардия, предсердная тахикардия, трепетание и мерцание предсердий. Эти нарушения ритма чаще всего являются вторичными по отношению к левожелудочковой недостаточности. Для лечения больных обычно используют дигоксин. Если патологический ритм сохраняется в течение более двух часов и частота желудочковых сокращений при этом превышает 120 в 1 мин или если тахикардия сопровождается появлением сердечной недостаточности, шока или ишемии (о чем свидетельствуют повторные боли или изменения на ЭКГ), то показано проведение электроимпульсной терапии.
Узловые нарушения ритма имеют различную этиологию, они не свидетельствуют о наличии какой-то специфической патологии, поэтому отношение врача к подобным больным должно быть индивидуализированным. Необходимо исключить передозировку дигиталиса как причину узловых аритмий. У некоторых больных со значительно нарушенной функцией левого желудочка утрата нормальной продолжительности систолы предсердий приводит к значительному падению сердечного выброса. В таких случаях показано проведение предсердной стимуляции или стимуляции венечного (коронарного) синуса. Гемодинамическое действие стимуляции этих двух видов идентичное, однако преимущество стимуляции венечного (коронарного) синуса состоит в том, что при этом достигается более стабильное положение катетера.
Синусовая брадикардия. Мнения о значении брадикардии как фактора, предрасполагающего к развитию фибрилляции желудочков, противоречивы. С одной стороны, известно, что частота желудочковой тахикардии у больных с продолжительной синусовой брадикардией в 2 раза больше, чем у больных с нормальной частотой сердечных сокращений. С другой стороны, синусовую брадикардию у госпитализированных больных рассматривают как показатель благоприятного прогноза. Опыт использования передвижных блоков интенсивной кардиологической помощи свидетельствует о том, что синусовая брадикардия, возникающая в первые часы острого инфаркта миокарда, более определенно связана с появлением в последующем эктопических желудочковых ритмов, чем синусовая брадикардия, возникающая в более поздние сроки острого инфаркта миокарда. Лечение при синусовой брадикардии следует проводить в тех случаях, когда (на ее фоне) имеется выраженная эктопическая активность желудочков или когда она вызывает нарушения гемодинамики. Устранить синусовую брадикардию можно, слегка приподняв ноги больного или ножной конец кровати. Для ускорения синусового ритма лучше всего использовать атропин, вводя его внутривенно в дозе 0,4 — 0,6 мг. Если после этого сохраняется пульс менее 60 ударов в 1 мин, возможно дополнительное дробное введение атропина по 0,2 мг до тех пор, пока общая доза препарата не составит 2 мг. Стойкая брадикардия (менее 40 в 1 мин), сохраняющаяся, несмотря на введение атропина, может быть устранена с помощью электрической стимуляции. Введения изопротеренола следует избегать.
Нарушения проводимости. Нарушения проводимости могут возникнуть на трех различных уровнях проводящей системы сердца: в области предсердно-желудочкового узла, предсердно-желудочкового пучка (Гиса) или в более дистальных отделах проводящей системы (гл. 183). При появлении блокады в области предсердно-желудочкового узла, как правило, возникает замещающий ритм (escape?) предсердно-желудочкового соединения, при этом комплексы QRS обычной продолжительности. Если же блокада возникает дистально по отношению к предсердно-желудочковому узлу, замещающий ритм возникает в области желудочков, при этом комплексы QRS меняют свою конфигурацию, их продолжительность увеличивается. Нарушения проводимости могут возникнуть во всех трех периферических пучках проводящей системы, распознавание таких нарушений имеет значение для выявления больных с риском развития полной поперечной блокады. В тех случаях, когда возникает блокада любых двух из трех пучков, говорят о наличии двухпучковой блокады. У таких больных часто развивается полная атриовентрикулярная.блокада (полный поперечный блок). Таким образом, больные с комбинацией блокады правой ножки пучка Гиса и левым передним или левым задним гемиблоком или больные с вновь возникшей блокадой левой ножки пучка Гиса подвержены особенно высокому риску развития полной (поперечной) блокады.
Смертность больных с полной атриовентрикулярной блокадой, сопутствующей переднему инфаркту миокарда, составляет 80—90% и почти в 3 раза превышает смертность больных с полной атриовентрикулярной блокадой, сопутствующей нижнему инфаркту миокарда (30%). Риск смерти в последующем среди больных, выживших а острой стадии инфаркта миокарда, у первых также значительно выше. Различие в смертности объясняют тем фактом, что блокада сердца при нижнем инфаркте миокарда обычно вызвана ишемией предсердно-желудочкового узла. Предсердно-желудочковый узел — небольшая дискретная структура и даже ишемия или некроз небольшой выраженности могут вызвать его дисфункцию. При инфаркте миокарда передней стенки появление блокады сердца связано с нарушением функции всех трех пучков проводящей системы и, следовательно, является только следствием обширного некроза миокарда.
Электрическая стимуляция является эффективным средством учащения сердечного ритма у больных с брадикардией, развившейся как следствие атриовентрикулярной блокады, однако нет уверенности в том, что такое учащение пульса всегда является благоприятным. Например, у больных с инфарктом миокарда передней стенки и полной поперечной блокадой прогноз определяется главным образом размером инфаркта и коррекция дефекта проведения необязательно благоприятно повлияет на исход болезни. Электрическая стимуляция, однако, может оказаться полезной у больных с нижнезадним инфарктом миокарда, у которых полная поперечная блокада сочетается с развитием сердечной недостаточности, гипотонией, выраженной брадикардией или значительной эктопической активностью желудочков. Такие больные с инфарктом миокарда правого желудочка часто плохо реагируют на стимуляцию желудочков вследствие потери предсердного «удара», у них может потребоваться проведение двухжелудочковой, последовательной атриовентрикулярной, стимуляции.
Некоторые кардиологи считают необходимым профилактическую установку катетера для проведения стимуляции у больных с нарушениями проводимости, известными как предшественники полной (поперечной) блокады. По этому поводу единства суждений нет. Постоянную стимуляцию рекомендуют проводить больным, у которых имеется постоянная бифасцикулярная блокада и преходящая блокада III степени во время острой фазы инфаркта миокарда. Ретроспективные исследования у небольших групп таких больных показывают, что вероятность внезапной смерти снижается в тех случаях, когда проводится постоянная кардиостимуляция.
Сердечная недостаточность. Транзиторные нарушения функции левого желудочка той или иной степени возникают примерно у 50 % больных с инфарктом миокарда. Наиболее частыми клиническими признаками сердечной недостаточности являются хрипы в легких и S3 на S4-ритм галопа. На рентгенограммах часто выявляются признаки застоя в легких. Появление рентгенологических признаков легочного застоя, однако, не совпадает по времени с появлением таких клинических его признаков, как хрипы в легких и одышка. Характерными гемодинамическими признаками сердечной недостаточности служат повышение давления наполнения левого желудочка и давления в легочном стволе. Следует помнить, что эти признаки могут быть следствием ухудшения диастолической функции левого желудочка (диастолическая недостаточность) и/или уменьшения ударного объема с вторичной дилатацией сердца (систолическая недостаточность) (гл. 181). За небольшим исключением, терапия при сердечной недостаточности, сопутствующей острому инфаркту миокарда, не отличается от таковой при других заболеваниях сердца (гл. 182). Основное различие заключается в применении сердечных гликозидов. Благоприятное действие последних при остром инфаркте миокарда неубедительно. Это не удивительно, поскольку функция отделов миокарда, не захваченных инфарктом, может быть нормальной, в то же время трудно ожидать, что дигиталис может улучшить систолическую и диастолическую функции участков миокарда, захваченных инфарктом или ишемией. С другой стороны, очень хорошим действием при лечении больных с сердечной недостаточностью при инфаркте миокарда обладают диуретики, поскольку они уменьшают застой в легких при наличии систолической и/или диастолической сердечной недостаточности. Внутривенное введение фуросемида способствует снижению давления наполнения левого желудочка и уменьшению ортопноэ и одышки. Фуросемид, однако, следует назначать с осторожностью, поскольку он может вызвать массивный диурез и снизить объем плазмы, сердечный выброс, системное артериальное давление и как следствие этого уменьшить коронарную перфузию. Для уменьшения преднагрузки и симптомов застоя с успехом используют различные лекарственные формы нитратов. Изосорбида динитрат, принимаемый внутрь, или обычная мазь нитроглицерина имеют преимущество перед диуретиками, поскольку они снижают преднагрузку за счет венодилатации, не вызывая уменьшения общего объема плазмы.
Кроме того, нитраты могут улучшить функцию левого желудочка за счет своего влияния на ишемию миокарда, поскольку последняя вызывает увеличение давления наполнения левого желудочка. Лечение больных с отеком легких описано в гл. 182. Изучение вазодилататоров, уменьшающих постнагрузку на сердце, показало, что ее снижение приводит к уменьшению работы сердца и вследствие этого может существенно улучшить функцию левого желудочка, снизить давление наполнения левого желудочка, уменьшить выраженность застоя в легких и в результате вызвать увеличение сердечного выброса.
Мониторирование гемодинамики. Нарушение функции левого желудочка становится гемодинамически значимым, когда возникает нарушение сократимости 20 — 25 % миокарда левого желудочка. Инфаркт, захватывающий 40 % поверхности левого желудочка и более, обычно приводит к синдрому кардиогенного шока (см. ниже). Давление заклинивания легочных капилляров и диастолическое давление в легочном стволе хорошо коррелируют с диастолическим давлением в левом желудочке, поэтому их часто используют как показатели, отражающие давление наполнения левого желудочка. Установка баллонного плавающего катетера в легочном стволе позволяет врачу постоянно следить за давлением наполнения левого желудочка. Эту методику целесообразно использовать у больных, обнаруживающих клинические признаки гемодинамических нарушений или нестабильности. Катетер, установленный в легочном стволе, позволяет определять также величину сердечного выброса. Если, кроме того, проводится мониторирование внутриартериального давления, становится возможным вычислять периферическое сосудистое сопротивление, которое помогает контролировать введение сосудосуживающих и сосудорасширяющих препаратов. У некоторых больных с острым инфарктом миокарда обнаруживается значительный подъем давления наполнения левого желудочка (> 22 мм рт. ст.) и нормальный сердечный выброс (в пределах 2,6—3,6 л/мин на 1 м2), в то время как у других имеется относительно низкое давление наполнения левого желудочка ( >
Primary Menu
диссертации на соискание ученой степени
доктора медицинских наук
Санкт-Петербург
2008
Работа выполнена на кафедре кардиологии им. М.С. Кушаковского в ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования Федерального агентства по здравоохранению и социальному развитию»
Научный консультант:
доктор медицинских наук профессор Гришкин Юрий Николаевич
Официальные оппоненты:
доктор медицинских наук профессор Земцовский Эдуард Вениаминович
доктор медицинских наук профессор Панов Алексей Владимирович
доктор медицинских наук профессор Чурина Светлана Константиновна
Ведущая организация: ГОУ ВПО «Военно-медицинская академия им. С.М. Кирова»
Защита состоится “___” ____________________ 2008 г. в … часов на заседании Диссертационного совета Д.208.089.01 при ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования Росздрава» (191015, Санкт-Петербург, Кирочная ул. 41).
С диссертацией можно ознакомиться в фундаментальной библиотеке ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования Росздрава» (195196, Санкт-Петербург, Заневский пр. д. 1/82)
Автореферат разослан «___» ____________________ 2008 г.
Ученый секретарь диссертационного совета
доктор медицинских наук профессор А.М. Лила
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
У пациентов, перенесших острый инфаркт миокарда (ОИМ), гибель части функционирующего миокарда левого желудочка (ЛЖ) инициирует компенсаторные в своей основе изменения сердца, затрагивающие его размеры, геометрию и функцию. Комплекс этих изменений объединяется понятием постинфарктного ремоделирования [Белов Ю.В. 2003; Cohn J.N. 2000, Sutton M.G. 2000]. У части пациентов исходом ремоделирования является длительная стабилизация размеров и функции ЛЖ, что сопровождается достаточно благоприятным сердечным прогнозом. Вместе с тем, у других больных оно переходит в фазу дизадаптации, которая сопровождается гемодинамически невыгодным, чрезмерно выраженным и/или прогрессирующим увеличением ЛЖ и снижением его сократимости [Gaudron P. 1993]. В многочисленных исследованиях, проведенных в последние годы, была продемонстрирована связь увеличения конечно-диастолического объема (индекса) ЛЖ, его конечно-систолического объема (индекса) и снижения фракции выброса, связанных с неблагоприятным постинфарктным ремоделированием, с возрастанием риска сердечной смерти, повторного ОИМ, развития застойной сердечной недостаточности (СН), а также эмболического инсульта [Беленков Ю.Н. 2000; Pfeffer M.A. 1993; Schaer G. 2002; Solomon S.D. 2005].
Следовательно, возможность прогнозирования неблагоприятного характера постинфарктного ремоделирования ЛЖ равнозначна возможности идентифицировать в раннем периоде инфаркта пациентов с высоким риском сердечно-сосудистых осложнений и сердечной смерти в отдаленные сроки. Такое прогнозирование, в свою очередь, может играть существенную роль при оценке целесообразности выполнения эндоваскулярной / хирургической реваскуляризации в бассейне инфаркт-связанной артерии у больных, которым проводился тромболизис [Ляпкова Н.Б. 2007], а также более дифференцированно подходить к назначению в постинфарктном периоде медикаментозных препаратов, способных препятствовать ремоделированию [Беленков Ю. Н. 2005; Скворцов А. А. 2006; Kloner R.A. 2001]. В исследованиях последних лет была показана связь некоторых показателей острого периода инфаркта, в том числе, успешности проведенной реперфузии, ряда показателей, отражающих размеры инфаркта, и др. с вероятностью неблагоприятного постинфарктного ремоделирования [Solomon S.D. 2001; Bolognese L. 2002; Manes C. 2003]. Тем не менее, общепринятых подходов к выявлению пациентов, которым оно угрожает, не существует [Sutton M.J. 2002].
Развитие СН после инфаркта сопровождается ухудшением качества жизни и значительным снижением выживаемости больных [Новикова Н.А. 2002; Bouvy M.L. 2003; Bursi F. 2005]. При этом, несмотря на серьезные успехи, достигнутые за последние годы в лечении ОИМ, уровень смертности у пациентов с СН в течение первого года после ОИМ практически не снизился [Spencer F. 1999]. Поскольку ремоделирование ЛЖ является основным фактором, определяющим развитие СН после инфаркта миокарда [Cohn J.N. 2000], представляется важным изучить возможность прогнозирования развития СН на основании анализа показателей, влияющих на характер постинфарктного ремоделирования.
Цель исследования
Разработка критериев прогноза неблагоприятного течения постинфарктного ремоделирования левого желудочка на основании анализа доступных клинических, лабораторных и инструментальных показателей острого периода инфаркта миокарда.
Задачи исследования
-
Разработать предикторы успешности реперфузии, основанные на анализе концентрации сердечных ферментов в остром периоде инфаркта миокарда. Выявить электрокардиографические параметры острого периода инфаркта, позволяющие наилучшим образом прогнозировать результат реперфузии. Изучить частоту неблагоприятных изменений важнейших параметров постинфарктного ремоделирования – конечно-диастолического, конечно-систолического индекса левого желудочка и фракции выброса. Изучить возможность прогнозирования характера ремоделирования на основе анализа клинических показателей острого периода. Выявить ферментные и электрокардиографические показатели, позволяющие прогнозировать неблагоприятный характер ремоделирования. Найти важнейшие эхокардиографические предикторы неблагоприятных изменений основных параметров ремоделирования, в том числе изучить прогностические возможности показателей тканевого допплеровского исследования. На основании анализа выявленных предикторов неблагоприятной динамики конечно-диастолического, конечно-систолического индексов и фракции выброса разработать алгоритм прогнозирования неблагоприятного ремоделирования левого желудочка в целом. Выявить факторы, определяющие раннее (в течение первого года) развитие сердечной недостаточности после перенесенного острого инфаркта миокарда.
Научная новизна работы
Научная новизна работы состоит в выявлении показателей, доступных в остром периоде инфаркта миокарда, позволяющих прогнозировать характер постинфарктного ремоделирования.
Выявлены неинвазивные (ферментные и электрокардиографические) маркеры успешности реперфузии – фактора, способного существенно влиять на характер ремоделирования.
Среди клинических, лабораторных, электрокардиографических и эхокардиографических переменных острого периода инфаркта миокарда выявлены показатели, оказывающие наибольшее влияние на ремоделирование, а также найдены их количественные значения, позволяющие с большой вероятностью прогнозировать неблагоприятный вариант ремоделирования.
Предложен новый подход к анализу показателей тканевого допплеровского исследования острого периода инфаркта миокарда, позволяющий прогнозировать неблагоприятное постинфарктное ремоделирование.
Разработан алгоритм прогнозирования неблагоприятного ремоделирования в целом, основанный на полученных данных о предикторах постинфарктного ремоделирования.
Выявлены наиболее значимые предикторы развития важнейшего негативного следствия неблагоприятного ремоделирования – сердечной недостаточности – в раннем постинфарктном периоде.
Полученные данные позволяют оптимизировать выбор медикаментозного и хирургического лечения больного после острого инфаркта миокарда.
Положения, выносимые на защиту
-
Изучение «профиля» концентрации креатинкиназы и МВ-фракции креатинкиназы в остром периоде инфаркта миокарда позволяет оценить успешность тромболитической терапии «на уровне миокарда». Оценка ряда электрокардиографических параметров реполяризации левого желудочка, доступных для анализа в остром периоде инфаркта миокарда, позволяет делать вывод о результате миокардиальной реперфузии после тромболитической терапии. Неблагоприятные изменения конечно-диастолического, конечно-систолического индексов и фракции выброса левого желудочка в отдаленные сроки после острого инфаркта миокарда, можно прогнозировать на основании анализа ряда клинических, лабораторных и инструментальных показателей, доступных в остром периоде инфаркта миокарда. Анализ ряда предлагаемых нами параметров тканевого допплеровского исследования, отражающих количественные характеристики локальной сократимости и расслабления левого желудочка, получаемых в остром периоде инфаркта миокарда, позволяет прогнозировать характер постинфарктного ремоделирования левого желудочка. Анализ основных предикторов различных вариантов неблагоприятного постинфарктного ремоделирования левого желудочка позволяет прогнозировать неблагоприятный характер ремоделирования в целом. Исследование ряда показателей острого периода делает возможным прогнозирование раннего развития сердечной недостаточности после перенесенного инфаркта миокарда.
Практическая значимость работы
-
Предложен метод диагностики результатов тромболитической терапии, основанный на анализе варианта изменения концентрации общедоступных сердечных маркеров (креатинкиназы и её МВ-фракции) в течение первых суток острого инфаркта миокарда. Разработаны методы диагностики результатов миокардиальной реперфузии на основании анализа электрокардиографических параметров, получаемых в течение первых двух суток острого инфаркта миокарда (динамика максимальной и суммарной элевации сегмента ST, динамика суммарной амплитуды зубца Т). Выявлены важнейшие предикторы неблагоприятного варианта постинфарктного ремоделирования левого желудочка, заключающегося в значимом увеличении конечно-диастолического, конечно-систолического индексов, а также снижении фракции выброса левого желудочка. Найдены количественные значения этих предикторов, разделяющие пациентов с благоприятным и неблагоприятным прогнозом ремоделирования. Выявлены параметры тканевого допплеровского исследования, относящиеся к острому периоду инфаркта миокарда, позволяющие прогнозировать характер постинфарктного ремоделирования левого желудочка, в том числе, предложен расчет с этой целью ряда новых информативных параметров. Разработан алгоритм прогнозирования неблагоприятного постинфарктного ремоделирования левого желудочка, основанный на анализе доступных инструментальных и лабораторных показателей острого периода инфаркта. Продемонстрирована возможность прогнозирования развития сердечной недостаточности в течение первого года после острого инфаркта миокарда на основании анализа ряда показателей острого периода. Показано, какие именно эхокардиографические параметры, оцениваемые через 12 месяцев после острого инфаркта миокарда, имеют наибольшую корреляцию с наличием клинических проявлений сердечной недостаточности.
Личный вклад автора
Личное участие автора выразилось в определении основной идеи исследования, его планировании, выработке методов его выполнения, осуществлении сбора, обработки и анализа полученного материала. Автором непосредственно проводился отбор пациентов для включения в исследование, наблюдение в течение 12 мес. клиническое обследование, количественный анализ всех электрокардиограмм и ферментных показателей, лично выполнены все эхокардиографические исследования.
Результаты проведенного исследования внедрены в работу кардиоло-гических отделений и отделения эхокардиографии Санкт-Петербургского ГУЗ «Покровская больница», отделения рентгено-эндоваскулярной хирургии Санкт-Петербургского ГУЗ «Городская многопрофильная больница №2». Материалы диссертации включены в лекционные курсы и семинары кафедры кардиологии им. М.С. Кушаковского и кафедры клинической физиологии и функциональной диагностики ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования Росздрава».
Апробация работы
Основные результаты диссертации были представлены на Российских национальных конгрессах кардиологов (Томск, 2004 г; Москва, 2005 г.; Москва, 2007 г.); Всероссийском научно-образовательном форуме «Кардиология 2007» (Москва, 2007 г.); 5-м Съезде специалистов ультразвуковой диагностики в медицине (Москва, 2007 год); Научно-практической конференции «Использование передовых ультразвуковых технологий в исследовании пациентов с кардиоваскулярными заболеваниями» (СПб, 2007 г.); 7-й Международной конференции «Coronary artery disease: from prevention to intervention» (Венеция, Италия, 2007 г.); Совместном научном семинаре Биомедицинской секции Дома ученых им. М.Горького РАН, Северо-западного отделения Общества ядерной медицины и Санкт-Петербургского Эхокардиографического клуба «Современные проблемы кардиовизуализации» (СПб, 2008 г.).
Основные положения диссертации отражены в 28 опубликованных печатных работах, 10 из которых опубликованы в журналах ВАК РФ.
Структура и объем диссертации
Диссертация состоит из введения, обзора литературы, главы «Материалы и методы», 9 глав, посвященных анализу собственных материалов, заключения и списка литературы. Текст диссертации изложен на 281 машинописной странице, иллюстрирован 42 рисунками и 113 таблицами. Список литературы состоит из 266 наименований, в т.ч. 37 отечественных и 229 иностранных источников.
СОДЕРЖАНИЕ РАБОТЫ
Материал и методы исследования
В исследование включались пациенты, переносящие ОИМ с подъемом сегмента ST на электрокардиограмме (ЭКГ), которым планировалось выполнение тромболизиса, соответствовавшие приведенным ниже критериям.
Критериями включения были: 1) ишемические боли в груди длительностью не менее 20 мин. и развившиеся не более чем за 12 ч до планируемого момента начала тромболизиса; 2) элевация сегмента ST на ЭКГ при поступлении, составлявшая как минимум 0,1 мВ (1 мм) в 2 или более отведениях от конечностей, или, как минимум, в 2 или более соседних грудных отведениях.
Критериями исключения были: 1) наличие противопоказаний к системному тромболизису [Ryan T.J. 1999]; 2) полная блокада левой ножки пучка Гиса на ЭКГ; 3) кардиогенный шок при поступлении; 4) гемодинамически значимые клапанные пороки; 5) неудовлетворительное качество изображения при эхокардиографии (ЭхоКГ).
В качестве тромболитического агента применяли альтеплазу или стрептокиназу, в зависимости от наличия препарата, по стандартным схемам, согласно инструкции производителя. Помимо проведения тромболизиса, всем больным назначалась медикаментозная терапия согласно общепринятым стандартам.
Клиническое обследование включало оценку анамнеза и клинических параметров при поступлении и оценку класса СН по NYHA через 12 мес.
ЭКГ регистрировали перед началом тромболизиса, через 3 ч и через 48 ч после него (соответственно, ЭКГ-1, ЭКГ-2, ЭКГ-3). На ЭКГ-1 и ЭКГ-2 рассчитывали число отведений с элевацией ST; число отведений с патологическим Q (n отв.Q); элевацию ST в отведении, где она максимальна (мaксимальная элевация SТ, STmax); сумму величин элевации ST во всех отведениях, где она имела место (суммарная элевация SТ, STsum); суммарную амплитуду зубцов Т в отведениях с элевацией сегмента ST (соответственно, sumT1 и sumT2) и разницу этих амплитуд (sumT2 — sumT1). На ЭКГ-3 рассчитывалась суммарная амплитуда зубцов Т (sumT3) и вычислялась разность амплитуд «Т» на ЭКГ-3 и ЭКГ-1 (sumT3 — sumT1).
Выполнялся анализ концентрации креатинкиназы (КК) и МВ-фракции креатинкиназы (МВ) в венозной крови до тромболизиса (КК1 и МВ1) и затем еще 4 раза с 6-часовыми интервалами (КК2 и МВ2, КК3 и МВ3 и т.д.), т.е. на протяжении первых 24 часов инфаркта. Взаимная иерархия значений концентрации фермента в этих 5 анализах кодировалась цифрами от 1 до 5, расположенными в ряд, тогда как позиция цифры в ряду соответствовала порядковому номеру анализа фермента — таким образом строился «профиль» концентрации фермента. Например, для КК ряд 1 5 4 3 2 отражал следующую иерархию величин КК: концентрация КК1 – первая снизу (наименьшая), КК2 – пятая снизу (наибольшая), КК3 – 4-ая снизу, КК4 – 3-я, КК5 – вторая. Кроме этого, учитывались максимальные концентрации КК (КKmax) и МВ (МВmax).
ЭхоКГ выполнялась на приборах Combison-320, Siemens Sonoline 60, Vivid-3 Expert. ЭхоКГ проводилась до тромболизиса, при выписке (8,8±0,2 сут. от поступления), через 6 и через 12 мес. после ОИМ (соответственно, ЭхоКГ-1, ЭхоКГ-2, ЭхоКГ-6 и ЭхоКГ-12) по стандартному протоколу. Стандартное исследование в одномерном режиме [Sahn D.J. 1978] обязательно включало измерение митрально-септальной сепарации (EPSS). В В-режиме определялись конечно-диастолический объем ЛЖ (КДО), конечно-систолический объем ЛЖ (КСО) по методу Simpson [Wahr D.W. 1983], рассчитывались конечно-диастолический индекс (КДИ) как КДО/BSA и конечно-систолический индекс (КСИ) как КСО/BSA, мл/м2, где BSA – площадь поверхности тела. Также вычислялась фракция выброса ЛЖ (ФВ) по формуле: ФВ (%)=[(КДО — КСО) / КДО] 100. Регионарная сократимость ЛЖ оценивалась согласно распространенной модели деления ЛЖ на 16 сегментов, полуколичественным методом по общепринятой четырехбалльной системе (1 – норма; 2 – гипокинезия; 3 – акинезия; 4 – дискинезия) [Smart S.C. 1997]. Чтобы охарактеризовать степень нарушения локальной сократимости количественно, рассчитывали индекс локальной сократимости ЛЖ (ИЛС), как сумма баллов/16.
В допплеровском режиме выполнялось стандартное исследование кровотока на клапанах.
При ЭхоКГ-2 также выполнялось исследование продольных скоростей движения 12 базальных и срединных сегментов миокарда ЛЖ в импульсном тканевом допплеровском режиме [Алехин М.Н. 2002]. Полученные графики скорости миокарда сохранялись в цифровом формате, после чего проводились измерения на сохраненных изображениях. Измерялись максимальные систолические (Sm) и диастолические (Em) скорости всех сегментов. Затем рассчитывались суммы этих скоростей для нормально сокращающихся сегментов (Sm sokr и Еm sokr) и сегментов с нарушенной сократимостью (Sm dys и Еm dys), а также индексы этих скоростей, т.е. их отношение к общему числу сегментов с нарушенной сократимостью (соответственно, ind-Sm sokr, ind-Sm dys, ind-Em sokr и ind-Em dys). Кроме того, оценивалось число сегментов с нарушенной сократимостью, в которых регистрировался положительный пик изоволюметрического сокращения, и аналогичным образом рассчитывался индекс IVC (ind-IVC).
Общая характеристика обследованных пациентов
Всего в исследование было включено 187 пациентов. Анализ способности ферментных и электрокардиографических маркеров предсказывать результат миокардиальной реперфузии был выполнен у той части обследованных пациентов, которым выполнялись ЭхоКГ-1 и ЭхоКГ-2, а также были получены соответствующие лабораторные и ЭКГ-данные – у 107 и 106 больных, соответственно. В связи исключением из наблюдения ряда пациентов (перенесших коронарную реваскуляризацию; перенесших повторный инфаркт; потерянных для контакта и умерших), анализ факторов, влияющих на 12-месячную динамику КДИ был выполнен у 102 пациентов, анализ динамики КСИ и ФВ – у 115 больных, прогнозирование раннего развития СН – у 123 пациентов. Анализ прогностического значения тканевых допплеровских параметров был выполнен у 55 из обследованных пациентов – у тех, кому проводилось ТДИ при ЭхоКГ-2 и была выполнена заключительная ЭхоКГ-12.
Возраст включенных в исследование больных составлял 59±1 лет (35 – 80 лет). Преобладали пациенты мужского пола (146 человек, 78%). Распределение пациентов по наличию основных клинических факторов сердечного риска было следующим: >1 – 94 пациента (50%); 1 – 72 пациента (39%); 0 – 21 (11%). 60 пациентов (32%) к моменту поступления имели анамнез стенокардии напряжения длительностью более 1 мес. У 24 пациентов (13%) данный ОИМ был повторным. Большинство включенных пациентов (153 пациента, 82%) на момент поступления были отнесены к I классу по Killip; 34 (18%) – ко II и III классам. Пациенты с IV классом по Killip, как отмечено выше, в исследование не включались. У большинства больных был диагностирован Q-инфаркт (165, 88%), у 118 пациентов (63%) – передний инфаркт миокарда. Системный тромболизис был выполнен, преимущественно альтеплазой (166 пациентов, 89%), 21 больному – стрептокиназой. Время от начала болей в груди до начала реперфузии составляло от 20 до 555 мин (в среднем 224±6 мин.)
Максимальные концентрации КК в течение первых суток ОИМ составляли 3478±177 Ед/л (от 168 до 15476 Ед/л), МВ – 539±27 Ед/л (от 25 до 1960 Ед/л).
У обследованных пациентов не отмечалось увеличения исходных диастолических размеров ЛЖ: показатели КДИ для мужчин (57,0±0,8 мл/м2) и женщин (55,8±1,7 мл/м2) не превышали норму. Не был увеличен и диастолический размер ЛЖ, измеряемый в М-режиме (47,7±0,6 мм). Показатель ИЛС, отражающий размер зоны сократительной дисфункции ЛЖ, связанной с развитием инфаркта, был существенно увеличен (1,75±0,03). Исходное снижение показателей глобальной сократимости было умеренным: средняя ФВ составляла 49,4±0,9% (от 22,6 до 73,4%).
Статистический анализ
Статистический анализ проводился, главным образом, с помощью программы Statistica 6.0 (StatSoft, Inc. 1984-2001). Кроме того, использовалась программа SAS 8.2 (SAS Institutes Inc. Cary, NC).
Значения непрерывных переменных представлены как среднее ± стандартная ошибка среднего. Сравнение средних показателей в двух группах проводилось с помощью теста Стьюдента, при количестве групп более двух – методом 99% доверительных интервалов (ДИ) с поправкой Бонферрони. Различия числа исходов между двумя группами оценивались по таблицам 2х2 раздела непараметрической статистики. Поиск «точек разделения» непрерывных переменных проводился с помощью методики «регрессионного дерева» (C&RT) программы Statistica, в ряде случаев – функции out-ROC модуля логистической регрессии программы SAS. Точки разделения категорийных переменных находили с помощью функции «Tables and banners» программы Statistica. Оценка независимого влияния ряда переменных на конечный показатель осуществлялась с помощью логистической регрессии, степень влияния фактора выражалась в виде отношения шансов (ОШ) с указанием 95% ДИ. Перед составлением регрессионных моделей в ряде случаев проводился корреляционный анализ изучаемых переменных. Достоверность различия везде определялась как p<0,05.
Расчет отношения правдоподобия (likelihood ratio, LR) для прогнозирования неблагоприятного ремоделирования в целом проводился по формулам: LR+ = Se/(1-Sp); LR- = (1-Se)/Sp, где (LR+) – отношение правдоподобия при наличии изучаемого предиктора; (LR-) – отношение правдоподобия при отсутствии изучаемого предиктора; Se – чувствительность предиктора в отношении неблагоприятного ремоделирования; Sp – специфичность предиктора [Sackett D.L. 2000]. Для упрощения расчета вычислялся десятичный логарифм LR каждого предиктора, lg (LR+) и lg (LR-), затем их значения, в зависимости от наличия [lg (LR+)] или отсутствия [lg (LR-)] того или иного предиктора у конкретного пациента, суммировались, и вычислялся суммарный логарифм отношения правдоподобия lg(LR). Далее рассчитывалось суммарное отношение правдоподобия, учитывающее влияние всех предикторов (LR): LR=10lg(LR). После этого, исходя из предтестового отношения шансов развития неблагоприятного ремоделирования (ОШpre), равного 0,25 [Jeremy R.W. 1989; Gaudron P. 1993], вычислялось посттестовое отношение шансов (ОШpost): ОШpost =ОШpre LR. Наконец, находили посттестовую вероятность неблагоприятного ремоделирования (Рpost): Рpost= ОШpost /(ОШpost+1)100%.
НЕИНВАЗИВНАЯ ОЦЕНКА ЭФФЕКТИВНОСТИ РЕПЕРФУЗИИ ПРИ ОСТРОМ ИНФАРКТЕ МИОКАРДА
Первым этапом исследования было изучение диагностической ценности ряда электрокардиографических и ферментных показателей острого периода инфаркта в отношении эффективности коронарной реперфузии – фактора, способного оказать существенное влияние на постинфарктное ремоделирование. В качестве эталонного метода оценки эффективности реперфузии «на уровне миокарда» использовалась динамика показателей локальной сократимости ЛЖ в остром периоде. Согласно имеющимся в литературе данным, она отражает исход реперфузии «в целом», как на уровне эпикардиальной артерии, так и на уровне микроциркуляции, поскольку определяется конечным состоянием кровоснабжения «зависимого» миокарда, и, в связи с этим, лучше соответствовала задачам нашего исследования, чем коронарография.
Оценка эффективности реперфузии при остром инфаркте миокарда с помощью ферментов – сердечных маркеров: общая креатинкиназа и МВ-фракция креатинкиназы
Характер перфузии зависимого миокарда на протяжении 24 ч после тромболизиса может динамически меняться в результате повторных эпизодов реканализации-реокклюзии [Krucoff M. 1993]. Поэтому, с нашей точки зрения, анализ «ферментного профиля» позволяет оценивать конечный результат тромболизиса точнее, чем обычно применяемые показатели – время до наступления пиковой концентрации фермента или скорость увеличения концентрации в первые 60-90 мин после тромболизиса [Laperche Т. 1995].
При анализе имевших место вариантов профилей концентрации сердечных ферментов была выявлена их большая вариабельность: количество различных профилей КК составило 28, а профилей MB – 29. Тем не менее, у большинства больных (в 75% исследованных случаев для КК и в 70% случаев для MB) наблюдался один из 7 наиболее часто встречавшихся профилей.
Единственным профилем, позволявшим прогнозировать результат реперфузии на уровне статистической достоверности, был профиль КК 1 5 4 3 2, т.е. с ранним максимумом (на 6-ом часу) и непрерывным снижением уровня фермента при всех последующих анализах. Среди пациентов с этим профилем КК реперфузия была успешной у 25 (95% ДИ 51,9 – 83,6), неудачной – у 11 (95% ДИ 16,4 – 48,1), p<0,05. Данный профиль регистрировался наиболее часто (у 34% пациентов) и наблюдался в 40% случаев успешной реперфузии (УР). Тем не менее, у оставшихся 2/3 пациентов предсказать результат реперфузии на основании индивидуальных профилей ферментов не удавалось. В связи с этим индивидуальные профили были объединены в совокупности, что значительно повысило их диагностическую ценность.
Совокупности объединяли все профили данного фермента с ранним (6 ч; 12 ч; 6 или 12 ч) пиком его концентрации. Включаемые в совокупности профили КК, кроме того, характеризовались непрерывным снижением концентрации после пика без повторных подъемов. При составлении совокупностей профилей MB учитывался только факт раннего достижения максимальной концентрации.
Проведенный анализ показал, что диагностической ценностью в отношении УР обладают только совокупности КК и MB, которые допускают возможность пика фермента как на 6, так и на 12 ч (их обозначали, соответственно, «-КК» и «-MB»). Достоверная диагностика результата реперфузии была возможна и при комбинировании таких совокупностей КК и MB («-КК +-MB» и «-КК или -MB»). Диагностическая ценность полученных ферментных предикторов реперфузии отражена в таблице 1.
Все полученные предикторы продемонстрировали не очень высокую специфичность, т.е. могут регистрироваться у пациентов в случае неуспешной реперфузии, однако их чувствительность, как правило, превышала аналогичный показатель для обычно используемых ферментных предикторов (80%) [Zabel М. 1993]. Отметим, что более высокую диагностическую ценность показала КК, а не MB, несмотря на большую специфичность последней в отношении повреждения миокарда.
Таблица 1