Патогенез острой левожелудочковой недостаточности
Дифференциальная диагностика при острой сердечной недостаточности
Рекомендации на амбулаторный этап
Агрессивная тактика
Больные с ОКС с высокис риском сердечно-сосудистых осложнений подлежат отбору по критериям риска для выполнения инвазивных диагностических и лечебных манипуляций или АКШ в ранние сроки (от 24-48 часов до 14 суток, лучше в первые сутки или после четвёртых)
Прямая реваскуляризация миокарда (ПРМ) в условиях ИК:
— АШ, АКШ+МКШ (количество шунтов по результатам КАГ)
— ПРМ с одновременной пластикой левого желудочка (объём операции по данным КАГ и вентрикулографии)
— ПРМ с одновременной пластикой или протезированием клапанов (по КГ и ЭхоКГ)
1) Пожизненый приём аспирина 80-325 мг/сутки при отсутствии противопоказаний, а также в течение 3 месяцев тиклид или оптерон по 250 мг 2 раза/сутки или плавикс 75 мг/сутки в течение 3 месяцев
2) Медикаментозная терапия (иАПФ, по показаниям – бета-АБ и нитраты, после АКШ антагонисты кальция в качестве профилактических средств при склонности к вазоспазму – дилтиазем или амлодипин в течение 3-6 месяцев)
3) Контроль уровня липидов плазмы крови и поддержание их нормальных значений с помощью нормального питания и статинов (дозы не менее 20 мг)
4) Контроль уровня АД и поддержание его в пределах менее 130/80 мм рт.ст.
5) Соблюдение режима физической активности, выроботанного индивидуально на основании нагрузочных тестов
6) Полное прекращение курения
7) Борьба с избыточным весом
Острая сердечная недостаточность — является следствием нарушения сократительной способности миокарда и уменьшения систолического и минутного объемов сердца, проявляется крайне тяжелыми клиническими синдромами: отеком легких, кардиогенным шоком, острым легочным сердцем.
Острая левожелудочковая недостаточность может развиваться в двух вариантах —
1) СН, проявляющаяся застоем в малом круге кровообращения (отек легких и сердечная астма)
2) СН, проявляющаяся симптомами падения сердечного выброса (кардиогенный шок
Классификация ОСН
ЛевожелудочковаяПравожелудочковая
Сердечная астма Острое легочное сердце
Отек легких
Кардиогенный шок.
1) Падение сократительной способности миокарда возникает как результат перегрузки, снижения функционирующей массы миокарда.
2)Полноценно работающий правый желудочек создает повышенное давление в малом круге кровообращения.
3) Бронхиолы и легочные капилляры находятся в одном "интерстициальном ложе". По мере нарастания гидростатического давления более 28-30 мм рт.ст. происходит проникновение жидкой части крови в интерстициальную ткань и формирование начальной фазы отека легких — "сердечной астмы".
4) Далее жидкость проникает в альвеолы (гидростатическое давление более 30 мм рт.ст) – альвеолярный отек, или отек легких.
Факторы, провоцирующие острый отек легких:
ü Острый ИМ, в том числе с большим объемом поражения ЛЖ
ü ИМ, осложненный разрывом МЖП; разрывом папиллярных мышц
ü Декомпенсация хронической СН, обусловленной любым заболеванием сердца
ü Остро развившаяся клапанная недостаточность (митрального, трикуспидального, аортального)
ü Резкое повышение системного АД (гипертонический криз)
ü Острая тахи- или брадиаритмия
Домашний доктор

Острая сердечная недостаточность
Острая сердечная недостаточность — внезапное или быстро прогрессирующее ослабление сократительной способности миокарда с последующим расстройством кровообращения.
Причиной острой сердечной недостаточности может быть перегрузка сердца повышенным объемом крови или давлением (при пороках сердца, легочном сердце), а также снижение сократительной функции миокарда при уменьшении его массы и дегенеративных изменениях. У новорожденных и грудных детей острая сердечная недостаточность часто возникает при врожденных пороках сердца, фе-тальном фиброэластозе эндокарда, врожденной дисфункции коры надпочечников, синдроме дыхательных расстройств, нарушении мозгового кровообращения.
У дошкольников ее причинами, наряду с врожденными пороками сердца, являются неревматические острые миокардиты, перикардиты, кардиомиопатии, острые пневмонии.
У детей старшего возраста, кроме описанных выше причин, ост-Рая сердечная недостаточность может возникать при ревматических пороках сердца, септических эндокардитах, артериальной гипертензии и артериальном кризе, остром и хроническом гломерулонефрите, системных заболеваниях соединительной ткани, диффузном токсическом зобе, бронхиальной астме.
Острая сердечная недостаточность также может развиться в любом возрасте при чрезмерной физической нагрузке, отравлении различными химическими веществами, передозировке наркотиками и поражении электрическим током.
В патогенезе острой сердечной недостаточности у детей основная роль принадлежит энергодинамической недостаточности, в результате которой увеличивается активность Na-K-АТФ-азы, уменьшается синтез актомиозина, наступает дисбаланс электролитов, что ведет к снижению сократительной способности миокарда. Уменьшение ударного выброса крови из полостей сердца, снижение скорости кровообращения, переполнение сосудов легких уменьшают дыхательную поверхность, что способствует развитию кислородной недостаточности и метаболического ацидоза. В результате гипоксии повышается проницаемость клеточных мембран, нарушается микроциркуляция, уменьшается коронарный кровоток, энергетическое снабжение миокарда становится неполноценным, что приводит к более глубокому нарушению гемодинамики. Гемодинамическая недостаточность возникает чаще при врожденных и приобретенных пороках сердца. Под влиянием гипоксии активизируется гемопоэз, нарушаются тканевая проницаемость, микроциркуляция. В связи с венозным застоем и особенно недостаточным кровоснабжением почек снижается клубочковая фильтрация, увеличивается выделение ренина, альдостерона и антидиуретического гормона, что приводит к задержке в организме воды, натрия, параллельно может усиливаться выведение калия.
В результате этого увеличивается объем циркулирующей крови, повышается венозное давление, возникают отеки. Постепенно из-за венозного застоя и гипоксии развивается соединительная ткань в различных органах (печени, легких, почках), наступают необратимые дистрофические изменения.
Угасание сердечной деятельности обусловливается нарушением предсердно-желудочковой и синоаурикулярной проводимости, прогрессирующим снижением сократительной функции миокарда, ведущим к нарушению кровообращения в коронарных сосудах, расширению полостей сердца.
Клиническая картина
Клинически различают сердечную недостаточность левожелудоч-ковую и правожелудочковую. Синдром острой сердечной недостаточности протекает по типу острой левожелудочковой недостаточности, проявляющейся в виде двух форм — сердечной астмы и отека легких.
Основными симптомами сердечной астмы у детей являются внезапное начало (дети просыпаются с ощущением острого недостатка воздуха — удушья), чувство страха смерти, одышка. Дети младшего возраста проявляют крайнее беспокойство, иногда длительно кричат в связи с нарастающей одышкой, отказываются от груди. Дети старшего возраста принимают вынужденное положение сидя с опущенными ногами, опираются руками о кровать и наклоняют голову вперед, чтобы облегчить дыхание. При возникновении сердечной астмы кожные покровы и слизистые оболочки быстро бледнеют, затем появляется и усиливается цианоз лица, губ, кожа покрывается холодным липким потом.
Отмечается нарастающая инспираторная одышка или смешанная, без углубления дыхания, частый сухой кашель. Аускультативно определяется ослабленное или жесткое дыхание в раннем периоде, с присоединением отека легких, возникает кашель с обильной пенистой мокротой розового цвета, появляются при аускультации легких и среднепузырчатые хрипы. Дыхание становится шумным, клокочущим.
При пальпации области сердца отмечается резкое ослабление верхушечного толчка и смещение его влево. При выслушивании выявляются глухость тонов сердца, различные кардиальные шумы, нарушения сердечного ритма. Тахикардия. Пульс малого наполнения и напряжения. В начальном периоде регистрируется кратковременное повышение, а затем снижение артериального давления.
При присоединении правожелудочковой сердечной недостаточности характерно постепенное нарастание симптомов — набухание шейных вен, увеличение и болезненность печени, селезенки. Развитие застойных явлений в органах брюшной полости сопровождается тошнотой, рвотой, поносом. При дальнейшем развитии недостаточности появляются пастозность мягких тканей, затем отеки. Преобладает ночной диурез.
Усиливается общая вялость, развиваются головокружения, заторможенность, мышечная гипотония или судорожный синдром, ареф-лексия, потеря сознания. Тахикардия сменяется брадикардией, та-хипноэ — аритмичным дыханием. Наступает синдром гипоксической комы в связи с отечностью и гипоксией головного мозга.
Дифференциальный диагноз
Острую сердечную недостаточность необходимо дифференцировать с острой сосудистой недостаточностью, бронхиальной астмой, острой пневмонией, острым миокардитом, гипертоническим кризом, Церебральной и гипогликемической комой, острой надпочечниковой недостаточностью.
Неотложная помощь
- Должна начинаться немедленно, чтобы избежать отека легких и угнетения дыхательного центра.
- Обеспечить полный покой в постели с приподнятым изголовьем.
- Освободить от стесняющей одежды.
- Согреть грелками.
- Дать кислород или открыть окно, форточку для поступления свежего воздуха.
- Ввести внутривенно коргликон или строфантин медленно. В 10—15 мл изотонического раствора или 20%-ного раствора глюкозы.
- Разовые дозы 0,006%-ного коргликона:
- дети до 1 года — 0,1 мл;
- 2—3 лет — 0,2 мл;
- 4—7 лет — 0,3—0,4 мл;
- старше 7 лет — 0,5—0,8 мл.
- Разовые дозы 0,05%-ного раствора строфантина:
- дети первого года жизни — 0,05—0,1 мл; •2—3 лет —0,1—0,2 мл;
- 4—7 лет — 0,2—0,4 мл.
Примечание: при брадикардии, анурии, экссудативном перикардите назначение гликозидов противопоказано.
Ввести лазикс подкожно (1%-ный раствор — 2—3 мг на 1 кг веса в сутки (в 1 мл — 10 мг), внутривенно в сочетании с 2,4%-ным раствором эуфиллина (доза — 0,2 мл на год жизни, но не более 5 мл).
При возбуждении, чувстве страха смерти, одышке — введение седуксена (1%-ный раствор — 0,1—0,2 мл на год жизни) или раствора дроперидола (0,25%-ный раствор — 0,1—0,25 мл на год жизни).
Для предотвращения падения артериального давления и снижения проницаемости альвеолярно-капиллярных мембран подкожно или внутримышечно ввести преднизолон (1—3 мг на 1 кг в сутки), кокарбоксилазу (25—100 мг в сутки).
При повышении артериального давления наложить поочередно на конечности венозные жгуты на 10—15 мин, но не более часа суммарно. Контроль артериального давления обязателен! Внутримышечное введение для снижения артериального давления дибазола (0,2 мл на год жизни), 2%-ного раствора но-шпы (0,2 мл на год жизни), 2%-ного раствора папаверина (0,05 мл на год жизни).
При понижении артериального давления подкожно или внутримышечно ввести раствор кордиамина (0,1 мл на год жизни), 10%-ный раствор сульфакамфокаина (0,1 мл на год жизни), 10%-ный раствор кофеина (0,1 мл на год жизни), при отсутствии эффекта от этих препаратов ввести 1%-ный раствор мезатона (0,02 мл на кг массы) подкожно или внутривенно медленно в 10—15 мл 20%-ного раствора глюкозы. • При нарастании симптомов, ведущих к остановке сердечной деятельности или асистолии, проводить реанимационные мероприятия.
Острая сердечная недостаточность(ОСН)- ее виды, причины, и патогенез, некоторые принципы диагностики и патогенетической терапии.
Жизнь — или смерть — если не успеть помочь, а для этого нужно разобраться и принять необходимые лечебные меры.
Пять форм ОСН:
а) тампонада сердца,
б) полная атрио-вентрикулярная блокада,
в) мерцание, фибрилляция желудочков,
г) инфаркт миокарда и
д) острая закупорка легочной артерии.
Тампонада сердца — синдром острой сердечной недостаточности, вызванной внутриперикардиальным сдавлением сердца жидкостью (гемотампонада, перикардит острый экссудативный) или газом.
Патогенез нарушений:
1) механическое сдавление тонкостенных отделов сердца и крупных вен → уменьшение наполнения его полостей. Развивается синдром низкого сердечного выброса (резкое уменьшение сердечного и МОС), уменьшение тканевого кровотока, олигоурия, повышение потребления, повышение потребления O2 и увеличение содержания в крови молочной и пировиноградной кислоты и
2) патологический вагусный рефлекс — из-за растяжения перикарда → раздражение nervus vagus → может быть остановка сердца, АД понижается, а венозное повышается. При наличии большого выпота, когда резко ограничивается диастола и сильное затруднена работа сердца — возниает кислородное голодание мозга: беспокойство, чувство тревоги. Нарастает бледность кожи и затем цианоз. Это легко воспроизводится в эксперименте.
Диагностика — клинически — резкий застой крови в венах лица, шеи.
Терапия — максимально быстро освободить полость прикарда от жидкости или газа методом пункции.
Полная атрио-вентрикулярная блокада — различают 4 степени атрио-вентрикулярной блокады:
1 степень — удлинение времени предсердно-желудочкового проведения;
2 степень — выпадение некоторых желудочковых комплексов после постепенного удлинения интервала P-Q, но после выпадения желудочкового сокращения проводимость на непродолжительное время улучшается, а затем вновь периоды Венкебаха — Самойлова.
При блокаде 3 степени из предсердий в желудочки проводится лишь каждый 2, 3, 4-й импульс и
4 стадия — полная поперечная блокада.
Причины: гипоксия, тяжелая патология миокарда с нарушением метаболизма, инфаркт миокарда, интоксикация, рубцы, ревматизм. Нет синхронизации сокращений предсердий (60-70/мин) и желудочков (40-50). Если обе систолы вместе — холостое сокращение желудочков и снижение МО. Нарушение предсердно-желудочковой проводимости — частая причина нарушения сердечного ритма, уступающая по частоте лишь экстрасистолии, мерцательной аритмии и пароксизмальной желудочковой тахикардии.
Диагностика — ЭКГ.
Патогенетическая терапия — вживление кардиостимулятора — водителя ритма (только для желудочков или всего сердца) либо со стабильным ритмом 60-70, либо один — регистрирующий электрод в области синусно-предсердного узла, а второй — стимулирующий — в обл атриовентрикулярного узла — воспроизводит ритм и будет полная синхронизация сердечных сокращений (с кардиостимулятором живет и работает академик Амосов).
Мерцание желудочков — форма мерцательной аритмии — нарушение ритма сердца с частыми и нерегулярными возбуждениям миокарда и полной разнородностью сердечных сокращений по частоте, силе, причем длительность сердечных циклов значительно колеблется и носит случайный характер. При мерцании частота волн на ЭКГ более 6300/ мин (обычно 500-800/ мин), а при трепетании — менее 300/мин. Глянцевая поверхность миокарда при этом мерцает, напоминая рябь на поверхности воды, в связи с чем это состояние получило название «мерцание» предсердий.
Фибрилляция — наличие сокращений миокардиальных волокон при отсутсвии сокращения всего миокарда как целого. Сердечные волокна сокращаются разрозненно и разновременно не выполняя насосную функцию: УО и МО = 0, гибель через 5 мин, человек не может жить.
Причины: тяжелая гипоксия, ишемия миокарда, интоксикация, нарушение электролитного баланса, повреждение механическое и электротоком, низкая темпиратура, нервно-психическое возбуждение, применение симпатомемитических средств при наркозе.
Наиболее распространенные теории:
1) наличие множества гетеротропных очагов, из-за которых мышечные волокна сокращаются изолированно, а не все вместе, и
2) теория циркуляции волны возбуждения на основе механизма повторного входа из-за множественныых локальных нарушений проводимости в миокарде и проводящей системе сердца. При этом ритм сокращения пораженных волокон отличается от других волокон и создаются условия для фибрилляции желудочков.
Диагностика — ЭКГ — нет цикла.
Патогенетическая терапия — дефибрилляция:
1) приведение всех миокардиоцитов одномоментно в одно состояние абсолютной рефрактерности, применяя одиночный короткий 0,01 сек мощный разряд электрического тока (при прямой дефибрилляции 10-12 А, при наружной — до 30 А) и
2) затем ритмическая стимуляция сокращений сердца электрическим током малой силы как в кардиостимуляторе.
Однако есть определенная опасность — при дефибрилляции гибнут миокардиоциты.
Инфаркт миокарда (ИМ) (infarctus myocardii) — острое заболевание, обусловленное развитием одного или нескольких очагов некроза в серд. мышце, проявляющиийся различными нарушениями сердечной деятельности и клиническими синдромами, связанными с развитием острой ишемии и некроза миокарда. Некроз может быть и не сосудистого происхождения — электролитно-стероидный. Различают крупноочаговый и мелкоочаговый ИМ с указанием зоны поражения (перегородка, стенка. ). В зависимости от распространения некроза по толщине стенки выделяют:
а) трансмуральный (поражение распространяется на всю толщину миокарда и прилежащие эндокард и перикард),
б) интрамуральный — некроз развивается внутристеночно,
в) субэпикардиальный — некроз в слое миокарда, прилежащем к висцеральному листку перикарда и
г) субэндокардиальный — у эндокарда.
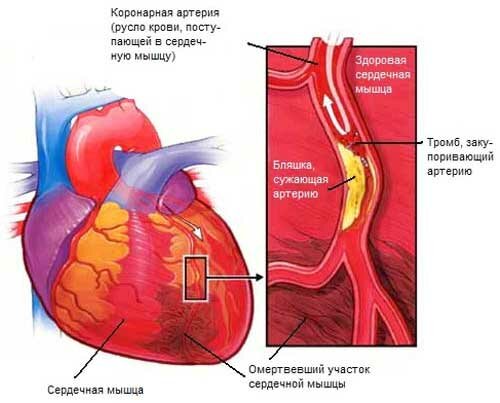
Наиболее частой причиной ИМ является прекращение притока крови к участку миокарда в измененных атеросклерозом коронарных артериях. Эмболия коронарных артерий встречается крайне редко. Чаще всего ИМ развивается при ишемической болезни сердца (ИБС). Огромное влияние имеют функциональные расстройства коронарного кровообращения, рефлекторный спазм коронарных артерий. К факторам риска относят пожилой возраст, увеличение содержания липидов в сыворотке крови, артериальную гипертензию, генетическую предрасположенность, сахарный диабет, ожирение, подагру, гиподинамию, повышенную эмоциональность, курение.
Большое значение в развитии ИМ придают нарушениям микроциркуляции, гиперкоагуляция и гиперагрегация, повышение адгезивных свойств тромбоцитов. Резкое сужение просвета коронарных артерий (например, атеросклеротической бляшкой) может создать условия для возникновения острой коронарной недостаточности.
В формировании клинических проявлений ИМ участвует ряд патогенетических факторов:
1) Перераздражение интерорецепторов миокарда, эндокарда и висцерального листка перикарда с иррадицией раздражения в спинной мозг, подкорковые структуры и кору головного мозга, что формирует стрессовую реакцию. Это активирует систему гипоталамус — гипофиз — кора надпочечников с повышением в крови катехоламинов — первая фаза стресса. С ней связаны артериальная гипертензия и тахикардия, гипергликемия, эозинопения. Однако чрезвычайно интенсивная боль может вызвать развитие артериальной гипотензии и быть причиной коллапса(collapsus).
2) Острое уменьшение УО вследствие прекращения сократительной деятельности некротизирующегося учаска миокарда является одной из причин развития как преходящей артериальной гипотензии, так и необратимого кардиогенного шока, сердечной астмы, отека легких, поражения внутренних органов. Снижение МО как реакция системы кровообращения, на его поддержание развивается спазм периферических сосудов, повышение АД = централизация кровообращения (мозг, сердце за счет остальных органов).
3) Развитие резорбционно-некротического синдрома и асептического воспаления в связи с высвобождением из некротизированных клеток ферментов и токсических продуктов → увеличение количества тромбоцитов, нейтрофильный лейкоцитоз, увеличение СОЭ.
4) Перераспределение электролитов в области, прилежащей к очагу некроза ведет к возникновению электрической нестабильности миокарда в периинфарктной зоне и создает предпосылки к развитию нарушений ритма: желудочковые экстрасистолии и тахикардии. На ЭКГ — монофазная кривая. В дальнейшем формируется соединительно-тканный рубец, кардиосклероз, истончение стенки сердца и формирование аневризмы.
Диагностика: ЭКГ и лабораторное определение ферментов поврежденных клеток.
Патогенетическая терапия: поддержание сократительной функции –
а) стимуляторы деятельности сердца;
б) разгрузка его – снижение ОЦК — мочегонные средства, жгуты на конечности;
в) снять болевой синдром;
д) борьба с тромбозом — гепарин, фибринолизин — только в ранние сроки.
До 5-6 часов может быть реинфузионный синдром — продукты распада тканей вызывают вторичное нарушение миокарда и системы кровообращения.
Для снижения опасности ИМ — тренировка в состоянии гипоксииумеренное стрессирование. Тренированное сердце дает в 3 раза меньше зону некроза — клетки более устойчиы. Японцы считают, что 5 мин движения с пульсом 100/мин — достаточно для профилактики, или бег по 15 мин несколько раз в неделю.
Острая закупорка легочной артерии — тромбоз и эмболия. Патогенез — первые отделы сердца моментально переполняются кровью — острейшая смерть — рефлекс Китаева. Пример тромбоэмболии легочной артерии.
Хроническая сердечная недостаточность (ХСН) часто развивается при недостаточности кровообращения, сопровождается стенокардией в двух формах:
1) повышение уровня метаболизма миокарда при неспособности его обеспечить при физических или эмоциональных нагрузках — стенокардия напряжения;
2) при нормальной метаболической активности миокарда сужен просвет коронарных артерий — стенокардия покоя.
ХСН имеет 3 стадии:
1) Начальная, скрытая, проявляется только при физической нагрузке, а в покое гемодинамика и функции органов не нарушены.
2) Выраженная, длительная недостаточность кровообращения с застойными явлениями в малом и большом круге кровообращения, с нарушениями функций органов и обмена веществ в покое.
Период А — незначительные расстройства гемодинамики и нарушения функции сердца или только какого-либо его отдела.
Период Б — конец длительной стадии с глубокими нарушениями гемодинамики.
3) Терминальная, дистрофическая стадия недостаточности кровообращения с тяжелыми, стойкими нарушениями метаболизма и функции всех органов и необратимыми изменениями внутренних органов.
Причины:
1. хроническая коронарная недостаточность → коронаросклероз, ИБС;
2. пороки сердца — врожденные и приобретенные нарушения клапанного аппарата сердца: недостаточность → ретроградный возврат и переполнение камер сердца, стеноз → препятствие кровотоку → увеличение периферического сопротивления;
3. патологические процессы в миокарде — миокардиты, миокардиодистрофии;
4. экстракардиальные причины:
а) гипертоническая болезнь,
б) увеличение ОЦК,
в) болезни легких → затруднение кровотока в правом отделе сердца,
г) гипертиреоз — все это истощает энергитику сердца.
Клинические проявления ХСН: Одышка — наиболее ранний и частый симптом. Одышка возникает из-за накопления в крови молочной и других кислот, изменения pH, снижение ЖЕЛ. Для выраженной одышки характерны ночные приступы удушья, которые могут перейти в отек легких.
Отеки — один из характерных признаков СН — вначале скрытые, сначала на ногах, пояснице, затем по всей подкожной клетчатке. Постепенно увеличивается печень в связи с застойными явлениями при правожелудочковой недостаточности. Набухают и пульсируют шейные вены. Увеличивается селезенка. Страдают функции почек, ЖКТ.
На гипоксию реагируют различные системы, но ведущая роль принадлежит сердцу.