Применение непрямых антикоагулянтов при мерцательной аритмии
Е.Н. Данковцева, Д.А. Затейщиков
Мерцательная аритмия (МА) — самое распространенное нарушение сердечного ритма. Особую опасность при МА представляют тромбоэмболические осложнения (прежде всего, ишемический инсульт), развивающиеся как при рецидивирующей, так и постоянной форме этого заболевания.
В обзоре рассматриваются возможные механизмы развития тромбоэмболических осложнений при МА, приводятся критерии и факторы риска их развития, схемы риск-стратификации для первичной профилактики тромбоэмболий у пациентов с неклапанной МА. Подробно обсуждается роль эхокардиграфии в качестве предиктора тромбоэмболических осложнений при МА. Подчеркивается, что важнейшим элементом лечения МА является профилактика тромбоэмболий с помощью антитромботической терапии, которая в настоящее время базируется на применении оральных антикоагулянтов, среди которых в качестве препарата выбора может рассматриваться варфарин. Подробно обсуждаются механизмы антикоагулянтного действия варфарина, результаты клинических исследований эффективности и безопасности этого препарата, применявшегося как в виде монотерапии, так и в сочетании с другими антитромботическими средствами. Приводятся схемы терапевтического применения варфарина в различных клинических ситуациях, базирующиеся на поддержании оптимального уровня антикоагуляции.
Мрцательная аритмия (МА; фибрилляция предсердий) является наиболее часто встречающимся нарушением сердечного ритма. Ее частота увеличивается у пациентов обоего пола после 40 лет и резко возрастает после 65 лет, встречаясь приблизительно у 10% населения в возрасте старше 80 лет. Клиническая и социальная значимость МА, наряду с другими аспектами, состоит в том, что она является важным независимым фактором риска развития инсульта. В Framingham Heart Study риск инсультов у пациентов с МА увеличивался с 1,5% (в возрасте 50-59 лет) до 23,5% (в возрасте 80-89 лет) [7]. В исследовании Stroke Prevention in Atrial Fibrillation (SPAF) частота ишемических инсультов составила 3,2% при рецидивирующей и 3,3% при постоянной форме МА [42].
Возможные механизмы развития тромбоэмболических осложнений при мерцательной аритмии
Хотя известно, что источником эмболии при ишемическом инсульте и системной артериальной окклюзии у пациентов с МА обычно является левое предсердие, патогенез тромбоэмболии до конца не изучен. Более 25% инсультов при МА могут возникать вследствие серьезных сердечно-сосудистых заболеваний, других кардиальных источников эмболии или связаны с атероматозным поражением проксимального отдела аорты [17,37,64].
При МА отмечается уменьшение скорости кровотока в ушке левого предсердия, связанное со снижением его сократительной функции. Хотя принято считать, что для формирования тромба требуется продолжительность МА около 48 ч, иногда, при чреcпищеводной эхокардиографии, тромбы обнаруживаются и до истечения этого периода времени [15,21,29,47,55,83]. Дисфункция эндотелия трудна для демонстрации, но она является важным механизмом, приводящим к формированию тромба при МА. Последняя ассоциируется также с некоторым повышением уровня биохимических маркеров коагуляции и активации тромбоцитов, которые могут отражать системную гиперкоагуляцию. Как при персистирующей форме МА, так и во время ее пароксизма выявляются нарушения гемостаза, связанные с продолжительностью приступа. Они ассоциируются с увеличением системного уровня фибриногена и D-димера, который указывает на активное внутрисосудистое тромбообразование. Повышение уровней тромбоглобулина и тромбоцитарного фактора 4 у некоторых пациентов с МА свидетельствует об активации тромбоцитов. Уровни некоторых из этих маркеров коагуляционной активности снижаются до нормальных значений во время терапии антикоагулянтами, уровни других – увеличиваются немедленно после восстановления синусового ритма и затем нормализуются [10,11,36,44,56-58,65,80].
У пациентов с ревматическим митральным стенозом во время проведения митральной баллонной вальвулопластики было продемонстрировано местное нарушение коагуляции в левом предсердии. Уровни фибринопептида А, комплекса тромбин/антитромбин III, фрагмента протромбина F1.2 были повышены в левом предсердии по сравнению с таковыми в правом предсердии и бедренных венах, что свидетельствует о региональной активации коагуляционного каскада. Связаны ли эти изменения с МА неизвестно, но региональная коагулопатия ассоциируется со спонтанным эхо-контрастированием в левом предсердии [31,59,81,102].
Некоторые доказательства вклада нарушенной коагуляции в тромбообразование следуют из исследовательского анализа SPAF III, в котором гормональная заместительная терапия (ГЗТ) была расценена как независимый фактор риска инсульта. Известно, что ГЗТ влияет на коагуляцию и является фактором риска венозных тромбоэмболий. Однако предполагаемая связь между использованием ГЗТ и инсультом при МА требует подтверждения до того, как эти данные будут перенесены в клинику [40].
Таким образом, в процессе образования тромба при МА участвуют сложные тромбоэмболические механизмы, включающие стаз крови в левом предсердии/ушке левого предсердия, эндотелиальную дисфункцию и системную (возможно, и локальную) гиперкоагуляцию.
Определение риска тромбоэмболических осложнений
К факторам риска тромбоэмболических осложнений МА относят возраст старше 65 лет, артериальную гипертензию, застойную сердечную недостаточность, ИБС, сахарный диабет, инсульт, преходящее нарушение мозгового кровообращения или эмболию в другие органы в анамнезе [9,41,67,89,90]. Наибольший риск эмболических осложнений при МА наблюдается при недавно начавшейся аритмии, в первый год ее существования и непосредственно после восстановления синусового ритма [42].
Количество системных эмболий при поражении митрального клапана (стеноз или недостаточность) также возрастает при наличии МА. У пациентов с ревматическим поражением митрального клапана и МА риск эмболий в 7 раз выше, чем у больных с синусовым ритмом; при сочетании поражения митрального клапана и МА признаки системных эмболий обнаруживаются в 41% аутопсий. При митральном стенозе эмболии отмечаются в 1,5 раза чаще, чем при недостаточности митрального клапана [85]. Возможно, это связано с тем, что недостаточность митрального клапана способствует возникновению турбулентного регургитационного потока, уменьшающего стаз крови в левом предсердии [32,68].
Важно подчеркнуть, что абсолютная частота инсультов значительно различается (до 25 раз) между отдельными категориями пациентов с МА. Так, у молодых больных с идиопатической МА она составляет всего 0,5% в год, а у пожилых пациентов с инсультом в анамнезе – достигает 12%. В целом адекватно подобранная доза варфарина снижает вероятность развития инсультов при МА, но у больных с низким риском этого осложнения абсолютное снижение частоты инсультов при проведении этой терапии невелико [40]. Поэтому оценка риска инсульта у конкретного пациента с МА имеет важное значение при решении вопроса о проведении антикоагулянтной терапии. Для стратификации риска ишемического инсульта при МА предложены 3 схемы (табл. 1 ) [53,90].
Роль эхокардиографии в определении риска тромбоэмболических осложнений
Наиболее часто тромб при МА возникает в ушке левого предсердия, которое не может рутинно обследоваться при помощи трансторакальной эхокардиографии. Чреcпищеводная допплеровская эхокардиография является чувствительным и специфичным методом оценки функции ушка левого предсердия и определения в нем тромботического материала. Спонтанное эхоконтрастирование в левом предсердии и ушке левого предсердия, наблюдаемое при чреcпищеводной эхокардиографии, — хорошо известный предиктор тромбоэмболий при неревматической МА и отражает сниженный кровоток и гиперкоагуляционное состояние в левом предсердии. Спонтанное эхоконтрастирование наблюдается не только в левом предсердии или других камерах сердца, но и в аорте. Имеются сообщения об ассоциации между спонтанным эхоконтрастированием в аорте и риском эмболий периферических артерий [40,68].
Среди пациентов высокого риска с МА предикторами тромбоэмболий являются следующие эхокардиографические особенности: нарушение систолической функции левого желудочка при трансторакальной эхокардиографии, тромб, спонтанное эхоконтрастирование или снижение скорости кровотока в ушке левого предсердия, сложные атероматозные бляшки в грудной аорте, выявленные при чреcпищеводной эхокардиографии. Другие эхокардиографические признаки, такие как диаметр левого предсердия и фиброкальцифицирующие эндокардиальные изменения, вариабельно ассоциируются с тромбоэмболиями и могут взаимодействовать с другими факторами. Указывает ли отсутствие этих изменений на группу пациентов низкого риска, которые могут без опасения избежать применения антикоагулянтов, не установлено, и их наличие не нашло пока отражения в схемах риск-стратификации [87,89,96,103].
Предупреждение тромбоэмболий с помощью антитромботической терапии
За последние 10 лет было проведено большое количество рандомизированных клинических исследований, которые изменили тактику антитромботической терапии у миллионов пациентов с МА (табл. 2 ) [40].
Исследования SPAF проводились в 1987-97 гг. и спонсировались U.S. NIH/NINDS. Первое из них (SPAF I) показало превосходство варфарина и аспирина над плацебо при профилактике инсульта у пациентов с МА, последующие исследования сравнивали варфарин с аспирином (SPAF II), а также интенсивную терапию варфарином с менее интенсивной терапией варфарином в сочетании с аспирином (SPAF III). К настоящему времени с целью тестирования различных типов и комбинаций антитромботической терапии для профилактики инсульта при МА проведено около 25 рандомизированных исследований. В целом в этих исследованиях антитромботическая терапия обеспечивала снижение риска инсульта приблизительно на 60% [40].
Пять исследований со сравнительно сходным дизайном были посвящены антикоагулянтной терапии в качестве средства первичной профилактики ишемического инсульта у пациентов с неклапанной (неревматической) МА. Исследования SPAF, Boston Area Anticoagulation Trial for Atrial Fibrillation и Stroke Prevention in Nonrheumatic Atrial Fibrillation Trial были проведены в США; исследование Atrial Fibrillation, Aspirin, Anticoagulation (AFASAK) — в Дании; Canadian Atrial Fibrillation Anticoagulation study было приостановлено раньше предполагаемого срока завершения из-за убедительного доказательства эффективности антикоагулянтной терапии в других исследований. Результаты всех 5 исследований были сходными; анализ показал 69% общее снижение риска и более чем 80% снижение риска у пациентов, которые были оставлены на терапии варфарином. Отмечались небольшие различия в частоте больших или внутричерепных кровотечений в группе варфарина и контрольной группе, частота небольших кровотечений в группе варфарина превышала таковую в контрольной группе на 3% [45,46].
Европейское исследование по вторичной профилактике инсульта сравнивало антикоагулянтную терапию, аспирин и плацебо у пациентов с МА, перенесших неинвалидизирующий инсульт или транзиторную ишемическую атаку в течение предшествующих 3 месяцев. По сравнению с плацебо, риск инсульта при применении варфарина снижался на 68%, а при использовании аспирина – только на 16%. У пациентов из группы варфарина не было отмечено внутричерепных кровотечений [45,46].
В исследовании SPAF-II варфарин по способности предупреждать ишемический инсульт заметно превосходил аспирин, но его применение ассоциировалось с возрастанием частоты внутричерепных кровотечений, особенно среди пациентов старше 75 лет, у которых она составляла 1,8% в год. При этом следует отметить, что интенсивность антикоагулянтной терапии в исследованиях SPAF была выше, чем в большинстве других исследований, посвященных первичной профилактике инсульта. Чаще всего внутричерепные кровотечения развивались при уровне МНО выше 3,0. В исследовании SPAF III варфарин (МНО 2,0-3,0) по эффективности намного превосходил комбинацию фиксированной дозы варфарина (1-3 мг/день; МНО 1,2-1,5) с аспирином (325 мг/день) у пациентов высокого риска по развитию тромбоэмболий, тогда как у пациентов низкого риска достаточной была монотерапия аспирином [39,45,46].
К задачам антитромботической терапии при МА относятся: предотвращение образования тромбов в предсердиях при постоянной форме МА, предотвращение увеличения и отрыва имеющихся стабильных тромбов при постоянной форме МА, профилактика образования тромбов при пароксизмальной МА (в т.ч. при подготовке к кардиоверсии), профилактика «нормализационных эмболий» [1].
Для профилактики тромбоэмболий при МА сегодня используются 3 группы антитромботических препаратов: антиагреганты, антикоагулянты прямого и непрямого действия. При этом наиболее эффективными, как показали многочисленные клинические исследования, являются непрямые антикоагулянты.
Механизм действия непрямых антикоагулянтов
Непрямые антикоагулянты представляют собой антагонисты витамина К, являющегося кофактором для посттрансляционного карбоксилирования глутаматных остатков N-терминальных участков витамин К-зависимых белков (факторы свертывания II, VII, IX и X) [22,45,46,69]. Непрямые антикоагулянты реализуют свой основной фармакологический эффект посредством нарушения цикла превращения витамина К, результатом чего становится продукция печенью частично карбоксилированных и декарбоксилированных белков со сниженной прокоагулянтной активностью. Помимо этого, указанные препараты угнетают карбоксилирование регуляторных антикоагулянтных протеинов С и S, и при их врожденном дефиците могут оказывать и прокоагулянтное действие.
Эффект непрямых антикоагулянтов может быть нейтрализован витамином К1 (получаемым с пищей или назначенным с лечебной целью). Пациенты, получившие большую дозу витамина К1, могут в течение недели оставаться резистентными к варфарину, так как витамин К1 аккумулируется в печени.
Следует отметить, что варфарин вмешивается и в процесс карбоксилирования гамма-карбоксиглутаматных белков, синтезирующихся в костях [60,79,84]. Этот эффект способствует возникновению фетальных аномалий костной ткани при приеме варфарина матерью во время беременности, однако нет доказательств его влияния на костный метаболизм при назначении детям или взрослым [20,45,46].
В зависимости от химической структуры непрямые антикоагулянты представляют собой производные монокумарина и индадионы. За несколько десятилетий применения этих препаратов в клинической практике обнаружены несомненные преимущества монокумаринов перед другими оральными антикоагулянтами: они реже вызывают аллергические реакции и обеспечивают более стабильный антикоагулянтный эффект [3]. Наиболее активно применяющимися производными монокумарина являются варфарин и аценокумарол. При этом варфарин является препаратом выбора в силу более стабильного воздействия на процесс свертывания крови. Применение некогда популярного фенилина (группа индадионов) ограничено его токсичностью [2].
Фармакокинетика и фармакодинамика варфарина
Варфарин представляет собой рацемическую смесь двух оптически активных R- и S-изомеров в приблизительно равной пропорции. Он обладает высокой биодоступностью, быстро всасывается из желудочно-кишечного тракта и достигает максимальной концентрации в крови у здоровых добровольцев через 90 мин после приема внутрь [19,50,78]. Время полужизни рацемического варфарина составляет от 36 до 42 ч, в крови он находится в связанном с белками плазмы (главным образом, с альбумином) состоянии и только 1-3% свободного варфарина оказывают влияние на превращение витамина К в печени. Варфарин накапливается в этом органе, где оба его изомера метаболически трансформируются различными путями. На дозозависимый эффект варфарина влияют генетические и внешние факторы, включающие недавно открытую мутацию гена, кодирующего один из изоферментов системы цитохрома Р450 (2С9). Эта мутация, вероятно, влияет на вариабильность ответа на одну и ту же дозу варфарина у здоровых субъектов [6,63,72]. Пациенты с генетической резистентностью к варфарину требуют 5-20-кратного увеличения дозы, по сравнению со средними значениями, необходимыми для достижения антикоагулянтного эффекта. Этот феномен приписывается нарушенной аффинности рецепторов к варфарину.
Различные заболевания, лекарства и диетические факторы также могут вмешиваться в ответ на варфарин. Кроме того, вариабельность антикоагулянтного ответа наблюдается и вследствие небрежного лабораторного тестирования, некомплаентности пациента и недопонимания между пациентом и врачом. Сопутствующая терапия способна влиять на фармакокинентику варфарина путем снижения абсорбции в желудочно-кишечном тракте или нарушения его метаболического клиренса. Например, эффект варфарина ослабляется колестирамином, уменьшающим его абсорбцию, и потенцируется препаратами, которые угнетают клиренс варфарина стереоселективным или неселективным путем. Стереоселективные взаимодействия влияют на оксидативный метаболизм S- или R-изомера варфарина. Ингибирование метаболизма S-варфарина клинически более важно, так как этот изомер в 5 раз активнее в качестве антагониста витамина К, чем R-изомер [19,76]. Клиренс S-изомера ингибируется фенилбутазоном, сульфинпиразоном, метронидазолом и триметоприм-сульфаметоксазолом, каждый из которых потенциирует эффект варфарина на протромбиновое время [19,71,76,77,98]. В то же время циметидин и омепразол, ингибирующие клиренс R-изомера, оказывают на протромбиновое время (ПВ) у пациентов, получающих варфарин, лишь умеренный потенцирующий эффект [73]. Антикоагулянтное действие варфарина блокируется барбитуратами [71], рифампицином [73] и карбамазепином [71], которые увеличивают его метаболический клиренс путем индукции печеночной смешанной оксидазной активности. Хотя длительный прием алкоголя потенциально может повышать клиренс варфарина посредством сходного механизма, употребление даже большого количества вина, как было показано в одном из исследований [74], мало влияет на протромбиновое время при терапии этим антикоагулянтом [24].
Пациенты, длительно получающие варфарин, чувствительны к колебаниям уровня витамина К, поступающего с пищей [71,92]. Увеличение потребления витамина К с пищей достаточно для снижения антикоагулянтного ответа, что наблюдается у пациентов, находящихся на диете с целью снижения веса, получающих зеленые овощи или содержащие витамин К добавки. Снижение потребления витамина К1 с пищей, напротив, потенцируют эффект варфарина, что наблюдается, например, при синдроме мальабсорбции. Дисфункция печени усиливает ответ на варфарин посредством нарушенного синтеза факторов коагуляции. Гиперметаболическое состояние, вызванное лихорадкой или гипертиреозом, усиливает действие варфарина, возможно путем увеличения катаболизма витамин К-зависимых факторов свертывания.
Wells с соавт. [101] провели критический анализ исследований, посвященных возможным взаимодействиям лекарственных средств и пищевых продуктов с варфарином. Данные о взаимодействиях, сгруппированные по типу и степени доказательности исследований, представлены в таблице 3 .
Мониторинг терапии оральными антикоагулянтами
Определение ПВ – метод, который наиболее часто используется для мониторинга при лечении непрямыми антикоагулянтами. ПВ отражает снижение уровня трех из четырех витамин К-зависимых прокоагулянтных факторов свертывания (II, VII и X). В течение первых нескольких дней терапии варфарином удлинение ПВ отражает, главным образом, снижение уровня фактора VII, позднее – также факторов X и II. Измерение ПВ производится путем добавления кальция и тромбопластина к цитратной плазме. Тромбопластином называется фосфолипидно-белковый экстракт из тканей легкого, мозга или плаценты различных млекопитающих. Он содержит тканевой фактор и фосфолипиды, необходимые для активации фактора X фактором VII. При очевидной простоте выполнения самого теста оценка его результатов представляет серьезную проблему, так как ПВ, определенное в одном и том же образце крови в разных лабораториях, может существенно различаться, что не позволяет правильно интерпретировать результаты, а это принципиально важно для оценки эффективности лечения. Причинами такого различия могут быть: реактивы (тип тромбопластина), метод определения, техника выполнения, оценка результатов [2]. Тромбопластины различаются по биологической активности, в зависимости от источника их получения и технологии приготовления [82,104]. Неактивный тромбопластин вызывает меньшее удлинение ПВ по сравнению с активным при одной и той же степени снижения витамин К-зависимых факторов свертывания [45,46].
В настоящее время предложено измерять активность тромбопластина путем оценки Международного Индекса Чувствительности (МИЧ). МИЧ отражает чувствительность данного тромбопластина к снижению витамин К-зависимых факторов свертывания по сравнению с первичным Референтным стандартом тромбопластина, определенным ВОЗ (МИЧ = 1); более чувствительным является реагент с более низким значением МИЧ. В 80-е гг. прошлого века большинство лабораторий в США использовали низко чувствительные тромбопластины со значением МИЧ 1,8 и 2,8, в то время как в Европе применялись реагенты с МИЧ от 1,0 до 1,4. Позднее более чувствительные тромбопластины стали использоваться и в американских лабораториях. Рекомбинантные человеческие препараты, составленные из релипидированного синтетического тканевого фактора, имели уровни МИЧ от 0,9 до 1,0 [99]. Различия в чувствительности тромбопластинов были главной причиной для клинически значимых различий в дозах оральных антикоагулянтов, применяемых в разных странах. В настоящее время значения МИЧ предприятиям-изготовителям рекомендуется указывать на образцах выпускаемого тромбопластина.
Результаты протромбинового теста выражают в виде показателя МНО (Международного нормализованного отношения):
МНО = (ПВ пациента/ПВ контрольной нормальной плазмы)МИЧ
МНО базируется на значении МИЧ в отношении плазмы пациентов, получающих стабильную дозу антикоагулянтов в течение, как минимум, 6 недель. Поэтому МНО недостаточно точный показатель в начале курса терапии варфарином, особенно когда результаты получены в разных лабораториях. Тем не менее, МНО более применим, чем неконвертированное отношение ПВ [49], и его определение рекомендуется как в начальную фазу лечения, так и во время поддерживающей терапии варфарином. Хотя точность этого показателя у пациентов с заболеваниями печени остается предметом обсуждений, и в этом случае определение МНО предпочтительней определения ПВ [51].
Оптимальный уровень антикоагуляции
Требуемая интенсивность антикоагуляции состоит в балансе между предупреждением ишемического инсульта и избежанием геморрагических осложнений. Считается, что максимальная защита от ишемического инсульта при МА достигается при уровне МНО от 2 до 3 [5,48,95], а МНО от 1,6 до 2,5 ассоциируется с неполной эффективностью, оцениваемой приблизительно в 80% от достигаемой при антикоагуляции высокой интенсивности (рисунок ) [43,48].
Противопоказания к проведению антитромботической терапии
Абсолютными противопоказаниями к применению непрямых антикоагулянтов являются внутреннее кровотечение, геморрагический инсульт в анамнезе, любой инсульт в предшествующие 6 месяцев, геморрагические диатезы, опухоль спинного мозга, травма спинного мозга, операция или биопсия в предшествующие 6 недель, желудочно-кишечные, гинекологические или урологические кровотечения в предшествующие 3 месяца, цирроз печени с варикозным расширением вен.
К относительным противопоказаниям относят тяжелую артериальную гипертензию, тяжелую почечную или печеночную недостаточность с коагулопатией, менструацию, беременность, пункцию артерии.
Тактика антитромботической терапии при восстановлении синусового ритма
Традиционный подход к кардиоверсии при МА неизвестной давности или длительностью 48 ч включает применение непрямых антикоагулянтов в течение 3 недель до восстановления синусового ритма и 4 недель после него.
Ранее высказывалось мнение, что чреспищеводная эхокардиография может использоваться для идентификации пациентов без тромбоза ушка левого предсердия, которые не нуждаются в антикоагуляции, но последующие исследования и мета-анализ некоторых из них показали, что такой подход ненадежен [16,61,66]. Восстановление синусового ритма приводит к транзиторной механической дисфункции левого предсердия и его ушка (так называемая «станация»), которая может наблюдаться после спонтанной, фармакологической или электрической кардиоверсии, а также радиочастотной катетерной аблации при трепетании предсердий, и может сопровождаться появлением спонтанного эхоконтрастирования. Восстановление механической функции может задерживаться на несколько недель; длительность этого периода частично зависит от продолжительности МА до кардиоверсии. Поэтому у некоторых пациентов без тромбоза левого предсердия до кардиоверсии (по данным чреспищеводной эхокардиографии) впоследствии развиваются тромбоэмболические события. По-видимому, формирование тромбов происходит в период станации, и они выбрасываются после восстановления механической функции, что и объясняет большое число тромбоэмболий в первые 10 дней после кардиоверсии. Пациенты, у которых при чреспищеводной эхокардиографии обнаруживается тромбоз ушка левого предсердия, относятся к группе риска по развитию тромбоэмболий после кардиоверсии МА или трепетания предсердий. Антикоагулянты должны им назначаться как минимум в течение 3-4 недель до и после фармакологической или электрической кардиоверсии [12,13,28,30,38,62]. Протокол быстрой антикоагуляции предусматривает проведение перед кардиоверсией чреспищеводной эхокардиографии с последующей терапией оральными антикоагулянтами в течение 4 недель [25].
Кардиоверсия у пациентов с острой (недавно начавшейся) МА, сопровождающейся симптомами или признаками гемодинамической нестабильности, не должна откладываться до достижения требуемого уровня антикоагуляции. При отсутствии противопоказаний назначается гепарин: внутривенная болюсная инъекция с последующей продолжительной инфузией в дозе, достаточной для достижения АЧТВ в 1,5-2 раза выше рекомендованного контрольного уровня. В дальнейшем показано назначение оральных антикоагулянтов (МНО от 2,0 до 3,0) в течение не менее 3-4 недель [4].
Антикоагулянтная терапия должна проводиться вне зависимости от использованного для восстановления синусового ритма метода кардиоверсии (электрический или фармакологический). Кардиоверсия без проведения чреспищеводной эхокардиографии возможна при продолжительности пароксизма МА не более 48 ч. В этих случаях необходимость антикоагуляция до и после этой процедуры определяется в зависимости от степени риска тромботических осложнений [4].
В последнее время в литературе все чаще появляются данные о том, что контроль частоты сердечных сокращений в сочетании с применением непрямых антикоагулянтов может быть реальной альтернативой для пациентов с рецидивирующей МА [33,93].
Антитромботическая терапия при постоянной форме МА
Антитромботическая терапия (оральные антикоагулянты или аспирин) должна назначаться всем пациентам с МА для предотвращения тромбоэмболий (за исключением больных с идиопатической мерцательной аритмией). Терапия оральными антикоагулянтами в дозе, достаточной для поддержания целевого уровня МНО (от 2,0 до 3,0), должна проводиться у всех пациентов с высоким риском инсульта в отсутствие противопоказаний. Аспирин в дозе 325 мг в день является альтернативой оральным антикоагулянтам у пациентов низкого риска или у больных с противопоказаниями к их применению [4].
Подбор дозы оральных антикоагулянтов
Терапию рекомендуется начинать с поддерживающих доз: 2,5-5 мг варфарина, 1-4 мг аценокумарола. Более низкие стартовые дозы показаны лицам старше 60 лет, уроженцам Азии, в особенности лицам китайского происхождения, пациентам с нарушением функции почек и печени, артериальной гипертензией, застойной сердечной недостаточностью, а также при сопутствующей терапии препаратами, потенцирующими действие оральных антикоагулянтов. Перед назначением препарата необходимо оценить противопоказания к его применению, факторы, влияющие на продолжительность антикоагулянтного эффекта, и предполагаемую длительность терапии. До начала лечения следует выполнить общий анализ крови (включая подсчет тромбоцитов), общий анализ мочи, биохимический анализ крови с определением параметров функционального состояния печени (билирубин, активность трансаминаз, гамма-ГГТ) и почек, определить ПВ и АЧТВ. [2].
Варфарин и аценокумарол принимаются один раз в день в фиксированное время после еды. Контроль МНО проводится через 8-10 ч после приема препарата (табл. 4 ). При обычном алгоритме наблюдения на протяжении первой недели МНО рекомендуют определять ежедневно, затем через 5-10 дней, 2 и 3 недели. Все последующие измерения проводятся с интервалом в 4 недели, за исключением ситуаций, когда прием сопутствующей терапии или другие заболевания могут изменить эффективность антикоагулянтов. Коррекция дозы варфарина проводится с учетом уровня клинически необходимой гипокоагуляции. С этой целью учитывают суммарную недельную дозу (27,5-42,5 мг) препарата (табл. 5. 6 ), используя прием его чередующихся доз (табл. 7 ) [2].
Осложнения антикоагулянтной терапии
Кровотечения являются наиболее значимыми и опасными осложнениями терапии оральными антикоагулянтами. Частота внутричерепных кровотечений – наиболее опасное осложнение антикоагулянтной терапии из-за высокой вероятности фатального исхода или инвалидности, составляет около 2% от всех кровотечений. Риск внутричерепных кровотечений резко возрастает при достижении уровня МНО >4,0-5,0. Возраст пациента и интенсивность антикоагуляции – наиболее важные предикторы больших кровотечений [8]. Факторами риска кровотечений являются: возраст старше 65 лет, желудочно-кишечное кровотечение в анамнезе (язвенная болезнь без кровотечения в анамнезе не ассоциируется с увеличением риска кровотечения), тяжелые сопутствующие заболевания (артериальная гипертензия, цереброваскулярная болезнь, тяжелые заболевания сердца, почечная недостаточность, онкологические заболевания). Сопутствующая терапия аспирином также ассоциируется с увеличением частоты кровотечений даже у пациентов, получающих низкие дозы варфарина [54].
Другим серьезным осложнением терапии оральными антикоагулянтами являются кожные некрозы, связанные с врожденным дефицитом протеина С. Это осложнение почти всегда заканчивается летальным исходом и чаще развивается в первые недели терапии, преимущественно у женщин [2].
Отмена антикоагулянтной терапии
Рекомендации, касающиеся необходимости снижения дозы или отмены варфарина при возникновении кровотечения, зависят от выраженности геморрагического синдрома и ургентности ситуации. Если МНО умеренно повышено (менее 5,0) и нет признаков кровотечения, рекомендуется приостановить прием варфарина и ограничиться наблюдением. У пациентов с низким риском кровотечения, у которых МНО находится в пределах 5,0-9,0, варфарин отменяется на 1-2 дня, после чего лечение может быть возобновлено в более низкой дозе. У пациентов с повышенным риском кровотечения, пропускается одна доза варфарина и перорально назначается витамин К1 (1,0-2,5 мг). Если МНО остается высоким в течение 24 ч, следует дополнительно назначить витамин К1 в дозе 1,0-2,0 мг. Когда МНО превышает 9,0, а клинически значимое кровотечение отсутствует, назначается витамин К1 в дозе 3-5 мг перорально, возможно повторное его применение через 24-48 ч, если МНО не снижается. При более тяжелых кровотечениях или значительном повышении МНО требуется немедленная отмена оральных антикоагулянтов. При этом назначается витамин К1 (10 мг путем медленной в/в инфузии) и рассматривается возможность трансфузии свежезамороженной плазмы или концентрированного комплекса тромбина. Инфузия витамина К1 может потребоваться каждые 12 часов. Угрожающие жизни кровотечения требуют остановки терапии варфарином, назначения концентрата протромбинового комплекса и 10 мг витамина К1 путем медленной в/в инфузии. Витамин К1 внутривенно следует применять с осторожностью из-за возможности анафилактических реакций [97].
При подготовке к хирургическому или инвазивному диагностическому вмешательству применение антикоагулянтов может быть прервано на срок до 1 недели. У пациентов высокого риска (в т.ч. с протезированными клапанами сердца) или в случае, когда ряд процедур требует прерывания оральной антикоагулянтной терапии на более длительный период, может быть назначен нефракционированный или низкомолекулярный гепарин – внутривенно или подкожно соответственно [4,18,40,86]. У пациентов с низким риском тромбоэмболических событий или при минимальных хирургических вмешательствах прием оральных антикоагулянтов может быть приостановлен за несколько дней до операции, и хирургическое вмешательство должно выполняться, когда МНО ниже или равно 1,5, хотя некоторые специалисты считают допустимым в день операции уровень МНО до 2,0. Отмена антикоагулянтов с назначением витамина К должна избегаться, так как время, требующееся для реинициации терапевтической антикоагуляции варфарином при этом пролонгируется.
У пациентов с высоким риском тромбоэмболий оральные антикоагулянты также должны быть отменены за несколько дней до операции. Важно подчеркнуть, что у этой категории больных МНО должно мониторироваться ежедневно, и допускается внутривенное назначение гепарина, когда МНО опускается ниже 2,0. Хирургическое вмешательство может быть выполнено, когда МНО снизится до 1,5. Гепарин должен быть отменен за 4 часа до начала операции. Антикоагуляция гепарином и варфарином должна быть возобновлена после операции в кратчайшие возможные сроки; гепарин может быть отменен, когда МНО составит 2,0 или выше [97].
Антикоагулянтная терапия у пожилых пациентов
Хорошо известно, что больные преклонного возраста являются группой повышенного риска по развитию кровотечений, связанных с антикоагулянтной терапией, поэтому оральные коагулянты должны назначаться им с большой осторожностью, даже при наличии четких показаний. Использование минимальной эффективной интенсивности антикоагуляции особенно важно у пациентов старше 75 лет, у которых большие и незначительные кровотечения особенно часты (последние нередко приводят к отмене антикоагулянтов). Целевое МНО 2,0 обеспечивает минимизацию больших кровотечений в сравнении с МНО 2,5, поэтому оно (в пределах 1,6-2,5) рекомендуется для первичной профилактики у пациентов старше 75 лет [14,40,52].
В последнее время все чаще появляются работы, посвященные сравнительной оценке двух принципиально различающихся подходов к лечению рецидивов мерцательной аритмии [33,93]. Так, было показано, что тактика, направленная на восстановление синусового ритма, не имеет преимуществ по влиянию на выживаемость по сравнению с контролем ЧСС при рецидивирующей мерцательной аритмии. В исследовании, включавшем 4060 пациентов, наметилась тенденция к увеличению смертности в группе контроля ритма. В этой же группе отмечалось значительно большее количество побочных эффектов от применения противоаритмических препаратов, а также большее количество госпитализаций на одного пациента. Частота ишемических инсультов была низкой, приблизительно 1% в год в обоих группах. Наибольшее количество инсультов отмечалось после отмены варфарина, а также при субтерапевтическом уровне МНО во время инсульта [93].
Таким образом, рациональное назначение антикоагулянтной терапии больным с МА позволяет существенно снизить риск тромбоэмболических осложнений.
мерцательная аритмия
Варфарин
Если Вам имплантировали механический клапан, то такие медицинские препараты, как, антикоагулянты или «разжижители крови» (обычно Варфарин и Фенилин), могут быть прописаны врачом, чтобы предотвратить образования сгустков крови.
Вы должны принимать только те лекарства, которые прописал или разрешил врач. Аспирин, например, нельзя принимать не посоветовавшись с врачом.
Эти препараты продляют период времени, в течение которого ваша кровь сворачивается. Действие антикоагулянтов должно тщательно контролироваться с помощью анализа крови, называемого протромбиновым временем (время Квика) и показателем международного нормализованного соотношения (МНО).
Врач может прописать дозировку для удержания протромбинового времени в рамках определенных параметров.
Препарат обычно принимают один раз в день в одно и то же время. Важно его принимать строго в сответствии с предписанием врача. Врач также скажет как часто необходимо контролировать протромбиновое время.

Время от времени ваше лечение будет корректироваться на основании результатов вашего обследования.
Лечение антикоагулянтами ограничивает естественную способность организма останавливать кровотечение. По этой причине вы должны быть особенно осторожны с теми видами деятельности, которые могут привести к порезам или кровоизлияниям.
Любой ушиб головы может привести к серьезной травме. Если это произойдет, у вас могут начаться приступы головокружения, головная боль, слабость или онемение в конечностях, изменения в зрении или потеря сознания.
Все возникающие проблемы обсуждайте с врачом.
Меры предосторожности при приеме актикоагулянтов
Если вы принимаете антикоагулирующие препараты, Вы должны обязательно предупреждать об этом зубного или лечащего врача. В некоторых случаях перед тем или иным лечением необходимо отрегулировать дозировку или прекратить на время принимать данные препараты с тем, чтобы избежать обильного кровотечения.
варфарин
Непатентованное название препарата
Варфарин натрия
Состав
Каждая таблетка содержит:
варфарина натрия 2,5 мг
Вспомогательные вещества: индиготин (Е-132), лактоза 50 мг, кукурузный крахмал, повидон, кальция гидрофосфат, магния стеарат (Е-572).
Описание
Таблетки от бледно-голубого до голубого цвета, круглой формы с насечками для разделения таблетки.
Фармакотерапевтическая группа
Антикоагулянт непрямого действия
Фармакологические свойства
Варфарин блокирует в печени синтез витамин К зави симых факторов свёртывания крови, а именно, фактора II, VII, IX и X. Концентрация этих компонентов в крови снижается, процесс свёртываемости замедляется. Оптимальное противосвёртывающее действие наблюдается на 3-ий — 5-ый день от начала применения препарата.
Действие варфарина прекращается через 3-5 дней после приема последней дозы. Препарат почти полностью всасывается из желудочно- кишечного тракта.
Связывание с белками на 97-99%. Терапевтическая концентрация в плазме составляет 1 — 5 мкг/мл (0,003 — 0,015 ммоль/л). Варфарин находится в виде рацемического соединения, при этом в организме человека левовращающий изомер обладает большей активностью, чем правовращающий. Метаболиты, которые образуются в печени, являются неактивными или слабоактивными соединениями. Они реабсорбируются из желчи, при этом левовращающий изомер метаболизируется быстрее.
Время полувыведения рацемического варфарина составляет около 40 часов. Он выводится через почки.
Показания к применению
Лечение и профилактика тромбозов и эмболии кровеносных сосудов:
- острый венозный тромбоз и эмболия легочной артерии (вместе с гепарином)
- послеоперационный тромбоз
- повторный инфаркт миокарда
- в качестве дополнительного мероприятия при проведении хирургического или медикаментозного (тромболитического) лечения тромбоза, а также при электрической конверсии мерцания предсердий
- рецидивирующий венозный тромбоз
- повторная эмболия легочной артерии
- наличие протезов сердечных клапанов или протезов кровеносных сосудов (возможна комбинация с оцетилсалициловой кислотой)
- тромбоз периферических, коронарных и мозговых артерий
- вторичная профилактика тромбоза и тромбоэмболии после инфаркта миокарда и при мерцании предсердий
Противопоказания
Беременность, тяжелые заболевания печени или почек, тяжелая артериальная гипертензия.
Способ применения и дозы Больным, которым предстоит хирургическое вмешательство (при высоком риске тромботических или эмболических осложнений), лечение желательно начать за 2-3 дня до операции.
В случае острого тромбоза лечение варфарином следует дополнить назначением гепарина до того момента, пока полностью не проявится эффект от пероральной антикоогулянтной терапии (не ранее, чем на 3-5 сутки лечения).
Начальные дозы Варфарин Никомед составляют 2,5 — 5 мг в сутки. Дальнейший режим дозирования устанавливают инди видуально, в зависимости от результатов определения протромбинового времени или международного нормализованного соотношения (МНО).
Протромбиновое время (ПТИ) должно быть увеличено в 2 — 4 раза от исходного, а МНО должно достигать 2,2 — 4,4 в зависимости от заболевания, опасности тромбоза, риска развития кровотечений и индивидуальных особенностей больного.
При определении МНО следует учитывать индекс чувствительности тромбопластина и использовать этот показатель в качестве поправочного коэффициента (1,22 — при использовании отечественного тромбоплостина из мозга кролика «Неопласт» и 1,20 — при использовании тромбопластина фирмы Рош Диагностика).
Пожилым и ослабленным больным обычно назначают более низкие дозы препарата. Полная суточная доза должна приниматься в один прием, в одно и то же время суток.
При протезировании клапанов сердца, остром венозном тромбозе вен или эмболии (на начальных этапах), тромбозе левого желудочка и для профилактики сердечного приступа нужно достигать максимально эффективного противосвертывающего эффекта, МНО должно достигать 2,8 — 4,5.
В случае мерцания предсердий и при проведении поддерживающей терапии при тромбозе вен и эмболии добиваются умеренного противосвертывающего эффекта (МНО 2,8 — 3,0).
При совместном применении варфарина с препаратами ацетилсалициловой кислоты показатель МНО должен находится в пределах 2,0-2,5. — контроль во время лечения.
Перед началом терапии определяют показатель МНО (соответственно протромбиновому времени с учетом коэффициента чувствительности тромбопластина). В дальнейшем проводят регулярный, каждые 4-8 недель, лабораторный контроль. Продолжительность лечения зависит от клинического состояния больного. Лечение можно отменять сразу.
Побочное действие
Наиболее часто — кровоточивость.
Редко — диарея, повышение активности ферментов печени, экзема, некроз кожи, васкулиты, выпадение волос.
Передозировка
Оптимальный уровень лечения лежит на границе развития кровотечений, поэтому пациент может иметь незначительные кровотечения, например, микрогематурия, кровточивость десен и т.п. если больной не имеет «местных» причин для кровотечения, например, мочекаменной болезни, серьезной опасности от такого кровотечения нет до тех пор, пока Протромбиновое время составляет более чем 5%. В легких случаях достаточно снизить дозу препарата или прекратить лечение на короткий срок.
Антидот .
В случае тяжелого кровотечения можно назнчить небольшие дозы витамина К до восстановления коагулянтной активности. При жизнеугрожающих кровотечениях необходимо немедленное переливание концентрата факторов протромбинового комплекса или свежезамороженной плазмы или цельной крови.
Особые указания
Обязательным условием терапии варфарином является строгое соблюдение больным приема назначенной дозы препарата. Не следует назначать варфарин пациентам с кровотечением любой локализации.
Необходимо проявлять особую осторожность при нарушении свертываемости крови, тромбоцитопении, язвенной болезни желудка и 12-перстной кишки в стадии обострения, кровоизлиянии в головной мозг, алкоголизме и нарушении функции почек. Риск кровотечения увеличивается при одновременном использовании с препаратами ацетилсалициловой кислоты или другими нестероидными противовоспалительными средствами (НПВС) вследствие подавления ими функциональной активности тромбоцитов.
Препарат не следует назначать беременным женщинам в связи с выявленным тератогенным действием, развитием кровотечений у плода и гибелью плода. Варфарин выводится с материнским молоком в незначительном количествех и не оказывает влияния на свертываемость крови у ребенка, поэтому препарат можно применять в период лактации, однако желательно воздержаться от кормления грудью в первые 3 дня терапии варфарином.
В случае потребления больших количеств алкоголя увеличивается опасность гипопротромбинемии и развития кровотечений.
Взаимодействие с другими лекарственными средствами
НЕ РЕКОМЕНДУЕТСЯ начинать или прекращать прием других лекарственных средств, а также изменять дозы принимаемых препаратов без консультации с лечащим врачом. Значительное число лекарственных средств вступает во взаимодействие с пероральными антикоагулянтами. Наиболее важные из них: антибиотики широкого спектра действия, салицилаты, НПВС, клофибрат, барбитураты, фенитоин, пероральные противодиабетические препараты. Сочетание варфарина с НПВС в значительной степени увеличивает опасность кровотечения.
Это частично обусловлено их непосредственным действием на механизм свёртываемости крови и частично фармакокинетическим действием варфарина. Кроме того, проявляется ингибирующее действие НПВС на гемостатическую функцию тромбоцитов. Это действие наблюдается при использовании других ингибиторов функции тромбоцитов, таких как дипиридамол и вальпроевая кислота. Следует избегать комбинаций с подобными препаратами. Также следует избегать сочетанного применения варфарина с препаратами, обладающими выраженным ингибирующим действием на систему цитохрома Р450, например, циметидином и хлорамфениколом, при приёме которых в течение несколько дней увеличивается опасность кровотечения. В подобных случаях циметидин можно заменить, например, ранитидином или фамотидином. При необходимости лечения хлорамфениколом антикоагулянтную терапию возможно временно прекратить.
Прием диуретиков в случае выраженного гиповолемического действия может привести к увеличению концентрации факторов свёртываемости, что уменьшает действие антикоогулянтов. В случае сочетанного применения варфарина с другими препаратами, указанными в приведенном ниже списке, необходимо проводить контроль (МНО) в начале и в конце лечения, и, по возможности, через 2-3 недели от начала терапии. Это относится к сочетанию с лекарственными средствами, индуцирующими ферменты печени (барбитураты, фенитоин, карбамазепин) и, тем самым, ослабляющими антикоагулянтное действие варфарина.
При использовании препаратов, которые могут повысить риск развития кровотечения путем уменьшения нормальной коагуляции или путем ингибирования факторов свертывания крови, или умеренного ингибирования ферментов печени, например слабительные средства, стратегия антикоагулянтной терапии должна зависеть от частоты проведения лабораторного контроля. Если возможен частый лабораторный контроль терапии, то при необходимости терапии подобными средствами дозу варфарина можно изменить (повысить или уменьшить) на 5-10%. Если проведение лабораторного контроля терапии затруднено, то лечение варфарином необходимо прекратить в случае необходимости назначения указанных препаратов.
Следует подчеркнуть, что приведённый перечень препаратов, взаимодействие с которыми необходимо учитывать, является далеко неполным.
Ослабление действия варфарина происходит при его совместном применении с барбитуратами, витамином К, глютетимидом, гризеофульвином, диклоксациллином, карбамазепином, коэнзимом 010, миансерином, парацетамолом, ретиноидами, рифампицином, сукралфатом, феназоном, холестриомином.
Усиление действия варфарина наблюдается при его совместном применении с аллопуринолом, амиодароном, анаболическими стероидами (алкилированными в положении С-17), ацетилсалициловой кислотой и др. НПВС, гепорином, глибенкламидом, глюкагоном, даназолом, диозоксидом, дизопирамидом, дисульфирамом, изониозидом, кетоконазолом, кларитромицином, клофибротом, левамизолом, метронидазолом, миконазолом, нолидиксовой кислотой, нилютомидом, омепразолом, пароксетином, прогуанилом, противодиабетическими средствами — производными сульфаниламидов, симвастатином, сульфаниламидами, томоксифеном, тироксином, хинином/хинидином, флювоксамином, флюконазолом, фторурацилом, хинолонами, хлоралгидратом, хлоромфениколом, цефалоспоринами, циметидином, эритромицином, этакриновой кислотой.
Этанол может усиливать действие варфарина.
Форма выпуска
Пластиковые флаконы, каждый из которых содержит 50 и 100 таблеток ВАРФАРИН НИКОМЕД 2,5 мг.
Условия хранения
Хранить при комнатной температуре до 25°С в недоступном для детей месте.
Если Вам назначили варфарин
Середавкина Н.В. Решетняк Т.М.
Как кровь движется по сосудам?
Сердце представляет собой мышцу, выполняющую функцию насоса. Благодаря этому кровь распространяется по всему организму по артериям и венам, достигая самых мелких сосудов. Давление крови в ногах очень низкое, поэтому кровь от ног не может вернуться к сердцу самостоятельно. Кровоток должны подтолкнуть движения стоп, сокращения икроножных и бедренных мышц. Чтобы предотвратить возвращение крови в обратном направлении к нижним отделам ног под действием силы гравитации, в венах существуют специальные клапаны.
Процесс образования кровяных сгустков происходит в нашем организме каждый день. Когда кровеносный сосуд повреждается даже в результате небольшого пореза, к месту раны устремляются тромбоциты. Прилипая друг к другу, они образуют кровоостанавливающий сгусток и закрывают поврежденный участок. При этом начинается процесс свертывания крови, по ходу которого белки свертывающей системы активизируются один за другим. В результате молниеносной цепочки биохимических реакций вырабатывается очень прочная и эластичная субстанция — фибрин. Фибриновые нити покрывают тромбоциты сетью, в которую также попадают эритроциты (красные клетки крови). Именно поэтому кровяной сгусток имеет красный цвет. Когда целостность поврежденного кровеносного сосуда восстанавливается, кровоостанавливающий сгусток растворяется под действием особых фибринолитических ферментов.
Свертывание крови является нормальной защитной реакцией организма на повреждение сосудистой стенки. Однако при некоторых состояниях свертывание крови может оказаться повышенной и опасной, тромбы могут образовываться не только в местах травматического повреждения сосуда, но и внутри просвета сосуда или в сердце.
Такие тромбы могут нарушать деятельность органа, в котором они образуются (развивается тромбоз), либо отрываться и попадать в сосуды других органов (мозга, почек и др.), также нарушая их работу (такое состояние называется тромбоэмболия). И тромбоз, и тромбоэмболия являются грозными осложнениями.
Чем опасен тромбоз глубоких вен нижних конечностей?
Тромбоз глубоких вен нижних конечностей (ТГВ) и тромбоэмболия легочной артерии (ТЭЛА — отрыв части или всего сгустка крови из вены ног и по кровотоку, попадая в лёгочную артерию, является причиной инфаркта лёгкого), хотя и различаются, однако, некоторые процессы динамики заболевания взаимосвязаны, поэтому в зарубежной литературе эти два заболевания часто объединяются под одним названием — венозный тромбоэмболизм. Около 200 000 новых случаев венозных тромбоэмболий в год регистрируется в США, включая 94 000 случая — с ТЭЛА. Частота смертности не леченых случаев ТЭЛА достигает 30%, являясь причиной смерти приблизительно 50 000 случаев в год. Частота тромбоэмболических осложнений гораздо выше у больных с инфарктами миокарда и инсультами.
Многие ревматические заболевания являются факторами риска кардиоваскулярных и цереброваскулярных заболеваний. Тромбозы артериальные и/или венозные одно из проявлений антифосфолипидного синдрома (АФС). Развитие тромбозов при АФС
связывается с наличием определенных аутоантител — антифосфолипидных антител. Среди тромбозов при АФС самая частая локализация — глубокие вены нижних конечностей и, соответственно, частое осложнение у больных АФС тромбоэмболия легочной артерии.
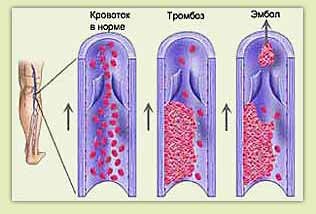
По локализации тромбы в нижних конечностях могут образовываться в подкожных венах и глубоких венах. Тромбоз глубоких вен ног в свою очередь может затрагивать проксимальные и дистальные вены. На рисунке 1 демонстрируется связь между тромбозом ног и его осложнением тромбоэмболией лёгочной артерии.
Около 50% больных с проксимальным ТГВ переносят бессимптомную ТЭЛА1
Бессимптомный ТГВ находят у 80% больных с ТЭЛА2
1. Pesavento R, et al. Minerva Cardioangiol 1997;45(7-8):369-375.
2. Girard P, et al. Chest 1999;116(4):903-908.
Рисунок 1. Связь между тромбозом ног и тромбоэмболией лёгочной артерии
Тромбозы в ногах могут:
- в редких случаях рассасываться самостоятельно без каких-либо осложнений, чаще тромбозы поверхностных вен;
- могут спровоцировать жизненно опасное состояние (эмболию легочной артерии), когда тромб отрывается от сосудистой стенки, попадает в легкие и существенно нарушает функцию дыхательной системы;
- почти в 90% случаев у пациентов, которые не получают необходимого лечения, в нижних конечностях возникают болезненные симптомы, включая варикозное расширение вен, отек ноги, обесцвечивание и воспаление кожи над областью тромба. В ряде случаев над этим участком на коже образуется язва.
Примерно в 80% случаев тромбоз глубоких вен протекает бессимптомно и свыше 70% случаев ТЭЛА диагностируется посмертно.
Клинические проявления венозного тромбоза недостаточно специфичны, но на них необходимо обращать внимание. К ним относятся:
- Распирающие боли в нижней конечности, усиливающиеся в вертикальном положении
- Отек, уплотнение мышц голени
- Гиперемия и цианотичность (синюшность) кожи ноги
- Повышение кожной температуры в зоне тромбоза по сравнению со здоровой стороной;
- Болезненность при пальпации по ходу пораженного сосуда
- Симптом Хоманса — боль в икроножных мышцах при тыльном сгибании стопы
В каждом случае, когда ток крови в венах замедляется, возникает риск возникновения тромбов.
Образование в венах сгустков крови часто является результатом:
- хирургических вмешательств;
- длительного нахождения на постельном режиме;
- обездвиженности вследствие наложения гипсовой повязки;
- длительного (более 4 часов) пребывания в положении сидя (например, при путешествии на самолете, автобусе, в машине,);
- беременности и родов;
- индивидуальной недостаточности компонентов противосвертывающей системы. Факторами высокого риска тромбообразования являются:
- возраст (40 лет и более);
- беременность;
- ожирение;
- прием гормональных контрацептивов.
Высокий риск тромбозов может наблюдаться в течение нескольких недель после хирургического вмешательства.
Имеется целый ряд врождённых факторов риска тромбоза — это изменения в самих факторах или белках, которые участвуют в свёртывание крови. Определённые состояния, присоединение любой патологии (воспаления, онкологии, инфекции) могут спровоцировать несостоятельность этих белков и у человека могут развиться тромбозы. Антифосфолипидный синдром является приобретённым тромбофилическим заболеваниям. Тромбозы в этих случаях связаны с появлением аутоантител — антител к фосфолипид-связывающим белкам крови. Больные с антифосфолипидным синдромом требуют длительной, иногда пожизненной профилактике тромбозов.
Как можно уменьшить риск развития тромбоза?
- Необходимо регулярно выполнять физические упражнения:
- продолжительное пребывание без движения в постели — один из факторов наибольшего риска образования тромбов. Поэтому активные физические упражнения в данный период помогут уменьшить этот риск;
- упражнения, которые можно выполнять в постели включают сокращение и расслабление мышц голеней и стоп так часто, как только это возможно. Ноги нужно бинтовать специальным эластичным бинтом и носить особые стягивающие колготки/гольфы (компрессионный трикотаж). При этом стимулируются икроножные мышцы, усиливается их «насосная» функция, создаются благоприятные условия для венозного кровотока. Аналогичный результат может быть достигнут при выполнении упражнения, имитирующего езду на велосипеде, и при отталкивании ногами от спинки кровати.
- Лечение венозных тромбозов и эмболий
- Возвышенное положение пораженной нижней конечности
- Эластический трикотаж: бинты с последующим переходом на эластические чулки со 2-й степенью компрессии (давление на уровне лодыжек 25-32 мм рт. ст.)
Лекарственная терапия включает в себя применение антикоагулянтов
Что такое антикоагулянты?
Антикоагулянтами называют лекарственные препараты, воздействие которых на организм снижает свертываемость крови. Они предотвращают образование кровяных сгустков (тромбов).
Для предотвращения либо лечения тромботических осложнений бывает необходимо снизить свертываемость крови, т.е. заставить кровь сворачиваться несколько медленнее, чем в норме. Именно в таких случаях и применяют антикоагулянты.
В 1939 году группа американского биохимика К. Linka выделила из сладкого клевера (более известного, как белый донник) вещество дикумарол, и с 1947 года, после многолетних исследований, препараты этой группы используются как лекарственное средство.
Механизм действия антикоагулянтов
Синтез целого ряда факторов свертывания крови связан с воздействием витамина К. Антикоагулянты нарушают связь витамина К с предшественниками факторов свертывания II, VII, IX и X, нарушая синтез нормальных конечных форм этих веществ в печени.
Антикоагулянты, используемые в настоящее время
В настоящее время существует целый ряд антикоагулянтов, выпускаемых в таблетках (маркумар, синкумар, дикумарин, тромексан, фенилин, дипаксин). Однако все больше специалистов назначают варфарин, малотоксичный и по длительности действия наиболее легко поддаётся лабораторному мониторингу. Варфарин, а также другие производные кумарина, блокирует в печени синтез витамин К зависимых факторов свёртывания крови, а именно, фактора II, VII, IX и X и естественные антикоагулянты крови. Концентрация этих компонентов в крови снижается, процесс свёртываемости замедляется. Начало противосвертывающего действия наблюдается через 36-72 часа от начала приема препарата с развитием максимального эффекта на 5-7 день от начала применения. После прекращения приема препарата восстановление активности витамин К-зависимых факторов свертывания крови происходит в течение 4-5 дней. Варфарин в 97-99% связывается белками крови и метаболизируется на клетках печени ферментом цитохром Р450. Основным катализатором метаболизма варфарина является фермент CYP2C9. Полиморфизмы в генах цитохрома P-450, приводящие к возникновению аллельных вариантов генов CYP2C9*2 и CYP2C9*3, сопровождаются понижением активности кодируемых этими генами ферментов (а не уменьшением содержания их). Поскольку эти ферменты участвуют в выведении варфарина из организма, то у больных с мутациями варфарин задерживается в организме на более длительное время, и они требуют его меньших доз. Пациенты с подобным полиморфизмом гена цитохрома Р450 могут иметь повышенную чувствительность к варфарину и повышенный риск развития кровотечений. Подавление активности ещё одного фермента, участвующего также в метаболизме варфарина, эпоксидредуктазы приводит к истощению содержания в плазме активного витамина К и, соответственно, накоплению неактивных факторов свертывания крови, а следовательно и ингибированию всего процесса свертывания. Появление полиморфизма в этом гене (VKORC1) приводит к снижению уровня экспрессии гена и биосинтеза кодируемого им белка. Поскольку белка-мишени для варфарина становится меньше, то требуется меньше варфарина для подавления активности эпоксидредуктазы витамина К, и с помощью меньших доз варфарина можно ингибировать процесс свертывание крови. Поэтому при планировании длительного приёма варфарина целесообразно исследование полиморфизма генов, кодирующих метаболизм варфарина. Варфарин выводится из организма в виде неактивных метаболитов с желчью, которые реабсорбируются в ЖКТ и выделяются с мочой.
Контроль уровня свертываемости при терапии варфарином
Пациент, получающий терапию антикоагулянтами, постоянно балансирует между недостаточной дозой препарата, когда могут развиваться тромботические осложнения, и избыточным снижением свертываемости, когда возрастает риск кровотечений. Безопасное пребывание в пределах приемлемого «коридора» свертываемости требует тщательного и регулярного контроля свертываемости.
Контролируемым во всем мире параметром в настоящее время избран показатель MHO (Международное нормализованное отношение, INR). Он отражает время формирования сгустка крови (протромбиновое время) с поправкой на чувствительность реактива (тромбопластина), используемого в конкретной лаборатории.
При подборе терапии (зачастую в стационаре) контроль свертывания проводится несколько раз в неделю. По достижении показателей, приемлемых в данной ситуации, проводя регулярный, в среднем, каждые 2-4 недели, лабораторный контроль в амбулаторных или домашних условиях.
Уровень свертываемости может колебаться даже при стабильной дозе препарата. Восприимчивость организма к действию антикоагулянтов зависит от многих факторов: особенности питания, физической активности, сопутствующих болезней, функционального состояния печени и почек, сопутствующей терапии.
Контроль свертываемости рекомендуется делать чаще:
- Когда меняется сопутствующая терапия
- При простудном или любом другом заболевании
- При смене климата
- При смене привычной диеты
- При смене привычного образа жизни