Узловая тахикардия: методы лечения
Здоровье – это самый важный аспект в нашей жизни. Мы должны его ценить, ухаживать и всегда заботиться. Потому что его не купишь не за какие деньги и со временем оно не умеет улучшаться, а как раз совсем наоборот. Тем более с последними новостями об окружающей среде, да и о экологии в целом можно только ждать улучшение.
А тем временем не следует забывать о здоровье, по статистике самые распространенные диагнозы – это диабет и сердечные заболевания. К сожалению – это действительно так, особенно среди подростков и молодых людей цифры начинают расти. Давайте обсудим такую тему, как кардиология, а именно углубимся в проблемы аритмий сердца.
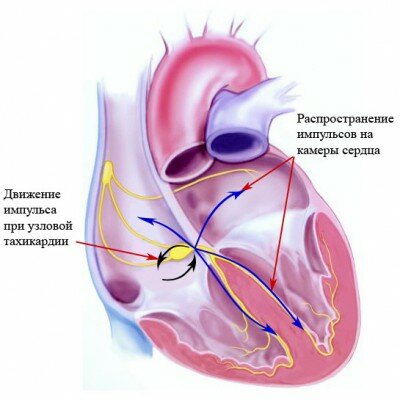
Поговорим о тахикардии и ее наиболее распространенном виде – это узловая тахикардия. В общем понятие тахикардия – это учащение сердцебиения. Ее в основном понимают как не диагноз, а последствие. Например, волнение, страх, нарушение баланса организма или множество других факторов.
Узловая тахикардия имеет еще два сопутствующих вида – это предсердная и желудочковая. Все они значительно отличаются друг от друга и относятся к пароксизмальной тахикардии.
Лечение такой тахикардии производится в основном в два метода:
- Определенный курс приема лекарств
- Радиочастотная абляция
Первый метод, наверняка понятен всем, он применяется когда у пациента приступы появляются довольно редко. А второй подходит для более сложных приступов тахикардии, его суть состоит в том, что бы с помощью специального оборудования и непосредственно катетера прожигать маленький участок в сердце для полного излечения от болезни.
Понравилось? Лайкни и сохрани у себя на страничке!
КЛИНИКО-ИНСТРУМЕНТАЛЬНАЯ ОЦЕНКА НЕМЕДИКАМЕНТОЗНЫХ СПОСОБОВ ЛЕЧЕНИЯ ПАРОКСИЗМАЛЬНОЙ РЕЦИПРОКНОЙ УЗЛОВОЙ ТАХИКАРДИИ
Аннотация
Изложены результаты клинико-инструментальной оценки немедикаментозных способов лечения (радиочастотной аблации быстрых и медленных путей) у больных с реципрокной узловой атриовентрикулярной тахикардией.

Проблема лечения пароксизмальной реципрокной атриовентрикулярной узловой тахикардии (ПРАВУТ) является весьма актуальной, так как 85-90% наджелудочковых тахикардий приходится на долю атриовентрикулярных реципрокных пароксизмальных тахикардий [1], среди которых ПРАВУТ занимает важное место.
Основой разработки способов радикального лечения ПРАВУТ явилось положение, согласно которому продольная диссоциация АВ-соединения на быстрые и медленные пути, наблюдаемая у больных с данной патологией, поддерживает функционирование петли re-entry [2, 3, 4, 6, 7]. При этом выход петли re-entry в предсердия располагается экстранодально [1, 4, 5].
Возникает возможность влиять на антероградное и ретроградное звено re-entry и тем самым купировать механизм поддержания тахикардии, оставляя интактным атриовентрикулярный (АВ) узел, что сохраняет больному синусовый ритм (CР) с антероградным проведением на желудочки.
Первые попытки радикального лечения ПРАВУТ проходили в условиях искусственного кровообращения на открытом сердце [1]. В ходе этих операций в паранодальной зоне наносились повреждения хирургическим способом, а также с применением различных видов энергии (криодеструкция, электродеструкция постоянным током, ультразвуковая деструкция, энергия лазера). Однако травматичность операций, значительное число осложнений сдерживало их широкое применение в клинике.
Разработка и внедрение в клиническую практику в последние два десятилетия различных методик катетерной аблации вывели эту область аритмологии на качественно новый уровень и открыли широкие перспективы эффективного и малотравматичного радикального лечения резистентных к консервативной терапии тахиаритмий.
Предметом настоящего исследования явилось изучение клинико-электрофизиологических критериев радикального немедикаментозного лечения ПРАВУТ с помощью радиочастотной катетерной аблации зон быстрых и медленных путей АВ-соединения.
МАТЕРИАЛ И МЕТОДЫ
Подвергнуты анализу результаты радиочастотной аблации (РЧА) 138 больных с ПРАВУТ, среди которых было 45% мужчин и 55% женщин. Средний возраст больных составил 53,2±15,4 года (от 12 до 82 лет). Аритмический анамнез — 14,7±9,3 лет. У 8% больных приступы тахикардии развивались ежедневно. 29% больных страдали приступами тахикардии несколько раз в неделю. Средняя ЧСС во время ПРАВУТ составляла в среднем 179±35,6 уд/мин.
У подавляющего числа больных (95%) антиаритмическая терапия (ААТ) была неэффективной. В 72% случаев купирование приступов тахикардии происходило только при в/в введении антиаритмических препаратов (ААП). У 4 больных для купирования гемодинамически значимой тахикардии использовалась электро-импульсная терапия (ЭИТ). На фоне приступов тахикардии у 58% больных отмечалось снижение артериального давления, а у 34% регистрировались признаки коронарной недостаточности.
В 22% случаев наблюдалось сочетание ПРАВУТ с пароксизмальной фибрилляцией предсердий. У 8% больных наряду с продольной диссоциацией АВ соединения отмечалось функционирование антеградных или ретроградных дополнительных проводящих путей на фоне различных вариантов синдрома WPW.
Двое больных наряду с ПРАВУТ имели приступы трепетания предсердий 1 типа. Всем больным до операции выполнялась чреспищеводная электростимуляция левого предсердия, в ходе которой оценивались следующие электрофизиологические параметры: АВ-проведение, наличие разрывов кривой, эффективный рефрактерный период (ЭРП) АВ-соединения, возможность провокации ПРАВУТ, время ретроградного проведения на фоне тахикардии (R-P').
На фоне максимального АВ-проведения возбуждения измерялось соотношение St-R/R-R. Неинвазивный контроль за электрофизиологическими параметрами осуществлялся на установке «Cardiocomp-2» / «Cordelectro», Каунас, Литва. Непосредственно перед выполнением радиочастотной аблации (РЧА) выполнялся полный протокол эндокардиального электрофизиологического исследования (эндоЭФИ).
Кроме указанных выше параметров оценивалась ретроградная вентрикулоатриальная (ВА) проводимость. Регистрировалась электрограмма (ЭГ) пучка Гиса с оценкой интервалов AH и HV. На фоне синусового ритма (СР) регистрировалась низкоамплитудная, фрагментированная ЭГ медленных путей АВ-соединения.
Во время пароксизмов тахикардии выполнялось картирование правого предсердия с выявлением зон их максимально раннего ретроградного возбуждения. Для выполнения эндокардиального ЭФИ и аблации в правые камеры сердца вводились 4-5 электродов через бедренные и подключичные вены. Катетеризировался коронарный синус, правый желудочек и правое предсердие, регистрировалась ЭГ пучка Гиса, вводился электрод для РЧА. Использовался комплекс приборов «Биоток-500», «Биоток», Томск, Россия.
После выполнения аблации зон медленных или быстрых путей интраоперационно выполнялось контрольное ЭФИ, провокация ПРАВУТ с применением фармакологических проб (атропин). Обследование больных, включая чреспищеводное ЭФИ, повторялось в отдаленном периоде в сроки от 6 мес до 5 лет (в среднем 2,4 года). Анализировались результаты РЧА в 2 группах: 1 — РЧА быстрых путей АВ-соединения; 2 — РЧА медленных путей АВ-соединения.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты РЧА быстрых путей АВ соединения .
Работами ряда авторов установлено, что быстрые пути, являющиеся ретроградным звеном в механизме типичной («slow-fast») узловой АВ тахикардии расположены паранодально в передней септальной зоне правого предсердия, что анатомически соответствует вершине треугольника Коха в правом предсердии.
Анализ результатов картирования передне-септальной зоны на фоне спровоцированной типичной (slow-fast) ПРАВУТ у 28 больных показал, что наиболее раннее возбуждение правого предсердия регистрировалось чаще всего в двух зонах: 1 — проксимальнее зоны устойчивой регистрации ЭГ пучка Гиса (33%) случаев); 2 — ниже АВ узла у фиброзного кольца трехстворчатого клапана (30%). Несколько реже быстрые пути локализовалась проксимальнее и выше зоны устойчивой регистрации ЭГ пучка Гиса с максимальной амплитудой (16%).
Подвергнуты анализу результаты немедикаментозного лечения ПРАВУТ с применением «переднего» доступа, то есть с помощью эндокардиального радиочастотного электровоздействия в передне-септальной зоне правого предсердия у 43 больных.
В качестве показаний к использованию данного способа у этой группы больных можно привести три: а) применение «переднего» доступа на этапе освоения способов немедикаментозного лечения ПРАВУТ (25 больных); б) невозможность локализовать зону медленных путей АВ соединения и отсутствие клинического результата РЧ аблации медленных путей (14 больных); в) сочетание ПРАВУТ с синдромом укороченного интервала P-Q (синдром LGL) — 4 больных.
В среднем использовалось 6±5,2 (от 1 до 17) аппликации РЧ тока при обязательном мониторировании интервала St-R (на фоне стимуляции предсердий) в случае возникновения ускоренного ритма АВ соединения.
Процедуру аблации прекращали в следующих случаях: 1) невозможность провокации тахикардии; 2) купирование разрыва кривой АВ-проводимости; 3) возникновение ретроградной ВА блокады; 4) уменьшение ВА проводимости более чем на 40% при невозможности индукции тахикардии. Среднее время флюороскопии составило 26±18 сек.
Общая эффективность РЧ аблации и модификации быстрых путей АВ-соединения составила 91%. Случаев развития полной АВ блокады не было отмечено. У 7 больных (16%) зафиксирована АВ блокада I степени. У 14 пациентов (32%) имела место транзиторная АВ блокада I степени в ходе вмешательства с последующим восстановлением интервала P-Q до исходного к окончанию операции. У всех больных с синдромом LGL (СLC) отмечено увеличение интервала P-Q до нормальных значений после аппликаций РЧ тока выше и проксимальнее АВ узла с одновременным купированием ПРАВУТ.
Рецидивы узловой АВ тахикардии имели место у 4 больных (9%). Причем в двух случаях приступы тахикардии рецидивировали спонтанно в ближайшем послеоперационном периоде (на 1-2-е сутки после операции). У одной больной тахикардия была вызвана в ходе ЧП ЭКС через неделю после операции. В одном случае приступы узловой АВ-тахикардии стали возникать в отдаленном периоде через два месяца после вмешательства.
У трех больных с рецидивами тахикардии выполнены повторные успешные операции. В одном случае больная от повторного вмешательства отказалась, так как приступы появлялись редко, длились от 2-х до 10 минут (до операции 2-4 часа), стали купироваться вагусными приемами, чего не было до операции.
Больные обследованы в отдаленном периоде. Случаев развития полной АВ блокады не отмечено. У одной больной при суточном мониторировании ЭКГ отмечены эпизоды АВ блокады II степени I типа в ночные часы. У этой больной после радикального лечения ПРАВУТ имела место АВ блокада I степени. Признаки диссоциации АВ-соединения на два канала в отдаленном периоде выявлены у двух больных, причем в одном случае после пробы с атропином. Наличие двойного проведения у этих пациентов не сочеталось с возможностью провокации ПРАВУТ.
Анализированы результаты изменений электрофизиологических показателей функционирования АВ-соединения у 43 больных, которым выполнялась трансвенозная РЧ аблация и модификация быстрых путей. Результаты измерений приведены в табл. 1.
Результаты аблации и модификация «быстрых» путей АВ-проведения (n=43)
Тахикардии 2 страница
#image.jpg
Рис.184-3. Внутрисердечная регистрация электрограммы левого обходного проводящего атриовентрикулярного пути во время суправентрикулярной тахикардии. Представлены внутрисердечные электрограммы, зарегистрированные на фоне нормального синусового ритма (НСР) и суправентрикулярной тахикардии (СВТ), в области верхней части правого предсердия (ВПП), венечного синуса (ВС), пучка Гиса (ПГ) и правого желудочка (ПЖ), а также отведениях I, aVF и V1 ЭКГ. Во время НСР комплексы QRS и интервалы ПГ и ПЖ не изменены. Во время СВТ отмечается патологическая последовательность ретроградной активации предсердий. Местом наиболее ранней активации является венечный синус, затем ПГ и ВПП. Выявление такой последовательности активации позволяет диагностировать наличие левого обходного атриовентрикулярного проведения возбуждения ретроградно от желудочков к предсердию. (Из: М. Е. Josephson. — In: Update IV, Harrison’s Principles of Internal Medicine/Eds. K. J. Isselbacher et al. — New York: McGraw-Hill Book Company, 1983.)
Обходные атриовентрикулярные пути, проводящие возбуждение антеградно, проявляются типичными изменениями ЭКГ — укорочением интервала Р—R (менее 0,12 с), деформацией восходящей части комплекса QRS, получившей название волны А, и расширением комплекса QRS. Эта электрокардиографическая картина является результатом прохождения импульсов, возбуждающих желудочки, как по обходному пути, так и по узловой проводящей системе Гиса — Пуркинье (рис. 184-4). Относительное участие каждого из указанных проводящих путей в активации желудочков определяет степень преждевременности возбуждения.
#image.jpg
Рис. 184-4. ЭКГ при синдроме Вольффа—Паркинсона—Уайта. Имеется короткий интервал Р—R (0,11 с), широкий комплекс QRS (0,12 с) и неровность на восходящем колене комплекса QRS вследствие ранней активации желудочков импульсом, приходящим по обходному пути (волна D, d в I отведении). Отрицательные волны А в отведении V1 являются диагностическим признаком правого обходного проводящего пути.
При пароксизмальной суправентрикулярной тахикардии у больных с синдромом Вольфа — Паркинсона — Уайта импульс проводится антеградно по физиологическим атриовентрикулярным проводящим путям и ретроградно по обходному пути. В этом случае тахикардия характеризуется теми же признаками, что и атриовентрикулярная тахикардия, в основе которой лежит феномен циркуляции возбуждения. Редко, лишь у 5 % пациентов, страдающих синдромом Вольфа — Паркинсона — Уайта, в основе тахикардии лежит обратный механизм: антеградно импульс проводится по обходному пути, а ретроградно — по физиологическим путям через предсердно-желудочковый узел. В этом случае на ЭКГ тахикардия характеризуется широкими комплексами QRS, так как желудочки активизируются импульсами, приходящими исключительно, по обходным путям. У больных с синдромом Вольфа — Паркинсона — Уайта нередко можно выявить мерцание или трепетание предсердий. И вследствие того, что проводимость обходного пути выше, чем предсердно-желудочкового узла, возбуждение желудочков во время мерцания или трепетания предсердий наступает очень быстро, что приводит к фибрилляции желудочков.
Электрофизиологическое обследование пациентов с подозрением на наличие синдрома Вольфа — Паркинсона — Уайта преследует следующие цели: 1) подтвердить диагноз; 2) установить локализацию обходного пути; 3) оценить роль обходного пути в генезе аритмии; 4) определить рефрактерный период обходного пути и риск развития во время мерцания или трепетания предсердий потенциально опасных для жизни нарушений ритма; 5) выбрать метод лечения: применение специфических препаратов, электростимуляция или хирургическое лечение.
Лечение. Лечение больных должно быть направлено на уменьшение частоты возникновения преждевременных предсердных и желудочковых комплексов, способных спровоцировать тахикардию; удлинение рефрактерного периода обходного пути (рефрактерный период длительностью менее 220 мс сопровождается быстрым возбуждением желудочков во время трепетания предсердий) и блокирование проведения импульсов по физиологической проводящей системе предсердно-желудочкового узла. Специфическая антиаритмическая терапия может быть подобрана с помощью электрофизиологических исследований.
При развитии угрожающего жизни быстрого возбуждения желудочков у больных с синдромом Вольфа — Паркинсона — Уайта и фибрилляцией предсердий необходима электроимпульсная терапия. Другим методом замедления желудочкового ритма является внутривенное введение лидокаина 2—4 мг/кг или новокаинамида 15 мг/кг в течение 15—20 мин. Лицам с синдромом Вольфа — Паркинсона — Уайта и фибрилляцией предсердий следует с осторожностью применять сердечные гликозиды, верапамил или b-адреноблокаторы, поскольку эти препараты укорачивают рефрактерный период дополнительных путей проведения, тем самым увеличивая ритм сокращений желудочков, а следовательно, повышая риск развития фибрилляции желудочков. Несмотря на то что электростимуляция предсердий и желудочков может почти всегда купировать приступ пароксизмальной суправентрикулярной тахикардии у больных с синдромом Вольфа — Паркинсона — Уайта, она способна индуцировать фибрилляцию предсердий. Хирургическая абляция эффективна более чем у 90 % больных, обеспечивая стойкое выздоровление.
Ускоренная атриовентрикулярная проводимость при отсутствии признаков преждевременного возбуждения. Электрокардиографическая картина, характеризующаяся коротким интервалом Р—R, не более 0,12 с, и неизмененным комплексом QRS, является следствием прохождения возбуждения по обходному пути, частично или полностью минуя предсердно-желудочковый узел. У таких больных возникающая ПСВТ развивается по механизму циркуляции возбуждения на уровне предсердно-желудочкового узла или при наличии скрытого обходного пути (синдром Лауна — Ганонга — Левина). Лечение аналогично лечению больных с подобными нарушениями ритма без изменений интервала Р—R. При отсутствии эффекта от эмпирически выбранной лекарственной терапии может быть использована программная электростимуляция миокарда. Последовательное введение различных антиаритмических препаратов на этом фоне позволяет подобрать специфическое индивидуальное лечение.
Непароксизмальная узловая тахикардия. Этот вариант нарушения ритма сердца встречается при состояниях, сопровождающихся повышением автоматизма или триггерной активности предсердно-желудочкового соединения. Чаще всего это наблюдается в случае интоксикации препаратами наперстянки, инфаркта нижней стенки миокарда левого желудочка, миокардита, повышения уровней катехоламинов эндогенного происхождения, острого приступа ревматизма или после хирургической коррекции порока клапана сердца.
Для непароксизмальной узловой тахикардии характерно постепенное развитие. Стабилизации ритма предшествует период «разогрева», во время которого частота сердечных сокращений варьирует от 70 до 150 в 1 мин, а при интоксикации препаратами наперстянки — еще больше. Непароксизмальная узловая тахикардия распознается по неизмененному комплексу QRS, идентичному таковому при синусовом ритме. Частота сердечных сокращений зависит от вегетативного тонуса и может повышаться под влиянием катехоламинов, ваголитических препаратов или физической нагрузки или замедляться при надавливании на сонный (каротидный) синус. Если непароксизмальная узловая тахикардия развивается в результате интоксикации препаратами наперстянки, то в этом случае она сопровождается атриовентрикулярной блокадой и/или диссоциацией. В раннем послеоперационном периоде ретроградное проведение возбуждения, как правило, бывает следствием высокого симпатического тонуса.
Лечение. Лечение должно быть направлено на устранение основного этиологического фактора. Поскольку прием сердечных гликозидов является наиболее частой причиной данного нарушения ритма, его необходимо прекратить. Если непароксизмальная узловая тахикардия сопровождается другими серьезными проявлениями интоксикации препаратами наперстянки, такими как повышенная возбудимость миокарда предсердий и желудочков, следует провести активное лечение лидокаином или b-адреноблокаторами. В ряде случаев целесообразно рассмотреть вопрос об использовании дигиталисных антител (Fab-фрагментов). Не следует предпринимать попыток купировать данное нарушение ритма с помощью электроимпульсной терапии, особенно в случае интоксикации препаратами наперстянки. При сохраненной антриовентрикулярной проводимости проведение электрической стимуляции предсердий позволяет подавить узловой очаг возбуждения и обеспечить синхронность сокращений предсердий и желудочков, необходимую для поддержания максимального сердечного выброса. Непароксизмальная узловая тахикардия не является хронически рецидивирующим состоянием. Вот почему исключение факторов, способных спровоцировать ее, нередко помогает решить проблему.
Желудочковая тахикардия. Под стойкой желудочковой тахикардией понимают ускорение ритма сокращений желудочков, сохраняющееся в течение более 30 с или требующее прекращения вследствие гемодинамического коллапса. Желудочковая тахикардия обычно сопровождает некоторые формы структурных поражений сердца, чаще всего хроническую ишемическую болезнь сердца, приведшую к инфаркту миокарда. Стойкая желудочковая тахикардия может также встречаться при неишемических кардиомиопатиях, метаболических расстройствах, медикаментозной интоксикации, у больных с синдромом длинного интервала Q—Т. В ряде случае она может возникнуть у лиц без явных заболеваний сердца и предрасполагающих факторов. У пациентов с заболеванием сердца встречается также нестойкая желудочковая тахикардия, включающая три последовательных сокращения длительностью около 30 с. Если нестойкая желудочковая тахикардия обычно не проявляется клинически, то стойкая практически всегда вызывает субъективные ощущения и часто приводит к дестабилизации гемодинамики и/или ишемии миокарда. В большинстве случаев причиной повторяющихся эпизодов стойкой желудочковой тахикардии выступает не острая ишемия, а фиксированный анатомический очаг. Имеются данные о том, что острая ишемия играет незначительную роль в генезе мономорф ной стойкой желудочковой тахикардии, наблюдаемой у больных с хроническим инфарктом миокарда. В то же время она может способствовать трансформации стабильной желудочковой тахикардии в фибрилляцию желудочков, которая часто начинается именно с желудочковой тахикардии.
Электрокардиографическая диагностика желудочковой тахикардии основывается на регистрации сердечного ритма с частотой более 100 сокращений в 1 мин, характеризующегося широкими комплексами. Обычно ритм при желудочковой тахикардии регулярен, но иногда можно отметить ее незначительные нарушения. Предсердная активность может не совпадать с желудочковой (рис. 184-5); может отмечаться ретроградная деполяризация предсердий. Тахикардия начинается обычно внезапно, но в случае непароксизмальных тахикардии развитие может быть постепенным. Конфигурация комплексов QRS во время приступа желудочковой тахикардии может быть одинаковой — мономорфная желудочковая тахикардия (рис. 184-6) или меняться от сокращения к сокращению — полиморфная желудочковая тахикардия, при которой изменяются амплитуда и направление комплексов QRS, получила название двунаправленная тахикардия. Пароксизмальная желудочковая тахикардия обычно провоцируется преждевременными желудочковыми комплексами.
Очень важно различать суправентрикулярную тахикардию, сопровождающуюся нарушением внутрижелудочковой проводимости, и желудочковую тахикардию, так как клинические осложнения и лечение при этих двух видах нарушений ритма совершенно различны. Правильной диагностике способствует сравнение ЭКГ, зарегистрированных в 12 отведениях на фоне синусового ритма и во время тахикардии. Если на ЭКГ, зарегистрированной во время синусового ритма, имеются признаки блокады ножки пучка Гиса и морфологически комплексы QRS схожи с комплексами при тахикардии, то это говорит о выраженности суправентрикулярной тахикардии. Если же на фоне синусового ритма имеются изменения, характерные для инфаркта миокарда, то можно предположить наличие анатомического субстрата, необходимого для развития желудочковой тахикардии. Подтвердить желудочковое происхождение аритмии можно с помощью следующих данных, полученных при регистрации ЭКГ в 12 отведениях во время тахикардии: 1) расширение комплекса QRS более 0,14 с в условиях отсутствия антиаритмической терапии; 2) атриовентрикулярная диссоциация или вариабельная ретроградная проводимость; 3) вверх направленная ось комплекса QRS; 4) соответствие морфологии комплексов QRS во всех грудных отведениях: все зубцы положительные или отрицательные; 5) другие изменения комплекса QRS, сопровождающиеся его расширением, но без типичных признаков блокады правой или левой ножки пучка Гиса. Тахикардия с широкими причудливыми комплексами и нерегулярным ритмом позволяет заподозрить у пациента фибрилляцию предсердий с проведением возбуждения по обходному атриовентрикулярному пути. С другой стороны, комплексы, ширина которых превышает 0,2 с, нетипичны для желудочковой тахикардии при отсутствии медикаментозной терапии и более характерны для преждевременного возбуждения желудочков.
#image.jpg
Рис.184-5. Желудочковая тахикардия с атриовентрикулярной диссоциацией.
Стрелкой показаны зубцы Р, которые полностью не зависят от основного желудочкового ритма. Атриовентрикулярная диссоциация является характерным признаком желудочковой тахикардии.
#image.jpg
Рис.184-6. ЭКГ при желудочковой тахикардии. а — форма зубцов ЭКГ при желудочковой тахикардии в сочетании с блокадой правой ножки пучка Гиса. Наряду с ЭКГ-картиной желудочковой тахикардии имеет место расширение комплекса QRS (не менее 0,14 с), верхняя ось, монофазные зубцы R в отведении V1 и отношение зубцов Р и S в отведении V6 менее 1; б—форма зубцов ЭКГ при желудочковой тахикардии в сочетании с блокадой левой ножки пучка Гиса. Характерным ЭКГ-признаком является наличие желудочковой тахикардии с широкими медленно поднимающимися зубцами R в отведениях I и V6.
Диагноз желудочковой тахикардии может быть поставлен на основании анализа взаимоотношений электрограммы предсердно-желудочкового пучка (Гиса) и желудочковой активности. В трех из четырех случаев желудочковой тахикардии на электрограмме отсутствуют регулярные зубцы, соответствующие предсердно-желудочковому пучку (Гиса) (рис. 184-7). Иногда электрическая активность предсердно-желудочкового пучка (Гиса) обнаруживается либо до, либо после комплексов QRS, что обусловлено ретроградной активацией системы Гиса — Пуркинье. У больных с тахикардией, характеризующейся широкими комплексами со сложными деформациями их, диагноз желудочковой тахикардии подтверждается в том случае, если стимуляция предсердий приводит к нормализации формы комплексов QRS и величины интервала «пучок Гиса — миокард желудочков». Независимо от формы комплексов QRS, т. е. наличия признаков блокады правой или левой ножки пучка Гиса (см. рис. 184-6), желудочковая тахикардия, вызванная ишемической болезнью сердца, исходит из эндокарда левого желудочка.
#image.jpg
Рис.184-7. Внутрисердечные электрограммы при суправентрикулярной и желудочковой тахикардии.
Электрограммы пучка Гиса (ЭГПГ) представлены вместе с ЭКГ в I, aVF и V1 отведениях и калибровкой времени. Как в левой, так и в правой части рисунка приведены примеры тахикардии, сочетающейся с блокадой правой ножки пучка Гиса и характеризующейся широкими комплексами QRS. Слева — суправентрикулярная тахикардия, отличающаяся отклонением изолинии на ЭГПГ (Г), которое предшествует каждому комплексу QRS. При этом интервал ГЖ остается в пределах нормы. Во время желудочковой тахикардии отклонение изолинии ЭГПГ отсутствует (стрелка), но имеется атриовентрикулярная диссоциация [обратите внимание на одиночную предсердную волну (П)]. (Из: J. A. Kastor et al.)
Более чем у 95 % больных со стойкой желудочковой тахикардией данная аритмия может быть спровоцирована во время программной стимуляции миокарда.
У большинства пациентов тахикардия индуцируется преждевременным желудочковым импульсом. При этом морфологически стойкая мономорфная желудочковая тахикардия, как правило, идентична спонтанной аритмии. Клиническое значение полиморфной желудочковой тахикардии, индуцируемой стимуляцией миокарда, неясно. Было показано, что полиморфная желудочковая тахикардия и даже фибрилляция желудочков могут быть спровоцированы более агрессивной электростимуляцией миокарда, т. е. при использовании трех или четырех дополнительных стимулов, у некоторых здоровых людей и у пациентов, у которых никогда ранее клинически нарушения ритма сердца не проявлялись.
По меньшей мере у 75 % больных стойкая мономорфная желудочковая тахикардия может быть купирована программной или быстрой электростимуляцией миокарда. В остальных случаях требуется проведение электроимпульсной терапии. Возможность несколько раз подряд индуцировать и купировать стойкую мономорфную желудочковую тахикардию помогает подобрать лекарственный препарат или режим электростимуляции, позволяющие избавиться от этой аритмии. На протяжении нескольких дней можно проводить серийные исследования различных антиаритмических средств, в результате чего появляется возможность предсказать вероятность успешного применения тех или иных препаратов или устройств.
Воспроизводимое купирование желудочковой тахикардии с помощью программной стимуляции миокарда позволяет оценить эффективность длительного лечения пароксизмов нарушения ритма с помощью различных антитахикардиальных электрокардиостимуляторов. К сожалению, быстрая электростимуляция, представляющая собой наиболее эффективную форму антиаритмической терапии, может привести к усугублению тахикардии и/или спровоцировать фибрилляцию желудочков.
Клинические проявления. Симптомы желудочковой тахикардии зависят от частоты сокращений желудочков, длительности тахикардии, наличия и выраженности основного заболевания сердца. Быстрая тахикардия, сочетающаяся с тяжелым нарушением функции миокарда и поражением сосудов мозга, часто сопровождается гипотензией и обмороками. Неполноценное предсердное наполнение желудочков и нарушение последовательности их активации являются важными факторами, приводящими к снижению сердечного выброса во время желудочковой тахикардии.
Прогноз желудочковой тахикардии зависит от тяжести основного заболевания. Если стойкая тахикардия развивается в течение первых 6 нед после острого инфаркта миокарда, то в этом случае прогноз неблагоприятен, так как смертность в течение первого года после инфаркта достигает 85 %. Возникновение нестойкой желудочковой тахикардии после инфаркта миокарда сопровождается трехкратным увеличением риска смерти по сравнению с группой пациентов без нее. Однако причинно-следственные взаимоотношения между нестойкой тахикардией и последующей внезапной смертью не были установлены.
Лечение. До начала лечения больного, страдающего тем или иным видом аритмии, в каждом конкретном случае необходимо оценить возможный риск и вероятность достижения успеха. Это очень важно, поскольку антиаритмические препараты сами могут провоцировать появление новых или усугублять уже имеющиеся нарушения ритма вместо того, чтобы скорригировать их. В целом течение желудочковой тахикардии у пациентов без органических заболеваний сердца благоприятное. Больным, у которых нестойкая желудочковая тахикардия не сопровождается появлением клинических симптомов, лечения не требуется, подобное нарушение ритма не несет опасности для их жизни. Стойкая желудочковая тахикардия у пациентов, не имеющих органических заболеваний сердца, обычно требует коррекции, так как при этом возникают клинические симптомы, характерные для данного нарушения ритма. Подобные варианты тахикардии эффективно купируются с помощью b-адреноблокаторов, варапамила или хинидин-подобных препаратов. Если желудочковая тахикардия у пациентов с органическим заболеванием сердца сопровождается нестабильностью гемодинамики, ишемией миокарда, застойной сердечной недостаточностью или гипоперфузией центральной нервной системы, то необходимо как можно скорее восстановить синусовый ритм с помощью электроимпульсной терапии (см. ниже). В том случае, если указанные изменения на фоне желудочковой тахикардии у пациента с органическим заболеванием сердца отсутствуют, то лечение можно начать с применения лекарственных препаратов. Новокаинамид является, видимо, самым эффективным средством. Его введение если не прекратит тахикардию, то в любом случае приведет к замедлению ее ритма. Если у больных со стабильной гемодинамикой введение указанных препаратов не приводит к нормализации ритма, то трансвенозным доступом в верхушку правого желудочка можно ввести катетер для электростимуляции, после чего тахикардия может быть быстро купирована.
Терапия, основывающаяся на результатах программной электростимуляции миокарда, является, видимо, наиболее эффективным методом лечения, так как позволяет подобрать наиболее подходящий антиаритмический препарат, исключающий рецидив стойкой желудочковой тахикардии. В условиях постоянного мониторного контроля можно исследовать свойства разнообразных антиаритмических средств и отбирать из них те, которые наиболее эффективно блокируют развитие желудочковой тахикардии и от применения которых можно ожидать длительного антиаритмического действия (см. раздел «Фармакологическая антиаритмическая терапия»).
Как средство купирования тахикардии, устойчивой к воздействию фармакологических препаратов, может быть использована электростимуляция. Необходимыми условиями осуществления данной манипуляции являются стабильность тахикардии, ее медленный ритм. Кроме того, важно, чтобы пациент знал о готовящемся вмешательстве. В момент написания этой книги, однако, не было данных о разрешении клинического применения автоматических приборов для коррекции желудочковой тахикардии. Имеются отдельные сообщения об использовании радиочастотных электрокардиостимуляторов, управляемых врачами.
Создание эндокардиальных катетеров и развитие методики интраоперационного картирования позволили разработать хирургические методы лечения при желудочковой тахикардии. Наиболее успешно хирургические вмешательства по этому поводу проводятся в тех учреждениях, где имеются квалифицированные специалисты, способные выполнять и анализировать полученные данные картирования. В подобных центрах эффективность лечения таких больных довольно высока, несмотря на то что у большинства пациентов желудочковая тахикардия сопровождается ишемической болезнью сердца, выраженным нарушением функции левого желудочка и поражением нескольких коронарных артерий. При этом операционная смертность варьирует от 8 до 15 %. После операции у 85— 90 % больных удается поддерживать нормальный ритм сердечных сокращений. Правда, у 60 % из них это достигается с использованием антиаритмических препаратов.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет