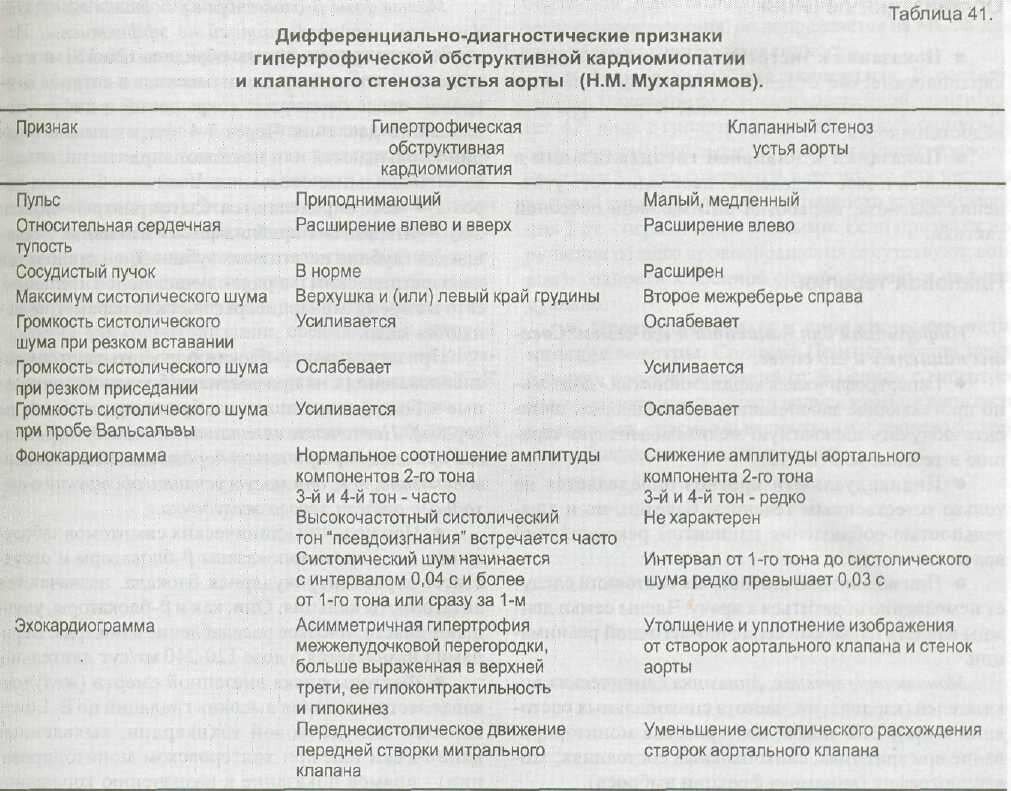
Обструктивной гипертрофической кардиомиопатии
ЛЕЧЕНИЕ КАРДИОМИОПАТИЙ
Основные принципы лечения кардиомиопатий представлены в таблице 12.
При дилатационной кардиомиопатии лечение направлено на уменьшение явлений застойной сердечной недостаточности, устранение нарушений сердечного ритма и предупреждение тромбоэмболических нарушений.
С учетом систолического характера застойной сердечной недостаточности, основным средствами ее лечения являются диуретики, кардиотонические препараты и периферические вазодилататоры.
Диуретики высокоэффективны в отношении уменьшения симптомов перегрузки объемом, связанной с задержкой Na и воды, включая ортопноэ. Однако, уменьшение внутрисосудистого объема жидкости обычно сопровождается рефлекторной стимуляцией ренин-ангиотензиновой и смипато-адреналовой систем. В свзяи с этим, диуретики обычно применяются в комбинации с сердечным гликозидами и/или ингибиторами АПФ.
1. Терапевтическое лечение:
— Бета-адреноблокаторы /в больших дозах, в основном при
гипертрофической кардиомиопатии/;
— Симптоматическое лечение сердечной недостаточности:
*ингибиторы АПФ
*периферические вазодилататоры
*сердечные гликозиды /только при ДКМП, при
сердечные гликозиды противопоказаны /
*негликозидные кардиотоники
2. Хирургическое лечение:
— Пересадка сердца /в США к настоящему времени
осуществлено более 20000 трансплантаций сердца с 70-90%
выживаемостью/;
— Миотомия гипертрофированной перегородки.
Традиционно назначаемые больным дилатационной кардиомиопатией сердечные гликозиды безусловно эффективны лишь в случаях сопутствующей мерцательной артмии. Их клиническая эффективность при застойной сердечной недостаточности и синусовом ритме долгое время являлось предметом дискуссии. В последние годы считается, что в таких случаях они могут применяться только в сочетании с ингибиторами АПФ и диуретиками, причем предпочтение отдается дигоксину в маленьких дозах /0,125-0,375 мг в сутки/. Более детально о лечении застойной сердечной недостаточности мы будем говорить в соответствующей лекции.
В последние годы активно изучается клиническая эффективность селективных бета-блокаторов в лечении ДКМП /метопролола, карведилола, бисопролола/, однако эти препараты можно применять только после стабилизации состояния больных с помощью стандартной терапии ингибиторами АПФ, диуретиками и дигоксином.
При нарушениях ритма, которые часто встречаются при ДКМП /пароксизмальная тахикардия — в 40-60%, мерцательная аритмия — в 25-30% случаев/, предпочтение отдают амиодарону /кордарону/, который, обладая высокой противоаритмической активностью, существенно не ухудшает сократимость миокарда и обладает свойствами периферического вазодилататора.
В связи с частыми тромбоэмболическими осложнениями /у 10-44% больных ДКМП, причем в 7-11% случаев они служат причиной летального исхода/ во всех случаях мерцательной аритмии, а также при наличии в анамнезе хотя бы одного тромбоэмболического эпизода /независимо от ритма сердца/, больным показано лечение непрямыми антикоагулянтами.
В странах с высокоразвитой кардиохирургией дилатационная кардиомиопатия является показанием к трансплантации сердца. Показаниями к трансплантации являются тяжелая рефрактерная сердечная недостаточность и плохой ближайший прогноз, отсутствие неконтролируемой инфекции, пептической язвы желудка, тяжелой почечной и печеночной недостаточности, а также других сопутствующих заболеваний. В настоящее время максимальная выживаемость после пересадки сердца составляет 20 и более лет. К настоящему времени в мире выполнено уже более 20000 операций трансплантации сердца. При современной иммуносупрессивной терапии выживаемость больных в течение года достигает 90%, в течение 5 лет — 70-80%, а более 65% больных спустя год после операции возвращаются к труду.
При гипертрофической кардиомиопатии препаратами выбора являются бета-адреноблокаторы /пропранолол 120-240 мг/сутки/, которые уменьшают внутрижелудочковый градиент давления и способствуют увеличению наполнения левого желудочка, а также оказывают антиаритмическое действие. К сожалению, возможность их применения ограничена степенью выраженности сердечной недостаточности и низким АД. Применяется также антагонист кальция верапамил /изоптин 120-240 мг/сутки/ и антиадренергический препарат кордарон /200-600 мг/сутки/. Сердечные гликозиды при субаортальном стенозе противопоказаны, так как могут увеличивать систолическую обструкцию кровотока. При высоком внутрижелудочковом градиенте давления /более 50 мм рт.ст./ применяется хирургическая резекция межжелудочковой перегородки с одновременным протезированием митрального клапана.
На ранних стадиях рестриктивной кардиомиопатии при выраженной эозинофилии используют глюкокортикоиды и иммунодепрессанты. Салуретики и периферические вазодилататоры назначают по показаниям, а для предупреждения тромоэмболий используют антикоагулянты и антиагреганты.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Гипертрофическая кардиомиопатия
Это заболевание характеризуется гипертрофией левого желудочка, в типичных случаях без дилатации, при этом отсутствует явная причина болезни. Таким образом, гипертрофия левого желудочка не является вторичной по отношению к таким заболеваниям, как артериальная гипертензия и субаортальный стеноз, нарушения гемодинамики при которых в первую очередь сказываются на левом желудочке.
Два характерных признака заболевания, ни в коем случае не являющихся, однако, обязательными, привлекают повышенное внимание: 1) асимметрическая гипертрофия перегородки (АГП), при которой преимущественно гипертрофирована верхняя часть межжелудочковой перегородки по сравнению с толщиной заднебазальной свободной стенки левого желудочка; 2) затрудненный отток крови из левого желудочка (динамическая обструкция) вследствие сужения субаортальной области из-за среднесистолического противопоставления передней створки левого предсердно-желудочкового (митрального) клапана и гипертрофированной перегородки, т. е. систолическое движение клапана вперед (СДВ). В первоначальных исследованиях динамической обструкции отводилась ведущая роль, вследствие чего заболевание называли идиопатическим гипертрофическим субаортальным стенозом (ИГСС), гипертрофической обструктивной кардиомиопатией (ГОКМП) и мышечным субаортальным стенозом. Сейчас стало понятно, однако, что у большинства больных с гипертрофической кардиомиопатией подобная обструкция фактически отсутствует. Множественные патофизиологические изменения являются результатом не столько систолической, сколько диастолической дисфункции, характеризующейся увеличенной ригидностью гипертрофированной мышцы сердца. Это состояние приводит к увеличению давления наполнения и сохраняется, несмотря на повышенную сократимость левого желудочка.
При гипертрофической кардиомиопатии гипертрофия носит своеобразный характер, она отличается от вторичной гипертрофии, наблюдаемой при артериальной гипертензии. У большинства больных гипертрофирована межжелудочковая перегородка, толщина которой диспропорционально увеличена по сравнению с толщиной свободной стенки. У других больных выявляют диспропорциональное увеличение верхушки или свободной стенки левого желудочка: у 10 % или более больных наблюдают концентрическое вовлечение желудочка, тем не менее во всех случаях имеет место аномальное, беспорядочное расположение клеток мышцы сердца в области перегородки независимо от того, имеется обструкция или нет. У больных без обструкции может выявляться аналогичное поражение стенки левого желудочка.
По крайней мере у 50 % больных с гипертрофической кардиомиопатией болезнь наследуется по аутосомно-доминантному типу с высокой степенью пенетрантности; в остальных случаях болезнь возникает спорадически. Эхокардиографические исследования подтвердили, что примерно у половины родственников первого порядка [т. е. родителей, сибсов (родных братьев и сестер), детей] с наследственной гипертрофической кардиомиопатией наблюдаются признаки гипертрофии перегородки, хотя признаки обструкции и клинические признаки. заболевания у многих отсутствуют.
В отличие от обструкции, вызываемой фиксированным уменьшением клапанного кольца, как это наблюдается при клапанном аортальном стенозе, обструкция при гипертрофической кардиомиопатии (если она имеется) носит динамический характер, степень ее выраженности изменяется при многократных обследованиях больного; изменяется она даже от одного сокращения к другому. Обструкция является результатом дальнейшего сужения исходно уменьшенного размера выносящего тракта за счет движения вперед левого предсердно-желудочкового (митрального) клапана против гипертрофированной перегородки в систолу (СДВ). СДВ можно обнаружить не только при гипертрофической кардиомиопатии, но и при ряде других состояний, однако при гипертрофической кардиомиопатии она имеется как правило.
Динамическая обструкция может быть результатом трех основных механизмов: 1) увеличенной сократимости левого желудочка, что приводит к уменьшению его систолического объема и увеличению скорости изгнания крови через выносящий тракт, в результате чего наблюдается движение передней створки левого предсердно-желудочкового (митрального) клапана в сторону, противоположную перегородке, как следствие сниженного давления растяжения; 2) сниженного объема желудочка (преднагрузка), что приводит к дальнейшему уменьшению размеров выносящего тракта; 3) сниженного сопротивления кровотока в аорте (постнагрузка), что увеличивает скорость кровотока через субаортальную область и также уменьшает систолический объем желудочка. Все вмешательства, увеличивающие сократимость миокарда, так же как физическая нагрузка, введение изопротеренола, дигиталисных гликозидов, а также вмешательства, уменьшающие объем желудочка, такие как проба Вальсальвы, внезапное принятие больным положения стоя, прием нитроглицерина, амилнитрита, тахикардия могут увеличить обструкцию. Напротив, повышение артериального давления при приеме фенилэфрина (мезатон), приседаниях, длительном напряжении рук, увеличение венозного возврата при подъеме нижних конечностей, увеличение объема циркулирующей крови способствуют увеличению объема желудочка и уменьшают обструкцию. Иногда гипертрофированная перегородка выбухает в. выносящий тракт правого желудочка, препятствуя тем самым изгнанию крови и из этой камеры сердца.
Гипертрофическая кардиомиопатия встречается в сочетании с лентигинозом и другими нарушениями нервных окончаний. Аналогичные грубые анатомические и гемодинамические нарушения могут обнаруживаться у детей, родившихся от матерей, страдающих диабетом, а также от больных с атаксией Фридрейха.
Клинические проявления гипертрофической кардиомиопатии. У многих больных гипертрофическая кардиомиопатия протекает бессимптомно; некоторые из них имеют родственников с установленным диагнозом. К сожалению, первым клиническим проявлением заболевания может быть внезапная смерть, которой часто подвержены больные дети и подростки, нередко во время или после физической нагрузки. Клинические проявления болезни чаще всего характеризуются одышкой, возникающей в основном вследствие уменьшения эластичности стенок левого желудочка, что приводит к нарушению наполнения левого желудочка и увеличению диастолического давления в нем, а также к увеличению давления в левом предсердии. Другие симптомы включают стенокардию, усталость, синкопе или «около синкопе» (жалоба на появление серой пелены перед глазами). Клиническая симптоматика не связана с наличием и выраженностью обструкции кровотока. У большинства больных с обструкцией обнаруживается двойной или тройной верхушечный толчок, быстро возрастающий пульс на сонных артериях и добавочный IV сердечный тон. Отличительная особенность обструктивной гипертрофической кардиомиопатии — наличие систолического шума ромбовидной формы, характер которого в типичных случаях грубый; он чаще всего выслушивается через значительный промежуток после I сердечного тона (поскольку в фазу ранней систолы выброс происходит беспрепятственно) в нижней части грудины, слева от нее, а также в области верхушки. В области верхушки шум в большей степени голосистолический, и дующий, отражающий митральную регургитацию, которая обычно сопровождает обструктивную гипертрофическую кардиомиопатию.
Лабораторные исследования гипертрофической кардиомиопатии. На ЭКГ обычно выявляют признаки гипертрофии левого желудочка и уширение зубца Q во многих отведениях, что заставляет предполагать наличие ранее перенесенного инфаркта миокарда, однако фактически является результатом измененных электрокардиографических признаков гипертрофии перегородки. У многих больных при холтеровском электрокардиографическом мониторировании регистрируют нарушения ритма, как предсердные (суправентрикулярная тахикардия и фибрилляция предсердий), так и желудочковые (желудочковая тахикардия). Рентгенография грудной клетки может не выявить отклонений, хотя нередко отмечают незначительное или умеренное увеличение контура (силуэта) сердца. Не наблюдается увеличения корня аорты и кальцификации клапанов, что облегчает дифференцирование этого состояния от клапанного аортального стеноза. Основным методом диагностики гипертрофической кардиомиопатии служит эхокардиография, выявляющая гипертрофию левого желудочка. В типичных случаях толщина перегородки в 1,3 раза и более превышает толщину верхней задней части свободной стенки левого желудочка. Перегородка может иметь необычный вид орнаментированного стекла, что, видимо, связано с нарушением ее клеточной архитектуры и миокардиальным фиброзом. У больных с обструкцией обнаруживают систолическое движение вперед митрального клапана. Для гипертрофической кардиомиопатии характерно уменьшение полости левого желудочка, при этом увеличивается подвижность задней стенки и уменьшается подвижность перегородки. В редких случаях при гипертрофической кардиомиопатии наблюдается массивная гипертрофия верхушки, при этом на ЭКГ видны гигантские отрицательные зубцы Т, а при ангиографии — «лопатообразной» формы левый желудочек.
Двухмерная эхокардиография особенно ценна для выявления всех характерных изменений, включая размеры и форму полости левого желудочка. Кривая непрямой регистрации пульса сонных артерий имеет необычно резкий подъем и часто обнаруживает конфигурацию остроконечного корпуса («spike-and-dome») при наличии градиента давления при оттоке из левого желудочка. Радионуклид пая сцинтиграфия с таллием-201 и сканограммы объема крови позволяют визуализировать размер и ориентацию межжелудочковой перегородки.
Двумя типичными гемодинамическими признаками гипертрофической кардиомиопатии являются повышение диастолического давления в левом желудочке вследствие нарушения его сократимости и при наличии обструкции градиент систолического давления между основной и септальной частью левого желудочка. При отсутствии градиента его часто можно вызвать с помощью провокаций, например инфузий изопротеренола, ингаляций амилнитрита, пробой Вальсальвы.
Лечение гипертрофической кардиомиопатии.
Часто используются адреноблокаторы. Они могут в некоторой степени уменьшать выраженность стенокардии и синкопе. Внутрижелудочковый градиент давления в покое (под действием адреноблокаторов) обычно не изменяется, однако эти препараты могут ограничить прирост градиента, возникающий во время нагрузки. Тем не менее не существует доказательств, что адреноблокаторы предохраняют больного от внезапной смерти, которая наступает в основном вследствие аритмий. Не установлено также, имеют ли какие-либо другие антиаритмические препараты эффект в отношении внезапной смерти. Существуют, однако, экспериментальные данные о том, что амиодарон уменьшает частоту опасных для жизни суправентрикулярных желудочковых аритмий. Препараты, блокирующие кальциевые каналы, в частности верапамил и нифедипин, являются перспективными препаратами, способными повысить эластичность левого желудочка, уменьшить диастолическое давление в нем, увеличить толерантность к физической нагрузке и в некоторых случаях уменьшить выраженность обструкции выброса из левого желудочка. У некоторых больных для уменьшения сократимости левого желудочка и градиента оттока используют дизопирамид. Хирургическая миотомия/миоэктомия гипертрофированной перегородки может привести к длительному симптоматическому улучшению, однако высокая летальность, достигающая 10 %, заставляет использовать эту операцию лишь у больных с выраженным заболеванием и высокой степенью обструкции, резистентных к медикаментозной терапии,
Лучше всего при возможности избегать назначения дигиталиса, диуретиков, нитратов, адренергических агонистов, особенно в случаях, когда известно о наличии градиента давления при оттоке из левого желудочка.
Прогноз гипертрофической кардиомиопатии.
Естественное течение гипертрофической кардиомиопатии весьма вариабельно, у многих больных состояние здоровья со временем улучшается или стабилизируется. В поздних стадиях заболевания часто развивается мерцание предсердий, с его появлением самочувствие больного значительно ухудшается в основном вследствие того, что теряется вклад предсердий в заполнение утолщенного желудочка. Такой ритм, если он существует длительно, свидетельствует о неблагоприятном прогнозе. Менее чем у 10 % больных развивается инфекционный миокардит. Поэтому целесообразна профилактика эндокардита, особенно у больных с обструкцией в состоянии покоя и больных с митральной регургитацией. Иногда гипертрофическая кардиомиопатия может приводить к дилатации левого желудочка и его дисфункции с исчезновением градиента давления. Чаще всего больные с гипертрофической кардиомиопатией даже в случае бессимптомного течения заболевания или при стабильном клинически выраженном течении умирают внезапно. Парадоксально, что особенно высокий риск внезапной смерти отмечают у лиц молодого возраста с невыраженной обструкцией или без обструкции. Поскольку внезапная смерть часто наступает во время или сразу после физической нагрузки, всем больным с гипертрофической кардиомиопатией независимо от наличия или отсутствия симптомов заболевания следует избегать значительных физических нагрузок. Хотя гемодинамический фактор и играет определенную роль, большинство смертей, особенно внезапных, происходит, по-видимому, вследствие желудочковых аритмий. Адреноблокаторы оказались неэффективными в предупреждении внезапной смерти. Профилактический эффект блокаторов кальциевых каналов или антиаритмических препаратов не доказан.
Из доступных препаратов лишь амиодарон представляется перспективным в отношении профилактики внезапной смерти.
Гипертрофическая кардиомиопатия
Наиболее частый морфологический признак гипертрофической кардиомиопатии: асимметричное утолщение мускулатуры левого желудочка сердца. Сердце получается «однобоким». Соответственно «сдвинуты вбок» и его функции. Собственно, нарушаются и другие функции организма, например, дыхательная. Одышка – один из классических симптомов этой болезни. Гемодинамические нарушения (проблемы с кровообращением) вызывают и другие неприятные симптомы, в частности создают риск возникновения инсульта.
В прежние времена решающим патологическим признаком гипертрофической кардиомиопатии считали именно гемодинамические нарушения. Поэтому и называли болезнь по-другому: идиопатический гипертрофический субаортальный стеноз, или IHSS. Но поскольку основной причиной нарушенного кровообращения является заболевание сердечной мышцы, то изменилось и название.
В международной клинической практике применяется современная аббревиатура НСС, в российской – ГКМП. Но обе эти «шифровки» означают одно и то же: гипертрофическую кардиомиопатию. Она относится к классу врожденных первичных кардиомиопатий (заболеваний сердечной мышцы). Вместе с миокардитом и дилатационной кардиомиопатией это наиболее часто встречающееся расстройство миокарда – если, конечно, не включать сюда статистику по инфарктам. Однако инфаркт миокарда – это следствие нарушения кровообращения в коронарной зоне, вызывающего гипоксию сердечной мышцы. А кардиомиопатии – это самостоятельные заболевания, развивающиеся вне зависимости от состояния коронарных сосудов, поэтому и статистика здесь своя.
Бессимптомное развитие гипертрофической кардиомиопатии
В классическом представлении, гипертрофическая кардиомиопатия – болезнь неизлечимая, но и не очень опасная. Мол, в большинстве случаев гипертрофия сердечной мышцы не вызывает слишком острых симптомов, не отражается на качестве жизни и не сокращает век. Поэтому «ничего с ней не поделаешь, да и не надо».
Современная медицина существенно изменила представления об этом «тихом омуте». Прогнозы при прогрессирующем развитии сердечномышечной гипертрофии не всегда благополучны. Обструктивная форма гипертрофической кардиомиопатии резко повышает риск летального исхода. Другое дело, что непосредственной причиной смерти выступают другие факторы: аритмия, острая сердечная недостаточность, инсульт. Но в основе – дисфункции сердечной мышцы, ее нарушенное строение. Вот и утверждай после этого, что «от гипертрофической кардиомиопатии не умирают».
С другой стороны, современная медицина развивает средства лечения этой болезни. Как утверждают кардиологи Германии. при раннем выявлении признаков гипертрофической кардиомиопатии она вполне поддается лечению. Удается не только сдержать процесс гипертрофических изменений миокарда, но и выполнить коррекцию (хирургическим путем), вернуть ему нормальный размер и форму.
Словом, гипертрофическая кардиомиопатия – это болезнь, которую нельзя упускать, нельзя запускать и вполне можно вылечить. Многие кардиологические и кардиохирургические клиники Германии (например, Немецкий кардиоцентр в Мюнхене или Третья медицинская клиника в Клиническом комплексе Пассау) применяют отличные методики интервенционного и консервативного лечения гипертрофической кардиомиопатии.
Гипертрофическая кардиомиопатия как наследственное заболевание
Болезнь, как уже отмечено, является врожденной, встречается в среднем у одного человека из пятисот и очень часто – у прямых родственников. Таким образом гипертрофическая кардиомиопатия – наследственное заболевание. Оно передается аутосомно-доминантным путем, то есть от одного из родителей и проявляется у половины потомства (вторая половина остается здоровой и не имеет дефектных генов).
В настоящее время выявлено свыше двухсот генетических дефектов, «ответственных» за развитие гипертрофической кардиомиопатии. Они могут проявляться в десяти различных генах, кодирующих протеины в саркомерах миокарда. Единственный дефект в единственном гене почти никогда не приводит к заболеванию. Но чем больше дефектов и чем больше затронуто генов – тем выше риск морфологических и функциональных нарушений сердечной мышцы из-за ошибочного кодирования саркомеров.
Саркомеры – это протеиновые комплексы в составе «сократительных единиц» мышечной ткани. Из саркомеров состоят миофибриллы – структурные элементы мышечных клеток, благодаря которым ткань обладает способностью сокращаться. Мутации в генах, кодирующих саркомеры миокарда, «отзываются» нарушениями его строения, что и ведет к гипертрофии сердечной мышцы. Причиной гипертрофии становится, в частности, неправильное, поперечное разрастание мышечных клеток (в нормальной ткани они группируются вдоль, по направлению мышечных волокон). Избыток поперечно сгруппированных клеток с наросшими излишками соединительной ткани (фиброз) – это и есть участок патологического утолщения сердечной мускулатуры.
Впрочем, даже наличие целого комплекса специфических гендефектов не всегда ведет к «хаосу» в расположении клеток, к возникновению и развитию заболевания. При отсутствии заболевания человека с нарушенными генами считают «тихим носителем мутаций». Такими «тихими носителями» являются, например, дети и подростки до 13 лет с мутировавшими генами. Болезнь «просыпается» в более зрелом возрасте. Но может и не проснуться вовсе.
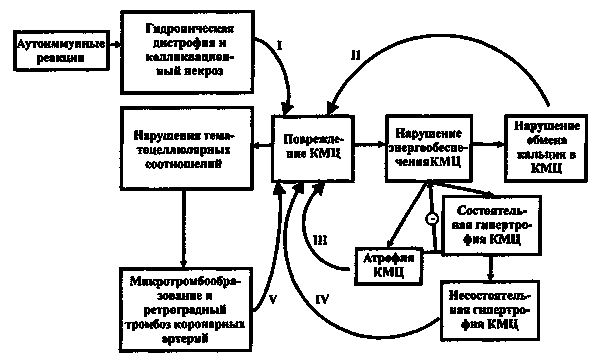
Патогенез
Гипертрофические участки не только нарушают структуру миокарда и внутренних отделов сердца, но также создают помехи сердечной деятельности. Характер помех, в частности, зависит от расположения утолщений.
Примерно в каждом четвертом случае утолщение локализуется в районе примыкания аорты, то есть на выводящем участке левого желудочка. Обычно это левостороннее утолщение межжелудочковой перегородки. Оно мешает левому желудочку нагнетать кровь в аорту. В зависимости от степени гипертрофии помехи возникают при нагрузке либо даже в состоянии покоя.
В случае серьезных помех, в том числе и в состоянии покоя, диагностируются обструктивная форма гипертрофической кардиомиопатии (HOCM) и функциональный стеноз аортального клапана. Напомним, что обструктивная форма заболевания – это особо высокий риск опасных осложнений, вплоть до внезапной остановки сердца или летального инсульта.
Если помехи возникают только при нагрузке, то диагностируется гипертрофическая кардиомиопатия с динамической обструкцией.
Если, несмотря на утолщение сердечной мышцы, кровь нагнетается в аорту без особых помех, диагностируется необструктивная форма гипертрофической кардиомиопатии (HNCM).
Наряду с утолщением сердечной мышцы образуется и ее уплотнение с пораженной стороны. Скажем, если затруднена нагнетательная функция левого желудочка, то мышца с этой стороны «трудится» в особо жестком режиме. Она становится сильней, крепче и, следовательно, плотней. Это происходит как при обструктивной, так и при необструктивной форме гипертрофической кардиомиопатии.
Связь с другими заболеваниями
Чрезмерное уплотнение мышечной ткани ухудшает «втягивающую» функцию желудочка. Это значит, что в диастолической фазе (фазе расслабления) левый желудочек забирает недостаточно крови из легочной вены, чем обусловлены застой в малом круге кровообращения, нарушения дыхательной функции, одышка, недостаток кислорода, поступающего к тканям через большой круг кровообращения. При обструктивной форме уплотнение сердечной мышцы особо выражено. Соответственно в наибольшей степени выражены и вышеперечисленные симптомы. В этом случае констатируют диастолическую сердечную недостаточность.
Чем, увы, не исчерпываются патологические следствия затрудненного нагнетания крови в аорту. На участке сужения сказывается гидродинамический эффект Вентури: скорость потока возрастает, из-за чего образуется «сила подсоса», воздействующая на расположенный рядом митральный клапан. Из-за «принудительного подсоса» митральный клапан становится неплотным. В нормальном состоянии его лепестки пропускают кровь из левого предсердия в левый желудочек в диастолической фазе, а в систолической (фазе сокращения) – перекрывают обратный ток крови. Если же из-за постоянного подсоса митральный клапан становится неплотным, то в систолической фазе его лепестки смыкаются не полностью. Образуется обратный кровоток из левого желудочка в левое предсердие. Так на фоне врожденной гипертрофии сердечной мышцы развивается приобретенный порок сердца.
И еще одно следствие гипертрофической кардиомиопатии – прогрессирующая аритмия, проявляющаяся в основном при нагрузках на сердце, но нередко и в состоянии покоя. Аритмия и диастолическая сердечная недостаточность сопровождаются приступами стенокардии, головокружением, обмороками. В особо острых случаях – риск внезапной остановки сердца.