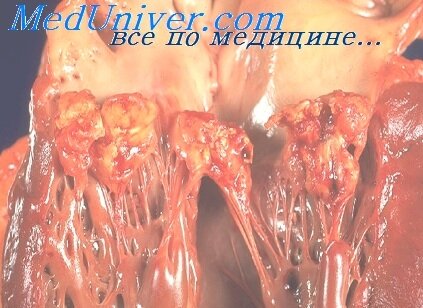
ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ
Классификация
В зависимости от основных возбудителей и связанных с этим особенностей антибактериальной терапии инфекционные эндокардиты подразделяют на следующие основные категории:
• инфекционный эндокардит естественных клапанов;
• инфекционный эндокардит у наркоманов, использующих в/в путь введения наркотических веществ;
• инфекционный эндокардит искусственных (протезированных) клапанов:
• ранний (развивающийся в течение 60 дней после операции) — чаще вследствие контаминации клапанов или в результате периоперационной бактериемии;
• поздний (развивающийся более чем через 2 мес после операции) — может иметь одинаковый патогенез с ранним инфекционным эндокардитом, но более продолжительный инкубационный период; может также развиться в результате транзиторной бактериемии.
В зависимости от характера течения заболевания выделяют острый и подострый инфекционный эндокардит. Однако наиболее существенным является подразделение по бактериальной этиологии, так как это определяет выбор АМП и продолжительность терапии.
Основные возбудители
Инфекционный эндокардит может быть вызван самыми различными микроорганизмами, однако подавляющее большинство составляют стрептококки и стафилококки (80-90%).
Наиболее частые возбудители инфекционных эндокардитов представлены в табл. 1.
Таблица 1. Этиология инфекционного эндокардитав
Выбор антимикробных препаратов
Острый инфекционный эндокардит нуждается в немедленной антибиотикотерапии, в то время как лечение подострого эндокардита может быть отсрочено на 24-48 ч, пока проводится диагностическое обследование. Необходимость безотлагательного лечения острого эндокардита обусловлена тем, что одним из наиболее вероятных возбудителей является S.aureus, который может вызывать токсический шок, септические метастазы и быстрое разрушение сердечных клапанов.
Подострый инфекционный эндокардит обычно вызывается микроорганизмами, отличающимися низкой вирулентностью, и достаточно редко сопровождается септицемией или шоком. Некоторая отсрочка начала лечения дает возможность в течение 1-2 сут получить предварительные данные микробиологического исследования крови и проводить этиотропную терапию. Однако недопустимо откладывать начало применения АМП более чем на 48 ч.
Для излечения инфекционного эндокардита необходимо добиться эрадикации микроорганизмов из вегетаций, что возможно только при соблюдении следующих основных положений:
• использовать АМП, активные в отношении потенциальных и установленных возбудителей;
• применять бактерицидные АМП, так как в вегетациях микроорганизмы находятся в состоянии низкой метаболической активности;
• использовать комбинации АМП, обладающих синергизмом;
• вводить АМП парентерально для получения более высоких и предсказуемых сывороточных концентраций;
• антимикробная терапия должна быть длительной для обеспечения стерилизации вегетаций клапанов.
Эмпирическая антимикробная терапия
До получения результатов микробиологического исследования крови эмпирическая антимикробная терапия инфекционных эндокардитов должна быть направлена против основных возбудителей с учетом индивидуальных особенностей пациента (табл. 2).
Таблица 2. Эмпирическая антимикробная терапия инфекционного эндокардита
Наиболее частыми возбудителями подострого инфекционного эндокардита являются зеленящие стрептококки (S.mitis, S.sanguis, S.mutans и др.) и S.bovis. Поэтому при подостром инфекционном эндокардите нативных клапанов терапия должна быть ориентирована на стрептококки. При ее неэффективности следует думать о других возбудителях, прежде всего энтерококках.
При остром инфекционном эндокардите препаратами выбора являются АМП, активные в отношении S.
aureus.
У «в/в наркоманов» антибиотикотерапия должна включать препараты, активные в отношении S.aureus и грамотрицательных палочек (во многих регионах у наркоманов отмечается высокая частота MRSA).
При инфекционном эндокардите искусственных клапанов препаратами выбора являются ванкомицин и гентамицин, так как высока распространенность MRSE.
После получения результатов микробиологического исследования крови необходимо скорректировать терапию. При отрицательных культурах крови следует продолжить проводимую терапию, если она была эффективной. Рекомендуемые комбинации АМП, дозы, кратность и длительность их введения в зависимости от этиологии эндокардитов приведены в табл. 3.
Таблица 3. Антимикробная терапия инфекционных эндокардитов установленной этиологии (в соответствии с рекомендациями Международного общества по химиотерапии, 1998)
ОСОБЕННОСТИ ЛЕЧЕНИЯ ИНФЕКЦИОННОГО ЭНДОКАРДИТА У ДЕТЕЙ
Существенных различий между этиологией инфекционных эндокардитов у детей и взрослых нет. Данные об оптимальной антимикробной терапии у детей ограничены, при этом большинство режимов антимикробной терапии было заимствовано у взрослых. В целом, указанные режимы были в равной степени эффективными и менее токсичными при использовании у детей.
ОСОБЕННОСТИ ЛЕЧЕНИЯ ИНФЕКЦИОННОГО ЭНДОКАРДИТА У ЛЮДЕЙ ПОЖИЛОГО ВОЗРАСТА
У пациентов старше 60 лет отмечается несколько большая частота развития инфекционных эндокардитов, что связано с наличием осложняющих факторов (заболевания сердечно-сосудистой системы). При этом у людей пожилого возраста наблюдается понижение функции почек, что может потребовать изменения доз и/или интервала дозирования при использовании пенициллинов и цефалоспоринов, ванкомицина и аминогликозидов.
Инфекционный эндокардит
Микробная инфекция эндокардиальной поверхности сердца, включая его клапаны, различными микроорганизмами является тяжелым состоянием, которое может привести к поражению многих органов и тканей и часто заканчивается летально. Даже в условиях адекватной терапии летальность составляет 10—30%, а при отсутствии своевременного распознавания и правильного лечения достигает 100%.
Клиническая классификация инфекционного эндокардита (ИЭ) основывается на трех признаках: 1) на клиническом течении, 2) на его субстрате и 3) на этиологическом принципе. Согласно первой из классификаций, ИЭ называется острым бактериальным эндокардитом (ОБЭ) при остром развитии симптоматики и тяжелом течении. Возбудителем болезни чаще всего является высоковирулентный и инвазивный микроорганизм, например, золотистый стафилококк. Из-за высокой агрессивности возбудителя ОБЭ может развиваться на ранее интактных клапанах. При менее остром течении говорят о подостром бактериальном эндокардитом (ПБЭ), который вызывается менее вирулентной флорой, например, зеленящим стрептококком. ПБЭ наиболее часто развивается у лиц с предшествующей патологией клапанов.
В зависимости от поражающегося у больного субстрата (второй классификационный принцип) ИЭ делится на: 1) эндокардит нативных клапанов (ЭНК), 2) эндокардит протезированных клапанов (ЭПК) и 3) эндокардит при внутривенной наркомании (ЭВН). До 60-80% инфекционного эндокардита приходятся на ЭНК. Для каждой из этих разновидностей характерны своя доминирующая микрофлора и свои особенности течения. Например, представитель микрофлоры кожи эпидермалъный стафилококк является частой причиной эндокардита протезированных клапанов, но почти не встречается при поражении нативных клапанов.
Третий классификационный принцип основан на микробиологической характеристике возбудителя (например, эндокардит, вызванный золотистым стафилококком). В оставшейся части этой главы будет использоваться деление эндокардитов по клиническому течению, но следует помнить, что на практике используются все три классификации.
Патогенез
В патогенезе эндокардита задействовано несколько факторв: 1) повреждение эндокарда, 2) тромбообразование в месте повреждения, 3) бактериемия и 4) адгезия бактерий к поврежденной эндокардиальной поверхности. Первые два фактора создают благоприятные условия для инфицирования, а два последних обусловливают инвазию возбудителя внутрь эндокарда. Наиболее частой причиной повреждения эндотелия является турбулентный кровоток вследствие патологии клапанного аппарата, когда высокоскоростные потоки крови механически повреждают поверхность эндотелия. Более чем у 70% больных удается выявить лежащие в основе эндокардита структурные и гемодинамические нарушения (таблица 8.6). Инородные тела в кровеносном русле, такие как центральные венозные катетеры и клапанные протезы, также могут вызывать повреждение эндотелия.
После повреждения эндокардиальной поверхности клапана к обнажившейся субэндокардиальной соединительной ткани прилипают тромбоциты, которые инициируют отложение фибрина и формирование стерильного тромба (так называемой вегетации). Этот процесс называется небактериальным тромботическим эндокардитом (НБТЭ) или марантическим эндокардитом. НБТЭ создает в эндокарде благоприятную среду для микроорганизмов: 1) фибриново-тромбоцитарные отложения облегчают адгезию бактерий, 2) фибрин закрывает прикрепившиеся микробы и, ингибируя хемотаксис и миграцию фагоцитов, предохраняет их от защитных сил макроорганизма.
При наличии НБТЭ поступление с кровотоком микроорганизмов к поврежденной поверхности может привести к развитию инфекционного эндокардита. В таблице 8.7 перечислены наиболее частые возбудители эндокардита и их относительная частота встречаемости. Способность микроорганизма вызывать эндокардит определяется тремя факторами: 1) проникновением в кровоток, 2) сохранением жизнеспособности микроорганизма в циркулирующей крови, 3) способностью к адгезии к эндокарду. Бактерии могут попадать в кровоток при повреждении кожного покрова или слизистых организма, например, из полости рта при стоматологических вмешательствах или с кожи при внутривенном введении препаратов. Хотя транзиторная бактериемия является относительно частым явлением, к развитию эндокардита приводят только те микроорганизмы, которые способны сохранять жизнеспособность в циркулирующей крови и прикрепляться к вегетациям. В частности, приблизительно 90% случаев эндокардита обусловлено грамположительной флорой, и в первую очередь из-за ее устойчивости к деструкции системой комплемента. Кроме того, частота развития эндокардита коррелирует со способностью определенных видов стрептококка продуцировать декстран, компонент клеточной стенки бактерии, ответственный за адгезию к тромбу.

После своей адгезии к поврежденной поверхности микроорганизмы защищаются от фагоцитарной активности покрывающим их фибрином. Теперь они могут свободно размножаться, в результате чего вегетации еще больше увеличиваются. Наличие инфицированных вегетации является источником постоянной бактериемии и может приводить к развитию ряда осложнений. Эти осложнения имеют в своей основе: 1) механическое повреждение сердца, 2) тромботические или септические эмболии и 3) иммунное повреждение, обусловленное отложением комплексов антиген-антитело. Так, локальное распространение инфекции внутри сердца может привести к прогрессирующему разрушению клапанов с исходом в сердечную недостаточность, образованию абсцессов или деструкции проводящей системы сердца. Кусочки вегетации могут вызывать периферические эмболии, наиболее часто в центральную нервную систему, почки и селезенку, провоцируя инфекционное поражение или инфаркты этих органов. Отложение иммунных комплексов может приводить к гломеру-лонефриту, артриту, васкулиту. Все эти осложнения могут оказаться фатальными.
Клинические проявления
Острый ИЭ отличается бурным быстро прогрессирующим течением; заболевание начинается с высокой лихорадки и потрясающего озноба. Напротив, подострый ИЭ начинается исподволь, с невысокой температуры и ряда неспецифических симптомов, таких как утомляемость, анорексия, слабость, миалгии, потливость по ночам. Подострый ИЭ часто напоминает другие болезни, например, грипп или инфекцию верхних дыхательных путей, и его ранняя диагностика требует высокой степени настороженности. При этом помогает наличие в анамнезе клапанного порока и других состояний, предрасполагающих к эндокардиту.
Системный воспалительный ответ на инфекцию обусловливает развитие таких симптомов, как лихорадка и спленомегалия, а также ряд лабораторных отклонений, таких как лейкоцитоз со сдвигом влево (увеличение процента нейтрофилов и незрелых гранулоцитов из-за острого воспаления), повышение скорости оседания эритроцитов и, более чем в 50% случаев, повышение уровня ревматоидного фактора в крови.
При объективном исследовании сердца можно выявить шум, отражающий первичную клапанную патологию, приведшую к ИЭ. В других случаях можно обнаружить также появление новых шумов вследствие обусловленной эндокардитом недостаточности одного или нескольких клапанов. Поражение клапанов правых отделов сердца, редко встречающееся у обычных людей, очень типично для наркоманов (ЭВН). В целом, шумы чаще выявляются при ПБЭ, чем при ОБЭ. С другой стороны, оценка динамики аускультативной картины при ОБЭ может оказаться особенно полезной, так как изменение характера шума с течением времени (например, усиление регургитации) может отражать быстропрогресси-рующую деструкцию клапанов, более характерную для ОБЭ. С течением времени повреждение клапанов может приводить к появлению признаков застойной сердечной недостаточности.
Инфицированные эмболы могут разноситься кровотоком практически во все внутренние органы, включая кожу, мозг, почки, кишечник и селезенку. Эмболии в центральную нервную систему отмечаются у 33% пациентов. Поражение почек, иммунного или эмболического генеза, может манифестироваться гематурией, болью в боку или почечной недостаточностью. Инфаркты легких (эмболии легочной артерии) и их инфицирование (пневмония ) наиболее часто встречаются при эндокардите правых отделов сердца. Эмболии и последующее инфицирование vasa vasorum могут привести впоследствии к локальному образованию аневризм (так называемые микотические аневризмы), которые ослабляют сосудистую стенку и могут разрываться. Микотические аневризмы могут обнаружиться в аорте, внутренних органах и на периферии, но особенно опасно их образование в церебральных сосудах, где их разрыв может вызвать фатальное внутричерепное кровоизлияние.
Другие физикальные признаки ИЭ связаны с септическими эмболи-ями или дистальным иммунокомплексным васкулитом. Например, образуются петехии — маленькие круглые образования красно-коричневого цвета на коже и слизистых. Под ногтями можно обнаружить следы от заноз — небольшие линейные кровоизлияния, возникающие в результате микроэмболий в ногтевое ложе. Безболезненные слегка выпуклые пятна на ладонях и стопах называются пятнами Джейнуэя. Нежные, размером с горошину эритематозные узелки, появляющиеся в первую очередь на внутренней стороне пальцев рук и ног, известны как узелки Ослера. Эмболии в сетчатку обусловливают появление так называемых пятен Рота, представляющих собой микроинфаркты; при исследовании глазного дна они выглядят как белые пятна с геморрагическим венчиком.
Диагностика и адекватное лечение эндокардита основаны на идентификации возбудителя с помощью посевов крови. Лечение затем может быть направлено на элиминацию конкретного возбудителя с учетом его чувствительности к антибиотикам. Этиологический агент может быть выделен в культуре приблизительно в 95% случаев. Этого не удается сделать в случае недавнего назначения антибиотиков или если микроорганизм требует особых питательных сред.
В диагностике применяются и другие методы. Электрокардиограмма может выявить инфекционное поражение проводящей системы сердца, которое может обусловливать блокады сердца различной степени и появление нарушений ритма. Эхокардиография существенно облегчает диагностику, когда удается непосредственно визуализировать вегетации. Она также полезна в выявлении таких осложнений эндокардита, как клапанные пороки и образование абсцессов. Чреспищеводная эхокардиография гораздо более чувствительна в выявлении вегетации, чем стандартное трансторакальное исследование.
Лечение эндокардита предусматривает длительное (4—6 недель) внутривенное введение этиотропных антибиотиков в больших дозах. Хирургическое вмешательство, обычно протезирование клапана, предпринимается только в случае неэффективности антибактериальной терапии или развитии жизнеугрожающих осложнений, таких как тяжелая клапанная дисфункция с явлениями сердечной недостаточности, повторные эмболии и формирование абсцесса миокарда.
Возможно, наиболее важным аспектом лечения является профилактика эндокардита, заключающаяся в назначении антибиотиков лицам из групп риска в связи с вызывающими бактериемию вмешательствами (таблица 8.8).
ЗАКЛЮЧЕНИЕ
Клапанные пороки сердца являются важной причиной инвалидизации и смертности. В настоящее время патофизиология этих состояний изучена достаточно основательно, что дает возможность использовать как простые диагностические методы, которые можно применить непосредственно у постели больного, так и сложные исследования гемодинамики. Краткий обзор наиболее типичных признаков самых частых клапанных пороков представлен в таблице 8.9.
Классификация инфекционного эндокардита
В классификации О. М. Буткевич и Т. Л. Виноградовой (1997) первый раздел посвящен этиологии ИЭ(зеленящий стрептококк, золотистый стафилококк, белый стафилококк, энтерококк, грамотрицательные микроорганизмы, патогенные грибы. другие возбудители, «абактериальная» форма или эндокардит неизвестной этиологии).
Во втором разделе классификации выделяются два клинико-морфологических варианта заболевания — первичный и вторичный ИЭ. Первичный инфекционный эндокардит развивается на неизмененных ранее клапанах, а вторичный — на фоне ранее существовавшей патологии сердца (ревматические пороки, врожденные пороки сердца, пролапс митрального клапана, искусственные клапаны сердца и др.).
В третьем разделе представлены клинические варианты течения инфекционного эндокардита: острое, подострое, затяжное (с относительно благоприятным и с неблагоприятным прогнозом течения) и иммунологический вариант.
§ является в патогенетическом плане сепсисом с первичной локализацией инфекции на клапанном аппарате, реже — на пристеночном эндокарде;
§ манифестирует яркой септической клиникой, выявляется уже на 5-7 день от начала заболевания клинически и по данным эхокардиографии, причем это не только собственно эндокардит, но и деструктивные изменения одного или более клапанов сердца (чаще всего, аортальная недостаточность), требующие немедленной хирургической коррекции;
§ заканчивается при отсутствии срочного кардиохирургического лечения гибелью больного, в редких случаях при массивной антибиотикотерапии удается перевести заболевание в подострое течение с более благоприятным прогнозом.
Подострый ИЭ развивается в течение 3-6 нед. — это клапанная инфекция (вальвулит, эндокардит) с персистирующей септицемией.
Затяжной ИЭ – маломанифестный подострый эндокардит, при этом клиника заболевания стертая, что обусловливает, его позднюю диагностику, в настоящее время термин употребляется редко.
Четвертый раздел классификации посвящен особым формам ИЭ.
Как и авторы предыдущих классификаций, А. А. Демин и В. П. Дробышева выделяют этиологический раздел; течение (острое, подострое); исход (выздоровление, ремиссия, неэффективность лечения, рецидив); клинико-морфологические формы (первичный, вторичный инфекционный эндокардит); в разделе «органы-мишени» приводятся формы поражения сердца, сосудов, почек, печени, селезенки, легких, нервной системы. Большого внимания заслуживает стратификация риска и предикторов эмболизации.