Постинсультные когнитивные расстройства: причины, клинические проявления, лечение
И.С. Преображенская
В статье подробно рассматриваются вопросы этиологии, патогенеза и клинические проявления сосудистых когнитивных расстройств. Отдельно детально обсуждены вопросы связи нарушений мозгового кровообращения и постинсультных когнитивных расстройств. Представлены критерии дифференциального диагноза сосудистых и нейродегенеративных когнитивных нарушений. Приведены современные данные о патогенетическом и симптоматическом лечении постинсультных когнитивных расстройств.
Сосудистые расстройства являются второй по частоте причиной когнитивных нарушений
(КН) после болезни Альцгеймера (БА). Согласно данным большинства исследователей, сосудистая деменция составляет 15 % среди всех случаев деменции. Частота смешанной деменции примерно равна таковой сосудистой деменции, также составляя 10–15 % [1, 3, 14]. Таким образом, сосудистая
деменция встречается втрое реже БА.Однако частота распространенности умеренных КН вследствие сосудистой патологии головного мозга может быть несколько выше [15, 16]. Следует отметить, что в отличие от БА частота сосудистых КН не одинакова в различных популяциях и прямо зависит
от наличия и выраженности сердечно-сосудистой патологии и сосудистых факторов риска. Так, в странах с низкой встречаемостью сердечно-сосудистых заболеваний, например в Японии, распространенность как умеренных КН сосудистой природы, так и сосудистой деменции чрезвычайно
низка. В то же время в странах с высоким распространением сосудистых факторов риска частота как дементных, так и недементных сосудистых КН превосходит БА.
Данные относительно распространенности сосудистых КН и БА в Российской Федерации отсутствуют.
Мы можем предположить, что частота встречаемости сосудистых КН в РФ будет несколько выше, чем в странах Евросоюза, в связи с бóльшей распространенностью и меньшей профилактикой сосудистых факторов риска. Это предположение в связи с отсутствием статистических данных нуждается
в дальнейшем исследовании и подтверждении.
Сосудистые КН могут быть следствием как острых, так и хронических процессов, приводящих к очаговому и/или диффузному поражению головного мозга и в дальнейшем – к нарушению внутримозговых связей [4, 8, 14]. Механизмы развития сосудистых КН крайне разнообразны. Так,
когнитивное снижение может быть результатом нарушения кровотока по магистральным артериям головы или же по внутричерепным и внутримозговым артериям. Снижение когнитивной функции может быть следствием кардио- или артерио-артериальных эмболий. В ряде случаев когнитивное
снижение может быть также обусловлено дисбалансом между артериальным притоком и венозным оттоком крови. В связи с этим сосудистые КН бесконечно многообразны по скорости развития патологических симптомов и особенностям клинической картины. Так, когнитивное снижение у пациента может быть следствием мультиинфарктного поражения головного мозга; в таком случае наиболее вероятным вариантом течения заболевания будет постепенное или, возможно, ступенеобразное нарастание выраженности симптомов. Когнитивное снижение также может быть следствием поражения инсультом т. н. стратегической зоны – отдела мозга, важного для когнитивного функционирования. К зонам, значимым для познавательного процесса, относят таламус, гиппокамп,
базальные ганглии, ствол головного мозга и лобные доли. Соответственно, при поражении стратегической зоны КН могут развиваться остро, на фоне инсульта или сразу после него. Инсульт при этом может быть первым; в таком случае при нейровизуализации врач может не увидеть других
признаков сосудистого церебрального процесса и ошибочно отнести КН к другим заболеваниям [4, 8]. Часто развиваются после большого по объему инсульта. Известно, что до определенного объема поражения компенсаторные возможности и имеющийся церебральный резерв позволяют сохранять когнитивные функции на стабильном уровне. При нарастании объема поражения обычно происходит декомпенсация и как следствие –развитие умеренных, а затем и тяжелых КН. Таким образом, объем поражения при инсульте является принципиально важным для развития КН.
Один из вариантов развития КН –это поражение головного мозга вследствие поражения мелких сосудов. В таком случае заболевание характеризуется неуклонным прогрессированием и по течению напоминает БА. В клинической картине в отличие от БА преобладают нарушения регуляции и скорости психических процессов – снижение беглости мышления и речи, инертность, импульсивность,
сложность усвоения новой программы действия. Рано развиваются и обычно выражены нарушения поведения; в неврологическом статусе также можно отметить признаки поражения лобноподкорковых связей – апраксию ходьбы, падения, нарушения речи по типу динамической дисфазии, нарушение
тазовых функций, феномен противоудержания, псевдобульбарный синдром, хватательные рефлексы.
Для пожилых пациентов частым является развитие КН вследствие церебральной гипоперфузии. В этом
случае механизм развития КН основывается на снижении частоты сердечных сокращений в ночное время, что особенно выражено у пожилых и старых больных. Аналогичные изменения могут быть следствием избыточной гипотензивной терапии или невыявленной ортостатической гипотензии.
Обычным течением гипоперфузионных КН является их развитие в ночное время или сразу после сна.
Просыпаясь, пациент не сразу может понять, спит он или нет; часто возбужден и принимает увиденный им сон за реальность. Подобные симптомы длятся несколько часов и затем постепенно исчезают, приводя к последующему развитию или нарастанию выраженности уже имеющихся КН. Связь инсульта и КН чрезвычайно многообразна. С учетом предыдущего состояния когнитивных функций, сопутствующей патологии, объема и локализации нарушения мозгового кровообращения частота развития деменции после инсульта варьируется в крайне широких пределах и составляет, по данным разных исследователей, от 4 до 41 % [5, 6, 9].
Выраженность КН неодинакова и в разные периоды развития ишемического инсульта. Так, проведенное В.А. Парфеновым и соавт. исследование показало, что КН той или иной степени выраженности встречаются среди 68 % пациентов в остром периоде ишемического инсульта; исследование проводилось в группе пациентов с легкой степенью неврологического дефицита, без афазии [9]. В постинсультном периоде КН отмечаются у 83 % пациентов; при этом у 30 % их выраженность соответствует деменции, а 53 % пациентов демонстрируют умеренные КН. Как умеренные, так и тяжелые КН вследствие расстройства мозгового кровообращения могут быть моно- и полифункциональными. Например, пациент может иметь тяжелое когнитивное снижение вследствие транскортикальной афазии или корсаковского синдрома или же быть дементным и, соответственно, демонстрировать социальную дезадаптацию вследствие снижения нескольких когнитивных функций. Та же закономерность типична и для сосудистых умеренных когнитивных расстройств.
В рамках развития КН после инсульта следует рассматривать возможное развитие или прогрессирование сопутствующих расстройств при БА. Многочисленные клинические и лабораторные исследования показали, что структуры гиппокампового круга крайне чувствительны к ишемии и могут поражаться при хронической обструктивной болезни легких, синдроме обструктивного сонного апноэ, сердечной недостаточности и несомненно вследствие церебральной гипоперфузии любой другой природы [4, 6]. Исследование, выполненное Braak [11], и ряд морфологических исследований, выполненных позднее, показали, что отложение амилоидного белка и гибель нейронов при БА начинаются задолго до того, как у пациента отмечаются первые симптомы болезни, и тем более задолго до развития у него деменции. Таким образом, нельзя исключать, что ряд пациентов, перенесших нарушение мозгового кровообращения, могут иметь и текущую, пока еще клинически не проявившуюся БА. В таком случае КН в постинсультном периоде могут быть следствием как самого нарушения мозгового кровообращения и текущего церебрального процесса, так и того, что церебральная ишемия и острая сосудистая катастрофа выступили факторами прогрессирования БА.
Проведенные исследования показывают, что деменция в постинсультном периоде отмечается среди 60 % пациентов (при анализе группы с легкой степенью неврологического дефицита) [8]. Ретроспективный анализ выраженности КН у той же группы пациентов до развития инсульта показал, что деменция была отмечена только у 26 % пациентов. Таким образом, нарушение мозгового кровообращения оказывает несомненное действие на развитие деменции. Детальный анализ КН показал, что у 32 % пациентов были выявлены первичные нарушения памяти, и это заставило предположить, что деменция в данном случае является результатом БА, а инсульт – лишь фактор инициации иного заболевания.
При проведении дифференциального диагноза между сосудистым и нейродегенеративным заболеваниями важно правильное понимание результатов нейропсихологического исследования пациента. Так, под первичными, или гиппокампальными, нарушениями памяти понимают значительную
разницу в количестве заученных слов или символов при непосредственном и отсроченном от запоминания воспроизведении [12]. При этом при введении подсказок, облегчающих запоминание
материала, подсказки не будут облегчать припоминание слов при отсроченном воспроизведении. Нарушения памяти такого рода не типичны для сосудистого поражения головного мозга; при появлении их у пациента, перенесшего инсульт, мы можем предположить два варианта развития событий. В первом случае инсульт разрушил гиппокамп пациента и таким образом первичные нарушения памяти являются результатом непосредственного структурного поражения гиппокампа. Во втором случае инсульт спровоцировал прогрессирование БА и тогда нарушения памяти являются
ее первыми клиническими проявлениями. Оценить, поражен ли инсультом гиппокамп, или нет, мы можем с помощью нейровизуализации; таким образом, нейровизуализация в сочетании с анализом результатов нейропсихологического тестирования поможет нам провести дифференциальный диагноз между сосудистым и нейродегенеративным поражениями у пациентов в постинсультном периоде. Атрофия височных долей, часто воспринимаемая врачами как первый признак развития БА, напротив, не является клинически значимой. Проведенные многочисленные исследования показали, что атрофия чаще всего никак не коррелирует с тяжестью симптомов у пациентов с БА; пациенты с умеренными и тяжелыми когнитивными нарушениями могут иметь одинаковую степень атрофического процесса.
Распространенность атрофии намного больше, чем клинические проявления БА; так, атрофия у пациентов, перенесших нарушение мозгового кровообращения, была выявлена в 60 % случаев, при том что клинические признаки БА отмечались лишь у 32 % больных [8].
Дополнительным дифференциально-диагностическим признаком может быть дальнейшая динамика когнитивных расстройств у пациентов в раннем и позднем восстановительных периодах. КН, имеющие непосредственную связь с инсультом, отличаются стационарным или регрессирующим течением, в то время как КН, являющиеся следствием БА, склонны к неуклонному прогрессированию.
Лечение постинсультных когнитивных расстройств должно быть в первую очередь направлено на максимально полное выявление и устранение сосудистых факторов риска. Многочисленные проведенные исследования показали, что устранение или уменьшение выраженности даже одного сосудистого фактора риска оказывает самое непосредственное влияние как на частоту развития повторных инсультов, так и на выраженность когнитивных расстройств [6, 7, 9]. Так, исследования, оценивавшие эффективность адекватного и постоянного приема антигипертензивных средств, показали, что поддержание артериального давления на оптимальном для пациента уровне приводит к уменьшению выраженности сосудистых когнитивных расстройств. Такие же данные были получены в отношении оптимизации уровня сахара, липидов крови, отказа от курения, снижения веса, оптимизации двигательной активности и т. д. Следует отметить, что многие из этих факторов являются общими как для сосудистого церебрального процесса, так и для БА – к примеру, известно, что снижение уровня холестерина уменьшает скорость амилоидогенеза и, соответственно, оказывает влияние на прогрессирование БА. Таким образом, выявление и лечение сосудистых факторов риска являются важным моментом в лечении постинсультных КН любой этиологии.
Симптоматическое лечение постинсультных когнитивных расстройств представляется сложным. Описывается возможное влияние на выраженность когнитивных расстройств ряда препаратов, таких как ноотропы, метаболические средства, содержащие гингко билоба и т. д. В настоящей статье нам бы хотелось подробнее обсудить возможный терапевтический эффект мемантина (Акатинол Мемантин).
Эффективность антагонистов NMDA-рецепторов при деменции давно известна и доказана многими
клиническими исследованиями [3, 5,10]. Данный препарат зарекомендовал себя как средство лечения нейродегенеративных и сосудистых деменций и, соответственно, может быть рекомендован к лечению постинсультной деменции любой этиологии. В настоящей статье хотелось бы остановить-ся на возможности применения этого препарата пациентами с умеренными КН сосудистой природы.
Проведенные исследования показали, что мемантин является препаратом, эффективным для лечения умеренных когнитивных расстройств. Так, исследование, выполненное А.Б. Локшиной, показало значительную эффективность этого препарата в лечении пациентов с дисциркуляторной энцефалопатией [5]. Интересными также представляются результаты региональной программы, в которой эффективность мемантина была оценена как у пациентов с предположительно нейродегенеративным, так и с предположительно сосудистым генезом когнитивных расстройств [10].
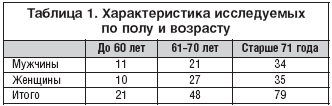
В исследовании приняли участие неврологи из 21 города РФ. Единый протокол осмотра пациентов, анализ качества протоколов и составление статистической базы были выполнены на базе кафедры нервных болезней ГБОУ ВПО 1 МГМУ им. И.М. Сеченова. Статистическую обработку полученных данных выполнил отдел медицинской статистики Научного центра неврологии РАМН.
В исследование были включены пациенты в возрасте 55 лет и старше, предъявившие жалобы на снижение когнитивных функций, у которых при выполнении клинического нейропсихологического исследования выявлены умеренные КН или легкая деменция: общий балл по краткой шкале оценки психических функций – КШОПС (MMSE – Mini Mental State Examination) – составил 22–28 баллов
включительно. У участников исследования не должно было быть тяжелой соматической патологии, острого нарушения мозгового кровообращения или тяжелой черепно-мозговой травмы в течение последнего года, алкоголизма, эпилепсии, паркинсонизма, рассеянного склероза; тяжелых двигательных расстройств, а также выраженной депрессии (оценка по шкале депрессии Гамильтона – более 14 баллов). В исследовании исключался прием ноотропных средств, дофаминергических препаратов, антидепрессантов и ингибиторов ацетилхолинестеразы. Всего в исследование были включены 240 пациентов, средний возраст которых составил 69,5 ± 5,5 лет. Больные были разделены на две группы – основную, которую составили 148 пациентов, принимавших во время наблюдения мемантин, и группу сравнения, включившую 92 пациента, не получавших лечение мемантином. Пациенты основной группы и группы сравнения были сопоставимыми по полу, возрасту, длительности заболевания, наличию таких факторов риска, как атеросклероз, ИБС, артериальная гипертензия, сахарный диабет, черепно-мозговая травма в анамнезе, наследственная отягощенность по деменции.
Эффективность терапии оценивали с помощью количественных нейропсихологических шкал, а также по динамике соматического и неврологического статуса и выраженности эмоциональных расстройств. Количественное нейропсихологическое тестирование включало КШОПС, батарею тестов для оценки лобной дисфункции (БЛД), тест повторения цифр в модификации С. Маттиса, тест на запоминание
5 слов по методике А.Р. Лурия, тест рисования часов, оценку беглости речи (тесты “литеральные ассоциации” и “категориальные ассоциации”). Выраженность эмоциональных расстройств оценивали с помощью шкалы депрессии Гамильтона. Указанное исследование было выполнено всем пациентам основной группы и группы сравнения перед началом лечения, а также через 1,5; 3 и 6 месяцев терапии. В течение всего времени наблюдения проводилась оценка безопасности лечения (оценка витальных показателей, регистрация всех возникающих нежелательных явлений).
Большинство пациентов основной группы получали 20 мг мемантина на протяжении всего исследования. Проведенное исследование показало, что на фоне терапии мемантином достоверно уменьшилась выраженность когнитивных расстройств, о чем свидетельствовало увеличение суммарного балла по КШОПС (p
достоверного улучшения, так и достоверного ухудшения когнитивных расстройств на протяжении всего периода наблюдения.
На фоне лечения мемантином было выявлено достоверное уменьшение выраженности нарушений программирования, обобщения и контроля за выполняемыми операциями (согласно данным оценки по БЛД). Отмечено статистически значимое нарастание общего балла БЛД (p
Анализ динамики нарушений памяти на фоне лечения мемантином показал, что у пациентов основной группы имело место достоверное уменьшение выраженности мнестических расстройств, что проявлялось как увеличением числа запоминаемых слов при заучивании материала (p
на протяжении всего периода наблюдения. Различия между группами, равно как и динамика показателей в основной группе, становились статистически значимыми через три месяца терапии
мемантином (p
У пациентов основной группы отмечено увеличение беглости речи (нарастание уровня внимания и
уменьшение выраженности зрительно-пространственных расстройств; p
исследуемых групп достигали статистической значимости на 3-й месяц наблюдения и сохранялись далее (p
Для оценки динамики КН в зависимости от их тяжести пациенты основной группы были разделены на две подгруппы в соответствии с общим баллом по КШОПС: 1-я подгруппа – 96 пациентов с общим баллом 22–24, что может соответствовать легкой деменции, и 2-я подгруппа – 52 пациента с общим баллом более 25, что соответствует умеренным КН. По возрасту пациентов подгруппы достоверно не различались.
Пациенты с изначально более выраженными КН (подгруппа 1) в целом лучше реагировали на лечение (общий балл КШОПС на 3-й и 6-й месяц наблюдения, p = 0,044). Однако в подгруппе пациентов с изначально меньшей выраженностью когнитивных расстройств отмечена большая позитивная динамика нарушений памяти и беглости речи (p
Был выполнен корреляционный анализ эффективности терапии в зависимости от наличия сосудистых факторов риска. Анализировали влияние артериальной гипертензии, атеросклероза, ИБС, инсульта в анамнезе, сахарного диабета. Также анализировалась эффективность лечения в зависимости от возможного наследственного отягощения по БА (наличие нарушений памяти и деменции в пожилом и
старческом возрасте у близких родственников). Результаты исследования показали, что эффективность лечения была одинаковой вне зависимости от степени отягощенности сосудистыми
факторами риска. Также не было отмечено достоверной взаимосвязи между эффективностью лечения и наследственным анамнезом у исследуемых пациентов.
Таким образом, проведенное исследование показало, что Акатинол Мемантин является эффективным
симптоматическим лекарственным средством лечения как умеренных КН, так и легкой деменции. При этом препарат одинаково эффективен при предположительных умеренных когнитивных расстройствах сосудистого генеза и дебюте БА.
Представленный опыт использования Акатинола Мемантина и имеющаяся на сегодня доказательная клиническая база позволяют рекомендовать этот препарат в качестве лечения постинсультных КН как умеренной, так и тяжелой степени.
Лечение постинсультных когнитивных нарушений. Применение Омарона
Парфенов В.А.
Причины и диагностика
Когнитивные нарушения отмечаются у 30–70% пациентов, перенесших инсульт [1,4–6]. Когнитивные нарушения могут быть легкими, умеренными и достигать степени деменции, вызывающей нарушение адаптации в профессиональной, общественной и бытовой сфере [5]. У пациентов, перенесших инсульт, легкие и умеренные когнитивные нарушения отмечаются примерно в половине случаев, деменция – в 10–20% случаев [1,4,6]. Постинсультные когнитивные нарушения обычно сочетаются с другой очаговой неврологической симптоматикой, вызванной инсультом.
В развитии постинсультных когнитивных расстройств может иметь значение не только перенесенный инсульт, но и предшествующее сосудистое поражение головного мозга («немые» инфаркты, лейкоареоз), сочетанное дегенеративное заболевание, например, болезнь Альцгеймера [1,4,6]. Поэтому возможность развития «чистых» форм постинсультной деменции, особенно после единичного инфаркта, ставится под сомнение, так как у пациентов с первым клинически значимым инсультом по данным нейровизуализации часто выявляются другие очаговые изменения белого вещества и подкорковых образований, а также атрофические изменения, характерные для нейродегенеративного процесса [1].
Когнитивные нарушения могут достигать степени деменции при инфаркте в стратегической для когнитивных функций зоне головного мозга (угловая извилина, зрительный бугор, хвостатое ядро, бледный шар, гиппокамп). Однако этот вариант когнитивных нарушений встречается относительно редко, его клиническая картина определяется локализацией поражения [1,6]. Например, при поражении доминантного зрительного бугра (обычно левого у правшeй), часто возникают брадифрения (снижение психической активности), дефицит внимания в сочетании с апатией, агнозией, апраксией и афазией.
Постинсультные когнитивные нарушения наиболее часто вызваны повторными (лакунарными и нелакунарными) инфарктами, многие из которых обнаруживаются только при нейровизуализации («немые» инфаркты головного мозга), и сочетанным поражением белого вещества головного мозга (лейкоареоз). Мультиинфарктная деменция (корковая, корково–подкорковая) представляет частый вариант постинсультной деменции [1,4,6]. У таких больных, помимо когнитивных нарушений, часто выявляются центральные парезы конечностей или рефлекторные изменения (оживление глубоких рефлексов, положительные рефлексы Бабинского, Россолимо). Атактические расстройства могут носить сенситивный, мозжечковый и вестибулярный характер, при деменции часто встречается апраксия ходьбы вследствие дисфункции лобных долей и разрыва корково–подкорковых связей. Для нарушений равновесия лобного генеза характерно замедление ходьбы, укорочение и неравномерность шага, затруднение в начале движений, неустойчивость при поворотах и увеличение площади опоры. Псевдобульбарный синдром проявляется рефлексами орального автоматизма, оживлением нижнечелюстного рефлекса, эпизодами насильственного плача или смеха, замедленностью психических процессов.
Нарушения памяти у больных, перенесших инсульт, представлены не столь выраженно, как при болезни Альцгеймера, и проявляются повышенной тормозимостью следов, замедлением и быстрой истощаемостью когнитивных процессов, нарушением процессов обобщения понятий, апатией [4–6]. Ведущими нарушениями могут быть замедленность мышления, трудности переключения внимания, снижение критики, понижение фона настроения и эмоциональная лабильность. Могут наблюдаться и первичные расстройства высших психических функций (апраксия, агнозия и т.д.), что наблюдается при локализации ишемических очагов в соответствующих отделах коры больших полушарий головного мозга.
Когнитивные нарушения могут возникать и вследствие внутримозгового кровоизлияния, при котором основным заболеванием часто является поражение мелких артерий, формирующееся на фоне длительной гипертонической болезни или амилоидной ангиопатии.
Диагноз постинсультных когнитивных нарушений основывается на клинических, неврологических и нейропсихологических данных, результатах магнитно–резонансной или компьютерной томографии головного мозга [4–6]. Для установления сосудистого характера когнитивных нарушений большую роль играет анамнез заболевания, наличие факторов риска цереброваскулярной патологии, характер течения заболевания, временная связь когнитивных расстройств и сосудистой патологии головного мозга. За последние десятилетия для диагностики сосудистой деменции было предложено несколько вариантов критериев диагноза. Одними из самых популярных критериев такого рода являются предложенные рабочей группой NINDS–AIREN в 1993 году критерии [11], согласно которым диагноз сосудистой деменции устанавливается в том случае, если у пациента одновременно выявляются деменция, признаки цереброваскулярного заболевания и между ними существует причинно–следственная взаимосвязь (развитие деменции в первые 3 месяца после инсульта).
Нейропсихологическое тестирование играет важную роль в диагностике синдрома сосудистых когнитивных нарушений. Краткая шкала оценки психического статуса (КШОПС), широко используемая для выявления когнитивной дисфункции, связанной с болезнью Альцгеймера, при когнитивных нарушениях сосудистой этиологии менее информативна и не может использоваться как метод выбора. Для выявления сосудистых когнитивных нарушений в качестве скрининговых нейропсихологических тестов (в дополнение к КШОПС) следует применять серию тестов для оценки лобной дисфункции, тест рисования часов [4,5].
Профилактика повторного инсульта
Важнейшее значение в ведении пациента, перенесшего инсульт и имеющего когнитивные нарушения, отводится вторичной профилактике инсульта, инфаркта миокарда и других сосудистых заболеваний [2,7,12].
Среди нелекарственных методов вторичной профилактики инсульта первостепенное значение имеют отказ от курения и злоупотребления алкоголем, регулярные физические нагрузки с учетом индивидуальных возможностей пациента, употребление в достаточном количестве свежих фруктов и овощей, растительного масла, свежей рыбы и ограничение потребления продуктов, богатых холестерином, и поваренной соли, снижение избыточного веса.
Нормализация артериального давления представляет собой одно из наиболее эффективных направлений вторичной профилактики инсульта, т.к. это снижает риск развития инсульта на 30–40% [7,12]. Выбор антигипертензивных средств проводится с учетом индивидуальных показаний, рекомендуется постепенное снижение повышенного артериального давления. Оптимальный уровень артериального давления, который следует достигнуть у больных, перенесших инсульт, окончательно не определен [7,12]. Если у больного нет выраженных стенозов или закупорок сонных артерий, следует стремиться к нормальному артериальному давлению (систолическое артериальное давление – 120–130 мм рт.ст. диастолическое артериальное давление – 80–85 мм рт.ст.). У больных, перенесших ишемический инсульт и имеющих гемодинамически значимый стеноз сонной артерии (особенно двусторонний) эффективность нормализации артериального давления остается сомнительной. В этих случаях необходима консультация сосудистого хирурга для решения вопроса о хирургическом лечении .
Больным, перенесшим ишемический инсульт, показаны антитромботические средства, статины и в части случаев реконструктивные операции на сонных артериях [1,7,12].
Статины являются одними из наиболее эффективных лекарственных средств для вторичной профилактики ишемического инсульта, особенно при наличии сочетанной ишемической болезни сердца, сахарного диабета, атеросклеротического поражения периферических артерий. Доказана эффективность аторвастатина в больших дозах (80 мг в сутки) у больных, перенесших некардиоэмболический инсульт. В настоящее время статины рекомендуются больным, перенесшим некардиоэмболический инсульт, а также больным с кардиоэмболическим инсультом при наличии других показаний [7].
Антитромботическая терапия показана всем больным, перенесшим ишемический инсульт. При кардиоэмболическом типе инсульта рекомендуются непрямые антикоагулянты, при некардиоэмболическом типе инсульта – антитромбоцитарные средства [1,7,12].
Применение непрямых антикоагулянтов рекомендуется больным с мерцательной аритмией, внутрижелудочковым тромбом, недавно (до трех месяцев) перенесенным инфарктом миокарда, ревматическим поражением митрального клапана, искусственным клапаном сердца и другой патологией, опасной повторением кардиоэмболического ишемического инсульта. Дозу варфарина подбирают постепенно, ориентируясь на международное нормализующее отношение, которое поддерживают на уровне 2–3.
При некардиоэмболическом типе инсульта рекомендуются антитромбоцитарные препараты: ацетилсалициловая кислота (АСК) (75–325 мг в сутки), клопидогрел (75 мг в стуки) или комбинация 200 мг дипиридамола медленного высвобождения и 25 мг АСК два раза в сутки. Прием антитромбоцитарных средств снижает риск развития повторного ишемического инсульта, инфаркта миокарда и острой сосудистой смерти в среднем на 20%. В Европейских рекомендациях по вторичной профилактике ишемического инсульта отмечается преимущество клопидогрела и комбинации 200 мг дипиридамола медленного высвобождения и 25 мг АСК над приемом одной АСК, поэтому их назначение вместо АСК рекомендуется во всех случаях, когда есть возможность длительного лечения этими лекарственными средствами [7]. Применение клопидогрела наиболее обосновано, когда больной, перенесший ишемический инсульт, имеет другие клинические проявления атеротромбоза: ишемическую болезнь сердца, артериальную недостаточность сосудов нижних конечностей.
Каротидная эндартерэктомия рекомендуется при выраженном стенозе (сужении 70–99% диаметра) сонной артерии на стороне перенесенного ишемического инсульта, сопровождающегося незначительной инвалидностью или без нее. Каротидную эндартерэктомию следует проводить только в специализированной клинике, в которой частота осложнений при этой операции не превышает 6%. Каротидную эндартерэктомию рекомендуется выполнить как можно быстрее после перенесенного ишемического события (оптимально в течение первых двух недель, но не позднее 6 месяцев с момента инсульта). При увеличении срока с момента ишемического поражения головного мозга эффективность каротидной эндартерэктомии постепенно снижается [7]. В тех случаях стеноза внутренней сонной артерии, когда каротидная эндартерэктомия противопоказана или стеноз расположен в недоступном для этой операции месте, можно использовать ангиопластику и установку стента. После установления стента рекомендуется в течение не менее одного месяца прием комбинации клопидогрела и АСК, в последующем прием одного из этих лекарственных средств [7,12].
Эффективность профилактики повторного ишемического инсульта значительно возрастает, когда у больного, перенесшего инсульт, используются все возможные эффективные лекарственные и нелекарственные средства.
Улучшение когнитивных функций
Для улучшения памяти и других когнитивных функций больным, перенесшим инсульт и имеющим когнитивные расстройства, рекомендуют посильную умственную нагрузку, тренировку памяти и лекарственные средства [4–6]. Большое значение имеет коррекция часто встречающихся у больных, перенесших инсульт, эмоциональных нарушений – депрессии и повышенной тревожности. Необходимо отменить или использовать в минимальных дозах лекарственные средства, ухудшающие когнитивные функции (средства с холинолитическим действием, анксиолитики, нейролептики, седативные средства).
Тренировка когнитивных функций (когнитивный тренинг) рекомендуется для улучшения и поддержки когнитивных возможностей пациентов, сохранения активного умственного уровня их повседневного функционирования. Положительные результаты когнитивного тренинга наиболее существенны при легкой и средней степени когнитивных нарушений. При проведении когнитивного тренинга необходимо опираться на сохранные когнитивные функции, целесообразно использование для тренировки привычных навыков, имеющихся интересов пациента.
При постинсультной деменции можно использовать ингибиторы ацетилхолинэстеразы (галантамин, донепезил, ривастигмин). Ингибиторы ацетилхолинэстеразы являются препаратами первого выбора в лечении болезни Альцгеймера, однако было доказано, что холинергический дефицит имеет место также и при сосудистой деменции [4,6,9]. Ингибиторы ацетилхолинэстеразы обладают способностью улучшать мозговой кровоток благодаря действию на сосуды или опосредованно через нейрональную активность. Наиболее изученными препаратами, показавшими хорошую эффективность при терапии сосудистой деменции, являются донепезил и галантамин.
Другим направлением нейротрансмиттерной терапии при постинсультной деменции является применение акатинол мемантина – антагониста NMDA–рецепторов к глутамату [5,9,10]. Повышение активности глутаматергической системы наблюдается как при нейродегенеративных заболеваниях, так и при сосудистых заболеваниях головного мозга. Глутамат является не только нейротрансмиттером, но нейротоксином. При различных по своей природе процессах, включая болезнь Альцгеймера и сосудистую деменцию, конечным этапом гибели клетки является эксайтотоксичность, обусловленная избыточным выбросом глутамата. Поэтому важной задачей становится коррекция обусловленных эксайтотоксичностью изменений при условии сохранности нормальной глутаматергической нейротрансмиссии. Действие акатинол мемантина основано на прямой селективной блокаде патологически возбужденных NMDA–рецепторов с уменьшением выраженности феномена эксайтотоксичности. Акатинол мемантин предохраняет нейроны от повреждения в условиях эксайтотоксичности и приводит к улучшению когнитивных функций больных.
При постинсультной деменции возможно и сочетанное применение ингибиторов ацетилхолинэстеразы и акатинол мемантина, поскольку данные препараты воздействуют на разные звенья патогенеза деменции, хотя не проводились исследования такой комбинации [9]. При выборе терапии следует также иметь в виду меньшее число побочных эффектов, связанных с применением мемантина, и его лучшую переносимость пожилыми пациентами в сравнении с ингибиторами центральной ацетилхолинэстеразы [9,10].
Для улучшения когнитивных функций у больных, перенесших инсульт, применяют пирацетам по 1,6–4,8 мг/сут. цитиколин по 1000–2000 мг в сутки, винпоцетин по 15–30 мг/сут. гинкго билоба по 120–160 мг/сут. церебролизин по 20–30 мл в/в на физиологическом растворе ежедневно в течение месяца, глиатилин по 1200 мг/сут. и другие лекарственные средства [1]. Вопрос об эффективности этих средств в отношении улучшения когнитивных функций остается не столь ясным, как использование ингибиторов центральной ацетилхолинэстеразы и акатинол мемантина. В настоящее время активно изучается эффективность применения этих средств у больных, перенесших инсульт и имеющих когнитивные нарушения.
Пирацетам представляет лекарственное средство, в отношении которого накоплен большой опыт в отношении его влияния на память и другие когнитивные функции как в экспериментальных, так и в клинических исследованиях [8,13,14]. В иностранной литературе на основании анализа результатов многоцентровых рандомизированных плацебо–контролируемых исследований отмечается, что ни одно из лекарственных средств не показало преимуществ в отношении улучшения каких–либо функций у пациентов, перенесших инсульт, однако при этом отмечаются положительные эффекты пирацетама, показанные в отношении речевых функций в некоторых плацебо-контролируемых исследованиях [8]. В последние годы в нашей стране широко используется препарат Омарон. представляющий комбинацию 400 мг пирацетама и 25 мг циннаризина.
Применение Омарона при умеренных постинсультных когнитивных
нарушениях
Нами проведено исследование эффективности и безопасности применения Омарона у больных, перенесших ишемический инсульт и имеющих умеренное когнитивное расстройство [3].
В исследование включено 90 пациентов, перенесших ишемический инсульт в сроки от одного до 12 месяцев и имеющих умеренное когнитивное расстройство. Методом рандомизации больные были разделены на две группы по 45 пациентов в каждой – группа лечения Омароном и контрольная группа. В контрольной группе 45 пациентов получали только базовую терапию (антигипертензивные, антитромбоцитарные стредства и другие лекарственные препараты) с целью профилактики повторного инсульта и других сердечно–сосудистых заболеваний. В группе лечения Омароном 45 пациентов в дополнение к базовой терапии получали Омарон по одной таблетке 3 раза в сутки в течение двух месяцев. Группы пациентов не различались по основным клиническим характеристикам (возраст, выраженность неврологических и когнитивных нарушений, степени инвалидности по шкале Ренкина).
За период наблюдения ни у одного из пациентов не развилось ни повторного инсульта, ни инфаркта миокарда или других сосудистых заболеваний. Проведение регулярной антигипертензивной терапии привело к нормализации артериального давления у большинства пациентов как в группе лечения Омароном, так и в контрольной группе без существенных различий между ними.
За два месяца наблюдения в обеих группах пациентов отмечено улучшение показателей неврологического статуса и уменьшение степени инвалидности, что в определенной степени могло быть проявлением естественного восстановления после перенесенного инсульта. В группе пациентов, принимавших Омарон, отмечена тенденция к более значительному восстановлению неврологических функций и уменьшению степени инвалидности.
При повторных обследованиях в группе лечения Омароном и в контрольной группе установлено достоверное улучшение показателей когнитивных функций по данным нейропсихологического исследования, что отражено в таблице 1. При этом в группе лечения Омароном отмечено достоверное улучшение когнитивных функций в сравнении с группой пациентов, получавших только базовую терапию.
Через один и два месяца лечения в группе Омарона установлены достоверно более низкие показатели депрессии и тревожности, чем в контрольной группе, что отражено в таблице 2.
Результаты применения Омарона у пациентов, перенесших инсульт и имеющих умеренное когнитивное расстройство, показали хорошую переносимость лекарственного средства, отсутствие существенных побочных эффектов при его комбинации с антигипертензивными, антитромбоцитарными средствами и статинами, которые используются у пациентов с целью профилактики повторного инсульта и других сердечно–сосудистых заболеваний. У пациентов, принимающих Омарон, отмечено улучшение когнитивных функций по показателям нейропсихологических тестов уже через месяц лечения, и оно было еще более значительным через два месяца лечения. Положительная динамика когнитивных функций наблюдалась и у пациентов в контрольной группе, что в определенной степени могло быть связано с нормализацией у них артериального давления, спонтанным улучшением когнитивных функций и определенным опытом в решении нейропсихологических тестов. Через один и два месяца лечения выраженность депрессивных и тревожных расстройств была достоверно меньше в группе лечения Омароном, чем в контрольной группе. Улучшение эмоционального состояния пациентов могло положительно влиять на их когнитивные функции и быть одной из причин их улучшения. Положительный эффект пирацетама на когнитивные функции, опосредованный улучшением эмоционального состояния, отмечают и другие авторы [13,14].
Таким образом, применение препарата Омарон у пациентов, перенесших инсульт и имеющих умеренное когнитивное расстройство, показало его положительное влияние на когнитивные функции и эмоциональное состояние пациентов. Установлены хорошая переносимость Омарона, отсутствие существенных побочных эффектов при его комбинации с другими лекарственными средствами, которые используются для профилактики повторного инсульта и других сердечно–сосудистых заболеваний.
Литература
1. Вахнина Н.В. Никитина Л.Ю. Парфенов В.А. Яхно Н.Н. Постинсультные когнитивные нарушения // Журнал неврологии и психиатрии им. С.С. Корсакова Инсульт. Приложение к журналу, 2008, вып. 22, с. 16–21.
2. Дамулин И.В. Парфенов В.А. Скоромец А.А. Яхно Н.Н. Нарушения кровообращения в головном и спинном мозге // Болезни нервной системы: Руководство для врачей. Т.1 / Под ред. Н.Н. Яхно. — 4–е изд. перераб. и доп. — М. ОАО «Издательство Медциина». — 2005. — С. 275 — 292.
3. Парфенов В.А. Беланина Г.Р. Вахнина Н.В. и др. Применение омарона у больных с умеренными постинсультными когнитивными нарушениями // Журнал неврологии и психиатрии им. С.С. Корсакова – 2009. – № 6
4. Преображенская И.С. Яхно Н.Н. Сосудистые когнитивные расстройства: клинические проявления, диагностика, лечение // Неврологический журнал — 2007. — Т.12. –№5. –С.45–50.
5. Яхно Н.Н. Когнитивные расстройства в неврологической практике// Неврологический журнал –2006. – Приложение № 1. – С.4–12.
6. Cerebrovascular disease, cognitive impairment and dementia. Second edition of Cerebrovascular disease and dementia. Edited by O’Brien J. Ames D. Gustafson L. Et al.–Martin Dunitz–2004.
7. European Stroke Organisation (ESO) Executive Committee; ESO Writing Committee. Guidelines for management of ischaemic stroke and transient ischaemic attack // Cerebrovasc Dis. – 2008; 25:457–507.
8. Flicker L, Grimley E.G Piracetam for dementia or cognitive impairment //Cochrane Database Syst Rev. 2001. – № 2. – :CD001011.
9. Kavirajan H. Schneider L.S. Efficacy and adverse effects of cholinesterase inhibitors and memantine in vascular dementia: a meta–analysis of randomised controlled trials. // Lancet Neurol. —2007. — Vol.6, N9. — p.782 — 792.
10. Orgogozo J.M. Rigaud A.S. Stoffler A. Efficacy and safety of memantine in patients with mild to moderate vascular dementia: a randomized, placebo–controlled trial (MMM 300). // Stroke. — 2002. — Vol.33, N7. — p.1834 — 1839.
11. Roman GC, Tatemichi TK, Erkinjuntti T. et al. Vascular dementia: diagnostic criteria for research studies. Report of the NINDS–AIREN International Workshop // Neurology. — 1993. — Vol.43, N2. — p.250 — 260.
12. Sacco R. L. Adams R. Albers G. et al. Guidelines for Prevention of Stroke in Patients With Ischemic Stroke or Transient Ischemic Attack: A Statement for Healthcare Professionals From the American Heart Association/American Stroke Association Council on Stroke: Co–Sponsored by the Council on Cardiovascular Radiology and Intervention: The American Academy of Neurology affirms the value of this guideline // Stroke – 2006; 37: 577 – 617.
13. Tariska P. Paksy A Cognitive enhancement effect of piracetam in patients with mild cognitive impairment and dementia // Orv Hetil. 2000. – Vol.141. –: P. 1189–1193.
14. Winblad B. Piracetam: a review of pharmacological properties and clinical uses // CNS Drug Rev. 2005. – Vol. 11. – P.169–182.
Динамика когнитивных нарушений у больных с ишемическим инсультом в каротидном бассейне тема диссертации и автореферата по ВАК 14.01.11, кандидат медицинских наук Дударова, Мадина Абоевна
Оглавление диссертации кандидат медицинских наук Дударова, Мадина Абоевна
Введение.
Цель и задачи исследования.
Глава 1. Обзор литературы.
1.1. Эпидемиология инсульта.
1.2. Когнитивные нарушения при инсульте.
1.2.1. Терминология.
1.2.2. Частота постинсультных когнитивных нарушений.
1.3. Факторы, влияющие на развитие постинсультных когнитивных нарушений.
1.4. Механизмы развития постинсультных когнитивных нарушений.
1.5. Особенности нейропсихологического профиля при постинсультных когнитивных нарушениях.
1.6. Клиническая значимость постинсультных когнитивных нарушений.
1.7. Диагностика постинсультных когнитивных нарушений.26 >
1.8. Общие подходы к лечению постинсультных когнитивных нарушений.
Глава 2. Материалы и методы исследования.
2.1. Клиническая характеристика больных.
2.2. Методы исследования.
2.2.1. Клинико-неврологическое исследование с количественной оценкой неврологических симптомов.
2.2.2. Исследование когнитивных функций.
2.2.3. Исследование аффективных нарушений.
2.2.4. Оценка повседневной активности и инвалидизации.
2.2.5. Исследование качества жизни.
2.2.6. Инструментальные методы обследования.
2.3. Оценка эффективности мемантина у больных с постинсультными когнитивными нарушениями в позднем восстановительном периоде ишемического инсульта.
Глава 3. Результаты исследования.
3.1. Характеристика больных в остром периоде инсульта и через 1 месяц после инсульта.
3.1.1 .Клиническая характеристика больных.
3.1.2.Данные КТ/МРТ.
3.1.3.Данные УЗ- исследования сонных артерий.
3.1 АНейропсихологические нарушения.
3.1.4.1.Анализ когнитивных нарушений.
3.1.4.2.Анализ аффективных расстройств.
3.2. Характеристика больных через 3 месяца после инсульта.
3.2.1.Клиническая характеристика больных через 3 месяца после инсульта.
3.2.2.Анализ когнитивных нарушений через 3 месяца после инсульта.
3.3. Характеристика больных через 6 месяцев после инсульта.
3.3.1.Клиническая характеристика больных через 6 месяцев после инсульта.
3.3.2.Нейропсихологические нарушения.
3.3.2.1.Анализ когнитивных нарушений через 6 месяцев после инсульта.
3.3.2.2.Анализ аффективных расстройств через 6 месяцев после инсульта.
3.4. Факторы, влияющие на выраженность когнитивных нарушений.
3.4.1.Связь когнитивных нарушений с нейровизуализационными данными.
3.4.1 .¡.Зависимость когнитивных нарушений от локализации ишемического очага.
3.4.1.2.3ависимость когнитивных нарушений от степени распространенности лейкоареоза и количества лакунарных очагов.
3.4.1.3. Зависимость когнитивных нарушений от степени выраженности церебральной атрофии.
3.4.2.Влияние аффективных расстройств на выраженность когнитивных нарушений.
3.4.3.Влияние демографических факторов на выраженность когнитивных нарушений.
3.4.4.Влияние фоновых заболеваний на выраженность когнитивных нарушений.
3.5.Влияние когнитивных нарушений на качество жизни и степень инвалидизации больных.
3.6. Эффективность мемантина у больных с постинсультными когнитивными нарушениями в позднем восстановительном периоде ишемического инсульта.
Глава 4. Обсуждение.
Введение диссертации (часть автореферата) На тему «Динамика когнитивных нарушений у больных с ишемическим инсультом в каротидном бассейне»
Инсульт — одна из наиболее актуальных медико-социальных проблем [3, 25]. Ведущей причиной инвалидности в странах Европы и США остается мозговой инсульт. В России живет более миллиона лиц, перенесших инсульт, при этом ежегодно происходит более 450 ООО новых случаев инсульта [8]. Инсульт служит не только одной из основных причин смерти (наряду с сердечно-сосудистыми и онкологическими заболеваниями), но и часто является причиной инвалидизации больных. Реабилитация больных с инсультом является очень важной медицинской и социальной проблемой. К труду возвращается только 20,2% работавших больных, а полная профессиональная реабилитация достигается лишь в 8% случаев. Реабилитационный потенциал наиболее велик, по данным независимых исследований, в первые полгода заболевания — острый и ранний восстановительный период инсульта [7, 56].
Традиционно в клинике инсульта основное внимание уделяют очаговому
•С. I > 1 неврологическому дефициту, связанному с физической инвалидизацией, прежде всего параличам. Между тем психические, и, прежде всего когнитивные, расстройства, возникающие у значительного числа пациентов после инсульта, оказывают на бытовую, социальную и профессиональную адаптацию едва ли не больший эффект, чем моторный дефицит.
Когнитивные нарушения возникают у 40-70 % больных, перенесших инсульт, в среднем у половины пациентов. Они могут быть представлены широким спектром по степени тяжести: от легких до выраженных когнитивных расстройств [154, 221]. Постинсультные когнитивные нарушения могут иметь гетерогенную природу. Их возникновение может быть связано с локализацией очага поражения в стратегической зоне мозга, наличием множественных инфарктов мозга, диффузного поражения белого вещества и/или дегенеративным процессом [11, 221, 248].
Основные факторы, определяющие риск развития когнитивных нарушений у больных с инсультом: пожилой возраст, низкий уровень образования, когнитивные нарушения до инсульта, артериальная гипертензия, сахарный диабет, кардиальная патология, эпилепсия, сепсис, повторный инсульт, дополнительные повреждения головного мозга по данным нейровизуализации [12, 14, 129, 166, 170].
Хотя многие авторы отмечают восстановление когнитивных функций в первые месяцы после инсульта, однако динамика когнитивных нарушений и факторы, влияющие на нее, остаются недостаточно изученными, что предопределяет актуальность настоящей работы. Остаются неясными связь когнитивных нарушений с нейровизуализационными изменениями, а также степень влияния когнитивных расстройств на повседневную активность пациентов, качество их жизни и прогноз восстановления. Недостаточно изученным остается лечение постинсультных когнитивных нарушений, на сегодняшний день не существует средств, эффективность которых была доказана в длительных исследованиях.
Цель исследования:
Исследовать динамику когнитивных нарушений у больных с ишемическим инсультом в каротидном бассейне в остром и раннем восстановительном периодах и их влияние на функциональный исход инсульта.
Задачи исследования:
1. Определить частоту и профиль когнитивных нарушений у больных с ишемическим инсультом в каротидном бассейне в остром и раннем восстановительном периодах.
2. Оценить динамику когнитивных нарушений у больных с ишемическим инсультом в каротидном бассейне в остром и раннем восстановительном периодах.
3. Выявить факторы, влияющие на выраженность когнитивных нарушений у больных с ишемическим инсультом в каротидном бассейне.
4. Оценить взаимосвязь когнитивных и аффективных нарушений у больных с ишемическим инсультом в каротидном бассейне.
5. Изучить влияние когнитивных нарушений на повседневную активность и качество жизни у больных с ишемическим инсультом в каротидном бассейне в остром и раннем восстановительном периодах.
6. Исследовать влияние мемантина на когнитивные функции у больных с постинсультными когнитивными нарушениями в позднем восстановительном периоде.
Научная новизна В результате комплексной оценки нейропсихологических функций у больных с легким и среднетяжелым ишемическим инсультом в каротидном бассейне показана гетерогенность профиля постинсультных когнитивных нарушений. Установлена связь между когнитивными нарушениями, повседневной активностью и качеством жизни у больных перенесших ишемический инсульт в каротидном бассейне.
Показано, что высокая частота когнитивных нарушений у больных, перенесших ишемический инсульт в каротидном бассейне, может быть связана с субклиническим поражением головного мозга, выявляющимся при КТ и МРТ в виде диффузного поражения белого вещества, инфарктов в немых зонах мозга и церебральной атрофии.
Постинсультные когнитивные нарушения являются предиктором неблагоприятного функционального исхода ишемического инсульта и негативно влияют на повседневную активность и качество жизни больных.
Показано, что мемантин улучшает качество жизни пациентов с постинсультными когнитивными нарушениями, уменьшая выраженность нейродинамических, регуляторных и операциональных когнитивных нарушений, а также уменьшая выраженность аффективных расстройств.
Практическая значимость
Разработаны скрининговые нейропсихологические тесты, позволяющие выявлять когнитивный дефицит у больных с ишемическим инсультом в каротидном бассейне в остром и раннем восстановительном периодах.
Показана важность оценки когнитивных нарушений у пациентов с ишемическим инсультом, как в конце острого периода, так и в раннем восстановительном периоде, как фактора, влияющего на функциональный исход ишемического инсульта. Показана целесообразность применения мемантина у больных с постинсультными когнитивными нарушениями в восстановительном периоде. 9
Заключение диссертации по теме «Нервные болезни», Дударова, Мадина Абоевна
109 Выводы
1. К концу острого периода легкого и среднетяжелого ишемического инсульта в каротидном бассейне когнитивные нарушения выявляются у 77% больных, а к концу раннего восстановительного — у 48% больных, при этом деменция выявляется соответственно у 15% и 8% больных.
2. На развитие постинсультных когнитивных нарушений влияет локализация очага поражения, выраженность сопутствующих микроваскулярных изменений головного мозга (распространенность лейкоареоза, численность лакунарных очагов), степень выраженности церебральной атрофии (по данным КТ и МРТ ), наличие артериальной гипертензии, сердечной недостаточности, возраст больных.
3. В раннем восстановительном периоде клинически значимое улучшение когнитивных функций наблюдается у 41% пациентов, причем более быстрое восстановление наблюдается в первые 3 месяца; если в первые 3 месяца после инсульта улучшались все группы когнитивных функций, то в последующие 3 месяца только нейродинамические и регуляторные функции.
4. Постинсультные когнитивные нарушения являются предиктором неблагоприятного функционального исхода ишемического инсульта и негативно влияют на повседневную активность и качество жизни больных.
5. Аффективные расстройства в виде депрессивной симптоматики и апатии выявляются у большинства больных, перенесших легкий и среднетяжелый ишемический инсульт; выраженность аффективных расстройств негативно коррелирует со степенью когнитивной дисфункции, качеством жизни больных и функциональным исходом заболевания; симптомы апатии были более тесно связаны с когнитивными нарушениями, чем симптомы депрессии.
6. Динамика общей выраженности когнитивных нарушений у пациентов с ишемическим инсультом в каротидном бассейне преимущественно зависит от исходной выраженности когнитивных нарушений, преимущественно зрительно-пространственных и мнестических, но не зависит от подтипа инсульта, оценки по шкале инсульта в остром периоде, выраженности аффективных расстройств.
7. Мемантин улучшает качество жизни пациентов с постинсультными когнитивными нарушениями, уменьшая выраженность нейродинамических, регуляторных и операциональных когнитивных нарушений, а также уменьшая выраженность аффективных расстройств.