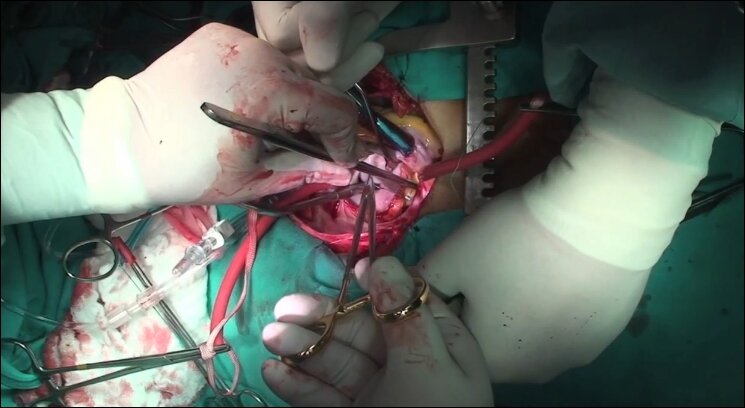
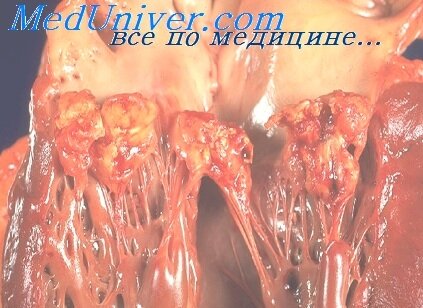
Инфекционный эндокардит
Эпидемиология и этиология инфекционного эндокардита. Симптомы поражения клапанов сердца. Клиническая картина инфекционного эндокардита. Бактериологическое исследование крови. Рабочая классификация инфекционного эндокардита. Его диагностика и лечение.
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже.
Подобные документы
Клинические проявления и диагностика инфекционного эндокардита. Локальное распространение инфекции. Особые формы инфекционного эндокардита, его рабочая классификация по происхождению и течению. Показания к хирургическому лечению инфекционного эндокардита.
презентация [2,4 M], добавлен 26.02.2015
Особенности течения инфекционного эндокардита. Основные патогенетические факторы. Особые формы инфекционного эндокардита, его рабочая классификация по происхождению и течению. Большие и малые критерии заболевания, особое место тейкопланина в его лечении.
реферат [48,5 K], добавлен 22.12.2010
Эндокардит — воспаление соединительнотканной (внутренней) оболочки сердца. Этиологические факторы, формы инфекционного эндокардита, классификация его видов по клиническому течению. Симптомы и осложнения ИЭ. Причины, классификация и диагностика миокардита.
презентация [8,4 M], добавлен 20.02.2014
Сущность, основные симптомы и этиология инфекционного эндокардита. Общая схема патогенеза заболевания. Признаки стеноза устья аорты. Понятие аортальной недостаточности, компенсаторные механизмы. Периферические симптомы недостаточности клапанов аорты.
презентация [587,7 K], добавлен 06.02.2014
Особенности стрептококковых и стафилококковых эндокардитов. Развитие перикардита, менингита, артрита, остеомиелита и других гнойных процессов. Основной критерий постановки диагноза, лечение, профилактика. Осложнения инфекционного эндокардита у детей.
презентация [89,9 K], добавлен 25.01.2013
Характеристика этиологии и патогенеза эндокардита, который представляет собой воспалительное заболевание эндокарда. Особенности ревматического и септического эндокардита. Лечение и профилактика миокардита — воспалительного заболевания сердечной мышцы.
реферат [34,2 K], добавлен 09.09.2010
Особенности понятия и классификация инфекционного эндокардита. Основные формы проявления заболевания и причины его рецидива. Диагностические критерии duke university. Основные принципы антибактериальной, эмпирической и противовоспалительной терапии.
реферат [22,5 K], добавлен 21.12.2008
Повышение температуры тела под влиянием болезни. Лихорадка как наиболее постоянный признак бактериального эндокардита. Признаки инфекционного эндокардита. Лимфаденопатия шейных лимфоузлов. Диагноз поддиафрагмального абсцесса. Холангит и абсцесс печени.
презентация [484,1 K], добавлен 09.03.2014
Этиология и патогенез инфекционного мононуклеоза, классификация форм по степени тяжести. Причины возникновения заболевания и характеристика возбудителя. Взаимодействия между вирусом и макроорганизмом. Диагностика и лечение инфекционного мононуклеоза.
презентация [1,4 M], добавлен 04.10.2014
Определение, эпидемиология, диагностика, клиника, дифдиагностика и этиология бактериального эндокардита. Его патогенез, факторы риска и патоморфология. Рекомендации по лечению больных с бактериальным эндокардитом. Нестрептококковая этиология заболевания.
презентация [2,4 M], добавлен 31.10.2013
Современный взгляд на рекомендации по антибиотикопрофилактике инфекционного эндокардита
Несмотря на то, что в настоящее время подробно изучен патогенез всех типов инфекционного эндокардита (ИЭ), включая острый (ОИЭ) и подострый инфекционный эндокардит (ПИЭ), многие врачи не имеют четких представлений об использовании антибиотиков для профилактики ИЭ. Очень часто пренебрегаются фундаментальные принципы первичной антибиотикопрофилактики, несмотря на то, что рекомендации по её проведению разрабатывались на протяжении последних 45 лет. Первые из них были предложены еще в 1955 году для предупреждения ревматической лихорадки.
Затем были многочисленные протоколы антибиотикопрофилактики ИЭ, включая известные рекомендации Европейского Консенсуса, Медицинские Письма и, наконец, руководства Американской Ассоциации Больничных Учреждений (American Hospital Association, АНА). Руководства постоянно пересматривались и совершенствовались, для того чтобы сделать их наиболее пригодными для рутинного использования.
Например, в настоящих рекомендациях АНА (1997), представляющих собой редактированную версию 1990 года, отказались от парентерального пути ведения антибиотиков за исключением пациентов группы высокого риска, которым будут проводиться лечебные или диагностические манипуляции на мочеполовых путях или желудочно-кишечном тракте [1].
Подавляющее большинство инфекционных эндокардитов развивается вторично в результате бактериемий, спонтанно возникающих в процессе повседневной активности (чистка зубов, кишечная перистальтика и др.). Однако любые манипуляции, нарушающие целостность слизистых оболочек, колонизированных микроорганизмами, могут приводить к бактериемии.
Стоматологические вмешательства, мини-аборты и тонзиллэктомии, в числе других рутинных медицинских манипуляций могут вызывать бактериемии. Таким образом, проведение антибиотикопрофилактики при ряде лечебно-диагностических процедур является обязательным, однако, к сожалению, многие врачи либо не понимают её значения либо не имеют мотивации для её проведения. В 1992 году было проведено исследование среди стоматологов Израиля, показавшее, что только 58% использовали приемлемые схемы антибиотикопрофилактики инфекционного эндокардита [2].
Более того, только 50% из тех, кто знал, какие антибиотики следует использовать, имели правильное представление о режиме их назначения. Около 29% знали, какие заболевания сердечно-сосудистой системы относятся к категории высокого риска развития ИЭ, и поэтому требуют проведения профилактики (таблица 1). В то же время о необходимости антибиотикопрофилактики при определённых стоматологических процедурах были осведомлены 64% врачей.
Необходимость профилактики инфекционного эндокардита
Экспериментальные модели инфекционного эндокардита позволили получить более чёткое представление о действии антибиотиков. Было показано, что их основной профилактический эффект заключается в подавлении бактериального роста на приклапанных тромбах, что помогает иммунной системе осуществлять свою защитную функцию. Антимикробные препараты, назначенные в течение 2 часов после процедуры, сопровождающейся бактериемией, могут успешно предупреждать развитие инфекции. На это указывают и то, что добавление пенициллиназы в эксперименте после исходного инфицирования тромба блокирует профилактическое действие ампициллина [3].
При лечении инфекционного эндокардита назначение антибиотиков позволяет достигнуть стерилизации вегетаций в более чем 90% случаев при ПИЭ и в 70% при ОИЭ. Тем не менее, у 15-25% пациентов, в конце концов, возникает необходимость в хирургической коррекции повреждённых клапанов сердца. Эти цифры значительно выше (70%) при ИЭ у пациентов с искусственными клапанами сердца. Помимо этого, необходимо помнить об угрозе нарастания ИЭ, вызванных энтерококками, устойчивыми к антибиотикам, и метициллинорезистентыми S. aureus (MRSA). Очевидно, что гораздо легче предупредить развитие инфекции эндокарда, чем иметь дело с ранними и поздними осложнениями инфекционного эндокардита.
Осознание пользы антибиотикопрофилактики является исключительно важным, особенно в связи с ростом частоты ОИЭ [4]. При этом типе ИЭ часто страдают пациенты, не имеющие предшествующих заболеваний сердца, поэтому им, зачастую, не проводится антибиотикопрофилактика. В настоящее время только 15-25% случаев ИЭ возникают вторично, после проведения инвазивных процедур. Лишь у 50% этих пациентов в анамнезе имеются указания на изменения со стороны клапанов сердца, что могло бы служить основанием для назначения антибиотиков с профилактической целью. Таким образом, при соблюдении современных рекомендаций можно предупредить только 10% ИЭ.
Возбудители инфекционного эндокардита могут широко варьировать, в зависимости от типа ИЭ. В целом, наиболее частым возбудителем является Staphylococcus aureus. В 50% случаев ПИЭ вызывается зеленящими стрептококками, более того, они занимают лидирующее место среди возбудителей ИЭ, возникающих после манипуляций в ротовой полости, дыхательных путях или пищеводе. Препаратом выбора для профилактики в этих случаях является амоксициллин. Ему отдаётся предпочтение по сравнению с феноксиметилпенициллином, учитывая лучшую абсорбцию в желудке и кишечнике. В соответствии с руководством АНА (1990), рекомендуемая доза амоксициллина для приема внутрь составляла 3 г за 1 час перед проведением инвазивного вмешательства и 1,5 г через 6 часов после первого приёма.
Позднее схема была упрощена до однократного приема 2 г антибиотика за 1 час до манипуляции. Несмотря на то, что эта доза обеспечивает сывороточную концентрацию, достаточную для предупреждения инфекции, степень всасывания амоксициллина может значительно варьировать у различных пациентов. В связи с этим, по-видимому, целесообразно вернуться к прежним рекомендациям.
У 5-10% населения имеются признаки пролапса митрального клапана (ПМК) – состояние, которое иногда является основанием для профилактического назначения антибиотиков. Несмотря на то, что в целом пациенты с ПМК не относятся к группе повышенного риска, ИЭ развивается у них в 5-10 раз чаще, чем в общей популяции. Пациенты, страдающие ПМК с регургитацией [5], нуждаются в проведении антибиотикопрофилактики. У 3% пациентов с регургитацией и/или утолщением передней створки митрального клапана в конечном итоге развивается инфекционный эндокардит.
В отделениях интенсивной терапии используются различные мониторирующие и терапевтические устройства (катетеры, эндотрахеальные трубки, катетеры для парентерального питания), которые нарушают целостность естественных защитных барьеров и могут приводить к инфицированию крови. Например, при применении катетеров бактериемия наблюдается в 4-14% случаев [6], что соответствует 120000 случаев госпитальных бактериемий в год.
Центральные катетеры являются причиной 30-90% инфекции крови в отделениях интенсивной терапии. Риск развития инфекции значительно повышается при использовании этих устройств в течение более 4 дней подряд. До 45% всех катетер-ассоциированных бактериемий наблюдается у пациентов с искусственными клапанами сердца, из них 15% пациентов инфицируются во время поступления бактерий в кровь.
Профилактические режимы
В связи с тем, что при использовании клиндамицина часто развивается псевдомембранозный колит (до 10% пациентов), целесообразно ограничить его применение с профилактической целью. Новые макролиды, азитромицин и кларитромицин, являются более дорогостоящими антибиотиками, чем эритромицин, и не имеют преимуществ по переносимости у многих пациентов. Достоинством макролидов является низкая частота развития тяжёлых аллергических реакций.
Это имеет особенно большое значение в случаях, когда не совсем ясна степень риска развития инфекционного эндокардита. По данным одного исследования, у пациентов с ПМК при внутривенном введении пенициллина наблюдался один случай фатальной анафилактической реакции на каждые 2-3 случая предупрежденных ИЭ [7]. Это, вероятно, и послужило основанием предложить эритромицин в качестве антибиотика выбора для профилактики ИЭ у больных с ПМК [8].
У пациентов с искусственными клапанами сердца для профилактики ИЭ антимикробные препараты назначаются внутрь. Однако, учитывая тяжёлые последствия ИЭ, развивающихся на искусственных клапанах, необходимо подумать о внутривенном введении антибиотика для достижения более предсказуемых концентраций. В качестве альтернативных режимов могут быть использованы новые макролиды и современные фторхинолоны (например, левофлоксацин и тровафлоксацин*). Однако, несмотря на их стабильное всасывание в ЖКТ, их эффективность при антибиотикопрофилактике остается не доказанной.
Как правило, инвазивные процедуры на сосудах (например, замена стентов) не требуют назначения антибиотиков. Манипуляции или хирургические вмешательства, проводимые в условиях правильной подготовки кожных покровов, не нуждаются в профилактическом назначении антибиотиков. Более того, имеются весьма ограниченные данные в поддержку эффективности антибиотикопрофилактики и при операциях на ротовой полости.
По данным одного исследования эффективность профилактики достигала 91% [9], тогда как в двух других исследованиях эффект был минимальным [10] или полностью отсутствовал [11]. Для того, что бы достоверно доказать эффективность антибиотикопрофилактики, в большинстве случаев в исследование необходимо включить чрезвычайно большое количество пациентов. Поэтому, подобные работы легче проводить у пациентов, относящихся к группе высокого риска [12].
Важно отметить, что ни один из предложенных режимов антибиотикопрофилактики не обладает активностью в отношении S. epidermidis, который является одним из основных возбудителей инфекционного эндокардита у пациентов с искусственными клапанами сердца [13] и практически всегда заносится во время имплантации клапана. По-видимому, даже ИЭ, развившиеся через один год после операции, обусловлены замедленным клиническим проявлением инфекции, которая началась ещё в операционной.
Однако особое внимание должно быть уделено пациентам, получающим антибиотики для предупреждения других инфекций, например, пенициллин для профилактики ревматической лихорадки. Около 15% зеленящих стрептококков, обитающих в ротовой полости у таких пациентов, являются промежуточно-резистентными или резистентными к пенициллину. При этом увеличения дозы пенициллина с целью профилактики ИЭ во время проведения инвазивных процедур не требуется. Чувствительность микрофлоры полости рта вернется к нормальному состоянию на 9-14 день после отмены пенициллина, хотя прерывание антибиотикопрофилактики на такой промежуток времени может быть неприемлемым для многих пациентов.
Следует помнить, что пенициллинорезистентные штаммы зеленящих стрептококков не намного более чувствительны к цефалоспоринам, поэтому могут быть использованы клиндамицин, эритромицин или кларитромицин. Кроме того, учитывая опасность развития псевдомембранозного колита при использовании клиндамицина, его не следует рассматривать в качестве подходящего антибиотика для антибиотикопрофилактики [14].
Неотъемлемыми факторами для достижения успеха при проведении антибиотикопрофилактики являются образовательные программы для пациентов и повышение их комплаентности. Неэффективность профилактики связывают с отсутствием у пациентов необходимых знаний [15]. По данным одного исследования, 78% пациентов получили необходимые инструкции, но только 20% из них могли воспроизвести ту или иную информацию об особенностях профилактики [16]. Эти цифры свидетельствуют о том, что необходимо расширять нефармакологические подходы к профилактике инфекционного эндокардита.
Например, основной путь для снижения частоты нозокомиальных бактериемий заключается в соблюдении строжайших правил стерильности во время установки и уходя за внутрисосудистыми катетерами. Соблюдение этих мер может способствовать значительному уменьшению нозокомиальных инфекций кровеносного русла и, следовательно, нозокомиальных ИЭ. Определенный эффект был отмечен при использовании катетеров, импрегнированных различными антисептическими веществами [17]. Простое полоскание рта антисептиком перед удалением зуба также может значительно снизить риск развития бактериемии.
Учитывая постоянное совершенствование устоявшихся и внедрение новых профилактических мероприятий, постоянное обновление руководств по антибиотикопрофилактике представляет сложную задачу. Поэтому практический опыт, зачастую, образует ту основу, на основе которой принимаются решения. Выбор профилактического антибиотика зависит от особенностей пациента, включая наличие осложнённого аллергологического анамнеза, состояния функции почек и возраста.
Каждый пациент должен рассматриваться комплексно, а не только с точки зрения наличия у него патологии сердца. И, несмотря на наличие новых классов антибиотиков, которые могут быть использованы для профилактики, в условиях роста резистентности следует, в первую очередь, ограничить применение именно этих многообещающих препаратов для сохранения их в нашем арсенале.
Источник информации:http://www. pharmacoepidemiology. ru
Статья опубликована на сайтеhttp://www. medolina. ru
Цель лекции — дать представление об этиологии, патогенезе, клинике, диагностике и лечении инфекционного эндокардита.
Задачи лекции. Раскрыть этиологию и патогенез инфекционного эндокардита. Дать понятие о значении реактивности организма и особенностей возбудителя в возникновении инфекционного эндокардита, описать факторы способствующие заболеванию. Раскрыть особенности острого и затяжного септического эндокардита. Охарактеризовать клинические проявления заболевания: варианты начала болезни, температурная кривая, поражение сердца и других органов (почек, печени и селезенки, кожи и др.). Показать возможности лабораторной диагностики заболевания. Осветить основные подходы к терапии инфекционного эндокардита. выбор антибиотиков, необходимость применения больших доз, длительности терапии, показания к хирургическому лечению
Определение
Инфекционный эндокардит (ИЭ) — это инфекционное заболевание, протекающее по типу сепсиса и поражающее клапанный аппарат сердца. Болеют преимущественно мужчины (в 70% случаев) среднего возраста.
Этиология и патогенез
Наиболее часто этиологической причиной (40-70% случаев) развития ИЭ является зеленящий стрептококк. Второе место занимают стафилококки (15% случаев). Несколько реже ИЭ вызывают энтерококки, пневмококки, кишечная палочка, протей, грибы (особенно кандиды и аспергиллы). Всего около 70 различных видов микроорганизмов могут явиться причиной инфекционного эндокардита.
Основным предрасполагающим фактором для развития ИЭ является изменение клапанного аппарата: пороки сердца, коарктация аорты, дефект межжелудочковой перегородки, синдром Марфана, наличие искусственного клапана сердца, пролапс митрального клапана. Однако иногда микроорганизмы, обладающие высокой вирулентностью, могут поражать клапаны сердца и у здоровых людей. Инфекционный процесс чаще захватывает левые отделы сердца. По частоте поражения инфекционным эндокардитом клапаны располагаются следующим образом: митральный клапан, клапан аорты, трикуспидальный клапан и клапан легочного ствола. Обязательным условием развития ИЭ является наличие бактерий в крови — бактериемия. Бактериемия зеленящим стрептококком может наблюдаться после стоматологических процедур, экстракции зуба, тонзилэктомии, особенно если сразу после проведения этих манипуляций больные начинают принимать пищу. Энтерококковая бактериемия и бактериемия, связанная с грамотрицательными бактериями, может быть результатом манипуляций на мочеполовом тракте, например при катетеризации мочевого пузыря или цистоскопии, урогенитальных операциях. Стафилококки проникают в кровь преимущественно при инфицировании внутривенных катетеров, при экстракции зубов, инфекции дыхательных и мочеполовых путей, установлению электрокардиостимулятора и т.д. Пневмококки являются достаточно редким возбудителем ИЭ и встречаются преимущественно при пневмококковой пневмонии и алкоголизме. Грибы попадают в организм обычно при выполнении внутривенных инъекций у наркоманов, а также при заражении шовного материала и искусственного клапана при операциях на сердце.
Однако наличие микробов в крови еще не достаточно чтобы вызвать заболевание. У практически здоровых людей тоже иногда встречается преходящая бактериемия. Для того, чтобы микробы проявили патогенное действие и произошла активация инфекции необходимо значительное изменение иммунитета, поэтому возникновение ИЭ способствуют различные факторы снижающие реактивность организма: болезни, интоксикации, переутомление, операции, беременность, роды, аборты и т.д. Циркулирующие в крови бактерии могут прикрепляться к эндокарду, особенно в измененных его участках. Нарушение кровотока возле пораженных клапанов способствует образованию тромботических наложений, которые становятся очагом осаждения микроорганизмов. Микроорганизмы прикрепляются к эндотелию, после чего они покрываются наложениями фибрина, образуя, так называемую, вегетацию. Поступление питательных веществ внутрь вегетации прекращается, и микроорганизмы переходят в статическую фазу роста. При этом они становятся менее чувствительными к действию антибиотиков, механизм действия которых заключается в ингибировании роста клеточной оболочки. Высоко патогенные микроорганизмы быстро вызывают деструкцию клапанов и их изъязвление, приводящих к развитию недостаточности клапанного аппарата. Вовлечение в процесс сухожильных хорд приводит к их разрыву и появлению острой недостаточности клапанов.
Рыхлые фибриновые вегетации могут отрываться от клапана и попадать в кровоток, вызывая эмболию. Если такой эмбол исходит из правых отделов сердца, то возникает тромбоэмболия ветвей легочной артерии. Если эмбол образовался в левых отделах сердца, то наблюдается эмболия сосудов головного мозга, селезенки, почек, желудочно-кишечного тракта, конечностей. Для грибкового эндокардита характерны эмболы большого размера, которые могут закупоривать просвет крупных сосудов. Одновременно с развитием эмболий могут развиваться метастатические абсцессы.
Длительное течение инфекционного эндокардита приводит к активации иммунной системы и созданию высокого титра антител к возбудителям. В крови появляются циркулирующие комплексы антиген-антитело, которые приводят к развитию гломерулонефрита, кожного васкулита.
Клиника.
Различают острое, подострое и хроническое течение болезни, а также первичный ИЭ — возникающий на неизмененных клапанах сердца, и вторичный — развивающийся на измененных клапанах.
Начало и течение болезни зависит от вирулентности микробов возбудителей и реактивности макроорганизма. Болезнь может начинаться остро, с ознобом, профузным холодным потом, высокой лихорадкой, тяжелой интоксикацией и внезапным развитием эмболий (чаще сосудов головного мозга и сетчатки глаза). Такое начало наиболее характерно для первичного инфекционного эндокардита.
Медленное постепенное развитие заболевания отмечается при его вторичной форме. В таких случаях ранние признаки болезни весьма разнообразны и малоспецифичны: недомогание, усталость, слабость, потеря аппетита, снижение массы тела, головная боль, потливость, субфебрильная температура, снижение трудоспособности. Такие больные в течение первых месяцев заболевания продолжают работать. Периодически у них улучшается самочувствие, однако, через некоторое время вновь проявление болезни обостряется.
Примерно у 30% больных заболевание развивается через 2-3 недели после перенесенной ангины, пневмонии, гнойного отита, гайморита, удаления зубов, цистоскопии, мочеполовых инфекций, абортов или родов. Такое начало часто развивается при ИЭ, вызванном зеленящим стрептококком.
Первыми признаками болезни могут быть и геморрагические явления в виде петехий, кровотечений (носовых, желудочных, маточных), некротической сыпи. Достаточно редко (в 6-7% случаев) болезнь начинается с отеков, как проявления нефрита.
Начало болезни с развития сердечной недостаточности (сердцебиение, одышка) встречается в среднем в 10% случаев, как правило, у больных при вторичном ИЭ, и является плохим прогностическим симптомом. Еще реже болезнь начинается с поясничных болей и гематуриии (при инфарктах почек), болей в левом подреберье (при инфаркте селезенки), в животе (при эмболии брыжеечных сосудов), в икроножных мышцах и пальцах рук и ног (эмболии периферический сосудов), суставах.
Течение ИЭ может быть различным. При высоко вирулентном возбудителе или при отсутствии адекватного лечения болезнь быстро развивается, и смерть наступает в течение 1-2 месяцев в результате тяжелой сердечной недостаточности, поражения почек, или окклюзии сосудов головного мозга. Острое течение ИЭ встречается не часто.
При маловирулентном возбудителе болезнь развивается медленнее, с развертыванием классической клинической картины. Если лечение неэффективно, то смерть наступает в течение 1-2 года после начала болезни от сердечной или почечной недостаточности, геморрагических или эмболических осложнений. Такое течение называется подострым и встречается в большинстве случаев ИЭ.
Возможен также переход болезни в хроническое течение с периодами ремиссии и рецидивов. Под влиянием современной антибактериальной терапии клиническая картина нередко бывает стертой, не развернутой, со слабыми проявлениями основных симптомов болезни.
Одним из важнейших признаков болезни является лихорадка (встречается в 90-95% случаев). Не редко наблюдаются 2х-3х недельные лихорадочные волны до 38-390 С, чередующиеся с одно-двух недельными периодами нормальной температуры или субфибрилитета. На фоне субфибрилитета могут развиваться одно-двух дневные подъемы температуры до 39-400С. Такие свечи считаются весьма характерными для затяжного септического эндокардита. Лихорадка может быть постоянной, ремитирующего, интермитирующего, гектического, а также инвертированного характера. Иногда наибольшее повышение температуры тела выявляется в необычные для измерения часы: 12-14-24 часа, в то время как утренние и вечерние часы она остается нормальная. Сопутствующая лихорадке головная боль обычно умеренная и усиливается, как и общая слабость, при повышении температуры тела.
Лихорадка может быть вызвана не только инфекционным процессом, но и возникать в результате рассасывания некротических тканей при инфаркте селезенки, почек, легких и т.д. Лихорадка может быть обусловлена также развитием абсцессов селезенки, печени, легких, в мозге и т.д. Иногда лихорадка обусловлена аутоиммунными процессами и снижается только под влиянием кортикостероидов и иммунодепрессантов.
Лихорадка может отсутствовать при тяжелой сердечной недостаточности, поражении почек, уремии, у лиц пожилого возраста и при введении антимикробных средств. Отсутствие снижения температуры в ходе лечения, обычно указывает на неадекватность терапии и побуждает к пересмотру диагноза или этиологического фактора лихорадки.
Озноб — частый и важный, но не постоянный признак ИЭ. Озноб может быть выражен не резко (познабливание), а иногда принимает потрясающий характер, сопровождаясь высоким подъемом температуры с последующим обильным потоотделением и падением температуры тела. Потоотделение не облегчает состояние больного, бывает профузным или же испариной покрываются только отдельные участки тела (голова, лоб, верхняя половина туловища и т.д.).
Кожа у больных бледная, бледновато-серая или желтовато-землистого цвета со своеобразным оттенком “кофе с молоком”. Слизистые оболочки бледные. Бледность кожи и слизистых объясняется анемией. Легкая желтушность может быть связано с повышенным гемолизом эритроцитов. Иногда встречается выраженная желтуха вследствие инфекционно-токсического гепатита. Одутловатость лица и отеки могут быть сердечного, почечного и дистрофического происхождения.
У 20-40% не леченных больных выявляются коротко живущие петехиальные высыпания, которые локализуются на конъюнктиве, твердом и мягком небе, шее, груди, предплечьях, кистях и ногах. Эти плоские красные элементы диаметром 1-2мм, обычно с центром серого или белого цвета бледнеют через 3-4 дня и исчезают.
Иногда может возникать интенсивная геморрагическая сыпь, которая характеризуется волнообразностью высыпаний и симметричностью расположения. Чаще она локализуется на нижних и верхних конечностях, но может быть на лице и других участках тела, а также на слизистых оболочках. Геморрагии могут приобретать некротический характер, оставляя после себя рубцы. При расположении геморрагии на лице они напоминают натуральную оспу. Геморрагическая сыпь может быть также следствием осложнения болезни, например уремии. Изредка у больных под ногтями появляются красновато-коричневые кровоизлияния в виде полосок.
В ряде случаев выявляются пятна Джейнуэя и узелки Ослера. Пятна Джейнуэя — это макулярные или папулезные эритематозные пятна или безболезненные кровоподтеки диаметром 1-5мм, появляющиеся на ладонях, подошвах, и усиливающиеся при подъеме конечностей. Пятна Джейнуэя более характерны для остро протекающего инфекционного эндокардита, вызванного высоко вирулентным возбудителем.
Узелки Ослера — красноватые узелкообразные кожные проявления диаметром до 1,5см, болезненные при сдавлении. Узелки Ослера проявляются наиболее часто на ладонях, пальцах, подошвах и под ногтями. Обычно эти узелки исчезают бесследно через несколько дней или несколько часов, но иногда происходит их некроз и нагноение. Узелки Ослера патогномоничны для классического затяжного инфекционного эндокардита, но появляются не часто (в 10% случаев).
Боли в суставах встречаются у 20% больных и иногда сопровождаются опуханием суставов. Чаще поражаются крупные суставы, но могут поражаться мелкие суставы стоп и кистей.
У 10-40% больных развивается утолщение концевых фаланг пальцев в виде барабанных палочек.
Боли в костях бывают достаточно часто. При этом имеется болезненность грудины, крестца, бедренной кости, голени. Эти боли возникают в результате периоститов, кровоизлияний в сосуды надкостницы. При успешном лечении, боли в костях уменьшаются или исчезают, если процесс затронул только мягкие ткани. При поражении надкостницы и кости боли иногда остаются, несмотря на выздоровление.
Сердцебиение и болевые ощущения в области сердца в начале заболевания обычно отсутствуют, позднее они появляются почти у всех больных. Боли в области сердца по интенсивности, длительности, локализации и характеру отличаются большим разнообразием: острые, тупые, приступообразные, кратковременные, длительные, колющие, ноющие, давящие, сжимающие и т.д. Патогенез болей связан с ишемией, возникающей на фоне гипертрофии миокарда и анемии, а также развивающейся вследствие тромбоэмболии или артериита коронарных сосудов. Болевые ощущения в области сердца могут быть и проявление миокардита — почти постоянного спутника ИЭ. При вторичном инфекционном эндокардите удается обнаружить изменения в характере и локализации сердечных шумов. Меняется их длительность, тембр и сила. Шумы становятся более интенсивными за счет изменений клапанного аппарата и развития анемии. Тоны сердца становятся глухими, часто ослабляется, а затем исчезает II тон на аорте в связи с недостаточностью ее клапанов.
На фоне старых шумов могут появиться новые шумы. Наиболее часто формируется диастолический шум на аорте, как результат формирующийся недостаточности аортальных клапанов. Не редко внезапно появляются своеобразные шумы, так называемый “птичий писк”, которые обусловлены перфорации створок клапанов, межжелудочковой перегородка, разрывом папиллярной мышцы. При первичном ИЭ, особенно острого течения сердечный шум отсутствует у 30% больных. Лишь позднее, спустя несколько недель или месяцев появляются признаки поражения клапанов сердца. Иногда шум в сердце вообще не выслушивается. В таких случаях надо подозревать наличие эндокардита правого сердца.
Осложнения.
Под влиянием терапии усиливаются отложения фибрина и коллагена на створках клапанов с последующей кальцификацией повреждений. В дальнейшем происходит рубцевание и деформация клапанов с формированием пороков сердца. Весь этот процесс занимает 2-3 месяца.
Миокардит почти всегда сопутствует развитию ИЭ. Для него характерны сердцебиение, глухость сердечных тонов и ослабление сердечных шумов, частое развитие сердечной недостаточности. а также различные тяжелые нарушения ритма и проводимости. Электрокардиографически выявляются экстрасистолия, пароксизмальная тахикардия, мерцательная аритмия и АВ-блокада вплоть до развития синдрома Адамса-Стокса-Морганьи. Характерно снижение вольтажа и смещение интервала S-Т.
Поражение перикарда в виде перикардита встречаются у 10 % больных, и, как правило, являются осложнением уремии или инфаркта миокарда.
Сердечная недостаточность является частым и серьезным осложнением ИЭ. Она редко развивается в начале заболевания, однако в дальнейшем появляется почти у всех больных. Начинается она с симптомов характерных для левожелудочковой недостаточности: тахикардии, одышки, приступов сердечной астмы, ритма галопа. Позднее присоединяется и правожелудочковая недостаточность. Развивается тотальная недостаточность сердца. Сердечная недостаточность связана с деструкцией клапанов сердца, миокардитом, а также абсцедированием миокарда и развитием инфаркта. Эта сердечная недостаточность характеризуется тяжелым течением, отсутствием эффекта от сердечных гликозидов и является причиной смерти даже в тех случаях, когда инфекция устранена.
Клапанные вегетации легко разрушаются, образуя при этом множественные эмболы, которые приводят к развитию инфарктов различных органов, чаще всего развивается инфаркт почек, легких, мозга, селезенки, сердца. Возможна тромбоэмболия периферических сосудов и сосудов кишечника. Основным симптомом закупорки сосудов является внезапная резкая боль в пораженном органе, обусловленная ишемией. Боль сопровождается более или менее выраженной коллаптоидной реакцией, подъемом температуры, лейкоцитозом, увеличением СОЭ и естественно нарушением функции органов. Поражение мелких сосудов и скрытую наклонность к геморрагиям можно выявить симптом Кончаловского-Румпеля-Лееде. Он заключается в том, что при сдавливании плеча жгутом или манжетой тонометра, на сгибательной поверхности локтя и дистальнее появляются множественные петехии. Хрупкость капилляров можно обнаружить и при помощи мягкой травмы кожи — синдром “щипка”.
Поражение почек при ИЭ проявляется в виде инфарктов, очагового и диффузного нефритов и почечной недостаточности.
Инфаркт почек диагностируется по приступу резкой или тупой боли в области поясницы с положительным симптомом Пастернацкого. Одновременно отмечается макро- и микрогематурия, протеинурия, преходящая артериальная гипертензия, повышение температуры тела. Указанные симптомы обычно исчезают в течение нескольких дней.
Очаговый нефрит проявляется изолированным мочевым синдромом: микрогематурией, альбуминурией, цилиндурией. При этом повышение артериального давления, отеков и развития почечной недостаточности не наблюдаются.
Диффузный гломерулонефрит — является частым осложнением ИЭ и существенно влияет на течение и прогноз заболевания. Характеризуется формированием почечных отеков, почечной недостаточности и артериальной гипертензии. При этом следует учитывать, что поскольку диастолическое давление у больных ИЭ за счет недостаточности аортальных клапанов обычно низкое (10-15 мм рт.ст.), то его повышение до цифр — 60-80 мм рт.ст, а тем более выше, может указывать на развитие диффузного нефрита.
При ИЭ центральная нервная система поражается часто (у 30-50% больных). Клинически это проявляется головной болью, головокружением, бессонницей, слабостью, апатией, вялостью. Может отмечаться своеобразная эйфория, менингиальные симптомы, бред, сонливость, нарушение зрения, диплопия, слюнотечение, паралич глазных мышц, маскообразное лицо, мышечное подергивание. Мозговые эмболии отмечаются у 30 % больных ИЭ. Стерильные эмболы вызывают инфаркт и кровоизлияние, а инфицированные — менингит, энцефалит, абсцесс мозга.
Признаки мозговых поражений могут быть как первыми симптомами заболевания, так и более поздними, проявляющиеся через месяцы и годы. Признаки поражения ЦНС у больных лихорадкой или сердечным шумом должны наводить на мысль о возможности инфекционного эндокардита.
Поражение селезенки при ИЭ заключается в ее гиперплазии и множественных инфарктах за счет эмболии тромбозов. Спленомегалия в настоящее время встречается у 30-40% больных. При остром течении ИЭ селезенка прощупывается не отчетливо, она мягкой консистенции и увеличена не резко. При хроническом течении селезенка в начале умеренно увеличена, при пальпации определяется плотноватый слегка болезненный край. С течением времени селезенка увеличивается более значительно, не редко до выраженной спленомегалии, и становится плотной, безболезненной.
При раннем и успешном лечении антибиотиками селезенка уменьшается и перестает пальпироваться. Наличие увеличенной селезенки указывает на малоэффективность лечения.
Инфаркты селезенки сопровождаются острыми внезапными болями в левом подреберье с иррадиацией в левое плечо и левую предсердную область. Одновременно отмечается рвота, озноб, повышение температуры, лейкоцитоз. При пальпации отмечается напряжение брюшной стенки и болезненность в левом подреберье. Имеется ограничение подвижности легкого слева. Иногда можно выслушать шум трения брюшины в области селезенки. Может развиваться реактивный плеврит. В течение 2х-3х дней описанная симптоматика, как правило, стихает, а затем постепенно исчезает.
ИЭ может приводить к формированию абсцессов селезенки. Такая инфицированная селезенка может быть причиной постоянной лихорадки и бактериемии.
Иногда первым проявлением ИЭ бывает разрыв селезенки. В таких случаях определение свободной крови или гноя в брюшной полости служит показанием для немедленного хирургического вмешательства.
Поражение печени при ИЭ связано с развитием сердечной недостаточности или инфекционно-токсического гепатита. Увеличение печени наблюдается примерно у 90% больных. Уже в ранней стадии болезни, одновременно с увеличением селезенки, определяется плотноватый, болезненный край печени, даже при отсутствии признаков застойной правожелудочковой сердечной недостаточности. Обычно эта гепатоспленомегалия протекает без выраженной желтухи и некроза печеночных клеток, но с признаками выраженной гипергаммаглобулинэмии.
У больных ИЭ иктеричность склер и кожных покровов встречается довольно часто. Билирубин сыворотки увеличен у 30% больных за счет главным образом свободного, но иногда и связанного билирубина. Лишь у незначительной части больных может развиться резкая желтуха с печеночной недостаточностью. Могут быть и другие осложнения абсцессы печени и тромбоэмболии.
Поражения желудочно-кишечного тракта при ИЭ связаны с развитием эмболий и застойных явлений. Больные часто жалуются на отсутствие аппетита, боли в животе, правом подреберье. Тошнота и рвота относятся обычно к поздним симптомам, зависящим от сердечной недостаточности, уремии или мозговых расстройств. Внезапные и резкие боли в животе наиболее часто вызываются инфарктами селезенки, почек, кишечника. При инфарктах кишечника отмечается понос с кровью. Диарея может быть обусловлена и уремией.
Поражение легких проявляется инфарктами, пневмониями и отеком при левожелудочковой сердечной недостаточности. Инфаркты легких характеризуются внезапной резкой болью в грудной клетке, ознобом, повышением температуры тела, коллаптоидной реакцией, с бледным цианозом, холодным потом, нитевидным пульсом. В легких можно выслушать влажные крепитирующие хрипы и шум трения плевры. К инфаркту может присоединиться пневмония.
Как осложнение ИЭ может развиться и поражение глаз. Наиболее тяжелым поражением глаз является окклюзия артерий сетчатки с внезапной полной или частичной потерей зрения. Этот признак бывает у 2-3% больных и может быть их первой жалобой.
Патогномоничным признаком ИЭ является симптом Лукина-Либмена. Этот симптом отмечается у 30-50% больных и заключается в появлении петехий с белым центром на конъюнктиве нижнего века, особенно на переходной складке. Давление на веко делает конъюнктиву бледной, отчего петехии выделяются контрастнее. Этот признак исчезает спустя несколько дней, но затем может опять появиться.
У 3-5% больных появляются, так называемые, пятна Рота на глазном дне. Это белые округлые пятнышки размером 1-2мм.
Бактериальный шок может осложнять течение ИЭ, вызванных преимущественно грамотрицательными бактериями: кишечной палочкой, клебсиеллой, протеем, энтеробактером, синегнойной палочкой и т.д. Причиной гемодинамических расстройств является эндотоксин, находящийся в оболочке микробов. Летальность при бактериальном шоке составляет 50-60%. Клинически бактериальный шок проявляется падением артериального давления, нарушением сознания, рвотой, диареей, мраморностью кожных покровов, появлением холодного цианоза и т.д.
Лабораторная диагностика.
ИЭ характеризуется поражением крови за счет угнетения деятельности костного мозга. Одним из наиболее характерных признаков является анемия. Обычно это анемия умеренная (Нb в пределах 80гр/л, эритроциты 3-4?106. ЦПК 0,7-0,8). У 15% больных анемия резко выражена — гемоглобин ниже 50 гр/л, эритоциты менее 2,5?106. С прогрессированием болезни анемия нарастает. При этом количество гемоглобина уменьшается быстрее чем количество эритроцитов, и ЦПК снижается (0,4-0,9), анемия приобретает гипохромный, железодефицитный характер.
При успешном лечении, быстро нарастает ретикулоцитоз, гемоглобин и число эритроцитов. С наступление выздоровления красная кровь обычно нормализуется.
Общее количество лейкоцитов чаще в норме и без особого изменения в формуле. У 30% больных отмечается умеренная лейкопения. У 25% больных имеется умеренный лейкоцитоз. Лишь в некоторых случаях лейкоцитоз более выражен ( от 12 до 20?103 ). По мере развития болезни количество эозинофилов уменьшается или они исчезают полностью, а при выздоровлении их количество увеличивается до 12-15%, а иногда и выше. У 15-20% больных выявляется моноцитоз. Количество тромбоцитов в большинстве случаев уменьшено.
Один из самых ранних и устойчивых показателей активности эндокардита является увеличение СОЭ. Обычно СОЭ резко увеличивается в пределах 40-60мм/час и выше. Под влиянием эффективного лечения СОЭ быстро снижается, что является дополнительным критерием правильного выбора терапии. Однако иногда эндокардит может протекать при незначительно повышенной или нормальной СОЭ, особенно в тех случаях, когда проводилось лечение антибиотиками. При врожденных пороках с полицитемией СОЭ может быть низкой (2-3 мм/час), несмотря на активный ИЭ. Развитие сердечной недостаточности также может снизить СОЭ до нормальных цифр. При устранении сердечной недостаточности СОЭ вновь увеличивается.
У 30% больных отмечается диспротеидемия — гиперглобулинемия. У половины больных находят значительные титры ревматоидного фактора. В 90% случаев положительными оказываются сулемоловая, типоловая и формоловая пробы. Бывает ложно положительная реакция Вассермана. Исследования культур крови в большинстве случаев дают положительные результаты. Для подтверждения бактериемии берут 3-5 проб крови по 20-30мл.
Эхокардиография позволяет выявить при ИЭ не только изменения внутрисердечной гемодинамики, определить поражение клапанов, но и выявить вегетации на клапанах, которые определяются как неравномерное утолщение его створок.
Лечение.
Для проведения эффективного лечения необходимо руководствоваться следующими основными принципами.
В лечении ИЭ используют исключительно препараты, обладающие бактерицидным действием.
Желательно в выборе препарата руководствоваться видом микроорганизма и его чувствительностью к антимикробным препаратам.
Терапия должна быть продолжительной: при стрептококковой этиологии не менее 4х недель, при стафилококковой — 6 недель, при грамотрицательных возбудителях — 8 недель.
При неустановленной этиологии химиотерапию проводят длительно (месяцами), методом проб и ошибок, подбирая эффективный антибиотик.
При нарастании признаков иммунного конфликта в форме гломерлонефрита, васкулита, миокардита, а также при проявлениях бактериального шока показано использование глюкокортикоидов.
При острых формах, вызываемых преимущественно стафилококками и граммотрицательными возбудителями целесообразно использование дезинтоксикационных средств.
При стрептококковой этиологии вводят бензилпеницилин 10 000 000 — 20 000 000 ед внутримышечно или внутривенно равными дозами каждые 4 часа (4 недели) с гентамицином (7-10 дней с интервалом в 7-10 дней) в дозе 3мг/1кг массы тела внутримышечно или внутривенно, равными дозами каждые 8-12 часов.
При стафилококковой этиологии — оксациллин 10-20 гр внутривенно, внутримышечно каждые 4-6 часов (4-6 недель) с гентамицином в дозе 3-5мг/1кг массы тела внутривенно. внутримышечно каждые 8-12 часов (7-10 дней с интервалом в 7-10 дней).
При энтерококковой этиологии бензилпеницилин 20 000 000 — 30 000 000 ед внутримышечно или внутривенно равными дозами каждые 4 часа (6 недели) со стрептомицином 1 гр внутримышечно равными дозами каждые 12 часов — 4 недели.
Лечение грибкового эндокардита — амфотерицин В 1,5 мг/кг внутривенно капельно 1 раз в сутки. Курс не менее 40-50 дней. Флуконазол назначают по 3-6 мг/кг внутривенно 1 раз в сутки.
При неустановленном возбудителе ИЭ лечение начинают и проводят, как при энтерококковом ИЭ, при отсутствии эффекта через 3-5 дней терапия осуществляется как при стафилококковом ИЭ.
В лечении ИЭ широко используется дезинтоксикационная терапия и экстракорпоральные методы очищения крови — плазмаферез и гемосорбция.
Для профилактики тромбоэмболических осложнений вводят дезагреганты — дипиридамол по 2-3 мг/кг, трентал — 600 мг/сут, аспирин -250 мг/кг.
При прогрессировании сердечной недостаточности, перфорации створок клапанов сердца и их отрыве, абсцессах миокарда, грибковом эндокардите, рецидивирующих тромбоэмболиях показано хирургическое лечение.