Синдром шаровидной верхушки — кардиомиопатия Takotsubo. Оценка риска при инфаркте миокарда
У некоторых пациентов с острым инфарктом миокарда стеноз КА при коронарной ангиографии отсутствует. У этих больных имеется типичный подъем сегмента ST на ЭКГ, а также повышенное содержание тропопина или мышечной фракции креатинфосфокиназы (КФК MIS). При ЭхоКГ отмечают типичные нарушения локальной сократимости; у этих больных могут развиваться такие же осложнения, как у пациентов с ИБС. Это можно наблюдать при следующих клинических ситуациях: спазм КА, субарахноидальное кровоизлияние, феохромоцитома, электроимпульсная терапия и синдром шаровидной верхушки. В процесс чаще всего вовлечен апикальный сегмент, появляется острая обструкция ВОЛЖ.
Синдром шаровидной верхушки изначально описали Satoh и соавт. как кардиомиопатию Takotsubo, или ампулу Takotsubo. Takotsubo — это устройство для ловли осьминогов с узким перешейком. ЛЖ очень напоминает это устройство своей шаровидной верхушкой и гипокинезией базальных сегментов. Исследования Mayo Clinic обнаружили следующие интересные факты, связанные с этим синдромом: (а) все больные были женского пола в периоде постменопаузы (средний возраст 71 год); (б) тропонин Т и КФК МБ были умеренно повышены, несмотря па акипезию/дискинезию верхушки с начальной ФВ ЛЖ в 39,5%, которая возвращалась к норме в течение нескольких дней; (в) у большинства больных был подъем сегмента ST, у некоторых развилась обструкция ВОЛЖ; (г) большинство больных находились в состоянии сильного психологического стресса или физического перенапряжения.
Эти пациенты отличались гемодинамической нестабильностью, нуждались в традиционной поддержке; почти все полностью выздоравливали. ЭхоКГ чрезвычайно полезна при ЭТОМ синдроме для мониторирования функциональной и гемодииамической реакции на лечение. Описана разновидность этого синдрома — среднежелудочковая форма, при которой в процесс не вовлекаются апикальный и банальный сегменты. Только средняя часть ЛЖ акииетичпа при вентрикулографии или ЭхоКГ. Клинически отличить ИМ с подъемом сегмента ST, наступивший вследствие коронарной окклюзии, от синдрома шаровидной верхушки сложно. Отсутствие стеноза КА не всегда свидетельствует о синдроме шаровидной верхушки, поскольку у некоторых больных может быть абортивное течение ИМ.
При сравнении результатов ЭхоКГ при синдроме шаровидной верхушки и ИМ с подъемом сегмента ST выявлено, что в первом случае площадь нарушений локальной сократимости была больше, но диастолическое наполнение лучше, что свидетельствовало о менее выраженном трансмуральном поражении. Перфузия при синдроме шаровидной верхушки относительно нормальная, что указывает на то, что нарушения локальной сократимости при этом больше связаны с увеличением потребности (например, при повышенном уровне катехоламинов), чем с недостаточностью кровоснабжения.
Синдром шаровидной верхушки — кардиомиопатия Takotsubo
Оценка риска при инфаркте миокарда
Самыми сильными прогностическими признаками после инфаркта миокарда являются степень систолической дисфункции, объем ЛЖ, тяжесть поражения коронарного русла, MP, диастолическая дисфункция и наличие СН. Резонно полагать, что у больных с высоким WMS1 более высока вероятность развития кардиальных событий. У большинства больных с СН (Killip II—IV) после ОИМ VVMSI > 1,7. В дополнение к WMSI рестриктивный тип диастолической дисфункции коррелирует с частотой развития СН после ИМ и с давлением наполнения ЛЖ.
Отношение Е/Еа. надежный параметр для оценки ДЗЛК, служит сильным предиктором долгосрочного прогноза после ОИМ. Объем ЛП, хроническая диастолическая дисфункция и хроническое повышение давления в ЛП являются сильными предикторами исходов ИМ. Стресс-ЭхоКГ чувствительна в определении остаточной ишемии, жизнеспособности миокарда и многососудистого поражения в ранние сроки после ИМ. Однако обычно больные в это время неспособны адекватно выполнять физическую нагрузку. Миокард какое-то время (несколько дней или недель) после успешной реперфузии инфаркт-связанной КА остается акинетичным.
Оценка жизнеспособности по увеличению сократимости (при ЭхоКГ с добутамином) или перфузии (при контрастной ЭхоКГ) прогнозирует функциональное восстановление миокарда. ЭхоКГ с добутамином и контрастом имеют сходные чувствительность и специфичность для прогноза фракционального восстановления; ЭхоКГ при перфузии миокарда лучше определяет состояние передней стенки, чем нижней и боковой стенок.
Оглавление темы «Оценка гемодинамики при ЭхоКГ»:
Ключевые слова
Обзор
Стресс-индуцированная кардиомиопатия, также называемая синдром преходящей дисфункции левого желудочка или Takotsubo-кардиомиопатия, становится все более известной, обычно характеризуется транзиторной систолической дисфункцией и обширной акинезией апикальных и / или средних сегментов левого желудочка, жалобами имитирующие острый коронарный синдром, но при отсутствии обструкции коронарных артерии [1, 2], сопровождаются изменениями на ЭКГ, а также ограниченным выбросом сердечных маркеров, не соответствующих этой степени акинезией.
Около 20 лет назад этот синдром описывался только у японских пациентов. Однако во всем мире на данный момент по статистике 2% из 300000 сердечных приступов приходится на это заболевание. Это говорит о большей информированности врачей, улучшении диагностики и установления четких критериев для постановки диагноза. Следует ожидать увеличения частоты своевременной диагностики такоцубо-кардиомиопатии при условии доступности неотложной коронароангиографии в большинстве кардиологических центров в первые 24 часа, как того и требуют современные рекомендации по оказанию неотложной помощи больным с острым коронарным синдромом [3].
Термин «такоцубо» (tako-tsubo) в переводе с японского языка означает приспособление для ловли осьминогов – керамический горшок с круглым основанием и узким горлышком. Именно такую форму у больных при эхокардиографии приобретает левый желудочек (ЛЖ) в систолу, что объясняется отсутствием сокращения его верхушки с одновременным избыточным сокращением базальных отделов [4].
Патогенетические механизмы включают в себя избыток катехоламинов спазм коронарных артерии, и микрососудистую дисфункцию [5, 6].
Потенциальная роль разрыва холестериновой бляшки и тромбоза со спонтанным тромболизисом не были установлены. Однако результаты внутрисосудистого ультразвукового исследования (ВСУЗИ) показали доказательство разрыва бляшки в середине левой передней нисходящей коронарной артерии в 5 из 5 пациентов с диагнозом стресс-индуцированной кардиомиопатии [7]. но другая серия ВСУЗИ не нашла никаких доказательств относительно этой гипотезы [8, 9] .
Связь развития стрессовой кардиомиопатии с физическим или эмоциональным стрессом [1, 10-15], показывают, что это расстройство может быть вызвано диффузным действием катехоламинов вызванным микрососудистым спазмом или дисфункцией, путем прямого токсического действия катехоламинов [16]. У некоторых пациентов с индуцированной стрессом кардиомиопатией, единственным очевидным стрессом является воздействие препаратов катехоламинов или бета-агонистов в обычных клинических дозах [17].
Возможность патогенной роли катехоламинов выявлена в ряде исследований определения в плазме катехоламинов [4,18-20]. Объединяя результаты из этих серий, плазменные уровни норадреналина были повышены в 74 % и составили следующие концентрации: эпинефрин-1264 пг/мл против нормальной концентрации 376 пг / мл; норэпинефрин-2284 пг/мл против 1100 пг / мл [21]. Повышение уровня катехоламинов и обратимые изменения левого желудочка наблюдались также в крысиной модели, вызванной стрессом [22]. Однако, высокий уровень катехоламинов в крови не является повсеместно встречаемым у обследуемых пациентов и некоторые исследования показали нормальный уровень [23].
Дальнейшая поддержка гипотезы действия катехоламинов обеспечивается наблюдениями подобной обратимой кардиомиопатии с глобальной или очаговой дисфункцией у пациентов с феохромоцитомой [24] и в условиях острого повреждения головного мозга, которые также постулируются связанными с действием катехоламинов [25]. По данным эндомиокардиальной биопсии в серии из восьми пациентов в период дисфункции левого желудочка [11, 13, 16] обнаружены гистологические признаки катехоламиновой токсичности [26, 27] — отсутствие признаков миокардита [28], обнаружение интерстициального фиброза [11], внутриклеточное накопление гликогена, множество вакуолей, дезорганизованность цитоскелета миокардиоцитов, увеличение белка внеклеточного матрикса [23, 27]. Эти изменения нивелировались почти полностью после функционального восстановления. Предположительно, что наибольший эффект в апикальной части миокарда может быть связан с более высокой плотностью бета-адренорецепторов в этом месте [29].
Эпидемиология
Стресс-индуцированного кардиомиопатия гораздо чаще встречается у женщин, чем у мужчин. В обзоре десяти проспективных серий, женщины составляли от 80 до 100 % случаев, со средним возрастным интервалом от 61 до 76 лет [31]. У женщин > 55 лет риск развития заболевания был в 4,8 раза выше, по сравнению с женщинами
Факторы риска
К факторам риска, которые обычно связаны с развитием стрессовой кардиомиопатии следует отнести курение, злоупотребление алкоголем, тревожные состояния и гиперлипидемия. Провоцирующими факторами могут выступать: физический стресс, внезапное падение артериального давления, тяжелая болезнь, операция или медицинская процедура (например, сердечный стресс-тест), сильная боль, насилие в семье, приступ астмы, получение плохих новостей (например, диагностика рака), несчастный случай, неожиданная потеря или болезнь близкого родственника, финансовый убыток, сильный страх, публичные выступления [34].
Наиболее распространенным симптомами являются острая загрудинная боль (58,8% случаев), а затем одышка (30% случаев), обмороки, тахикардия. Острыми осложнениями стресс-индуцированной кардиомиопатии являются остановка сердца, тахиаритмии (включая желудочковую тахикардию и фибрилляцию желудочков), брадиаритмии. Стресс-индуцированный гиперкинез левого желудочка может способствовать развитию шока и серьезной митральной регургитации [1, 10, 12], верхушечное тромбообразование и инсульт [17]. Вероятность развития острой сердечной недостаточности возможно предсказать на основе наличия или отсутствия следующих трех переменных. возраст > 70 лет, наличие физического стрессора и снижение фракции выброса левого желудочка ( ФВ ЛЖ )
Диагностическими критериями клиники Мейо являются [30, 34, 35]:
- Переходные гипокинезия, акинезия или дискинезия левого желудочка середины сегментов с или без апикального участия.
- Региональных аномалий движения стенки обычно выходят за рамки одного эпикардиальной коронарного распределения.
- Наличие стрессовых триггеров часто, но не всегда.
- Отсутствие обструкции коронарных артерий или ангиографических признаков острого разрыва бляшки.
- Электрокардиографические аномалии (либо изменение высоты ST- сегмента и / или инверсия зубца Т).
- Скромные высоты сердечного тропонина и креатинфостокиназы.
- Отсутствие феохромоцитомы или миокардита.
- Фракция выброса левого желудочка (ФВ ЛЖ )
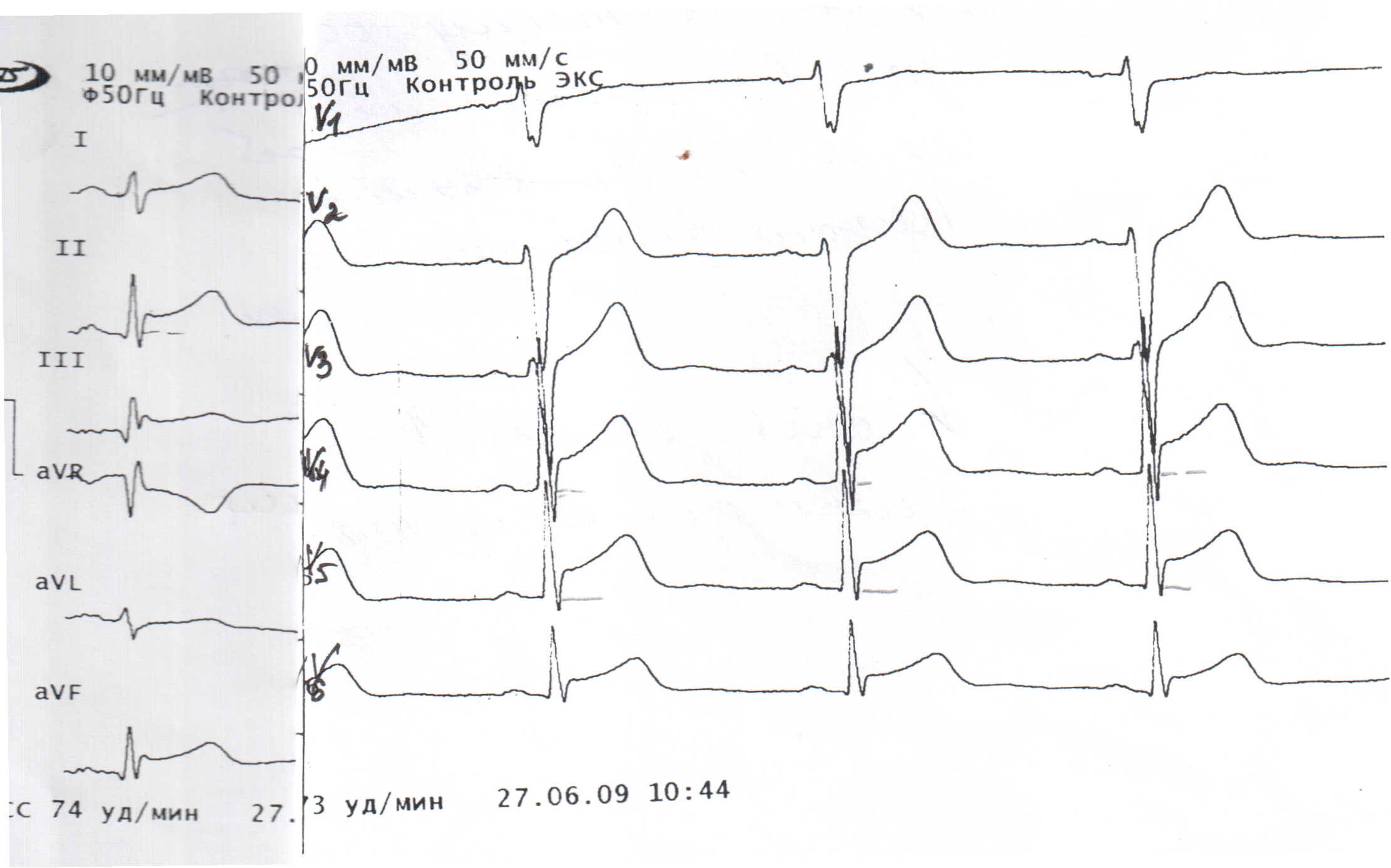
Электрокардиографические проявления имитируют острый коронарный синдром. Характерен инфарктоподобный подъем сегмента ST, наиболее распространенной в передних грудных отведениях ; диффузная инверсии зубца Т с продлением интервала QT. аномальные волны Q. неспецифические нарушения. Восстановление ЭКГ происходит на 2-3 неделе болезни.
Наиболее специфичные изменения при ЭХО-кг и контрастной вентрикулографии. Характерен акинез или дискинез верхушки и средней части ЛЖ с гиперконтрактильностью основания и обструкцией выходного тракта ЛЖ. При этом форма ЛЖ напоминает приспособление для ловли осьминогов. Общая систолическая функция снижается, а средняя ФВ ЛЖ варьируется в диапазоне от 20 до 49 процентов [1, 2, 31].
Ангиография является ценным методом диагностики. Принципиальное отличие кардиомиопатии токацубо от острого коронарного синдрома – отсутствие гемодинамически значимого стеноза коронарных артерий.
МРТ с гадолинием помогает в дифференциальном диагнозе с такими заболеваниями как инфаркт миокарда и миокардит. Гадолиний не накапливается при стресс-индуцированной кардиомиопатии, в отличие от инфаркта миокарда, в котором интенсивное (т.е. > 5 стандартных отклонений выше средней интенсивности сигнала дистанционного миокарда) субэндокардиально или трансмурально. При миокардите характерно неоднородное накопление гадолиния. МРТ может также дать определение тромбов в левом или правом желудочке, которые не могут быть обнаружены с помощью ЭХО-кг [11, 31].
Повышение сердечных сывороточных маркеров контрастирует с часто тяжелыми нарушениями гемодинамики. Распространенность повышения креатинкиназы-МВ и / или тропонина у пациентов было в 89,3% случаев, в 10,7% показало нормальный уровень этих сердечных ферментов. Средняя максимальная вариабельность креатинкиназы-MB и рост тропонина были 27,4 мкг/л (норма 5.2-115.7 мкг / л) и 18,7 мкг / л (норма 2.0-97.6 мкг/л), соответственно [1, 3, 20].
До настоящего времени отсутствуют формальные рекомендации по лечению больных с СКМП. Считается, что в острой фазе заболевания показано применение транквилизаторов, если развитию синдрома предшествовал эмоциональный стресс, а также устранение других возможных провоцирующих факторов, например боли. Назначаются ингибиторы АПФ, бетаадреноблокаторы, антикоагулянты, диуретики, антагонисты кальция. Кроме того, в таких случаях целесообразно выполнение внутриаортальной баллонной контрпульсации. При динамической обструкции выходного тракта ЛЖ противопоказано использование препаратов положительного инотропного действия. Продолжительность приема антикоагулянтов варьируются в зависимости от скорости восстановления функции сердца. На фоне поддерживающей терапии всегда происходит спонтанное выздоровление в течение 2 месяцев. В 5% случаев возникает рецидив заболевания, вероятно, провоцируемый ассоциированным пусковым механизмом.
Takotsubo кардиомиопатия представляет собой новый вариант кардиомиопатии, который стал диагностироваться в последние годы. Основным пусковым фактором заболевания является выраженный физический и эмоциональный стресс, относительно часто встречается у пожилых женщин. Патогенетические механизмы обуславливаются токсическим действием катехоламинов, поэтому сочетании α-и β-адреноблокаторов, добавление эстрогенов в терапию у женщин в постменопаузе может защитить от его развития или смягчить клинические проявления. Этот вид кардиомиопатии следует считать возможной причиной внезапной сердечной смерти в результате аритмии, в том числе у лиц без явных сердечных заболеваний. Чтобы лучше понять патогенетические механизмы, разработать рациональную систему профилактики и схем лечения, созданы регистры.
Наиболее значимые из них:
- многонациональное, проспективное и ретроспективное, обсервационное исследование пациентов с Takotsubo кардиомиопатией — международный Takotsubo регистр Цюрихского университета (InterTAK Registry) [36];
- многоцентровый регистр сети отделений кардиореанимации г.Токио [32];
- INTrial является надежной, проверенной и одобренной системой для онлайн ввода данных, проверки данных и управления данными для клинических испытаний, в том числе по кардиомиопатии takotsubo [37].
Кардиомиопатия Такоцубо
Стресс-индуцированная кардиомиопатия или кардиомиопатия Такоцубо (КТ) является недавно выявленным синдромом, связанным с расширением верхушечных или средних сегментов левого желудочка и его обратимой тяжелой дисфункцией.
Клинические признаки этого синдрома схожи с острым инфарктом миокарда, но не связаны с существенным стенозом коронарных артерий.
Кардиомиопатия Такоцубо диагностируется примерно у 1-2% пациентов с симптомами и анамнезом сходным с острым инфарктом миокарда.
Большинство пациентов с КТ являются женщинами в постменопаузе (90%), в возрасте 55-75 лет.
Этиология кардиомиопатии Такоцубо до конца не известна, но высокие уровни катехоламинов выявляются более чем у 70% пациентов. Исследования показали, что более высокая плотность бета-адренорецепторов находится в апикальном отделе левого желудочка и циркулирующие катехоламины активно влияют на этот сегмент, что приводит к снижению сократимости последних.
Причина высокой распространенности кардиомиопатии у женщин в постменопаузе неизвестна, но есть гипотеза, что снижение эстрогенов и их влияние на микрососудистую систему сердца после менопаузы может быть основной причиной.
Недавно были описаны новые формы кардиомипатии Такоцубо:
- Частичный (умеренный) апикальный вариант. который появляется у лиц среднего возраста (30-32 года).
- Обратный синдром Такоцубо — более редкий вариант с аналогичными патофизиологическми причинами, как при классическом Такоцубо, но с другим профилем пациентов и другой манифестацией симптомов — замечена у молодых женщин и проявляется гипердинамичной верхушкой левого желудочка и полной акинезией базальных сегментов.
Провоцирующими факторами, как правило, являются серьезные эмоциональные или физические нагрузки, а также другие причины гиперсимпатикотонии — повышение внутримозгового давления — массивные ишемические инсульты, геморрагические инсульты, ЧМТ (т.н. «церебро-кардиальный» синдром), прием симпатомиметиков. Эмоциональный стресс был частой причиной стресс-индуцированной кардиомиопатии в случае серии докладов, по этой причине она получила название «синдром разбитого сердца».
Наиболее распространенными симптомами являются боли в груди (2/3 пациентов) и одышка. сходными с острым инфарктом миокарда. Кардиогенный шок может выявляться у больных с выраженным снижением фракции выброса левого желудочка.
Подъем сегмента ST на ЭКГ отсутствует у 2/3 пациентов с КТ.
Изменения ЭКГ в динамике не коррелируют с тяжестью поражения миокарда и прогнозом .
Диффузное нарушение движения стенок сердца (боковых, задних, нижних, перегородочных, передних, верхушечных) приводит к систолическому «баллонированию» верхушечных сегментов.
Наиболее распространенными изменениями на ЭКГ являются удлинение интервала QT и тахикардия Torsades de Pointes . Кардиоферменты, как правило, умеренно повышены, мозговой натрийуретический пептид также повышен.
Основными критериями КТ являются:
- выраженные эмоциональные и физические нагрузки перед появлением болей в грудной клетке
- «ишемические» изменения на ЭКГ
- незначительные изменения коронарных артерий или отсутствие тромбоза на ангиографии
- дилатация апикальных или средних сегментов левого желудочка с компенсаторным гиперкинезом базальных сегментов при эхокардиографии
- непропорционально низкие уровни сердечных биомаркеров по сравнению со степенью дисфункции левого желудочка
- быстрое улучшение функции левого желудочка
Типичные изменения на ЭКГ:
- Элевация ST в прекордиальных отведениях при КТ более выражена в II,V3-V5 .
- Элевация или, по крайней мере, отсутствие депрессии ST в нижних отведениях
- Часто деперссия ST в aVR. Очень редко небольшая элевация сегмента ST в V1.