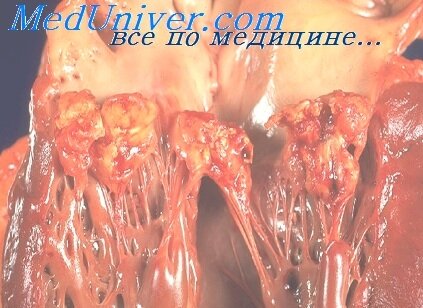
Инфекционный эндокардит
ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ -заболевание, развивающееся в результате инфекционного поражения клапанов сердца или эндокарда. Термин “инфекционный эндокардит” стал общепринятым с 1966 г. Он заменил устаревшие понятия “бактериальный эндокардит” и “затяжной септический эндокардит*. Истинная распространенность заболевания не установлена.
Этиология и патогенез. До 60-х гг. нынешнего века основной причиной развития инфекционного эндокардита был зеленящий стрептококк. На его долю приходилось до 90% всех случаев заболевания. Сейчас в большинстве стран мира заметно возросло число стафилококковых эндокардитов. В настоящее время структура возбудителей инфекционного эндокардита представлис ген примерно следующей: золотистый стафилококк — 35-40%, зеленящий стрептококк — 45-55 %, другие виды стрептококков -5 %, энтерококки — 5-7 % и некоторые другие микроорганизмы — около 5%. В Великобритании по-прежнему в 65-85% случаев инфекционный эндокардит вызывают стрептококки. Среди других микробных агентов высеваются стафилококки в 5-15% случаев, энтерококки в 5-15%, грамотрицательная кишечная флора в 2-6%, возбудитель не выделяется в 5-10% случаев.
Увеличение числа стафилококковых эндокардитов связано с бесконтрольным повсеместным назначением антибиотиков, нередко без достаточных оснований, снижением иммунной защиты организма, увеличением числа оперативных вмешательств на сердце и сосудах, а также значительным ростом числа инвазивных манипуляций на человеческом организме.
Причиной инфекционного эндокардита в отдельных случаях могут быть грибы рода Candida, Aspergillus, Histoplasma. Именно поэтому термин “бактериальный эндокардит” не охватывает всех случаев инфекционного поражения клапанов сердца.
Инфекционный эндокардит развивается в результате эпизодов бактериемии на фоне лечебных или диагностических манипуляций (экстракция или лечение зубов, эндоскопические манипуляции, катетеризация и т.п.), инфекций дыхательных или мочевыводящих путей и других патологических состояний. Чаще болеют мужчины (2:1) в возрасте 40-50 лет.
Инфекционный эндокардит чрезвычайно редко возникает на неповрежденных или неизмененных клапанах. Клапаны могут быть повреждены в результате перенесенного ревматического процесса. Фоном для развития эндокардита могут быть врожденные пороки сердца, пролабирование створок митрального клапана, аномалии строения аортального клапана (двустворчатый клапан) и другие. Неповрежденные клапаны и эндокард устойчивы к воздействию инфекционных агентов.
Итак, первичным патогенетическим фактором развития инфекционного эндокардита является макро- или микротравмативания эндокарда или клапанного аппарата сердца. Незаметно образуются тромботические вегетации. Микробный агент начинает размножаться на клапанах сердца, и формируется внутрисердечный очаг инфекции Этим создаются условия для дополнительного отложения тромбоцитом и фибрина. Микробные агенты как бы прикрываются снаружи и становятся труднодоступными для последующей антибиотикотерапии.В конечном итоге на клапанах сердца или эндокарде формируются тромботические и микробные вегетации.
Наиболее часто в патологический процесс вовлекается аортальный клапан, затем митральный, реже всего поражаются трикуспидальный клапан и клапан легочной артерии.
Если инфекционный эндокардит развивается на фоне имеющегося врожденного или приобретенного порока сердца, он называется вторичным. Такая форма эндокардита встречается у 2/3 больных. Первичный эндокардит возникает у больных без предшествующего порока сердца, что не исключает, а, вероятнее всего, подразумевает наличие менее явных, чем порок сердца, повреждений клапанов сердца (аномалии строения, синдром ПМК и др.).
Условно в течении инфекционного эндокардита выделяются 4 патогенетические фазы: доклиническая, инфекционно-токсическая, иммуновоспалительная и дистрофическая. Такое деление имеет определенное значение в комплексной терапии заболевания. В иммуновоспалительную фазу в схему лечения дополнительно включаются глкжокортикоидные гормоны.
Клиническая картина. Инфекционному эндокардиту свойственны отчетливая полисиндромность клинических проявлений и отсутствие патогномоничных признаков. Каждому патогенетическому механизму соответствуют определенные клинические или лабораторные проявления болезни. Поступление инфекционного агента в кровеносное русло с эпизодами бактериемии вызывает лихорадку, усталость, потерю аппетита, похудание, анемию, спленомегалию, образование антител.
Развитие микробно-тромботических вегетации может приводить к нарушению функции сердца, перфорации клапанов, развитию аневризмы синуса Вальсальвы. Отрыв фрагментов микробно-тромботических вегетации сопровождается периферическими эмболиями, септическими инфарктами.
Циркуляция в крови антигенов (микроорганизмы) и антител к инфекционному агенту приводит к формированию иммунных комплексов, появлению петехий, узелков Ослера, артрита, миокардита, гломерулонефрита.
Основным клиническим признаком инфекционного эндокардита является лихорадочный синдром. Обычно лихорадка носит черты инфекционной, сопровождается ознобами, холодными потами. Максимальные подъемы температуры тела чаще отмечаются в вечерние часы. Характер лихорадочной кривой может быть самым разнообразным, но более типичны гектическая, интермиттирующая и ремиттирующая кривые. Температура у разных больных может колебаться от субфебрильной до чрезмерно высокой. Это зависит от вида возбудителя и реактивности организма больного. У молодых пациентов чаще наблюдается высокая гектическая лихорадка, у пожилых — субфебрильная.
Начало заболевания может быть острым, с высокой лихорадкой и выраженной интоксикацией. У некоторых больных инфекционный эндокардит развивается незаметно, проявляясь недомоганием, слабостью, потливостью, субфебрильной температурой тела.
На фоне длительной лихорадки, интоксикации организма кожные покровы становятся бледными, напоминая цвет кофе с молоком. При сопутствующем поражении печени или повышенном гемолизе эритроцитов бледность кожных покровов сопровождается легкой желтушностью.
На коже грудной клетки, туловище нередко можно увидеть петехий. Они локализуются также в полости рта, глотки и конъюнктиве. Наличие петехиальных кровоизлияний в области переходной складки конъюнктивы обозначается как симптом Либмана-Лукина. При распространенном геморрагическом иммунном васкулите может появляться выраженная геморрагическая сыпь некротического характера. Иногда проявления геморрагического васкулита бывают первым важным клиническим признаком заболевания, откуда начинается диагностический поиск.
Вследствие микроэмболий в сосуды кончиков пальцев, ладоней могут появляться болезненные подкожные эритематозные узелки (узелки Ослера). При длительном течении инфекционного эндокардита пальцы кистей приобретают вид барабанных палочек.
Основным в клинике инфекционного эндокардита является поражение сердца. Без выявления признаков поражения эндокарда или клапанов сердца невозможно поставить достоверный диагноз заболевания. При первичном эндокардите манифестные симптомы. свидетельствующие о поражении сердца, появляются лишь через несколько недель или месяцев от начала заболевания. У большинства больных в патологический процесс вовлекаются эндокард и миокард, реже перикард.
Нередко отмечаются кардиалгии неопределенного характера. Весьма важно определить появление диастолического шума аортальной недостаточности. Именно аортальная недостаточность -наиболее частый порок, развивающийся в результате перенесенного инфекционного эндокардита. Причиной формирования порока сердца служат микробно-тромботические вегетации на створках клапана.
Систолический шум на верхушке или в точке Боткина выслушивается значительно чаще, однако важного диагностического значения он не имеет. Происхождение систолического шума может быть связано с наличием миокардита, анемии, пролабиронания створок митрального клапана, а также возможным его поражением.
В последние годы с увеличением числа оперированных больных по поводу пороков сердца возрастает число больных с так называемым протезным эндокардитом, который может быть ранним и поздним. Если инфекционный эндокардит развивается у больного в течение первых 2 мес после операции на сердце, такой эндокардит называется ранним. Причиной его развития в большинстве случаев бывает инфекция, попавшая в ток крови во время оперативного вмешательства.
Протезный эндокардит может возникнуть и спустя 2 мес после операции (поздний эндокардит). В подобных ситуациях инфицирование больных происходит таким же путем, как и неоперированных пациентов. О развитии протезного эндокардита следует подумать в тех ситуациях, когда у больных, оперированных по поводу пороков сердца, возникает необъяснимая лихорадка, обнаруживаются воспалительные изменения в крови. Таких пациентов необходимо консультировать у кардиохирурга.
Развитие эндокардита на фоне имеющегося врожденного или приобретенного порока сердца приводит к изменению тонов и шумов сердца, появлению новых аускультативных и клинических симптомов в виде быстро нарастающей сердечной декомпенсации или заметного прогрессирования порока сердца.
Миокардит при инфекционном эндокардите может быть ранним и поздним. Ранний миокардит развивается одновременно с началом инфекционного эндокардита. Его развитие связывается с поражением миокарда инфекционными агентами. Поздний миокардит возникает в иммуновоспалительную фазу эндокардита. Его патогенетические механизмы иные. Доминируют при этом иммунные процессы.
Клинически наличие миокардита проявляется тахикардией, не связанной с лихорадкой, глухостью сердечных тонов, нарушениями сердечного ритма и проводимости, соответствующими изменениями на ЭКГ. При эхокардиографии можно выявить снижение сократительной функции миокарда.
В иммуновоспалительную фазу инфекционного эндокардита возможно возникновение артритов, чаще крупных суставов, гломерулонефрита. Длительное течение эндокардита сопровождается развитием спленомегалии.
Характерен для инфекционного эндокардита тромбоэмболический синдром. Нередки тромбоэмболии почек, селезенки, головного мозга, сосудов сетчатки. При эндокардите правых отделов сердца, что типично для эндокардита у наркоманов, отмечаются тромбоэмболии ветвей легочной артерии. Появление тромбоэмболии сосудов почек, селезенки, головного мозга, легких и других органов сопровождается соответствующей клинической картиной. У многих больных тромбоэмболические осложнения на определенном этапе могут стать доминирующими в клинической картине заболевания.
По течению инфекционный эндокардит бывает острым (до 6 нед), подострым (от 6 нед до 3 мес) и затяжным (более 3 мес).
Лабораторные показатели. При исследовании крови выявляется нормохромная анемия, нередко анизоцитоз и пойкилоцитоз. Может наблюдаться нейтрофильный лейкоцитоз со сдвигом лейкоцитарной формулы влево. Часто обнаруживается токсогенная зернистость нейтрофилов. При тяжелом течении эндокардита возможна и лейкопения, анэозинофилия. Лейкоцитоз нарастает при развитии тромбоэмболических осложнений.
Характерно повышение СОЭ. Это один из самых простых и надежных показателей, свидетельствующих об активности патологического процесса в эндокарде. СОЭ может возрастать до значительных цифр (50-70 мм/ч).
Инфекционному эндокардиту свойственно увеличение уровня сх2 — и у-глобулинов. Обычно положительной бывает формоловая проба. Показателен НСТ-тест. У больных эндокардитом он может повышаться до 65-70% (у здоровых — до 30-32%). У некоторых пациентов вследствие диспротеинемии или развития антифосфолипидного синдрома появляется положительная реакция Вассермана.
Из крови может быть высеян возбудитель заболевания.
В моче часто отмечается небольшая протеинурия токсического генеза, или протеинурия и микрогематурия могут быть обусловлены развивающимся гломерулонефритом.
Для диагностики инфекционного эндокардита важнейшее значение имеет исследование крови на стерильность. Бакпосевы целесообразно выполнить до назначения больному антибактериальных препаратов. Исследование крови на стерильность проводится на высоте лихорадки и пятикратно в течение суток с двухчасовыми интервалами. Для увеличения вероятности ныделения возбудителя посевы крови целесообразно делать на несколько сред, по крайней мере на среду для грамположительной и грамотрицательной флоры.
Среди инструментальных методов диагностики наиболее значимо ультразвуковое исследование сердца. Основная цель эхо-кардиографии — поиск вегетации на клапанах сердца. Одновременно оценивается состояние сердечной мышцы, полостей сердца перикарда. В случае подозрения на инфекционный эндокардии, но отсутствия вегетации на клапанах при обычной эхокардиографии показано проведение чреспищеводной эхокардиографии
Дифференциальная диагностика инфекционного эндокардита проводится с заболеваниями, сопровождаюшимися длительной лихорадкой, в частности сепсисом, туберкулезом, холангитом, острым лейкозом, лихорадкой. Необходимо исключение также ревматизма, миеломной болезни, малярии и др.
Лечение инфекционного эндокардита проводится терапевтами, кардиологами, ревматологами, инфекционистами, кардиохирургами. Обычно больной продолжает лечение в том отделении стационара, где впервые был установлен диагноз заболевания. Лечение больных инфекционным эндокардитом весьма дорогостоящее.
Основу лечения составляет антибактериальная терапия. Используются антибиотики исключительно бактерицидного действия. Их рекомендуется вводить парентерально, предпочтительнее внутривенно. Лечение следует начинать, не дожидаясь результатов исследования крови на стерильность. Берутся высокие дозировки препаратов и, как правило, применяется комбинация 2 антибиотиков. Длительность антибиотикотерапии составляет не менее 4-6 нед.
В лечении инфекционного эндокардита могут быть использованы пенициллины, цефалоспорины, имепенемы, аминогликозиды, фторхинолоны и некоторые другие. Суточные дозы препаратов для лечения инфекционного эндокардита должны быть примерно следующими: пенициллин — 12-24, ампициллин -6-10, амоксициллин — 10-20, азлоциллин — 6-15, цефотаксим — 6, цефтриаксон — 2-4, имипенем (тиенам) — 1,5-3, гентамицин — 0,24-0,32, амикацин — 1, ципрофлоксацин — 0,4, ванкомицин — 2, рифампицин — 0,9, клиндамицин — 1,8 г. При получении результатов посевов крови на стерильность учитывается чувствительность флоры к антибиотикам. С учетом чувствительности к антибиотикам подбираются наиболее оптимальные, совместимые и проверенные практикой комбинации.
Начальное лечение эндокардита до получения результатов посевов (или при культуронегативном эндокардите) проводится пенициллином внутривенно и гентамицином внутримышечно. Второй курс культуронегативного эндокардита выполняется ванкомицином в комбинации с цефотаксимом.
Для лечения наиболее часто встречающегося стрептококкового эндокардита предпочтительны комбинации пенициллина и гентамицина, затем цефазолина и гентамицина. Последующие курсы можно проводить комбинацией ванкомицина и клиндамицина, а также цефтриаксона и гентамицина.
Лечение стафилококкового эндокардита при сохранении чувствительности к антибиотикам начинается с пенициллина, второй курс проводится комбинацией ванкомицина с рифампицином или клиндамицином. Показаны также цефазолин и гентамицин, фторхинолоны и рифампицин.
Энтерококковый эндокардит лечится комбинацией ампициллина и гентамицина, ванкомицина и имипенема, фторхинолонов и рифампицина или бакгрима. На эндокардит, вызванный грамотрицательной флорой, предпочтительнее воздействовать комбинацией цефотаксима (или мезлоциллина) и гентамицина.
Последующие курсы можно проводить цефтриаксоном, имипенемом в комбинации с гентамицином.
Лечение грибкового эндокардита проводится дифлюканом, амфотерицином В.
Кроме антибактериального лечения больным необходима дезинтоксикационная терапия, периодически вводятся ингибиторы протеолитических ферментов (контрикал, гордокс, овомин и др.). Целесообразно проведение ультрафиолетового облучения крови. При стафилококковом эндокардите показана инфузия стафилококковой плазмы и/или у-глобулина.
В иммуновоспалительную фазу заболевания артрит, миокардит, кожный васкулит и гломерулонефрит купируются добавлением кортикостероидных гормонов (метилпреднизолон, 12 — 24 мг/сут). При артритах дополнительно назначаются нестероидные противовоспалительные препараты. Выполняется также симптоматическое лечение по показаниям.
Критериями успешного излечения инфекционного эндокардита являются: 1) негативная гемокультура; 2) исчезновение клинических симптомов заболевания; 3) отсутствие лихорадки; 4) нормализация СОЭ.
В последние годы все чаще приходится прибегать к хирургическому лечению инфекционного эндокардита. Показания к хирургическому лечению — отсутствие эффекта от адекватной терапии (сохранение лихорадки, положительная гемокультура) в течение 2 нед. Оперативное лечение показано больным при прогрессировании сердечной недостаточности из-за клапанной регургитации, при дисфункции протеза или появлении парапротезной фистулы, а также при наличии рецидивирующих периферических тромбоэмболии.
Прогноз инфекционного эндокардита во всех случаях заболевания достаточно серьезный. Он зависит от вида возбудителя и состояния защитных сил организма. Тромбоэмболические осложнения заметно ухудшают прогноз болезни.
Профилактика. После выписки из стационара больные инфекционным эндокардитом должны наблюдаться кардиологом или ревматологом. В первые 2 мес наблюдение осуществляется не реже 1 раза в 2 нед с исследованием общего анализа кала и мочи, ежедневной термометрией. В последующем наблюдение за больным проводится 1 раз в мес. Профилактика ИЭ осуществляется у лиц группы риска (лица с пороком сердца, перенесшие ИЭ ранее, после протезирования клапанов, с двустворчатым аортальным клапаном, синдромом ПМК, пациенты после порюкоронарного шунтирования; наркоманы и некоторые другие). Для лиц, относящихся к группе риска, профилактика эндокардита должна проводиться в процессе исполнения любых дани юстичсских инвазивных манипуляций, хирургических вмешательств, лечебных манипуляций (лечение зубов и т.п.).
Профилактика эндокардита у подобной категории пациентов может осуществляться по различным схемам. Возможные рекомендуемые варианты бывают следующими. Первая схема: за 30 мин до манипуляции внутримышечно вводится I -2 г ампициллина и 80 мг гентамицина, через 6-8 час после манипуляции повторно однократно вводятся те же антибиотики в той же дозировке. Вторая схема: за 1 ч до манипуляции — 1г эритромицина внутрь и 0,5 г эритромицина дополнительно через 6 ч после завершения манипуляции.
Комментарии
Для того что бы оставить комментарий необходимо зарегистрироваться.
Инфекционный эндокардит
Инфекционный эндокардит при отсутствии интенсивной антибактериальной терапии неизбежно ведёт к летальному исходу.
Достигнутые в последние годы успехи в области клинической микробиологии, медицинской визуализации, кардиохирургии, антибактериальной терапии значительно улучшили диагностику и прогноз инфекционного эндокардита.
Для того, чтобы изучить эволюцию этого заболевания, учёные из Лозаннского Университета (Швейцария) провели обзор 26 публикаций, опубликованных с 1993 по 2003 г. и описывающих 3784 случая инфекционного эндокардита.
Несмотря на улучшения, произошедшие в области здравоохранения, заболеваемость инфекционным эндокардитом за последние 2 десятилетия практически не изменилась. Это объясняется эволюцией факторов риска заболевания. Ревматизм, который являлся в пре-антибиотическую эру основным фактором, предрасполагающим к развитию инфекционного эндокардита, в настоящее время встречается гораздо реже. Несмотря на это, появляются новые факторы риска: внутривенное использование наркотиков, дегенеративные изменения клапанов сердца у людей пожилого возраста, искусственные клапаны, внутрисосудистые протезы, нозокомиальные заболевания, процедуры гемодиализа. Среди пациентов с искусственными клапанами риск составляет 0,3-0,6% в год, причем нет значимых различий между механическими и биологическими протезами. Наибольший риск приходится на первые 2 месяца после имплантации. Нозокомиальный эндокардит встречается последнее время все чаще, прежде всего в связи с катетер-ассоциированной бактериемией, вызванной стафилококками и энтерококками. Вероятно, пациенты с пролапсом митрального клапана и митральной регургитацией также имеют повышенный риск.
В отношении этиологии инфекционного эндокардита, было подтверждено значение «традиционных» возбудителей. Staphilococcus aureus. Streptococcus spp. и энтерококки вызывают более 80% случаев заболевания. Также исследователями были подтверждены некоторые известные взаимосвязи между факторами риска и выявляемыми микроорганизмами, например, частое выделение Staphylococcus aureus у пациентов, использующих внутривенные наркотики. Наряду с этим были выявлены новые взаимосвязи. Так, у пожилых пациентов оказалась высокой частота выделения Streptococcus bovis. У некоторых пациентов были также идентифицированы микроорганизмы, которые раньше не определялись у пациентов с инфекционным эндокардитом: Bartonella spp. Tropheryma whipplei и др. Большие трудности представляет лечение пациентов с инфекционным эндокардитом, вызванным резистентными к антибиотикам микроорганизмами.
Хирургическое лечение показано 25-30% пациентов в острой стадии и 20-40% пациентов в отсроченный период. Наиболее частыми показаниями к оперативному лечению являются рефрактерная застойная сердечная недостаточность вследствие клапанной недостаточности, сохраняющийся сепсис, абсцесс клапанного кольца или миокарда, жизнеугрожающая эмболия. Операционная летальность составляет 8-16% (во время нахождения в стационаре), 24-25% в течение 5 лет и 40% в течение 10 лет.
Philippe Moreillon, Yok-Ai Que.
Infective endocarditis
Lancet 2004; 363: 139-49
Инфекционный эндокардит
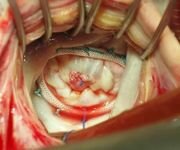 Под термином инфекционный эндокардит подразумевают любую инфекцию, поражающую эндокард, сердечные клапаны, эндотелий прилежащих сосудов, а также другие внутренние органы (почки, печень, селезенку и др).
Под термином инфекционный эндокардит подразумевают любую инфекцию, поражающую эндокард, сердечные клапаны, эндотелий прилежащих сосудов, а также другие внутренние органы (почки, печень, селезенку и др).
Некоторые авторы указывают, что точная цифра заболеваемости инфекционным эндокардитом неизвестна.
Некоторые авторы указывают, что точная цифра заболеваемости инфекционным эндокардитом неизвестна. В то же время в США приходится 0,16-5,4 случаев инфекционного эндокардита на 1000 госпитализаций, во Франции отмечается 18 заболеваний на миллион жителей (970 человек в год), четверть из которых лечится хирургическим путем.
Протезный эндокардит, возникающий на искусственных клапанах сердца, встречается у 1-13% больных. Благополучной считается ситуация, если частота возникновения протезного эндокардита в кардиохирургическом центре не превышает 2% среди оперированных больных без предшествующего инфекционного поражения клапанов сердца.
В целом заболеваемость инфекционным эндокардитом увеличивается. Это происходит за счет роста числа пациентов с дегенеративными, атеросклеротическими, травматическими поражениями клапанов сердца, увеличением числа пациентов с механическими и биологическими протезами, а также искусственными водителями ритма. Возрастает количество больных инфекционным эндокардитом, не имевших клапанной патологии и заболевших вследствие длительных внутривенных инфузий, наркомании, гемодиализа, применения химио- и стероидной терапии, воздействия факторов неблагоприятной экологической среды. Отечественные авторы отмечают особую роль ревматических пороков сердца, как субстрата для развития инфекционного эндокардита.
История
Первое описание больных, погибших от инфекционного эндокардита, произвел А.Riviere в 1646 г. Термин эндокардит был введен в 1834 г. F.Buyo. Клапанные вегетации впервые описал R. Wirchow в 1846 г. а в 1872 г. S.Winge, H.Heiberg доказали микробную этиологию эндокардита. В 1885 г. W.Osler впервые описал симптоматику, клиническое течение и морфологические особенности этого заболевания. До появления антибиотиков большинство больных умирало от неконтролируемой инфекции и только 12% — от сердечной недостаточности. Применение сульфаниламидов в 1937 г. привело к излечению 15% больных.
Революцией в лечении инфекционного эндокардита стало внедрение пенициллина. Впервые парентеральное введение пенициллина у больного с инфекционным эндокардитом применил в 1940 г. Henry Dawson. Он излечил инфекционный процесс на клапанах сердца подкожными инъекциями пенициллина в течении 2 дней. В 1944 г. A.Loewe впервые применил внутривенное введение пенициллина, добившись 100% выздоровления 7 пациентов с инфекционным эндокардит. В настоящее время около 80% больных может быть успешно излечено с помощью антибиотикотерапии.
Однако у 20% пациентов лекарственное лечение оказывается безуспешным, так как основной причиной смерти становится сердечная недостаточность вследствие пороков клапанов сердца. Поэтому следующей вехой явилось применение хирургического метода, который берет свое начало с 1962 г. когда N.Кау очистил от вегетаций трехстворчатый клапан. В 1963 г. D.Wallace произвел первое успешное протезирование аортального клапана в неактивную фазу заболевания, а в 1965 г. митральное протезирование у больного с активным инфекционным процессом. В дальнейшем хирургическое лечение получило широкое распространение во всем мире.