Инфекционный эндокардит — Заболевания сердечно-сосудистой системы детей
Страница 64 из 77
Этим термином объединяют такие заболевания, как острый и подострый бактериальные эндокардиты, эндокардиты небактериального происхождения, в частности вызванные вирусами, грибками и другими возбудителями. Заболевание и в настоящее время протекает тяжело, приводя в большом проценте случаев к смерти детей и подростков, несмотря на достигнутые в области лечения и профилактики успехи. Неэффективность профилактических и ранних лечебных мероприятий обусловлена рядом факторов: изменением природы патогенных микроорганизмов; недостаточной осведомленностью терапевтов, стоматологов и населения в целом об угрозе заболевания и существующих мероприятиях по его профилактике; поздней диагностикой заболевания, что представляет собой большие трудности; появлением в последние годы групп риска, в состав которых входят все увеличивающееся число лиц, страдающих наркоманией, а также перенесших операции на сердце, больных со сниженной сопротивляемостью организма инфекциям, которым требуется введение в сосуды катетеров.
Этиология. Примерно в 50% случаев инфекционный эндокардит вызывает зеленящий стрептококк. Однако его роль в этом постепенно уменьшается. За последние два десятилетия (в ‘/з случаев) чаще стал встречаться эндокардит, вызванный стафилококком. Другие микроорганизмы реже вызывают эндокардит; при этом примерно в 10% случаев возбудитель из крови не высевается. Не установлены связи между штаммом микроорганизма и типом врожденного дефекта, продолжительностью заболевания в возрастом ребенка. Однако стафилококковый эндокардит чаще встречается у больных без сопутствующих пороков сердца.
Эпидемиология. Инфекционный эндокардит чаще всего выступает в роли осложнения врожденного или ревматического порока сердца, однако он может встречаться у детей без патологии сердца. В последнее время подтверждается преимущественная предрасположенность к заболеванию инфекционным эндокардитом детей с врожденным пороком сердца. У детей грудного возраста он развивается крайне редко.
Чаще инфицирование эндокарда происходит при дефектах, при которых скорость поступления крови в камеру сердца или в сосуд высокая. Турбулентность потока обусловливает эрозию эндокарда или интимы, в которой обычно начинает размножаться микроорганизм (рис. 11—77). Таким образом, дети с дефектами межжелудочковой перегородки и поражением клапанного аппарата левых отделов сердца с сообщением между сосудами большого и малого кругов кровообращения относятся к группе высокого риска по заболеванию инфекционным эндокардитом, в то время как при вторичном дефекте межпредсердной перегородки, характеризующемся низкой скоростью шунта через внутрипредсердный дефект, частота заболевания им крайне низкая.
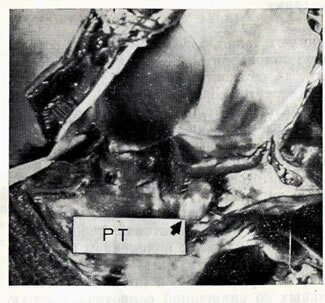
Рис. 11—77. Правый желудочек сердца. Непосредственно под клапаном легочной артерии виден обширный участок разрастающейся ткани (РТ) (стрелка).
К группе наиболее высокого риска относятся дети, перенесшие операцию на сердце и с паллиативным шунтом между аортой и легочной артерией. Однако все увеличивающаяся частота операций по протезированию клапанов и коррекции дефекта с помощью клапансодержащих протезов у детей со сложными пороками сердца может привести к увеличению частоты заболевания инфекционным эндокардитом.
Примерно у 30% больных инфекционным эндокардитом можно выявить предрасполагающий фактор. Примерно у 2/3 больных его можно связать с оперативным вмешательством или стоматологическими процедурами. Более того, можно сказать, что несоблюдение требований гигиены полости рта у детей, страдающих пороком сердца синего типа, повышает риск септицемии и инфицирования миокарда. Процент рецидивов инфекционного миокардита непосредственно после катетеризации сердца или операции на нем относительно низок. Однако на основании частоты их выполнения они встречаются в перечне важнейших факторов, предшествующих развитию инфекционного эндокардита.
Клинические проявления. Ранние симптомы и признаки обычно не выражены, особенно если заболевание обусловлено зеленящим стрептококком. Нередко единственным анамнестическим признаком может быть лихорадочное состояние, не сопровождающееся другими симптомами (за исключением наблюдаемого иногда уменьшения массы тела) в течение нескольких месяцев. В других случаях заболевание может начинаться остро и протекает тяжело на фоне высокой интермиттирующей температуры тела и выраженной слабости. Однако обычно его начало и течение промежуточны между этими двумя крайними формами. Симптоматика обычно неспецифична и заключается в незначительном повышении температуры тела во второй половине дня, быстрой
утомляемости, миалгиях, артралгиях, головных болях, иногда ознобах, тошноте и рвоте. В зависимости от вирулентности микроорганизма могут появиться признаки тромбоэмболии, а при физикальном обследовании выявляют патологию сердца. Относительно часто присоединяется спленомегалия, возможны петехиальные высыпания на коже. Обычно при аускультации сердца определяют изменение шумов или появление новых, особенно при поражении клапанного аппарата и сопутствующем врожденном пороке сердца.
При инфекционном эндокардите стафилококковой этиологии часто развиваются тяжелые осложнения со стороны ЦНС, в том числе эмболии сосудов, абсцессы мозга, микотические аневризмы и мозговые кровоизлияния, проявляющиеся признаками менингизма, увеличением внутричерепного давления, изменениями чувствительности.
Стафилококк может обусловить развитие миокардиальных абсцессов, иногда прорывающихся в полость перикарда. Эмболия легочных или сосудов большого круга кровообращения характерна лишь для грибкового эндокардита. Многие классические проявления на коже появляются в поздние стадии заболевания и поэтому у адекватно леченных больных не наблюдаются. К ним относятся узелки Ослера (нежные внутрикожные узелки на подушечках пальцев рук и ног размером с горошину), высыпания Джейнуэя (небольшого размера болезненные эритематозные или геморрагические высыпания на ладонных и подошвенных поверхностях) и кровоизлияния по типу заноз (линейной формы поражения под ногтевыми пластинками). Вероятно, высыпания представляют собой проявления васкулита, вызванного циркулирующими комплексами антиген — антитело.
Диагностировать инфекционный эндокардит можно с большой долей вероятности у ребенка с инфекцией на фоне основного заболевания.
Данные лабораторных исследований. Выбор адекватного лечения при инфекционном эндокардите основан на результатах посева крови. Все остальные данные имеют меньшее значение. У больного можно ожидать незначительно или умеренно выраженный лейкоцитоз. Часто увеличивается СОЭ, уровень гемоглобина редко достигает менее 90 г/л. Микрогематурия обычно свидетельствует о гломерулонефрите, обусловленном циркуляцией иммунных комплексов. При прогрессировании заболевания могут образовываться аутоантитела, а у некоторых больных периодически выявляются ревматоидный фактор (антиглобулины), криоглобулины или положительная реакция Кана.
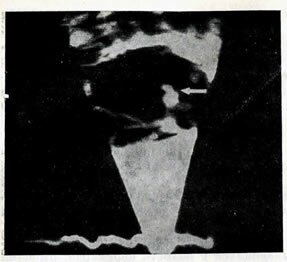
Рис. 11—78. Двухмерная эхокардиограмма ребенка, больного бактериальным эндокардитом. Стрелкой указан обширный участок разрастания ткани в левом предсердии, прикрепляющийся к створкам митрального
У каждого ребенка с предполагаемым инфекционным эндокардитом необходимо как можно быстрее произвести бактериологическое исследование крови. Это необходимо сделать, даже если ребенок чувствует себя хорошо и у него отсутствуют другие физикальные проявления. После тщательной подготовки участка венепункции забор крови производят в три пробирки. Загрязнение бактериями представляет собой особую проблему, поскольку флора, обитающая на коже, сама по себе может вызвать инфекционный эндокардит. Время забора крови не имеет значения, поскольку в течение дня бактериемия относительно постоянна. В 90% случаев возбудитель выявляется в первых двух пробах крови, поэтому дальнейший забор ее можно отложить на 2-3 дня.
В целях выявления локализации специфических разрастаний прибегают к помощи эхокардиографии (рис. 11—78), однако в раннюю стадию заболевания этот метод не всегда информативен. Значение недостаточности левого предсердно-желудочкового и аортального клапанов на функцию левого желудочка можно оценить с помощью ультразвуковых методов обследования.
Прогноз и осложнения. В доантибиотиковую эру инфекционный эндокардит считался фатальным заболеванием. Существенные успехи в его лечении были достигнуты в 50-е годы. С тех пор уровень выживаемости, хотя и медленно, но неуклонно повышается. Уровень смертности остается в пределах 20—25%. Осложнения отмечаются у 50—60% детей с подтвержденным диагнозом инфекционного эндокардита. Чаще всего из них встречаются недостаточность сердца вследствие разрастаний на аортальном или левом предсердно-желудочковом клапане. Образование абсцессов в миокарде и токсический миокардит могут привести к развитию застойной недостаточности без характерной динамики аускультативных данных.
При сопутствующих пороках левых отделов сердца или аорты основную опасность представляют собой тромбоэмболия сосудов большого круга, часто сопровождаемая неврологическими признаками. Тромбоэмболия сосудов малого круга чаще встречается у детей с дефектами межжелудочковой перегородки или тетрадой Фалло. Однако массивная, угрожающая жизни тромбоэмболия системы легочной артерии регистрируется крайне редко. Описаны такие осложнения септического эндокардита, как некротические аневризмы, разрыв синусов Вальсальвы, обструктивное поражение клапанов вследствие массивных специфических разрастаний, приобретенный дефект межжелудочковой перегородка и полная поперечная блокада сердца, обусловленная вовлечением в патологический процесс специализированной проводящей системы сердца.
Лечение. Немедленно после установления диагноза следует начинать лечение антибиотиками. Если заболевание вызвано вирулентным микроорганизмом, то даже малейшая задержка в лечении может привести к прогрессирующему повреждению эндокарда и вызвать тяжелые осложнения. Выбор антибиотиков, метод, их введения и продолжительность лечения представлены в табл. 11—9. Высокий уровень антибиотиков в крови должен поддерживаться в течение достаточно длительного времени с тем, чтобы обеспечить ликвидацию микроорганизмов, обитающих во внесосудистых специфических разрастаниях, в которые антибиотики проникают с большим трудом. Для того чтобы прекратить рост бактерий в центре этих разрастаний, уровень антибиотика в них должен в 5—20 раз превышать минимальный уровень, при котором прекращается рост in vitro. Для полной организации разрастаний требуется несколько недель, поэтому в течение этого’ времени следует продолжать лечение антибиотиками с тем, что- бы избежать рецидива роста микроорганизмов. Рекомендуемая продолжительность общего курса лечения составляет 4—6 нед. Для достижения бактерицидного эффекта уровень антибиотика’ в сыворотке, определенный методом разведения в пробирках, перед следующей инъекцией должен составлять примерно 1:8. В зависимости от клинического и лабораторного эффекта терапевтическая тактика может меняться, в некоторых случаях тре- буется более длительный курс лечения. Если инфекционный’ эндокардит вызван высокочувствительными к антибиотикам штаммами зеленящего стрептококка, рекомендуются более короткие курсы лечения препаратами пенициллина, принимаемыми внутрь.
Больные должны соблюдать постельный режим. При присоединении застойной недостаточности сердца продолжительность его увеличивается. При необходимости больным назначают препараты наперстянки, мочегонные средства и ограничивают потребление соли.
При вовлечении в процесс аортального или левого предсердно-желудочкового клапана производят операцию, поскольку у больного может развиться неконтролируемая недостаточность сердца. Иногда при микотических аневризмах или разрывах аортального синуса требуется немедленная операция. Несмотря на то что в целом перед операцией следует провести максимально длительный курс антибиотикотерапии, активный инфекционный процесс не относится к противопоказаниям к ее проведению у больного, находящегося в критическом состоянии в результате циональных нарушений проводящей системы предсердий, синусно-предсердного узла и атриовентрикулярного соединения (рис. 11—75). Он может встречаться в отсутствие врожденных пороков сердца и был описан у сибсов.
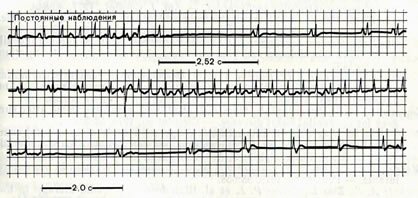
За периодами наджелудочковой тахикардии, вероятно, политопной этиологии, наступает длительная блокада проведения импульса из синусового узла, а затем — синусовая брадикардия.
Рис. 11—76. Изменения на электрокардиограмме при синдроме дисфункции синусового узла.
Таблица 11—9. Лечение инфекционного эндокардита
Инфекционный эндокардит
Кафедра педиатрии №1
Реферат
Тема: Инфекционный эндокардит.
Выполнила:
603 группа пед. Фак.
Иркутск 2008г.
Инфекционный эндокардит
Инфекционный эндокардит (ИЭ) – тяжелое инфекционное, чаще бактериальное системное заболевание с первичным поражением клапанов сердца и пристеночного эндокарда, которое сопровождается бактериемией, деструкцией клапанов, эмболическим, тромбогеморрагическим, иммунокомплексным поражением внутренних органов и без лечения приводит к смерти.
Эпидемиология
Инфекционный эндокардит у детей и подростков (в отличие от взрослых) – весьма редкое, а у грудных детей – редчайшее заболевание, частота которого составляет 3,0 – 4,3 случая на 1 млн детского и подросткового населения в год. В то же время по данным, поступающим из крупных медицинских центров Европы и США, удельный вес ИЭ среди детей и подростков в специализированных стационарах постепенно нарастает, что связывают с увеличением числа операций на сердце при врожденных пороках, постоянным расширением спектра инвазивных диагностических и лечебных медицинских манипуляций, а также распространением внутривенной наркомании.
При современном ИЭ у детей и подростков наблюдается тенденция к учащению поражения митрального и трикуспидального клапанов, а также клапанов легочной артерии как в отдельности, так и в виде многоклапанного процесса.
При подостром варианте течения ПИЭ у детей многоклапанное поражение встречается чаще, чем при остром ИЭ (соответственно 76 и 45% случаев). При вторичном инфекционном эндокардите (ВИЭ) независимо от характера течения частота мультиклапанного поражения одинакова и составляет примерно 70%.
Поражение неизмененного митрального клапана считается характерным для ИЭ у маленьких пациентов, в виде моноклапанной патологии встречается в 40% случаев.
Этиология
ИЭ является полиэтиологическим заболеванием.
Основные возбудители ИЭ у детей и подростков.
Инфекционный эндокардит у детей
Инфекционный эндокардит — острое или подострое воспаление клапанного и/или пристеночного эндокарда, вызываемое различными инфекционными агентами.
Инфекционный (в том числе абактериальный) эндокардит — одна из серьёзных причин смертности детей и подростков. Вариабельность и неспецифичность его клинической картины вызывают объективные трудности диагностики. Недостаточное знакомство педиатров, стоматологов и родителей с принципами профилактики инфекционного эндокардита, а также увеличение количества лиц, входящих в группы риска (наркоманы, пациенты после оперативных вмешательств на сердце, больные, находящиеся на иммуносупрессивной терапии, с длительной катетеризацией центральных вен и т.д.), приводят к увеличению количества случаев заболевания.
Инфекционный эндокардит может развиться на интактных клапанах (5-6%), но чаще осложняет врождённые (90%) и ревматические (3%) пороки сердца, особенно после оперативных вмешательств по их поводу.
Частота инфекционного эндокардита у детей неизвестна, однако количество больных детей постепенно увеличивается и составляет 0,55 на 1000 госпитализированных. Мальчики болеют в 2-3 раза чаще, чем девочки.
Наиболее частые возбудители инфекционного эндокардита в настоящее время — зеленящий стрептококк и золотистый стафилококк (до 80% случаев заболевания). Первый чаще вызывает заболевание на интактных, второй — на повреждённых клапанах. Реже инфекционный эндокардит вызывают другие микроорганизмы: энтерококки, менинго-, пневмо- и гонококки, эпидермальный стафилококк, хламидии, сальмонеллы, бруцеллы, НАСЕК-группа (объединение нескольких грамотрицательных палочек), а также вирусы и грибы; последние два упомянутых агента вызывают «абактериальную» форму инфекционного эндокардита (около 10% случаев заболевания). При катетеризации сердца и длительном стоянии катетера в центральных венах часто выявляют синегнойную палочку, при операциях на сердце и длительной антибиотикотерапии — грибы (кандиды, гистоплазмы).
Инфекционный эндокардит может быть врождённым и приобретённым.
Врождённый эндокардит развивается при острых или обострении хронических вирусных и бактериальных инфекций у матери и представляет собой одно из проявлений септицемии.
Приобретённый инфекционный эндокардит у детей первых 2 лет жизни возникает чаще на интактных клапанах; у детей более старшего возраста заболевание обычно развивается при наличии порока сердца (как и у взрослых). Предрасполагающим фактором к развитию инфекционного эндокардита выступает операция на сердце.
Предрасполагающие факторы выявляют приблизительно у 30% больных. Оперативные вмешательства, прежде всего на сердце, мочевом тракте и в полости рта, предшествуют развитию инфекционного эндокардита в 65% случаев.
Патогенез инфекционного эндокардита сложен и связан с несколькими факторами: изменённым иммунным ответом организма, дисплазией соединительной ткани сердца, повреждением коллагеновых структур клапанного и пристеночного эндокарда гемодинамическими и инфекционными воздействиями, нарушением реологических свойств и свёртывающей системы крови, особенностями самого возбудителя и др.
Наиболее часто инфекционный эндокардит развивается у пациентов с морфологическими дефектами структур сердца, при которых турбулентный, замедленный или усиленный ток крови приводит к изменению клапанного или предсердного эндокарда (тетрада Фалло, небольшой ДМЖП, открытый боталлов проток, коарктация аорты, пороки митрального клапана). Циркулирующий в крови инфекционный агент оседает на повреждённом или интактном эндокарде сердца и эндотелии крупных сосудов, вызывая воспалительную реакцию, расслоение богатых коллагеном краёв клапанов, отложение на них фибрина и образование тромботических масс (вегетации). Возможно и первичное тромбообразование, связанное с гемодинамическими и реологическими нарушениями (абактериальный эндокардит). В этом случае оседание микроорганизмов на уже изменённых клапанах происходит позднее.
В дальнейшем разрастающиеся вегетации могут отрываться и вызывать эмболии мелких и крупных сосудов большого и малого круга кровообращения.
Выделяют три фазы патогенеза: инфекционно-токсическую, иммуновоспалительную и дистрофическую.
Инфекционно-токсическая фаза формируется как ответная островоспалительная реакция макроорганизма. В этой фазе чаще выявляют бактериемию, тогда как собственно сердечные изменения выражены умеренно, заболевание протекает как острая инфекция с лихорадкой, интоксикацией, воспалительными изменениями периферической крови.
Иммуновоспалительная фаза связана с образованием антител как к антигенам возбудителя, так и к собственным тканям и криоглобулинам. Этот процесс протекает с участием комплемента и формированием ЦИК. Эта фаза сопровождается генерализацией процесса, поражением других внутренних органов и более отчётливыми изменениями в сердце. Её рассматривают как иммунокомплексную болезнь.
Дистрофическая фаза проявляется хроническим воспалением эндокарда и внутренних органов, формированием пороков, отложением солей кальция в клапанных структурах, гемодинамической сердечной недостаточностью. Возможны выявление порока сердца через несколько лет после выздоровления и повторное заболевание инфекционным эндокардитом.
Клиническая картина
В клинической картине ведущую роль играют три основных синдрома: инфекционно-токсический, кардиальный (текущий эндокардит) и тромбоэмболический.
Инфекционный эндокардит, особенно стрептококковой этиологии, может начинаться постепенно — с повторных эпизодов повышения температуры тела в вечерние часы, недомогания, артралгий, миалгий, потливости, немотивированной потери массы тела. Возможно и острое начало — с гектической лихорадки, резкого нарушения общего состояния, потрясающих ознобов и профузных потов (чаще при инфицировании стафилококком).
В инфекционно-токсическую фазу эндокардит может не иметь отчётливых клинических проявлений, хотя уже через несколько дней от начала заболевания можно выслушать протодиастолический шум недостаточности аортального клапана. При вторичном эндокардите меняются количество и характер шумов в области уже изменённого клапана. В этот период возможны проявления тромбоэмболии: геморрагическая сыпь, периодическая гематурия, инфаркты внутренних органов. Пятна Лукина-Либмана на конъюнктиве, пятна Джейнуэя на ладонях и стопах, полосчатые геморрагии под ногтями, свидетельствующие о васкулите, при своевременно начатом лечении возникают редко.
В иммуновоспалительную фазу происходят генерализация иммунопатологического процесса и присоединение миокардита, а иногда и перикардита, диффузного гломерулонефрита, анемии, поражения лимфатических узлов, печени, селезёнки. Цвет кожных покровов становится серовато-желтушным («кофе с молоком»), иногда развивается желтуха. Текущий процесс в сердце проявляется умеренным болевым синдромом, тахикардией, кардиомегалией и глухостью тонов (при сопутствующем миокардите). Появляются шумы, сопровождающие порок или деструкцию клапанного аппарата (отрыв хорд или створок клапана, их перфорация). Эмболии и инфаркты в эту фазу болезни наблюдают реже.
В дистрофической фазе на первый план выступает недостаточность — сердечная, почечная, иногда печёночная — как следствие тяжёлого поражения внутренних органов при генерализованном иммунопатологическом процессе.
В некоторых случаях особенности клинической картины инфекционного эндокардита позволяют предположить, какой именно инфекционный агент послужил причиной его развития. Об особенностях стрептококковых и стафилококковых эндокардитов уже упоминалось выше.
Пневмококковый эндокардит развивается в период реконвалесценции при заболевании пневмонией, локализуется на трёхстворчатом и аортальном клапанах, протекает с высокой лихорадкой, выраженным токсикозом, периферическими бактериальными эмболиями.
Бруцеллёзный эндокардит имеет такую же локализацию, что и пневмококковый. Иногда он вызывает образование бактериальных аневризм синуса Вальсальвы с переходом инфекции через стенку аорты на предсердия, желудочки и другие оболочки сердца с развитием внутрипредсердной и внутрижелудочковых блокад.
Сальмонеллёзный эндокардит приводит к деструкции аортального и митрального клапанов с образованием тромбов, повреждению эндотелия сосудов и развитию эндартериита и сосудистых аневризм.
Грибковый эндокардит сопровождается развитием инфарктов лёгких, пневмоний, увеита и эндофтальмита.
Осложнения инфекционного эндокардита включают сердечную и почечную недостаточность, последствия тромбоэмболии в виде инфарктов головного мозга и миокарда, абсцессов головного мозга и других органов. Перечисленные осложнения можно расценивать и как проявления терминальной фазы болезни. Возможно развитие перикардита, менингита, артрита, остеомиелита и других гнойных процессов.