Медикаментозная тахикардия
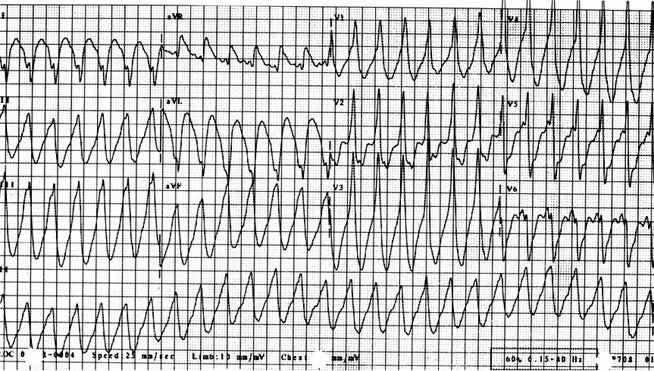
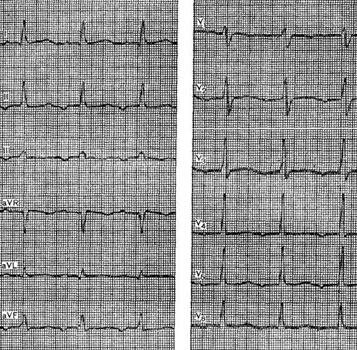
Препараты наперстянки ввиду особенно частого их назначения имеют наибольшую вероятность индукции желудочковой аритмии. Подобным нарушениям ритма нередко предшествуют симптомы общей интоксикации, но иногда их могут опережать сердечные эффекты. В некоторых случаях первым проявлением бывает бигеминия, обусловленная регулярными желудочковыми экстрасистолиями; другим серьезным признаком может быть так называемая двунаправленная тахикардия. Однако желудочковая тахикардия может наблюдаться и без каких-либо признаков интоксикации и бывает скорее стабильной (рис. 9.27), нежели пароксизмальной (см. рис. 9.10). За возникновение аритмии могут быть ответственны очень многие медикаменты, в том числе препараты, способные вызывать torsade de pointes [59, 60].
Некоторые препараты оказывают непрямое влияние, например диуретики, вызывающие гипокалиемию, другие же — непосредственное действие, например кардиоактивные препараты и большинство транквилизаторов, пролонгирующих реполяризацию. По нашему опыту, развитие аритмии наиболее вероятно при назначении хинидина, прокаинамида, фенотиазинов и трициклических антидепрессантов; если при использовании какого-либо препарата наблюдается torsade de pointes, следует особенно осторожно отнестись к его дальнейшему назначению. Кальциевый антагонист бепридил также способен вызвать аритмию, особенно у пожилых женщин с гипокалиемией [91] или в случае передозировки [D.
Krikler, М. Perelman и Е. Rowland, неопубликованные данные]. Способность индуцировать желудочковую тахикардию приписывается и ряду других препаратов [15], однако во многих публикациях описываются лишь одиночные случаи, в которых далеко не всегда ясна связь приема препарата с нарушением ритма.
Информация, релевантная «Медикаментозная тахикардия»
Синусовая тахикардия. 2. Наджелудочковые тахикардии а. Пароксизмальная реципрокная (ре-энтери) узловая тахикардия. б. Пароксизмальная реципрокная (ре-энтери) узловая тахикардия при наличии дополнительных проводящих путей.(синдром WPW и CLC). в.Пароксизмальная очаговая предсердная тахикардия. г.Пароксизмальная (ре-энтери) синусовая тахикардия. 3.
Эффективность радиочастотной абляции при желудочковой тахикардии различна у пациентов с ИБС, кардиомиопатиями, а также при разных формах идиопатической желудочковой тахикардии. Технологии картирования и абляции разные, в зависимости от типа желудочковой тахикардии. У пациентов без структурного заболевания сердца обычно определяют только единичные очаги желудочковой тахикардии и катетерная абляция
При широких комплексах QRS (>120 мс) важно дифференцировать наджелудочковую тахикардию от желудочковой тахикардии. Для отличия наджелудочковых тахикардий от желудочковых стойкие симптомы тахикардии непоказательны. Если диагноз наджелудочковой тахикардии невозможно подтвердить или установить, то тахиаритмию следует расценивать как желудочковую тахикардию и лечить соответственно. Тахикардия с
Аритмии сердца представляют собой нарушения частоты, ритмичности и (или) последовательности сердечных сокращений: учащение (тахикардия) либо урежение (брадикардия) ритма, преждевременные сокращения (экстрасистолия), дезорганизацию ритмической деятельности (мерцательная аритмия ) и т.д. Тахикардия – три или более последовательных сердечных цикла с частотой 100 и более в минуту. Пароксизм –
Госпитализация показана при впервые зарегистрированных пароксизмах наджелудочковых тахикардий с узкими комплексами QRS, при отсутствии эффекта от медикаментозной терапии (на догоспитальном этапе применяют только одно аритмическое средство), при появлении осложнений, потребовавших проведения электроимпульсной терапии, при часто рецидивирующих нарушениях
Для этой разновидности нарушения ритма сердца характерны два признака: 1. Тахикардия, т.е. возбуждение (и последующее сокращение) сердца с частотой 130—250 в мин. 2. Пароксизм, т. е. внезапное начало и внезапное окончание приступа тахикардии, которые, как правило, уловить клинически и зарегистрировать электрокардиографически удается крайне редко. Суть пароксизмальной тахикардии —
Алгоритм действий при пароксизмальной реципрокной АВ узловой тахикардии и ортодромной пароксизмальной реципрокной АВ тахикардии с участием дополнительных предсердно-желудочковых соединений (синдром WPW) на догоспитальном этапе. Врачебная тактика при пароксизме наджелудочковой пароксизмальной тахикардии с узким комплексом QRS определяется стабильностью гемодинамики пациента. Устойчивое
Высокоэффективно 1. Перед началом терапии антиаритмическими препаратами рекомендуется лечение, направленное на устранение обратимых причин ФП, вызывающих развитие повторных приступов. Эффективно 1. У пациентов с ФП может применяться медикаментозная терапия для поддержания синусового ритма и предотвращения кардиомиопатии, вызываемой тахикардией. 3. Целесообразно проводить медикаментозную
1. Наличие предсердно-желудочковой диссоциации, которая регистрируется на электрограмме пучка Гиса. Этот критерий является очень важным, но не абсолютным, так как выявляется, хотя и очень редко, при наджелудочковых тахикардиях с аберрантной желудочковой проводимостью. 2. Отсутствие потенциала Н перед желудочковыми комплексами или значительное укорочение интервала И—У на гисограмме. 3. Частая
Синдром ВПУ является, вероятно, наиболее важным причинным фактором пароксизмальной регулярной наджелудочковой тахикардии. В группе из 120 больных, последовательно поступивших в клинику в связи с пароксизмальной наджелудочковой тахикардией, электрокардиографические признаки синдрома ВПУ на фоне синусового ритма были обнаружены у 69 больных (57 %). Столь высокая частота синдрома ВПУ особенно
Амиодарон
Общие характеристики. Состав:
Активное вещество — амиодарона гидрохлорид 200 мг.
Вспомогательные вещества: крахмал картофельный, целлюлоза микрокри-сталлическая, магния стеарат, кросповидон (Коллидон CL-M), кремния диоксид коллоидный, гипромеллоза (гидроксипропилметилцеллюлоза).
Фармакологические свойства:
Фармакокинетика. Абсорбция медленная и вариабельная — 30-50 %, биодоступность — 30-50 %. Максимальная концентрация в плазме крови (Cmax) отмечается через 4-7 ч. Диапазон терапевтической плазменной концентрации — 1-2,5 мг/л (но при определении дозы необходимо иметь в виду и клиническую картину). Объем распределения – 60 л, что свидетельствует об интенсивном распределении в ткани. Обладает высокой жирорастворимостью, в высоких концентрациях находится в жировой ткани и органах с хорошим кровоснабжением (концентрация в жировой ткани, печени, почках, миокарде выше, чем в плазме крови — соответственно, в 300, 200, 50 и 34 раза). Особенности фармакокинетики амиодарона обусловливают необходимость применения препарата в высоких нагрузочных дозах. Проникает через гематоэнцефалический барьер (ГЭБ) и плаценту (10-50 %), секретируется с грудным молоком (25 % дозы, полученной матерью). Связь с белками плазмы крови – 95 % (62 % — с альбумином, 33,5 % — с бета-липопротеинами).
Метаболизируется в печени. Основной метаболит — дезэтиламиодарон — фар-макологически активен и может усиливать антиаритмический эффект основ-ного соединения. Возможно, также путем дейодирования (при дозе 300 мг выделяется примерно 9 мг элементарного йода). При продолжительном лечении концентрации йода могут достигать 60-80 % концентрации амиодарона.
Учитывая способность к кумуляции и связанную с этим большую вариабельность фармакокинетических параметров, данные по периоду полувыведения (T1/2) противоречивы. Выведение амиодарона после перорального приема осуществляется в 2 фазы: начальный период — 4-21 ч, во второй фазе T1/2 — 25-110 дней. После продолжительного перорального приема средний T1/2 – 40 дней (это имеет важное значение при выборе дозы, т.к. возможно, необходим, по крайней мере, 1 мес для стабилизации новой плазменной концентрации, в то время как полное выведение может продлиться более 4 месяцев). Выводится с желчью (85-95 %), почками выводится менее 1 % принятой внутрь дозы (поэтому при нарушенной функции почек нет необходимости в изменении дозировки). Амиодарон и его метаболиты не подвергаются диализу.
Фармакодинамика. Амиодарон-Акри — антиаритмический препарат III класса (ингибитор реполяризации). Обладает также антиангинальным, коронародилатирующим, альфа- и бета-адреноблокирующим, тирео-тропным и гипотензивным действием.
Антиаритмическое действие обусловлено влиянием на электрофизиологиче-ские процессы миокарда. Удлиняет потенциал действия кардиомиоцитов, увеличивает эффективный рефрактерный период предсердий, желудочков, атриовентрикулярного (AV) узла, пучка Гиса и волокон Пуркинье, добавочных путей проведения возбуждения.
Блокируя «быстрые» натриевые каналы, оказывает эффекты, характерные для антиаритмиков I класса. Тормозит медленную (диастолическую) деполяризацию мембраны клеток синусового узла, вызывая брадикардию и снижение AV проводимости.
Антиангинальный эффект обусловлен коронарорасширяющим и антиадренергическим действием, уменьшением потребности миокарда в кислороде. Оказывает тормозящее влияние на альфа- и бета-адренорецепторы сердечно-сосудистой системы (без полной их блокады). Уменьшает чувствительность к гиперстимуляции симпатической нервной системы, сопротивление коронарных сосудов. Увеличивает коронарный кровоток, урежает частоту сердечных сокращений, повышает энергетические резервы миокарда (за счет увеличения содержания креатинсульфата, аденозина и гликогена).
По своей структуре подобен тиреоидным гормонам. Содержание йода составляет около 37 % его молекулярного веса. Влияет на обмен тиреоидных гормонов, ингибирует превращение Т3 в Т4 (блокада тироксин-5-дейодиназы) и блокирует захват этих гормонов кардиоцитами и гепатоцитами, что приводит к ослаблению стимулирующего влияния тиреоидных гормонов на миокард (дефицит Т3 может привезти к его гиперпродукции и тиреотоксикозу). Начало действия (даже при использовании «нагрузочных» доз) – от 2-3 дней до 2-3 мес, длительность действия варьирует от нескольких недель до месяцев (определяется в плазме крови на протяжении 9 мес после прекращения его приема).
Показания к применению:
— лечение и предупреждение нарушений ритма сердца, связанных с синдромом Вольфа-Паркинсона-Уайта (WPW), пароксизмами мерцания и трепетания предсердий ; предсердной и желудочковой экстрасистолией; парасистолией, желудочковыми аритмиями у больных с миокардитом Шагаса;
— предупреждение повторной фибрилляции желудочков и предсердий;
— лечение желудочковой тахикардии ;
— лечение наджелудочковой тахикардии с целью восстановления синусового ритма при мерцании и трепетании предсердий;
— в период реабилитации после инфаркта миокарда, если в анамнезе есть указания на ранее отмечавшиеся эпизоды аритмии.
Способ применения и дозы:
Таблетки принимают внутрь целиком во время или после приема пищи, запивая достаточным количеством жидкости.
Режим дозирования устанавливается индивидуально и корректируется врачом.
Насыщающая доза составляет 600 мг/сутки (3 таблетки), разделенная на 2-3 приема. Курс лечения 8-15 дней. При необходимости дозу препарата Амиодарон-Акри можно повысить до 800-1200 мг/сутки (4-6 таблеток), на короткий период и под контролем ЭКГ. После достижения признаков насыщения переходят к поддерживающей терапии.
Поддерживающая доза. При поддерживающем лечении применяется наименьшая эффективная доза в зависимости от индивидуальной реакции пациента и обычно составляет от 200-400 мг/сутки (1-2 таблетки) в 1-2 приема. В случаях, когда это возможно через каждые 5 дней приема препарата делают двухдневный перерыв.
Средняя терапевтическая разовая доза – 200 мг.
Средняя терапевтическая суточная доза – 400 мг.
Максимальная разовая доза – 400 мг.
Максимальная суточная доза – 1200 мг.
Особенности применения:
Перед началом лечения, а также через каждые 3 месяца необходимо прово-дить ЭКГ контроль, при этом необходимо учитывать, что у пожилых пациентов отмечается более выраженная брадикардия. также необходимо провести рентгенологическое исследование легких, оценить функцию щитовидной железы (содержание гормонов), печени (ферментов). Частота и тяжесть побочных эффектов зависят от дозы препарата, поэтому следует применять минимально эффективные поддерживающие дозы.
При применении препарата Амиодарони возможны изменения на ЭКГ: удлинение интервала QT с возможным появлением зубца U. При появлении атриовентрикулярной блокады II и III степени, синоатриальной блокады, а также блокады ножек пучка Гиса лечение препаратом Амиодарон следует немедленно прекратить.
Прогрессирующая одышка и непродуктивный кашель могут быть признаками поражения легких. Рекомендуется проводить рентгенологическое исследование грудной клетки и легочные функциональные пробы (каждые 6 месяцев и в случае развития клинических признаков заболевания легких).
Перед началом терапии необходимо определить содержание электролитов плазмы крови. В период лечения препаратом Амиодарон регулярно проводят контроль активности ферментов печени. В период лечения периодически проводят анализ ЭКГ (ширина комплекса QRS и длительность интервала QT), трансаминаз (при повышении в 3 раза или удвоении в случае исходно повышенной их активности дозу уменьшают вплоть до полного прекращения терапии).
В процессе лечения следует проводить офтальмологическое исследование (выявление значительных отложений на роговице и нарушение зрения требуют отмены амиодарона). При отмене возможны рецидивы нарушений ритма.
Применение при беременности и в период лактации возможно только при угрожающих жизни нарушениях ритма при неэффективности другой антиа-ритмической терапии (вызывает дисфункцию щитовидной железы плода).
После отмены фармакодинамический эффект сохраняется в течение 10-30 дней.
Препарат содержит йод, поэтому может оказывать влияния на результаты тестов накопления радиоактивного йода в щитовидной железе. Поэтому перед началом лечения, во время его проведения и на протяжении нескольких месяцев после окончания лечения необходимо проводить исследования функции щитовидной железы. Перед проведением хирургических вмешательств, а также оксигенотерапии необходимо предупредить врача о применении препарата Амиодарон, поскольку отмечались редкие случаи развития острого респираторного дистресс-синдрома у взрослых в послеоперационном периоде.
Во избежание развития фотосенсибилизации пациентам следует избегать пребывания на солнце или использовать эффективные меры защиты.
Следует соблюдать осторожность при применении препарата во время проведения общей анестезии. возможен риск развития брадикардии. выраженного снижения артериального давления, нарушения проводимости и уменьшения ударного объема сердца.
В период лечения препаратом Амиодарон следует воздерживаться от вождения автотранспорта и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Противопоказан к применению во II и III триместре беременности, поскольку в этот период щитовидная железа новорожденного начинает аккумулировать йод, и применение амиодарона в этот период может спровоцировать развитие гипотиреоза из-за увеличения концентрации йода.
Амиодарон выделяется с грудным молоком в значительном количестве, по-этому препарат противопоказан к применению в период лактации.
Побочные действия:
Очень часто (≥ 10):
— нарушение вкуса;
— боль в эпигастральной области;
— отложение липофусцина в эпителии роговицы (часто субъективные жалобы при этом отсутствуют, но если отложения значительные и частично заполняют зрачок, возможны жалобы на появление цветных ореолов или нечеткость контуров);
— фотосенсибилизация (гиперемия кожи).
Часто (>1/100, <1/10):
— синусовая брадикардия (рефрактерная к холинолитикам);
— повышение уровня Т4 при нормальном или незначительно выраженном снижении Т3 (при отсутствии клинических признаков дисфункции щитовид-ной железы лечение прекращать не следует). При длительном применении возможно развитие гипотиреоза или гипертиреоза (необходимо отменить препарат);
— свинцово-синяя или голубоватая пигментация кожи (при длительном при-менении), после прекращения лечения пигментация медленно исчезает в течение 10-14 дней;
— экстрапирамидные расстройства;
— нарушение сна.
Не очень часто (>1/1 000, <1/100):
— синоатриальная блокада;
— АV блокада;
— «приливы» крови к коже лица;
— аритмогенное действие.
Редко (>1/10 000, <1/1 000):
— при длительном применении периферическая нейропатия. миопатия (симп-томы обратимы после отмены препарата).
Primary Menu
Глава 2 начинается с констатации факта, что анестезиологи проводят в операционных больше времени, чем врачи любой другой специальности. Одним из последствий этого является определенный риск осложнений, обусловленных длительным воздействием на анестезиолога следовых концентраций ингаляционных анестетиков. Было проведено несколько исследований, посвященных этой проблеме, но они значительно отличались по своей структуре, поэтому полученные данные оказались весьма противоречивыми и не позволили прийти к однозначным выводам. Вместе с тем можно сделать некоторые обобщения:
• У женщин-анестезиологов и анестезиологических сестер может быть немного повышен риск выкидышей и рождения детей с врожденными аномалиями.
• У женщин-анестезиологов и анестезиологических сестер может быть немного повышен риск злокачественных новообразований.
• У анестезиологов и среднего анестезиологического персонала может быть повышен риск заболеваний печени, причем не только за счет сывороточного гепатита.
• У женщин, работающих в операционной, может быть повышен риск заболеваний почек.
• У стоматологов и их помощников может быть повышен риск неврологических заболеваний вследствие постоянного контакта с закисью азота 1 .
Необходимо подчеркнуть, что ни одно из этих обобщений не подтверждено с абсолютной достоверностью. В экспериментах на животных не удалось выявить мутагенного, канцерогенного или те-ратогенного действия следовых концентраций современных ингаляционных анестетиков. Тем не менее из-за потенциального риска побочных эффектов Национальный Институт Профессиональной безопасности и Здравоохранения (National Institute for Occupatonal Safety and Health) считает допустимой концентрацию в воздухе операционной закиси азота менее 25 ppm (ppm — parts per million, т.е. количество частей газа на миллион частей смеси), а галогенсодержащих анестетиков — менее 0,5 ppm (менее 2 ppm в отсутствие закиси азота). Чтобы снизить концентрацию анестетиков в воздухе операционной до этого приемлемого уровня, необходимо использовать современные системы отвода использованных медицинских газов, обеспечить адекватную вентиляцию операционной, применять современные наркозные аппараты. Для определения следовых концентраций анестетиков в воздухе операционной необходимо специальное оборудование (например, инфракрасный анализатор, газовый хроматограф), поскольку большинство людей не может почувствовать запах ингаляционного анестетика в концентрации менее 30 ppm (особенно слаб запах закиси азота).
2. Инфекционные заболевания
Медицинский персонал больниц подвергается риску многих инфекционных заболеваний (например, вирусные заболевания верхних дыхательных путей, краснуха, туберкулез).
Герпетический панариций — воспаление пальца, обусловленное вирусом простого герпеса типа 1 и 2. Заражение обычно обусловлено проникновением контаминированной слюны через мелкие ранки и ссадины на руках анестезиолога. На месте входных ворот появляются болезненные пузырьки. Верификация диагноза: обнаружение гигантских эпителиальных клеток или ядерных включений при исследовании мазка материала, взятого из основания пузырьков; возрастание титра вируса простого герпеса; выявление вируса с помощью антисыворотки. Лечение: местное применение 0,5%-ной мази ацик-ловира. Профилактика: применение перчаток при манипуляциях в полости рта. Риск заболеть герпетическим панарицием особенно высок, если у больного какая-либо инфекция, иммунодефицит, злокачественное новообразование, нарушение питания.
1 На Западе его часто применяют в стоматологии для обезболивания. — Прим. пер.
Из дымка, образующегося при лазерном лечении кондиллом, папиллом и бородавок, выделена вирусная ДНК. В этом случае теоретически существует риск вирусной инфекции, который можно снизить системой удаления дымка, применением перчаток и высокоэффективных масок.
Очень серьезен риск попадания в кровь опасных для жизни вирусов гепатита В, гепатита С, вируса иммунодефицита человека (ВИЧ). Заражение этими болезнями может произойти при контакте с инфицированной слизистой, кожей, жидкостями организма, но чаще всего — при непреднамеренном уколе иглой, контаминированной инфицированной кровью. Риск заражения можно оценить, зная три фактора: распространенность инфекции в популяции больных; частота экспозиции (например, частота непреднамеренного укола иглой); частота серокон-версии после однократного контакта. Вероятность сероконверсии при контакте зависит от нескольких факторов: инфекционность возбудителя; тяжесть инфекции у больного; количество инфицированного материала, попавшего в организм медицинского работника; иммунный статус медицинского работника. Использование перчаток, безыгольных инъ-екторов и защищенных игл, позволяет снизить частоту некоторых (но не всех) повреждений.
Первая помощь при непреднамеренном уколе иглой заключается в обработке места укола антисептиком и оповещении соответствующего подразделения медицинского учреждения. Необходимо провести серологическое обследование медицинского работника и, по возможности, больного, при работе с которым произошло осложнение. Имму-ноглобулин оказывает некоторое защитное действие в отношении гепатита В. Эффективность применения зидовудина для профилактики ВИЧ-ин-фекции точно не установлена.
Выявление серологических маркеров гепатита В у анестезиологического персонала (15-50%) в несколько раз выше, чем в общей популяции (3-5%). Риск инфицирования пропорционален стажу работы. Летальность при фульминантном гепатите (который составляет 1 % от острых форм гепатита) достигает 60%. Хронические активные гепатиты ( 0 C.
Чем обусловлена экстренность операции?
При странгуляции вначале нарушается венозный отток от петли кишки, затем артериальный приток, после чего быстро развивается ишемия, инфаркт и перфорация стенки кишки. Острый перитонит может привести к выраженной дегидратации, сепсису, шоку и полиорганной недостаточности, что у пожилого больного с тяжелым заболеванием сердца сопряжено с неблагоприятным прогнозом. Несмотря на важность временного фактора, целесообразно не подавать больного в операционную сразу, а потратить несколько часов на оптимизацию ОЦК, водно-электролитного статуса и кровообращения. Кроме того, ввиду сложности и высокого риска осложнений требуется дополнительное время для подготовки лекарственных препаратов, наладки мониторов и другого анестезиологического оборудования.
Больного немедленно, без предварительной подготовки, доставили в свободную операционную, которая оборудована для операций на открытом сердце.
Какой мониторинг необходим в этом случае?
Учитывая недавно перенесенный инфаркт миокарда и имеющуюся сердечную недостаточность, целесообразно катетеризировать периферическую артерию и легочную артерию. Поскольку высока вероятность больших жидкостных сдвигов, показан непрерывный мониторинг АД. Кроме того, необходимо получать информацию, позволяющую судить о доставке кислорода к миокарду(АДдиаст ) и потребности миокарда в кислороде (АДсист. напряжение стенки ЛЖ, ЧСС). Вследствие дисфункции ЛЖ давление в ЛЖ и ПЖ могут изменяться непараллельно, поэтому мониторинг ЦВД не позволяет судить о функции ЛЖ и состоянии ОЦК; для этой цели следует применять мониторинг ДЗЛА. Очень информативна чреспищеводная ЭхоКГ, обеспечивающая раннюю диагностику ишемии миокарда и позволяющая оценить движения стенок ПЖ и ЛЖ.
Катетеризировать лучевую артерию достаточно легко. Катетеризация легочной артерии обеспечивает не непрерывный, а перемежающийся мониторинг ДЗЛА.
Какие лекарственные препараты, влияющие на сердечно-сосудистую систему, могут потребоваться во время индукции и поддержания анестезии?
Постоянная внутривенная инфузия нитроглицерина благоприятно влияет на соотношение между доставкой и потребностью кислорода в миокарде. Для урежения ЧСС целесообразно применять эсмолол, но из-за сопутствующей сердечной недостаточности это следует делать с осторожностью. Противопоказаны препараты, вызывающие тахикардию и выраженные колебания АД.
Была начата инфузия нитроглицерина, и во время стандартной тиопенталовой индукции анесте-
зии гемодинамика оставалась стабильной. В ходе лапаротомии отмечалось постепенное увеличение ЧСС и АД. Скорость инфузии нитроглицерина увеличили, после чего на ЭКГ отмечен подъем сегмента ST. ЧСС увеличилась до 130/мин, а АД до 220/140 мм.рт. ст. Кривая давления, получаемая от катетера Свана-Ганца, указывала на его расположение в правом желудочке. Была увеличена концентрация ингаляционного анестетика и начато дробное введение пропранолола по 1 мг в/в. В результате ЧСС снизилась до 115 уд/мин, но АД повысилось до 250/160 мм.рт. ст. Внезапно развилась желудочковая тахикардия с выраженным снижением АД. Был введен лидокаин и подготовлен к работе дефибрил-лятор, после чего желудочковая тахикардия сменилась фибрилляцией желудочков.
Как можно объяснить артериальную гипертонию, тахикардию и аритмию?
Дифференциальный диагноз при выраженной артериальной гипертонии и тахикардии включает феохромоцитому, злокачественную гипертермию и тиреотоксический криз. В данном случае было обнаружено, что удлинительная трубка, маркированная «нитроглицерин», по ошибке была подсоединена к инфузионному мешку с раствором адреналина.
Как объяснить парадоксальную реакцию на пропранолол?
Адреналин вызывает тахикардию (стимуляция 1 -адренорецепторов — прямое хронотропное действие; стимуляция 2 -адренорецепторов — опосредованное вазодилатацией увеличение ЧСС) pi подъем АД (стимуляция 1 -адренорецепторов). Пропранолол является неселективным -адреноблокатором, поэтому он устраняет тахикардию, обусловленную влиянием адреналина на -адренорецепторы. Пропранолол не влияет на вазоконстрикцию, обусловленную действием адреналина на 1 — адренорецеп-торы. Конечный итог введения пропранолола на фоне инфузии адреналина — снижение ЧСС и повышение АД.
Почему во время индукции анестезии не развилась артериальная гипотония?
Тот факт, что стандартная расчетная доза тио-пентала не привела к снижению АД у пожилого больного с дегидратацией и тяжелым сопутствующим заболеванием сердца, должен был вызвать удивление и навести на подозрения. Инфузия адреналина компенсировала гипотензивное действие тиопентала, так что гемодинамика оставалась стабильной.
Почему развилась желудочковая тахикардия?
Передозировка адреналина может вызвать опасные для жизни желудочковые аритмии. Высокая концентрация ингаляционного анестетика сенсибилизирует миокард к аритмогенному действию адреналина. Кроме того, расположенный в правом желудочке кончик катетера Свана-Ганца мог раздражать эндокард и пути проведения сердечного импульса.
Какие факторы способствовали этому осложнению анестезии?
Этому осложнению анестезии опосредованно способствовал ряд факторов: проведение операции в полночь (за рабочий день накопилась усталость врача); отсутствие предоперационной подготовки (невозможность оптимизации состояния больного); использование препаратов, подготовленных к работе другим анестезиологом; решение приступить к индукции анестезии и операции, несмотря на неправильное положение кончика катетера Свана-Ганца. Результатом этого стечения обстоятельств, неправильных решений и плохого состояния больного явился неблагоприятный исход.
Список литературы
Anderton JM, Keen RI, Neave R (editors): Positioning of Surgical Patient. Butterworths, 1988.
Berry AJ, Greene ES: The risk of needlestick injuries and needlestick-transmitted diseases in the practice of anesthesiology. Anesthesiology 1992;77:1007.
Bogner MS: Human Error in Medicine. Lawrence Erlbaum, 1994.
Brown DL (editor): Risk and Outcome in Anesthesia, 2nd ed. Lippincott, 1992.
Cheney FW et al: Standard of care and anesthesia liability. JAMA 1989;261:1599.
Eichhorn JH: Prevention of intraoperative anesthesia accidents and related severe injury through safety monitoring. Anesthesiology 1989;70:572.
Gravenstein N(editor): Manual of Complication during Anesthesia. Lippincott, 1991
Gravenstein JS, Holzer JF(editors): Safety and Cost Containment in Anesthesia. Butterworth, 1988.
Holzman RS: Latex allergy: An emerging operating room problem. Anesth Analg 1993; 76:635-41.
Kritchevsky SB, Simmons BP: Continuous quality im-rovement: concepts and applications for physician care. JAMA 1991; 266:1817.
Levy JH: Anaphylactic Reactions in Anesthesia and Intensive Care, 2nd ed. Butterworth-Heinemann, 1992.
Limn JN (editor): Epidemiology in Anaesthesia: The Techniques of Epidemiology Applied to anaesthetic Practice. Edward Arnold, 1986.
Martin JT: Compartment syndromes: Concept and perspectives for the anesthesiologist. Anesth Analg 1992;75:275.
Pierce E, Cooper J: Equipment-related anesthetic incidents. Int Anesthesiol CHn 1984;22:133.
Recommendations for Infection Control for the Practice of Anesthesiology. American Society of Anesthesiologists, 1992.
Silverstein JH, Silva DA, Iberti TJ: Opioid addiction in anesthesiology. Anesthesiology 1993;79:354.
Taylor TH, Major E (editors): Hazards and Comlica-tions of Anaesthesia, 2nd ed. Churchill Livingsto-ne,1993.
Weinger MB, Englund CE: Ergonomic and human factors affecting anesthetic vigilance and monitoring performance in the operating room environment. Anesthesiology 1990;73:995.