Спастичность: симптомы и лечение
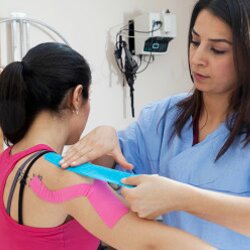 Понятие спастичности подразумевает определенное состояние мышц, при котором наблюдается ярко выраженный тонус, возрастающий при напряжении и вызывающий сопротивление при пассивном движении. Спастичность мешает свободно двигаться и говорить, пациент не может четко управлять своими конечностями.
Понятие спастичности подразумевает определенное состояние мышц, при котором наблюдается ярко выраженный тонус, возрастающий при напряжении и вызывающий сопротивление при пассивном движении. Спастичность мешает свободно двигаться и говорить, пациент не может четко управлять своими конечностями.
Точные причины появления спастичности до сих пор не изучены. Установлено, что спастичность проявляется при комбинированных поражениях некоторых структур головного и спинного мозга, что приводит к дисбалансу в нервных импульсах. Как правило, спастичность является следствием повреждения участков головного или спинного мозга.
Спастика наблюдается у пациентов:
-
после черепно-мозговой и спинальной травмы ; при гипоксии (недостатке кислорода); после инсульта ; после энцефалита и менингита; при адренолейкодистрофии; при фенилкетонурии; при рассеянном склерозе.
Симптомы спастичности
Спастичность проявляется непроизвольным подергиванием мышц. Ей также сопутствуют слабость и боль. При этом, боль не является постоянным спутником спастики. Чаще всего она появляется из-за резких движений, после которых следует спазм конечности, также боль может возникать при смене положения больного, например, когда его пытаются посадить.
Спастичные конечности не слушаются, становятся жесткими или, напротив, слабыми. Больной при спастичности мышц может чувствовать как сопротивление со стороны конечностей, так и слабость, что является последствием нервно-мышечной проводимости. При этом прием лекарственных средств может снять спастичность, но слабость в конечностях останется.
Другими симптомами спастичности являются клонусы, резкие сокращения отдельных мышц и их групп, проявляющиеся при растяжении, а также общая усталость и потеря ловкости.
В показаниях пациентов, как правило, спастичность определяется как «жесткость» мышц, слабость в конечностях, сопротивление конечности при сгибании.
Методы лечения спастичности
Спастика успешно поддается лечению. Существует несколько проверенных методов, облегчающих симптомы спастичности. После курса лечения спастичности проходит боль, снимается мышечный спазм, улучшается двигательная функция, благодаря чему больной может начать самостоятельно ухаживать за собой.
Физиотерапевтический метод лечения включает в себя гимнастику, массаж, иглорефлексотерапию. Больного учат менять положение: вставать, садиться, ходить. При этом задействуются ортопедические средства и аппараты, применяется бинтование конечностей и стимуляция мышц теплом или низкочастотными электрическими токами. Комплекс упражнений подбирается строго индивидуально, в зависимости от тяжести заболевания и проявления спастичности. Физиотерапия позволяет улучшить движения и снизить тонус мышц.
Более серьезным методом лечения спастичности является медикаментозная терапия. Как правило, она проводится с применением двух и более фармакологических препаратов, к числу которых относятся баклофен, датролен, габалептин, ботулинический токсин, бензодиазепины, имидазолин. Ботулинический токсин («Диспорт») вводится в мышцы паретичных конечностей для их расслабления. Действие такого препарата длится в течение 3-4 месяцев после введения.
Последним методом лечения спастичности является хирургическое вмешательство, при котором в спинномозговую жидкость вводится баклофен с помощью специальной ампулы с лекарством, вшитой под кожу в интратекальное пространство спинного мозга. Также существует еще один метод хирургического лечения спастичности – селективная дорсальная ризотомия. При ее проведении хирургическим путем пересекаются чувствительные нервные корешки. Данный метод используется в тяжелых случаях, когда спастичность мешает ходьбе.
Лечение спастичности может проходить только в специализированном учреждении, при этом оно включает в себя первоначальную диагностику и целый комплекс процедур, который проводится совместно различными специалистами в дополнение к основному курсу лечения.
В реабилитационном центре «Три сестры» созданы все условия для восстановления после черепно-мозговых и спинальных травм, инсульта и ДЦП. Специалисты центра индивидуально подходят к лечению каждого случая и бережно восстанавливают функции, утраченные пациентами после перенесенных травм и заболеваний. Центр известен не только высоким уровнем специалистов и качественным сервисом, но и теплым отношением к каждому пациенту, стремлением не только вылечить человека физически, но и сделать процесс восстановления комфортным и приятным.
Постинсультная спастичность
Двигательные нарушения у наших близких мы до сих пор почти не обсуждали, так как прямой связи с когнитивными расстройствами здесь нет, и не хотелось размывать основную тему нашего сайта. Однако недавнее обсуждение проблем, которые развиваются после инсульта, — а в России инсульт остается очень распространенной причиной развития деменции — показало, что эта тема важна.
Меня просили рассказать о ней без особой зауми, простыми словами. Я пообещал попробовать.
Читал в серьезном научном журнале, что после инсульта двигательные нарушения так или иначе проявляются у более чем 80% пациентов. Из–за гибели клеток, которые прежде регулировали работу мышц, они ослабевают (парез) либо выключаются полностью (паралич). Возможны также расстройство положения тела и координации движений. Это чревато падениями и – в лучшем случае – развивающимся страхом перед самостоятельной ходьбой, а в худшем – переломом. Появляющиеся вместе с этим «проблемы с головой» лишь увеличивают риски.
К счастью, даже в преклонном возрасте пластичность головного мозга позволяет ему перестроиться и постепенно восстановить утраченные двигательные функции. И здесь задача врачей (а после преодоления острого нарушения – и окружающих) создать необходимые условия для скорейшей реабилитации: основной метод — лечебная физкультура в сочетании с физио — и трудовой терапией.
Однако примерно в каждом третьем случае в постинсультный период начинает развиваться так называемая спастичность – повышенный тонус в мышце, мешающий ее растяжению и насильственно возвращающий конечность в определенное положение, что ограничивает общую подвижность. Спазм довольно плохо поддается физиотерапевтическому воздействию и препятствует нормальному восстановлению. Как оказалось, с таким явлением столкнулись и посетители нашего сайта.
Из–за постоянного тонуса, не снижающегося даже в состоянии покоя, начинают происходить изменения в мышцах, сухожилиях и суставах (фиброз, атрофия), развиваются болезненные деформации (контрактуры) и патологические позы, которые усугубляют проблему и серьезно осложняют жизнь пациенту.
Спастичность развивается не сразу, обычно – спустя несколько месяцев после инсульта. Впрочем, первые сигналы специалист может заметить уже через 2–3 недели. Изначально вялые мышцы приходят в тонус, который повышается и все сильнее проявляется при реакции на внешние стимулы (например, на попытку согнуть или разогнуть конечность). Через полгода, максимум год, спастичность превращается в проблему, которая заметно влияет на качество жизни пациента. Становится больно.
В верхней части туловища часто страдают плечо, локоть, запястье и пальцы. В нижней части тела спастичность может затронуть бедро, колено, лодыжку или пальцы ноги. В области руки обычно страдают мышцы–сгибатели, а на ноге – разгибатели.
Посмотрите на картинках из нашей газеты «Мемини».
Наверно, вы видели нечто подобное у больных с ДЦП.
Стоит ли говорить, что эта проблема плохо влияет на способность человека самостоятельно одеваться, питаться (просто не способен удерживать ложку), писать ручкой, страдает гигиена и т.д.
Если спастичность не лечить, то через 3–4 года формируются контрактуры — деформации суставов. Кости тоже деформируются. Возникают вынужденные болезненные позы.
О том, кто виноват, писать не буду. Сразу перехожу к вопросу «Что делать?».
Ответ простой: лечить.
Лечения спастичности может включать:
назначение лекарственных препаратов (центрального и местного действия),
физиотерапию,
эрготерапию.
(В редких случаях может быть принято решение о хирургическом лечении.)
Основу терапии составляет воздействие на мышцу, позволяющее снизить ее тонус. Ниже мы рассмотрим более подробно роль каждого из названных методов.
НАЗНАЧЕНИЕ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
В число пероральных (принимаемых через рот) лекарственных препаратов, наиболее часто используемых для уменьшения спастичности, входят:
миорелаксанты центрального действия – баклофен, тизанидин и др.
противосудорожные препараты – клоназепам, диазепам.
Обе группы препаратов помогают ослаблять сокращение мышцы и улучшать диапазон движения. Их прием снимает болезненные мышечные спазмы, усиливает действие лечебной физкультуры и вследствие этого предупреждает развитие контрактур. К сожалению, особенностью этих лекарств является то, что они действуют не только на спастичные мышцы, а на весь организм в целом. Для лечения спастичности эти препараты назначают в больших дозировках, что приводит к появлению побочных эффектов, в виде общей слабости, головокружений, изменений в настроении и заторможенности. Особенно неприятно это, если у больного после инсульта и без этого начинают развиваться когнитивные нарушения.
По этой причине всё больше специалистов склоняются к замене названных выше лекарств инъекциями ботулинического токсина типа А. По силе воздействия на мышцу ботулотоксин существенно превосходит все существующие лекарства, принимаемые в форме таблеток, и сопоставим с хирургическим вмешательством. При этом денервация мышцы при помощи токсина – предельно простая и безопасная процедура, которую может выполнять врач, прошедший соответствующее обучение. Препараты ботулотоксина хорошо переносятся, а вероятность межлекарственных взаимодействий при их использовании минимальна. В рекомендации Американской академии неврологии прямо указывается на необходимость предлагать пациентам ботулинический нейротоксин в качестве одного из методов снижения мышечного тонуса и улучшения пассивной функции у взрослых пациентов, страдающих спастичностью.
В нашей стране для лечения спастичности широко используются три препарата ботулотоксина: Ботокс (США), Диспорт (Англия), Ксеомин (Германия). Последний позиционируется производителем как препарат нового поколения, свободный от комплексообразующих белков. Кроме того, в России зарегистрирован китайский препарат Лантокс, но он, насколько я знаю, применяется преимущественно в косметологии.
ФИЗИОТЕРАПИЯ
Физиотерапия традиционно играет важную роль в лечении спастичности. К основным составляющим метода относят реабилитационные упражнения, массаж, иглорефлексотерапия, тепловое и электрическое воздействие на спастичные мышцы, применение ортопедических аппаратов.
Стандартная реабилитация предполагает ежедневное растяжение, помогающее восстанавливать силы в пораженных мышцах, поддерживать диапазон движения в суставе и предотвращать развитие контрактур. Регулярное растяжение может облегчить сокращение мышцы и уменьшить ригидность на период нескольких часов.
Важное место в процессе восстановления двигательных функций и в предупреждении патологических состояний занимает массаж. Он позволяет снимать боль, помогает восстанавливать работоспособности мышц, улучшает их кровоснабжение. Однако доверить выполнение массажа можно только спецалисту, так как спастические и гипотонические мышцы нуждаются в различном воздействии.
В России при комплексной терапии часто используется иглорефлексотерапия, однако контролируемые исследования, проведенные за рубежом, не показывают существенной эффективности этого метода лечения.
Электростимуляция широко используется для восстановления равновесия между тонусом мышц–сгибателей и мышц–разгибателей. Эффект обычно длится около 10 минут, когда стимуляция применяется впервые, но после нескольких месяцев подобных процедур эффект может быть более длительным. В качестве альтернативы спастичная мышца также может стимулироваться непосредственно для того, чтобы вызвать ее утомление.
В лечении спастичности могут использоваться фиксирующие конечность повязки, бандажи, жгуты, шины, ортезы. Они позволяют поддерживать и выравнивать спастичную конечность, а также исправлять ее деформацию и улучшать функции. Сегодня в медицинской инженерии разработано множество ортопедических приспособлений, обеспечивающих не только иммобилизацию и фиксацию в правильном положении, но также глубокое давление и поддержание тепла в тканях. Современные аппараты включают механизм настройки, управляющий необходимой функцией: от фиксации с помощью замка до обеспечения необходимых движения с посторонней помощью.
ЭРГОТЕРАПИЯ, ИЛИ ТЕРАПИЯ ТРУДОМ
Эрготерапия – это специально подобранные врачом практические действия, позволяющие пациенту восстанавливать навыки самообслуживания после инсульта. Можно считать это особым вариантом лечебной физкультуры, при котором у выполняемого упражнения появляется практический смысл: застегнуть пуговицу, использовать столовые прибор… С помощью трудотерапии – путем регулярного повторения одних и тех же движений – пациенты восстанавливают утраченные навыки повседневной жизни, когда это возможно. В противном случае, когда восстановить какие–то важные действия не удается, трудотерапия позволяет выбрать приспособления, компенсирующие потерю полезного навыка, либо сформировать новые двигательные модели, альтернативные тем, что использовались до заболевания.
Другим словами, функциональная терапия направлена на сохранение всех функций конечности через восстановление старых двигательных моделей и/или создание новых динамических стереотипов на основе нового расположения мышц, позволяющего нормальное выполнение движений. Важную роль здесь играет не только прилежание больного, но и помощь ухаживающего за ним лица.
ХИРУРГИЧЕСКОЕ ВМЕШАТЕЛЬСТВО
Две основные категории хирургических вмешательств, применяемых при спастичности, выполняются на уровне нервной системы (нейрохирургия) или костей, сухожилий и мышц (ортопедическая хирургия). Наиболее значимым показанием для хирургического лечения выступает развитие контрактуры. В этом случае ортопедическая хирургия нередко единственный метод лечения спастичности. С помощью операции мышцы можно денервировать, сухожилия и мышцы можно освобождать от контрактур, удлинять или перемещать, снижая тем самым спастичность. Мышцы могут быть денервированы методом отсечением определенных нервов в местах выхода из спинного мозга (дорсальная ризотомия). Эта операция используется в основном для лечения тяжелой спастичности мышц ног, мешающей передвижению пациента.
Если кратко суммировать, то идеальный вариант — расслабить ботулиническим токсином (действует примерно 3–4 месяца) и разрабатывать. Вот только цены.
Хотя я читал два исследования. В одном авторы доказывали, что если посчитать те расходы, которых можно избежать благодаря ботулино терапии (сиделка, вспомогательные средства), то в целом получается даже выгодно. В другом научным языком сказано примерно следующее: лучше потратиться и получить результат, чем пить в больших дозах таблетки (у нас они, кстати, тоже не бесплатные), без особых успехов.
Правда, оба исследования проводились за рубежом.
Постинсультная спастичность
РЕКЛАМА
В России более миллиона больных, перенесших инсульт. Более чем у половины из них остаются после него двигательные нарушения, которые существенно снижают качество жизни и способствуют стойкой инвалидности (инвалидизации) пациентов [1]: чаще всего это гемипарез или монопарез конечности с повышением мышечного тонуса по типу спастичности [1, 2, 9, 20].
Патогенез постинсультной спастичности
Спастичность выявляется при исследовании пассивных движений в паретичной конечности как повышенное сопротивление (сокращение) мышцы при ее быстром растяжении. Развитие спастичности при центральном парезе конечности связывается со снижением тормозных влияний на спинальные мотонейроны и интернейроны, что приводит к увеличению числа импульсов, достигающих альфа-мотонейронов в ответ на растяжение мышцы. Снижение тормозных влияний на спинальные мотонейроны и интернейроны объясняется комбинированным поражением пирамидных и экстрапирамидных путей внутри головного мозга вследствие инсульта, при этом важную роль в развитии спастичности отводят повреждению кортико-ретикуло-спинального тракта [2, 16, 20].
В экспериментальных исследованиях показано, что изолированное поражение пирамидного пути не вызывает спастичности, а приводит лишь к парезу в дистальных отделах конечностей, особенно утрате тонких движений руки. В случаях поражения головного мозга при инсульте обычно возникает поражение не только пирамидного пути, но и других двигательных путей, таких как кортико-ретикуло-спинальный тракт, что и сопровождается спастичностью. Поэтому постинсультная спастичность рассматривается как комбинированное поражение пирамидных и экстрапирамидных структур внутри головного мозга [2, 16, 20]. Экстрапирамидная система внутри головного мозга может быть повреждена вследствие поражения самих базальных ганглиев или приходящих либо исходящих от них путей.
В развитии церебральной спастичности при поражении головного мозга большую роль играет ослабление тормозных влияний преимущественно на альфа-мотонейроны, обеспечивающих движение антигравитационных мышц; это объясняет появление характерных проявлений постинсультного спастического гемипареза: приведение плеча, сгибание руки в локтевом и лучезапястном суставах, приведение бедра, разгибание колена и подошвенное сгибание в голеностопном суставе [2, 16, 20].
У больных инсультом спастичность обычно нарастает в паретичных конечностях в течение нескольких недель и месяцев, сравнительно редко (чаще всего при восстановлении двигательных функций) наблюдается спонтанное уменьшение спастичности. Во многих случаях у больных инсультом спастичность ухудшает двигательные функции, способствует развитию контрактуры и деформации конечности, затрудняет уход за обездвиженным больным и иногда сопровождается болезненными мышечными спазмами [2, 5, 9, 11, 20].
Если постинсультный парез сохраняется в течение длительного времени (несколько месяцев и более), то могут возникнуть структурные изменения сегментарного аппарата спинного мозга (укорочение дендритов альфа-мотонейронов и коллатеральный спрутинг афферентных волокон, входящих в состав задних корешков), которые способствуют прогрессированию спастичности [16]. Также развиваются вторичные изменения в паретичных мышцах, сухожилиях и суставах, которые усиливают двигательные расстройства и сопротивление, возникающее в мышце при ее растяжении, что необходимо учитывать при оценке мышечного тонуса в паретичных или парализованных конечностях [16, 20].
Восстановление утраченных двигательных функций максимально в течение двух-трех месяцев с момента инсульта, в дальнейшем темпы восстановления снижаются значительно. Через год после развития инсульта маловероятно уменьшение степени пареза, однако возможно улучшение двигательных функций и уменьшение инвалидности путем тренировки равновесия и ходьбы, использования специальных приспособлений для передвижения и снижения спастичности в паретичных конечностях [1, 2, 9, 11, 20].
Лечение постинсультной спастичности
Лечение постинсультной спастичности направлено на улучшение функциональных возможностей паретичных конечностей, ходьбы, самообслуживания больных. К сожалению, в части случаев возможности лечения спастичности ограничиваются только уменьшением боли и дискомфорта, связанного с высоким мышечным тонусом, облегчением ухода за парализованным пациентом или устранением имеющегося косметического дефекта, вызванного высоким мышечным тонусом [2, 11, 20].
Один из наиболее важных вопросов, который приходится решать при ведении больного с постинсультной спастичностью, сводится к следующему: ухудшает или нет спастичность функциональные возможности больного? В целом, функциональные возможности конечности у больного с постинсультным парезом конечности хуже при наличии выраженной спастичности, чем при ее легкой степени. Вместе с тем у части больных при выраженной степени пареза спастичность в мышцах ноги может облегчать стояние и ходьбу, а ее снижение может привести к ухудшению двигательной функции и даже к падениям [2, 11, 16, 20]. Перед лечением постинсультной спастичности необходимо определить возможности лечения у конкретного больного (улучшение двигательных функций, уменьшение болезненных спазмов, облегчение ухода за пациентом и др.) и обсудить их с пациентом и/или его родственниками. Возможности лечения во многом определяются сроками с момента заболевания и степенью пареза, наличием когнитивных расстройств [2, 11, 16, 20]. Чем меньше сроки с момента развития инсульта, вызвавшего спастический парез, тем более вероятно улучшение от лечения спастичности, потому что оно может привести к существенному улучшению двигательных функций, предотвратив формирование контрактур и повысив эффективность реабилитации в период максимальной пластичности центральной нервной системы. При длительном сроке заболевания менее вероятно существенное улучшение двигательных функций, однако можно значительно облегчить уход за больным и снять дискомфорт, вызванный спастичностью. Чем меньше степень пареза в конечности, тем более вероятно, что лечение спастичности улучшит двигательные функции [16, 20].
Лечебная гимнастика представляет наиболее эффективное направление ведения больного с постинсультным спастическим гемипарезом, она направлена на тренировку движений в паретичных конечностях и предотвращение контрактур [1, 2, 16, 20]. Однако больным, имеющим выраженную спастичность в сгибателях верхних конечностей, не следует рекомендовать интенсивные упражнения, которые могут значительно усилить мышечный тонус (например, сжимание резинового кольца или мяча, использование эспандера для развития сгибательных движений в локтевом суставе).
В качестве методов физиотерапии используются лечение положением, обучение пациентов стоянию, сидению, ходьбе (с помощью дополнительных средств и самостоятельно), бинтование конечности, применение ортопедических аппаратов, тепловые воздействия на спастичные мышцы, а также электрическая стимуляция определенных мышечных групп (например, разгибателей пальцев кисти или передней большеберцовой мышцы [4]).
Массаж мышц паретичных конечностей, имеющих высокий мышечный тонус, возможен только в виде легкого поглаживания. Напротив, в мышцах-антагонистах можно использовать растирание и неглубокое разминание в более быстром темпе.
Иглорефлексотерапия относительно часто используется в нашей стране в комплексной терапии больных, имеющих постинсультный спастический гемипарез, однако контролируемые исследования, проведенные за рубежом, не показывают существенной эффективности этого метода лечения [8].
У больных, перенесших инсульт и имеющих локальную спастичность в паретичных мышцах, можно использовать ботулинический токсин типа А или ботулотоксин (Ботокс, Диспорт). Использование ботулинического токсина показано, если у больного, перенесшего инсульт, имеется мышца с повышенным тонусом без контрактуры, а также отмечаются боль, мышечные спазмы, снижение объема движений и нарушение двигательной функции, связанные со спастичностью этой мышцы [2–4, 17, 20]. Действие ботулинического токсина при внутримышечном введении вызвано блокированием нервно-мышечной передачи, обусловленным подавлением высвобождения нейромедиатора ацетилхолина в синаптическую щель.
Клинический эффект после инъекции ботулинического токсина отмечается спустя несколько дней и сохраняется в течение 2–6 месяцев, после чего может потребоваться повторная инъекция. Лучшие результаты отмечаются при использовании ботулинического токсина в ранние сроки (до года) с момента заболевания и легкой степени пареза конечности. Применение ботулинического токсина может быть особенно эффективно в тех случаях, когда имеется эквино-варусная деформация стопы, вызванная спастичностью задней группы мышц голени, или высокий тонус мышц-сгибателей запястья и пальцев, ухудшающий двигательную функцию паретичной руки [20]. В контролированных исследованиях доказана эффективность Диспорта при лечении постинсультной спастичности в руке [3].
В качестве побочных эффектов от использования ботулотоксина могут быть кожные изменения и боли в месте инъекции. Они обычно самостоятельно регрессируют в течение нескольких дней после инъекции. Возможна значительная слабость мышцы, в которую введен ботулотоксин, а также слабость в мышцах, расположенных близко к месту инъекции, локальная вегетативная дисфункция. Однако мышечная слабость обычно компенсируется деятельностью агонистов и не приводит к ослаблению двигательной функции. Ограничение широкого применения ботулинического токсина в клинической практике во многом вызвано его высокой стоимостью.
Хирургические операции для уменьшения постинсультной спастичности используются редко, они возможны на четырех уровнях — на головном мозге (электрокоагуляция бледного шара, вентролатерального ядра таламуса или мозжечка), спинном мозге (селективная задняя ризотомия), периферических нервах (рассечение периферических нервов) и мышцах или их сухожилиях [2, 16, 20].
С помощью специальной помпы интратекально при постинсультной спастичности может использоваться баклофен [10, 13, 19]. Использование баклофеновой помпы в сочетании с лечебной гимнастикой, физиотерапией улучшает скорость и качество ходьбы больных с постинсультной спастичностью, способных к самостоятельному передвижению [10]. Имеющийся 15-летний клинический опыт применения баклофена интратекально у больных, перенесших инсульт, свидетельствует о высокой эффективности этого метода в уменьшении не только степени спастичности, но и болевых синдромов и дистонических расстройств [19]. Отмечено положительное влияние баклофеновой помпы на качество жизни больных, перенесших инсульт [13]. Широкое применение этого метода терапии в клинической практике ограничивает его высокая стоимость.
Лечение пероральными антиспастическими средствами
В клинической практике для лечения постинсультной спастичности наиболее часто используются пероральные антиспастические лекарственные средства [5, 11, 12, 16]. Применяемые внутрь антиспастические средства, уменьшая мышечный тонус, могут улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить действие лечебной физкультуры и вследствие этого предупредить развитие контрактур. При легкой степени спастичности применение миорелаксантов может привести к значительному положительному эффекту, однако при выраженной спастичности могут потребоваться большие дозы миорелаксантов, применение которых нередко вызывает нежелательные побочные эффекты [2, 5, 11, 20]. Лечение миорелаксантами начинают с минимальной дозы, затем ее медленно повышают для достижения эффекта. Антиспастические средства обычно не комбинируют. В нашей стране для лечения постинсультной спастичности наиболее часто используют баклофен (Баклосан), тизанидин (Сирдалуд) и толперизон (Мидокалм).
Баклофен (Баклосан) оказывает антиспастическое действие преимущественно на спинальном уровне. Препарат представляет аналог гамма-аминомасляной кислоты (ГАМК); он связывается с пресинаптическими ГАМК-рецепторами, приводя к уменьшению выделения возбуждающих аминокислот (глутамата, аспартата) и подавлению моно- и полисинаптической активности на спинальном уровне, что и вызывает снижение спастичности. Препарат оказывает также умеренное центральное анальгезирующее действие. Баклофен используется при спинальной (спинальная травма, рассеянный склероз) и церебральной спастичности различного генеза [5, 11, 16]. Начальная доза составляет 5–15 мг/сут (в один или три приема), затем дозу увеличивают на 5 мг каждый день до получения желаемого эффекта; препарат принимают во время еды. Максимальная доза баклофена для взрослых составляет 60–75 мг/сут. Побочные эффекты чаще проявляются сонливостью, головокружением в начале лечения, хотя в дальнейшем могут ослабевать. Иногда возникают тошнота, запор, диарея, артериальная гипотония; требуется осторожность при лечении больных пожилого возраста, перенесших инсульт.
Тизанидин (Сирдалуд) — миорелаксант центрального действия, агонист альфа-2-адренергических рецепторов. Препарат снижает спастичность вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот и активацией глицина, снижающего возбудимость интернейронов спинного мозга. Тизанидин (Сирдалуд) обладает также умеренным центральным анальгезирующим действием. Препарат эффективен при церебральной и спинальной спастичности, а также при болезненных мышечных спазмах [5, 11, 12, 15, 16, 20]. Начальная доза препарата составляет 2–6 мг/сут в один или три приема, средняя терапевтическая доза — 12–24 мг/сут, максимальная доза — 36 мг/сут. В качестве побочных эффектов могут возникать сонливость, сухость во рту, головокружение и незначительное снижение артериального давления, что ограничивает использование препарата при постинсультной спастичности [15].
Толперизон (Мидокалм) — мышечный релаксант центрального действия, который близок к лидокаину по химической структуре и стабилизирует мембраны нервных клеток. Толперизон снижает активность спинальных нейронов, участвующих в формировании спастичности, путем ограничения потока натрия через мембрану нервных клеток. Наиболее часто используется по 300–450 мг/сут в два или три приема. Около 40 лет толперизон успешно применялся при лечении спастичности различного генеза, были проведены небольшие исследования, показавшие его эффективность при церебральной спастичности [7, 14].
Недавно было проведено плацебо-контролируемое исследование [18], в котором показана эффективность, безопасность и хорошая переносимость толперизона у больных, перенесших инсульт и имеющих спастичность в паретичных конечностях. В многоцентровое исследование (два центра в Германии и один центр в Болгарии) было включено 120 больных (43 мужчины и 77 женщин) в возрасте от 20 до 78 лет (средний возраст — 63 года) с постинсультной спастичностью. Больные перенесли инсульт в сроки от 3 месяцев до 30 лет (в среднем 3,3 года с момента инсульта) и имели спастичность, выраженность которой достигала 2 баллов и более по шкале Эшуорта в одной или нескольких мышечных группах. У большинства (111 из 120) больных наблюдался гемипарез со спастичностью в верхней и нижней конечности, средняя степень спастичности составила 3 балла по шкале Эшуорта. По основным клиническим характеристикам группа больных, которые принимали толперизон, не отличалась от группы плацебо. В течение четырех недель больные получали толперизон или плацебо, доза которых подбиралась врачом для получения максимального эффекта и могла достигать от 300 до 900 мг толперизона. Далее больные продолжали принимать толперизон или плацебо в течение еще двух месяцев (восьми недель).
Главной целью исследования было изучение влияния толперизона на выраженность спастичности по шкале Эшуорта через 4 недели лечения (в сравнении с плацебо). Дополнительные цели исследования включали изучение влияния толперизона на ежедневную двигательную активность (по пятибалльной шкале), ходьбу в течение двух минут, максимальное расстояние при ходьбе (при спастичности в нижних конечностях), индекс Бартел, общее впечатление врача и больного о лечении.
Результаты проведенного исследования показали, что толперизон достоверно (р
Результаты проведенного исследования также показали тенденцию к улучшению ежедневной активности больных, получавших толперизон (р = 0,053). В конце лечения увеличилось расстояние, которое больные проходили за 2 минуты при приеме толперизона. По завершении исследования было установлено, что толперизон уменьшает степень инвалидности больных, оцениваемую по индексу Бартел. В среднем общий балл по индексу Бартел увеличился на 5,3 балла в группе толперизона и только на 1,7 балла в группе плацебо. Общая оценка эффективности лечения больными и врачами была достоверно выше в группе толперизона (р
В результате проведенного исследования отмечены хорошая переносимость и безопасность применения толперизона у больных, перенесших инсульт. В группе больных, принимавших толперизон, не отмечено серьезных нежелательных эффектов; побочные эффекты в группе толперизона возникали не чаще, чем в группе плацебо. Ни один из больных, получавших толперизон (62% больных получали препарат в дозе более 600 мг/сут), не прекратил лечение вследствие побочных эффектов. Полученные данные согласуются с результатами ранее проведенного исследования, показавшего отсутствие седативного эффекта при однократном и продолжительном приеме толперизона [6].
В целом авторы проведенного исследования отмечают эффективность толперизона при ведении больных с постинсультной спастичностью [18]. Применение толперизона не только снижает степень спастичности, но и улучшает ежедневную активность больных в повседневной жизни, облегчает их уход за собой при отсутствии нежелательных явлений, что выгодно отличает его от применения других антиспастических средств. Лечение толперизоном целесообразно начинать с суточной дозы 300 мг, которая при необходимости может быть увеличена до 900 мг/сут без существенных побочных эффектов.
Таким образом, ведущую роль в лечении постинсультной спастичности имеет лечебная гимнастика, которая должна начинаться уже с первых дней развития инсульта и быть направлена на тренировку утраченных движений, самостоятельное стояние и ходьбу, а также профилактику прогрессирования спастичности и развития контрактур. При локальной спастичности, вызывающей ухудшение двигательных функций, может быть эффективным локальное введение препаратов ботулинического токсина (Ботокса или Диспорта). В качестве пероральных лекарственных средств могут использоваться баклофен (Баклосан), тизанидин (Сирдалуд) и толперизон (Мидокалм). Результаты одного из последних многоцентровых плацебо-контролируемых исследований показывают эффективность, безопасность и хорошую переносимость толперизона при лечении постинсультной спастичности. Применение толперизона не только снижает выраженность постинсультной спастичности, но и улучшает ежедневную двигательную активность больных, их адаптацию в повседневной жизни при хорошей переносимости лечения.
Дамулин И. В. Парфенов В. А. Скоромец А. А. Яхно Н. Н. Нарушения кровообращения в головном и спинном мозге. В кн. Болезни нервной системы. Руководство для врачей / под ред. Н. Н. Яхно. М. Медицина, 2005, Т. 1. С. 232–303.
Парфенов В. А. Спастичность. В кн. Применение ботокса (токсина ботулизма типа А) в клинической практике: руководство для врачей / под ред. О. Р. Орловой, Н. Н. Яхно. М. Каталог, 2001. С. 91–122.





светлана 56 лет У меня случился инсульт год назад .Спастичность левой стороны тела началась на 2-й месяц и продолжается на протяжениигода .Принимала большое количество лекарств:медокалм, сердалуд, баклофен, тебантин., сделала 3 раза уклы ксеомина. Облгчение приносит только тебантин Дорогие уколы ботулотоксина не действуют никак, но я продолжаю их делать в надежде на положительный результат, а без тебантина не могу прожить и дня сразу скручивает пальцы на ногах и на руках.Постоянно занимаюсь ЛФ , только это и спасает+ тебантин утром и на ночь