Современное медикаментозное лечение стабильной ишемической болезни сердца (новые американские рекомендации по диагностике и лечению стабильной ишемической болезни сердца, 2012 г.)
Лупанов В.П.
В декабре 2012 г. в Journal of the American College of Cardiology опубликованы новые практические рекомендациям по диагностике и лечению больных стабильной ишемической болезнью сердца (ИБС) [1].
В редакционный комитет по подготовке рекомендаций вошли: Американский колледж кардиологии (ACCF), Американская ассоциация сердца (AHA), Американский колледж врачей (АСР), Американская ассоциация по торакальной хирургии (AATS), профилактическая ассоциация медицинских сестер (PCNA), Общество сердечно–сосудистой ангиографии и интервенционных вмешательств (SCAI), Общество торакальных хирургов (STS). Рекомендации содержат 120 страниц, 6 глав. 4 приложения, список литературы – 1266 источников.
В главе 4 этих рекомендаций рассмотрены вопросы медикаментозного лечения стабильной ИБС. В настоящей статье рассматриваются только вопросы медикаментозного лечения стабильной ИБС.
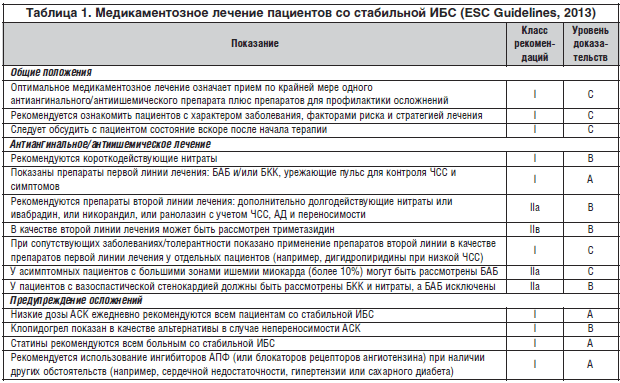
Рекомендации по лечению стабильной ИБС должны помочь практическим врачам принять правильные решения в различных клинических ситуациях. Для этого важно ориентироваться в классе рекомендаций (I, II, III) и уровнях доказательности (A, B, C) каждого из рекомендуемых вмешательств (табл. 1).
Пациентам со стабильной ИБС должно быть проведено лечение согласно рекомендациям (руководству) направленной медикаментозной терапии – guideline–directed medical therapy (GDMT) (новый термин, означающий оптимальную медикаментозную терапию, как это было определено ACCF/AHA; в первую очередь это относится к I классу рекомендаций).
Пакет рекомендаций GDMT содержит изменение образа жизни, прием препаратов, которые, как было показано, улучшают прогноз, и включает в себя (в соответствующих случаях):
– диету, снижение веса и регулярную физическую активность;
– если пациент курильщик – отказ от курения;
– прием ацетилсалициловой кислоты (АСК) 75–162 мг ежедневно;
– прием статинов в умеренных дозах;
– если пациент гипертоник – антигипертензивная терапия до достижения АД<140/90 мм рт.ст.;
– если пациент диабетик – надлежащий контроль гликемии .
Традиционные модифицируемые факторы риска развития ИБС – курение, артериальная гипертония, дислипидемия, сахарный диабет и ожирение – отмечаются у большинства пациентов и связаны с высоким коронарным риском. Поэтому влияние на основные факторы риска: контроль диеты, физическая нагрузка, лечение диабета, гипертензии и дислипидемии (4.4.1.1), прекращение курения и снижения веса должны быть частью общей стратегии лечения всех больных стабильной ИБС.
4.4.1. Модификация факторов риска
4.4.1.1. Влияние на липиды крови
Класс I
1. Модификация образа жизни, в том числе ежедневная физическая активность, настоятельно рекомендуется для всех пациентов со стабильной ИБС (уровень доказательности В).
2. Диетическая терапия для всех пациентов должна включать уменьшение потребления насыщенных жиров (<7% от общей калорийности), трансжирных кислот (<1% от общей калорийности) и общего холестерина (<200 мг/дл) (уровень доказательности В).
3. В дополнение к терапевтическим изменениям образа жизни следует назначать умеренные или высокие дозы статинов в отсутствие противопоказаний и документированных побочных эффектов (уровень доказательности А).
Класс IIa
1. Для пациентов, которые не переносят статины, целесообразно снижение холестерина липопротеинов низкой плотности с помощью секвестрантов желчных кислот (СЖК)*, ниацина** или их комбинации (уровень доказательности В).
Приводим резюме американских клинических рекомендаций, состоящих из медикаментозной терапии с целью предотвращения инфаркта миокарда и смерти (4.4.2) и терапии для облегчения синдромов (4.4.3).
4.4.2. Рекомендации
по дополнительной медикаментозной терапии для предотвращения
инфаркта миокарда и смерти
у больных стабильной ИБС
4.4.2.1. Антитромбоцитарная терапия
Класс I
1. Лечение АСК в дозе 75–162 мг ежедневно должно быть продолжено на неопределенный срок в отсутствие противопоказаний у пациентов со стабильной ИБС (уровень доказательности А).
2. Лечение клопидогрелом является разумным в тех случаях, когда АСК противопоказана пациентам со стабильной ИБС (уровень доказательности B).
Класс IIb
1. Лечение АСК в дозах от 75 до 162 мг ежедневно и клопидогрелом 75 мг/сут. может быть разумным у некоторых пациентов со стабильной ИБС высокого риска (уровень доказательности В).
Класс III
1. Дипиридамол не рекомендуется в качестве антиагрегантной терапии для пациентов со стабильной ИБС (уровень доказательности В).
4.4.2.2. Терапия b–блокаторами
Класс I
1. Терапия β–блокаторами должна быть начата и продолжаться в течение 3–х лет у всех пациентов с нормальной функцией левого желудочка после инфаркта миокарда или острого коронарного синдрома (уровень доказательности В).
2. β–блокаторы следует применять у всех больных с систолической дисфункцией левого желудочка (ФВ≤40%), сердечной недостаточностью или до инфаркта миокарда, если нет противопоказаний (рекомендуется использование карведилола, метопролола сукцината или бисопролола, которые, как было показано, снижают риск смерти (уровень доказательности А).
Класс IIb
1. β–блокаторы могут рассматриваться как хроническая терапия для всех других пациентов с ИБС или другими сосудистыми заболеваниями (уровень доказательности С).
4.4.2.3. Ингибиторы АПФ и блокаторы
рецепторов ангиотензина
(ренин–ангиотензин–альдостерон–блокаторы)
Класс I
1. Ингибиторы АПФ следует назначать всем больным со стабильной ИБС, которые также имеют гипертонию, сахарный диабет, ФВ левого желудочка 40% и меньше или хронические заболевания почек, если нет противопоказаний (уровень доказательности А).
2. Блокаторы рецепторов ангиотензина рекомендуются для пациентов со стабильной ИБС, которые имеют гипертонию, сахарный диабет, систолическую дисфункцию левого желудочка или хроническое заболевание почек и показания для ингибиторов АПФ, но их не переносят (уровень доказательности А).
Класс IIa
1. Лечение ингибитором АПФ разумно у пациентов как со стабильной ИБС, так и другими сосудистыми заболеваниями (уровень доказательности В).
2. Блокаторы рецепторов ангиотензина целесообразно использовать и у других пациентов, которые не переносят ингибиторы АПФ (уровень доказательности С).
4.4.2.4. Вакцинация против гриппа
Класс I
1. Ежегодная вакцинация против гриппа рекомендуется пациентам со стабильной ИБС (особенно в зимний период: январь–апрель) (уровень доказательности В).
4.4.2.5. Дополнительная терапия для снижения риска развития инфаркта миокарда и смерти
Класс III. Польза не доказана.
1. Терапия эстрогенами не рекомендуется у женщин в постменопаузе со стабильной ИБС с целью снижения сердечно–сосудистого риска или улучшения клинических исходов (уровень доказательности А).
2. Витамин С, витамин Е и β–каротин не рекомендуются с целью снижения сердечно–сосудистого риска или улучшения клинических исходов у пациентов со стабильной ИБС (уровень доказательности А).
3. Лечение повышенного уровня гомоцистеина фолиевой кислотой, витаминами В6 и В12 с целью снижения сердечно–сосудистого риска или улучшения клинических исходов у пациентов со стабильной ИБС не рекомендуется (уровень доказательности А).
4. Терапия хелатами (внутривенное введение ЕDТА – ethylene diamine tetraacetic acid) с целью улучшения симптомов или снижения сердечно–сосудистого риска у пациентов со стабильной ИБС не рекомендуется (уровень доказательности С).
5. Лечение чесноком, коэнзимом Q10, селеном и хромом с целью снижения сердечно–сосудистого риска или улучшения клинических исходов у пациентов со стабильной ИБС не рекомендуется (уровень доказательности С).
4.4.3. Медикаментозная терапия
для облегчения симптомов
4.4.3.1. Терапия антиишемическими
препаратами
Класс I
1. β–блокаторы следует назначать в качестве начальной терапии для облегчения симптомов у пациентов со стабильной ИБС (уровень доказательности B).
2. Блокаторы кальциевых каналов или длительно действующие нитраты следует назначать для купирования симптомов, когда β–блокаторы противопоказаны или вызывают неприемлемые побочные эффекты у пациентов со стабильной ИБС (уровень доказательности B).
3. Блокаторы кальциевых каналов или длительно действующие нитраты в комбинации с β–блокаторами должны быть назначены для облегчения симптомов в случаях, когда при начальной терапии β–блокаторами отсутствует их эффективность у пациентов со стабильной ИБС (уровень доказательности B).
4. Сублингвальный прием нитроглицерина или нитроглицерина спрей рекомендуется для немедленного облегчения стенокардии у пациентов со стабильной ИБС (уровень доказательности B).
Класс IIa
1. Лечение длительно действующими недигидропиридиновыми блокаторами кальциевых каналов (верапамил или дилтиазем) разумно для облегчения симптомов при недостаточной эффективности β–блокаторов в качестве начальной терапии у пациентов со стабильной ИБС (уровень доказательности B).
2. Лечение ранолазином может быть полезно, когда назначается в качестве замены для β–блокатора с целью облегчения симптомов у пациентов со стабильной ИБС, если начальное лечение β–блокатором приводит к неприемлемым побочным эффектам или является неэффективным, либо первоначальное лечение β–блокатором противопоказано (уровень доказательности В).
3. Лечение ранолазином в комбинации с β–блокаторами у пациентов со стабильной ИБС может быть полезным для облегчения симптомов, когда при начальной монотерапии β–блокатором оно неэффективно (уровень доказательности А).
Рассмотрим антиангинальные препараты, которые применяются либо не одобрены к применению в США в новых американских рекомендациях по лечению стабильной ИБС 2012 г. Различные уровни доказательств эффективности новых фармакологических средств в целом сильно различаются, препараты не лишены побочных эффектов, особенно у пожилых больных и при комбинированном назначении с другими препаратами.
4.4.3.1.4. Ранолазин – частичный ингибитор окисления жирных кислот, у которого установлены антиангинальные свойства. Он является селективным ингибитором поздних натриевых каналов, которые предотвращают перегрузку внутриклеточным кальцием – негативным фактором при ишемии миокарда. Ранолазин снижает сократимость, жесткость миокардиальной стенки, оказывает антиишемический эффект и улучшает перфузию миокарда без изменения сердечного ритма и АД. Антиангинальная эффективность ранолазина была показана в трех исследованиях у больных ИБС со стабильной стенокардией (МАRISA, CARISA, ERICA) [2]. Препарат метаболического действия, снижает потребность миокарда в кислороде, он показан для применения в сочетании с традиционной антиангинальной терапией у тех пациентов, у которых остаются симптомы при приеме традиционных средств [3,4]. По сравнению с плацебо ранолазин снижал частоту приступов стенокардии и увеличивал толерантность к физической нагрузке в большом исследовании у пациентов со стенокардией, перенесших острый коронарный синдром (MERLIN–TIMI) [5].
С 2006 г. ранолазин применяется в США и в большинстве европейских стран. При приеме препарата может происходить удлинение интервала QT на ЭКГ (приблизительно на 6 миллисекунд на максимально рекомендуемой дозе), хотя это не считается ответственным за феномен torsades de pointes, особенно у пациентов, которые испытывают головокружение [2,6]. Ранолазин также снижает гликированный гемоглобин (HbA1c) [7] у больных с сахарным диабетом, но механизм и последствия этого пока не установлены. Комбинированная терапия ранолазином (1000 мг 2 раза/сут.) с симвастатином увеличивает концентрацию в плазме симвастатина и его активного метаболита в 2 раза. Ранолазин хорошо переносится, побочные эффекты – запор, тошнота, головокружение и головная боль – встречаются редко [8]. Частота синкопе при приеме ранолазина – менее 1%.
4.4.3.1.5.1. Никорандил. Молекула никорандила содержит нитратную группу и остаток амида никотиновой кислоты, поэтому обладает свойствами органических нитратов и активаторов аденозинтрифосфат–зависимых калиевых каналов. Препарат сбалансированно снижает пред– и постнагрузку на миокард. Открывая АТФ–зависимые калиевые каналы, никорандил полностью воспроизводит эффект ишемического прекондиционирования: способствует энергосбережению в сердечной мышце и предотвращает необходимые клеточные изменения в условиях ишемии [9,10]. Доказано также, что никорандил уменьшает агрегацию тромбоцитов, стабилизирует коронарную бляшку, нормализует функцию эндотелия и симпатическую нервную активность в сердце. Никорандил не вызывает развития толерантности, не влияет на ЧСС и АД, проводимость и сократимость миокарда, на липидный обмен и метаболизм глюкозы. Никорандил рекомендуется к назначению в Европейских рекомендациях (2006 г.) и рекомендациях ВНОК (2008 г.) в качестве монотерапии при непереносимости или противопоказаниях к β–блокаторам или антагонистам кальция либо как дополнительное лекарственное средство при их недостаточной эффективности.
Антиангинальная активность никорандила была продемонстрирована во многих исследованиях [11]. Его прогностическая польза была показана в сравнении с плацебо у пациентов с коронарной болезнью сердца в исследовании IONA [12]. В этом исследовании (n=5126, период наблюдения 12–36 мес.) значительные преимущества в группе лечения (20 мг 2 раза/сут.) были найдены по нескольким составным показателям, в том числе по первичной конечной точке (смерть от ИБС, нефатальный ИМ или незапланированная госпитализация по поводу ИБС: отношение рисков 0,83, 95% доверительный интервал 0,72–0,97; р=0,014). Этот положительный результат был в основном обусловлен снижением острых коронарных событий. Любопытно, что в этом исследовании лечение никорандилом не сопровождалось снижением симптомов, оцениваемых по Канадской классификации.
Основным побочным эффектом при приеме никорандила является головная боль в начале лечения (частота отмены препарата 3,5–9,5%), которой можно избежать путем постепенного увеличения дозы до оптимального уровня. Возможно развитие аллергических реакций, кожной сыпи, зуда, желудочно–кишечных симптомов. Изредка развиваются такие нежелательные эффекты, как головокружение, недомогание и утомляемость. Изъязвления сначала были описаны в ротовой полости (афтозный стоматит) и встречались редко. Тем не менее, при последующих исследованиях было описано несколько случаев ульцерации перианальной области, толстой кишки, вульвовагинальной и паховой области, которые могут быть очень серьезными, хотя всегда обратимыми после прекращения лечения. Никорандил включен в первые российские «Национальные рекомендации по кардиоваскулярной профилактике»: класс рекомендаций I, уровень доказательности В [13].
4.4.3.1.5.2. Ивабрадин. Новый класс антиангинальных средств – ингибиторы активности клеток синусового узла (ивабрадин) – обладает выраженной селективной способностью к блокаде If–ионных каналов, которые ответственны за синоатриальный водитель ритма и вызывают замедление ЧСС [14]. В настоящее время ивабрадин является единственным применяемым в клинике пульс–замедляющим лекарственным средством, реализующим свои эффекты на уровне пейсмекерных клеток синоатриального узла, т.е. является истинным блокатором If–токов. Ивабрадин может применяться у больных стабильной стенокардией с синусовым ритмом как при непереносимости или противопоказаниях к применению β–блокаторов, так и для совместного применения с β–блокаторами, если последние не контролируют ЧСС (больше 70 уд/мин.), а увеличение их дозы невозможно. При хронической стабильной стенокардии препарат в дозе 5–10 мг/сут. понижает сердечный ритм и потребность миокарда в кислороде без отрицательного инотропного действия. Продолжаются дальнейшие испытания препарата, в том числе у больных с рефрактерной стенокардией и хронической сердечной недостаточностью. Одним из побочных эффектов ивабрадина является индукция фосфен–нарушений световосприятия (светящиеся точки, различные фигуры, появляющиеся в темноте), связанные с изменениями сетчатки глаз. Частота глазных симптомов – около 1%, они проходят самостоятельно (в первые 2 мес. лечения у 77% больных) либо при прекращении приема ивабрадина. Возможна чрезмерная брадикардия (частота появления – 2% при рекомендуемой дозе 7,5 мг 2 раза/сут.). Таким образом, новые фармакологические препараты – ивабрадин, никорандил, ранолазин – могут быть эффективны у части больных стенокардией, однако необходимо провести дополнительные клинические испытания.
4.4.3.1.5.3. Триметазидин. В основе антиишемического действия триметазидина лежит его способность повышать синтез аденозинтрифосфорной кислоты в кардиомиоцитах при недостаточном поступлении кислорода за счет частичного переключения метаболизма миокарда с окисления жирных кислот на менее кислородозатратный путь – окисление глюкозы [15,16]. Это увеличивает коронарный резерв, хотя антиангинальный эффект триметазидина происходит не за счет снижения ЧСС, снижения сократимости миокарда или вазодилатации. Триметазидин способен уменьшать ишемию миокарда на ранних этапах ее развития (на уровне метаболических нарушений) и тем самым предотвращать возникновение ее более поздних проявлений – ангинозной боли, нарушений ритма сердца. снижения сократительной способности миокарда.
B метаанализе, проведенном Coсhrane Collaboration [17], были сгруппированы сравнительные испытания триметазидина в сравнении с плацебо или другими антиангинальными препаратами у больных со стабильной стенокардией. Анализ показал, что по сравнению с плацебо триметазидин значительно сокращает частоту еженедельных приступов стенокардии, потребление нитратов и время наступления выраженной депрессии сегмента ST при нагрузочных пробах. Антиангинальная и антиишемическая эффективность триметазидина, принимаемого в сочетании с β–блокаторами, превосходит таковое действие пролонгированных нитратов и антагонистов кальция. Выраженность положительного эффекта триметазидина возрастает по мере увеличения продолжительности лечения. Дополнительные преимущества терапии препаратом могут быть получены у больных с систолической дисфункцией левого желудочка ишемической природы, в том числе после перенесенного острого ИМ. Использование триметазидина до оперативных вмешательств на коронарных артериях (ЧКВ, АКШ) позволяет уменьшить выраженность повреждения миокарда во время их проведения. Длительное лечение триметазидином после оперативных вмешательств снижает вероятность возобновления приступов стенокардии и частоты госпитализаций по поводу острого коронарного синдрома, уменьшает выраженность ишемии, улучшает переносимость физических нагрузок и качество жизни. Результаты клинических исследований и их метаанализы подтверждают хорошую переносимость терапии триметазидином, превосходящую переносимость ангиангинальных препаратов гемодинамического действия. Триметазидин можно использовать либо как добавление к стандартной терапии, либо как замену ей при ее плохой переносимости. Препарат не применяется в США, но широко используется в Европе, в РФ и в более чем 80 странах мира.
Заключение
Стабильная стенокардия (с учетом лиц, ранее перенесших инфаркт миокарда) является одной из наиболее распространенных форм ИБС. Рассчитано, что число лиц, страдающих стенокардией, составляет 30–40 тыс. на 1 млн населения. В США более 13 млн больных с коронарной болезнью сердца. из них около 9 млн имеют стенокардию [1].
Основные цели лечения стенокардии – облегчение боли и предотвращение прогрессирования заболевания путем снижения сердечно–сосудистых осложнений.
В американских рекомендациях дается определение успешности лечения. Первостепенными целями лечения больных со стабильной ИБС являются минимизация вероятности смерти при сохранении хорошего здоровья и функции сердца. Наиболее специфическими целями являются: снижение преждевременной сердечной смерти; предупреждение осложнений стабильной ИБС, которые прямо или косвенно ведут к ухудшению функциональной способности, включая нефатальный инфаркт миокарда и сердечную недостаточность; поддержание или восстановление уровня активности, функциональной способности и качества жизни, которые удовлетворяют пациента; полное или почти полное устранение симптомов ишемии; минимизация расходов на сохранение здоровья, снижение частоты госпитализаций и проведения повторных (часто необоснованных) функциональных методов исследования и лечения, уменьшение побочных эффектов излишних назначений лекарственных препаратов и методов обследования.
Врачи привыкли проводить симптоматическую терапию, направленную на снятие приступов стенокардии, уменьшение одышки или отеков, снижение АД или частоты сердечных сокращений до нормальных показателей. Однако необходимо и стратегическое мышление у постели больного: следует думать об отдаленном прогнозе, оценивать риск возможной смерти и тяжелых осложнений болезни. пытаться достичь целевых уровней основных показателей липидов крови, биохимических показателей и маркеров воспаления, нормализации массы тела больных и др. [18].
Как показано в новых американских рекомендациях, стратегическая терапия с помощью статинов, АСК и, по показаниям, прием β–адреноблокаторов, ингибиторов АПФ или антагонистов рецепторов ангиотензина II как раз и дает реальную и надежную возможность добиться снижения смертности и улучшения течения ИБС. Больным следует определенно знать, что конечной целью применения этих лекарств является предотвращение преждевременной смерти и коренное улучшение течения болезни и прогноза, а для этого необходимо длительно (по крайней мере, в течение 3–5 лет) применять указанные препараты. Индивидуальная терапия пациентов с высоким риском (к которому относятся больные со стенокардией) отличается от населения в целом увеличением усилий по предотвращению факторов риска (от появления до снижения их тяжести).
В последние годы наряду с традиционными классами препаратов, такими как нитраты (и их производные), β–блокаторы, блокаторы кальциевых каналов, к лечению ИБС могут быть добавлены другие препараты с различным механизмом действия (триметазидин, ивабрадин, отчасти никорандил), а также новый препарат (ранолазин), недавно утвержденный в США, снижающий ишемию миокарда и являющийся полезным дополнением к лечению. В американских рекомендациях указаны и те препараты (класс III), прием которых не приводит к облегчению течения стабильной ИБС и улучшению прогноза больных.

Литература
1. Fihn S.D. Cardin J.M. Abrams J. et al. 2012 ACCF/AHA/ACP/FCP/AATS/PCNA/SCAI/SNS Guideline for the Diagnosis and Management of Patients With Stable Ischemic Heart Disease // J. Am. Coll. Cardiol. 2012. Vol.60 № 24. P. e44–e164.
2. Nash D.N. Nash S.D. Ranolazine for chronic stable angina // Lancet. 2008. Vol. 372. P. 1335–1341.
3. Stone P.Y. The Anti–Ischemic Mechanism of Action of Ranolazine in Stable Ischemic Heart Disease // JACC. 2010. Vol. 56(12). P. 934–942.
4. Лупанов В.П. Ранолазин при ишемической болезни сердца // Рациональная фармакотерапия в кардиологии. – 2012. – Т. 8, № 1. – С. 103–109.
5. Wilson S.R. Scirica B.M. Braunwald E. еt al. Efficacy of ranolazine in patients with chronic angina observations from the randomized, double–blind, placebo–controlled MERLIN–TIMI (Metabolic Efficiency With Ranolazine for Less Ischemia in Non–ST–Segment Elevation Acute Coronary Syndromes) 36 Trial // J. Am. Coll. Cardiol. 2009. Vol. 53(17). P. 1510–1516.
6. Di Monaco. Sestito A. The patient with chronic ischemic heart disease. Role of ranolazine in management of stable angina // Eur. Rev. Med. Pharmacol. Sci. 2012. Vol. 16(12). P. 1611–1636.
7. Timmis A.D. Chaitman B.R. Crager M. Effects of ranolazine on exercise tolerance and HbA1c in patients with angina and diabetes // Eur. Heart J. 2006. Vol. 27. P. 42–48.
8. Gayet J–L. Paganelli F. Conen–Solal A.F. Update on the medical treatment of stable angina // Arch. Cardiovasc. Dis. 2011. Vol. 104. P. 536–554.
9. Horinaka S. Use of Nicorandil in cardiovascular disease and its optimization // Drugs. 2011. Vol. 71, №. 9. P. 1105–1119.
10. Лупанов В.П. Максименко А.В. Протективная ишемия в кардиологии. Формы кондиционирования миокарда (обзор) // Кардиоваск. терапия и профилактика. – 2011. – № 10(1). – С. 96–103.
11. Лупанов В.П. Применение никорандила – активатора калиевых каналов– в лечении больных с ишемической болезнью сердца // Справочник поликлинического врача. – 2011. – № 8. – С. 44–48.
12. IONA Study Group. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina (IONA) randomised trial // Lancet. 2002. Vol. 359. P. 1269–1275.
13. Кардиоваскулярная профилактика. Национальные рекомендации ВНОК // Кардиоваск. терапия и профилактика. – 2011. – № 10(6); Прил.2. – С. 57.
14. Tendera M. Borer J.S. Tardif J.C. Efficacy of I(f) inhibition with ivabradine in different subpopulations with stable angina pectoris // Cardiol. 2009. Vol. 114(2). P. 116–125.
15. Аронов Д.М. Арутюнов Г.П. Беленков Ю.Н. и др. Согласованное мнение экспертов о целесообразности использования миокардиального цитопротектора триметазидина (Предуктала МВ) в комплексной терапии больных с хроническими формами ишемической болезни сердца // Кардиосоматика. – 2012. – T. 3, № 2. – C. 58–60.
16. Лупанов В.П. Триметазидин МВ у больных с ишемической болезнью сердца (обзор) // Consilium Med. – 2010. – T. 12, № 1. – C. 5–11.
17. Сiapponi A. Pizarro R. Harrison J. Trimetazidine for stable angina // Cochrane Database Syst. Rev. 2005: CD003614.
18. Аронов Д.М. Лупанов В.П. Атеросклероз и коронарная болезнь сердца. Издание второе, переработанное. – М. Триада Х, 2009. – 248 с.
Национальные рекомендации по профилактике, диагностике и лечению артериальной гипертонии

#image.jpg Скачать в формате .pdf (600 Kb) >>
Рекомендации разработаны экспертами Всероссийского научного общества кардиологов в 2001 году и утверждены на Российском национальном конгрессе кардиологов 11 октября 2001 г. второй пересмотр Рекомендаций осуществлен в 2004 г.
Комитет экспертов по разработке рекомендаций по диагностике и лечению артериальной гипертонии: Белоусов Ю.Б. (Москва), Боровков Н.Н. (Нижний Новгород), Бойцов С.А. (Москва), Бритов А.Н. (Москва), Волкова Э.Г. (Челябинск), Галявич А.С. (Казань), Глезер М.Г. (Москва), Гринштейн Ю.И.(Красноярск), Задионченко В.С. (Москва), Калев О.Ф. (Челябинск), Карпов Р.С. (Томск), Карпов Ю.А. (Москва), Кобалава Ж.Д. (Москва), Кухарчук В.В. (Москва), Лопатин Ю.М. (Волгоград), Маколкин В.И. (Москва), Мареев В.Ю. (Москва), Мартынов А.И. (Москва), Моисеев В.С. (Москва), Небиеридзе Д.В. (Москва), Недогода С.В. (Волгоград), Никитин Ю.П. (Новосибирск), Оганов Р.Г. (Москва), Остроумова О.Д. (Москва), Ольбинская Л.И. (Москва), Ощепкова Е.В. (Москва), Поздняков Ю.М. (Жуковский), Сторожаков Г.И. (Москва), Хирманов В.Н. (Санкт-Петербург), Чазова И.Е. (Москва), Шалаев (Тюмень), Шальнова С.А. (Москва), Шестакова М.В. (Рязань), Шляхто Е.В. (Санкт-Петербург), Якушин С.С. (Рязань).
Глубокоуважаемые коллеги!
Вторая версия национальных рекомендаций по профилактике, диагностике и лечению артериальной гипертонии, также как и первая — результат совместной работы экспертов из всех регионов России. Настоящие рекомендации составлены с учетом новых данных, появившихся с момента опубликования первой версии в 2001 г. Основанные, главным образом, на результатах крупномасштабных международных исследований, они отражают актуальные вопросы классификации артериальной гипертонии, формулировки диагноза, а также алгоритмы врачебной тактики. Рекомендации представляют собой краткое и четкое изложение современных подходов к профилактике, диагностике и лечению артериальной гипертонии; они предназначены, прежде всего для использования в практическом здравоохранении. Всероссийское научное общество кардиологов надеется, что внедрение усовершенствованных рекомендаций позволит эффективно изменить к лучшему состояние проблемы диагностики и лечения артериальной гипертонии в России.
Президент Всероссийского научного общества кардиологов,
Академик РАМН
Р. Г. Оганов
Введение
С момента опубликования первых российских рекомендаций в 2001 г по профилактике, диагностике и лечению АГ накопились новые данные, которые потребовали пересмотра рекомендаций. В связи с этим по инициативе секции артериальной гипертонии![]() ВНОК и при поддержке президиума ВНОК был разработан и обсужден второй пересмотр Национальных рекомендаций по профилактике, диагностике и лечению артериальной гипертонии. В них приняли участие известные Российские специалисты. На конгрессе кардиологов в г. Томске второй пересмотр рекомендаций был утвержден официально.
ВНОК и при поддержке президиума ВНОК был разработан и обсужден второй пересмотр Национальных рекомендаций по профилактике, диагностике и лечению артериальной гипертонии. В них приняли участие известные Российские специалисты. На конгрессе кардиологов в г. Томске второй пересмотр рекомендаций был утвержден официально.
Артериальная гипертензия (артериальная гипертония) в РФ, как и во всех странах с развитой экономикой, является одной из актуальных медико-социальных проблем. Это обусловлено высоким риском осложнений, широкой распространенностью![]() и недостаточным контролем в масштабе популяции. В странах Запада АД должным образом контролируется менее чем у 30% населения, а в России у 17,5% женщин и 5,7% мужчин больных АГ. Польза от снижения АД доказана не только в целом ряде крупных, многоцентровых исследований, но и реальным увеличением продолжительности жизни в Западной Европе и США.
и недостаточным контролем в масштабе популяции. В странах Запада АД должным образом контролируется менее чем у 30% населения, а в России у 17,5% женщин и 5,7% мужчин больных АГ. Польза от снижения АД доказана не только в целом ряде крупных, многоцентровых исследований, но и реальным увеличением продолжительности жизни в Западной Европе и США.
В основу второй версии рекомендаций легли Европейские рекомендации по контролю АГ (2003). Особенностью второй версии, как и предыдущей, является то, что в соответствии с современными положениями, изложенными в последнем европейском руководстве, АГ![]() рассматривается как один из элементов системы стратификации индивидуального сердечно — сосудистого риска. АГ в силу своей патогенетической значимости и возможности регулирования является одной из важнейших составляющих этой системы. Такой подход к пониманию сути и роли АГ как ФР может реально обеспечить снижение ССЗ и смертности в России.
рассматривается как один из элементов системы стратификации индивидуального сердечно — сосудистого риска. АГ в силу своей патогенетической значимости и возможности регулирования является одной из важнейших составляющих этой системы. Такой подход к пониманию сути и роли АГ как ФР может реально обеспечить снижение ССЗ и смертности в России.
Список сокращений и условных обозначений
А — ангиотензин
АВ блокада — атриовентрикулярная блокада
АГ — артериальная гипертония
АД — артериальное давление
АИР — агонисты I1 -имидазолиновых рецепторов
АК — антагонисты кальция
АКС — ассоциированные клинические состояния
АКТГ — адренокортикотропный гормон
АО — абдоминальное ожирение
АРП — активность ренина в плазме крови
БА — бронхиальная астма
БАБ — бета-адреноблокаторы
иАПФ — ингибиторы ангиотензин-превращающего
фермента
ИБС — ишемическая болезнь сердца
ИМ — инфаркт миокарда
ИММ ЛЖ — индекс массы миокарда левого желудочка
ИМТ — индекс массы тела
ТИА — транзиторная ишемическая атака
УЗИ — ультразвуковое исследование
ФА — физическая активность
ФК — функциональный класс
ФН — физические нагрузки
ФР — факторы риска
ХОБЛ — хронические обструктивные болезни легких
ЦНС — центральная нервная система
ЭКГ — электрокардиограмма
ЭхоКГ — эхокардиография
Определение
Под термином «артериальная гипертензия»![]() подразумевают синдром повышения АД при «гипертонической болезни» и «симптоматических артериальных гипертензиях».
подразумевают синдром повышения АД при «гипертонической болезни» и «симптоматических артериальных гипертензиях».
Термин «гипертоническая болезнь» (ГБ), предложенный Г.Ф. Лангом в 1948 г, соответствует употребляемому в других странах понятию «эссенциальная гипертензия».
Под ГБ принято понимать хронически протекающее заболевание, основным проявлением которого является АГ, не связанная с наличием патологических процессов, при которых повышение АД обусловлено известными, в современных условиях часто устраняемыми причинами («симптоматические артериальные гипертензии»). В силу того, что ГБ — гетерогенное заболевание, имеющее довольно отчетливые клинико-патогенетические варианты с существенно различающимися на начальных этапах механизмами развития, в научной литературе вместо термина «гипертоническая болезнь» часто используется понятие «артериальная гипертензия».
Диагностика
Диагностика и обследование больных АГ проводятся в строгой последовательности, в соответствии со следующими задачами:
-
— определение стабильности и степени повышения АД;
— исключение симптоматической АГ или идентификация ее формы;
— оценка общего сердечно.сосудистого риска;
- выявление других ФР ССЗ и клинических состояний, которые могут повлиять на прогноз и эффективность лечения; определение у больного той или иной группы риска;
- диагностика ПОМ и оценка их тяжести.
Диагностика АГ и последующее обследование включает следующие этапы:
- повторные измерения АД;
- сбор анамнеза;
- физикальное обследование;
- лабораторно-инструментальные методы исследования: более простые на первом этапе и сложные — на втором этапе обследования.
Правила измерения АД
Точность измерения АД и, соответственно, гарантия диагностики АГ, определения ее степени зависят от соблюдения правил по измерению АД.
Для измерения АД имеют значение следующие условия:
Обновленные Рекомендации Европейского кардиологического общества (2013 г.) по лечению ишемической болезни сердца и кардиоваскулярной патологии у больных сахарных диабетом
Резюме. Внесены изменения в стандарты диагностики и лечения пациентов с ишемической болезнью сердца
 Участники Конгресса Европейского кардиологического общества, проходившего с 31 августа по 4 сентября 2013 г. в Амстердаме, Нидерланды, получили возможность кратко ознакомиться с обновленными Рекомендациями по диагностике и лечению стабильной ишемической болезни сердца (ИБС), а также по тактике ведения пациентов с сахарным диабетом или предиабетом и сопутствующей кардиоваскулярной патологией.
Участники Конгресса Европейского кардиологического общества, проходившего с 31 августа по 4 сентября 2013 г. в Амстердаме, Нидерланды, получили возможность кратко ознакомиться с обновленными Рекомендациями по диагностике и лечению стабильной ишемической болезни сердца (ИБС), а также по тактике ведения пациентов с сахарным диабетом или предиабетом и сопутствующей кардиоваскулярной патологией.Оба документа представлены 1 сентября 2013 г. в ходе заседания Европейского кардиологического общества и включают следующую информацию для европейских кардиологов:
- у пациентов со стабильной ИБС функциональная составляющая поражения коронарных сосудов играет более значимую, чем ранее, роль для проведения стентирования по сравнению с выраженностью ангиографических данных;
- оценка предтестовой вероятности (ПТВ) диагностики ИБС обновлена с включением более современных показателей по сравнению с расчетной шкалой 34-летней давности Даймонда и Форрестера (Diamond and Forrester Chest Pain Prediction Rule);
- для пациентов пожилого возраста с сахарным диабетом и кардиоваскулярной патологией критерии гликемического контроля несколько ослаблены в пользу качества жизни больных;
- у пациентов с сахарным диабетом и ИБС с поражением нескольких коронарных сосудов терапией выбора является проведение коронарного шунтирования, однако в случае предпочтения пациентом процедуры стентирования следует устанавливать элютинг-стенты.
Рекомендации повышают значимость ПТВ для диагностики стабильной ИБС, поскольку разработан «новый комплекс параметров предтестовой вероятности». Как и ранее, они базируются на данных Даймонда и Форрестера 1979 г. однако по сравнению с 1979 г. частота выявления стенозов коронарных артерий у пациентов с клиникой стенокардии значительно снизилась. Тем не менее, новые критерии ПТВ по-прежнему ориентированы на характеристику ангинозной боли (типичная стенокардия против атипичной стенокардии против загрудинной боли неангинозного характера), возраст и пол пациента.
Например, у пациента с подозрением на ИБС, с применением новых критериев, как представлено в презентации на Конгрессе, при ПТВ <15% следует искать другие причины и рассмотреть вероятность функциональной коронарной болезни. При средних значениях ПТВ (15%–85%) пациенту следует провести неинвазивное обследование. Если ПТВ высокая — >85%, устанавливают диагноз ИБС. У пациентов с тяжелой симптоматикой или «клинической картиной, предполагающей коронарную анатомию высокого риска», следует проводить терапию, предусмотренную Рекомендациями.
Рекомендации также повышают значимость современных визуализирующих технологий, особенно кардиальной магнитно-резонансной томографии и коронарной компьютерной томографии-ангиографии (КТА), однако с необходимостью трезвого критического подхода. По мнению авторов новых Рекомендаций, они старались создать умеренно консервативный документ, однако «не такой консервативный, как Американские рекомендации 2012 г. и не такой прогрессивный, как рекомендации NICE (National Institute for Health and Clinical Excellence — Национальный институт здоровья и качества медицинской помощи) 2010 г.».
Согласно Рекомендациям, коронарную КТА следует рассматривать при стабильной ИБС в качестве альтернативы визуализирующим стресс-технологиям у пациентов с умеренными значениями ПТВ для стабильной ИБС с ожидаемым высоким качеством данных визуализации. Следует также рассматривать применение данного метода у пациентов с умеренными значениями ПТВ для стабильной ИБС после неубедительных данных электрокардиографического исследования с нагрузкой или визуализирующего стресс-теста, а также у пациентов с противопоказаниями к проведению стресс-тестов, если получение полной диагностической картины при проведении коронарной КТА является ожидаемым.
Члены рабочей группы по подготовке Рекомендаций акцентируют также внимание на наличии трех «запрещающих» рекомендаций (ІІІС): не следует проводить оценку кальцификации у асимптоматических пациентов; не следует проводить коронарную КТА у асимптоматических пациентов в качестве скринингового теста; не следует проводить коронарную КТА с высокой вероятностью кальцификации сосудов.
Заслуживает внимания также, возможно, более агрессивное по сравнению с Американскими рекомендациями 2012 г. положение об обязательном проведении каждому пациенту, обратившемуся за медицинской помощью по поводу боли в грудной клетке, эхокардиографического исследования в покое при первом контакте.
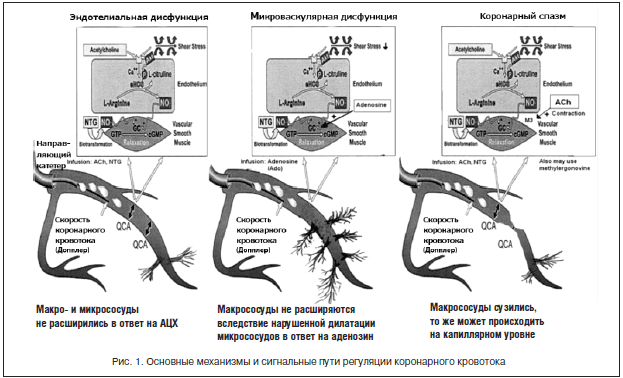
Рекомендации констатируют также, что микрососудистая стенокардия и вазоспазм являются гораздо более распространенными причинами стенокардии, чем полагали ранее. Проблема, по мнению авторов, заключается в том, что большинство практикующих врачей считают, что ИБС и, в частности, стенокардия, — это состояния, обусловленные стенозом коронарных артерий. Что, безусловно, является верным, однако не исчерпывает всех возможных причин развития заболевания.
На Конгрессе представлены также обновленные рекомендации по лечению стабильной ИБС.
Многих пациентов направляют в катетеризационные лаборатории без каких-либо симптомов ишемии. Катетеризацию сердца как метод, доступный в указанных лабораториях, применяют для измерения кровотока в коронарных артериях — так называемого фракционного резерва кровотока. Метод определения гемодинамически соответствующего поражения коронарных артерий при отсутствии данных, подтверждающих ишемию, относят к классу клинических рекомендаций І, доказательный уровень А. Может быть рассмотрено применение внутрикоронарного ультразвукового исследования или оптической когерентной томографии (класс клинических рекомендаций ІІ, доказательный уровень В) для характеристики сосудистых поражений и повышения эффективности стентирования.
Рекомендации также внесли свой вклад в весьма напряженные дебаты между хирургами и интервенционными кардиологами, соперничающими за пациентов, направляемых на коронарную реваскуляризацию. Сформулированы четкие конкретные рекомендации, по большей части базирующиеся на расчетной шкале SYNTAX, которые категоризируют пациентов по тяжести ИБС, обусловленной анатомией поражения коронарных сосудов.
Например, у пациентов с клинически значимым стенозом основной левой коронарной артерии — с вовлечением лишь одного сосуда — следует проводить перкутанное коронарное вмешательство (percutaneous coronary intervention — PCI) для стволовых или срединных поражений, однако при локализации сосудистых поражений дистальнее бифуркации необходимо консилиумное решение экспертов на предмет выбора PCI или коронарного шунтирования в качестве метода лечения. При мультисосудистом поражении следует применять шкалу SYNTAX, при значениях <32 необходимо консилиумное решение, при значениях >33 следует проводить коронарное шунтирование.
В Рекомендациях отсутствуют существенные изменения в отношении медикаментозной терапии стабильной ИБС, за исключением включения трех лекарственных средств, дебютировавших в качестве антиангинальных препаратов: ранолазин, никорандил и ивабрадин — все в качестве препаратов второй линии.
Новыми в Рекомендациях в отношении пациентов с сахарным диабетом с кардиоваскулярной патологией или высоким кардиоваскулярным риском являются пациенториентированные подходы в терапии: менее агрессивный гликемический контроль у больных пожилого возраста и упрощенная диагностика, во главу которой ставят определение гликозилированного гемоглобина или уровня глюкозы в крови натощак, с резервным применением теста на толерантность к глюкозе лишь в «случаях неопределенности».
Акцентировано также внимание на преимуществах коронарного шунтирования в качестве метода первого выбора при решении вопроса о проведении реваскуляризации по сравнению с PCI, которому отдавали предпочтение в последние годы.
Очевидно, что для снижения кардиоваскулярного риска посредством гликемического контроля требуется достаточно продолжительное время. По мнению авторов, при лечении пациентов в возрасте 70–80 лет с множественной сопутствующей патологией врач, намеревающийся несколько ужесточить гликемический контроль у данной группы пациентов, должен четко представлять себе цели, которых он надеется достичь. Ужесточение гликемического контроля часто ассоциируется с повышением частоты эпизодов гипогликемии и ухудшением качества жизни со множеством ограничений в повседневной жизни пациента. Жесткий гликемический контроль, необходимый для кардио- и ретинопротекции, не представляет ценности, если пациенты постоянно пребывают в состоянии гипогликемии.
Чрезвычайно важным, считают авторы, является индивидуальный подход к пациенту с обсуждением желательности или нежелательности для больного тех или иных ограничений, сопряженных с лечением. Такой подход требует открытого и честного обсуждения с пациентом всех возможных вариантов лечения и путей достижения терапевтических целей. С возрастом больные менее склонны придерживаться жесткого гликемического контроля с учетом всех сопутствующих ему сложностей. Качество жизни является категорией, которую практикующим врачам не следует игнорировать.
Еще одной группой больных, которая выиграет от менее агрессивного гликемического контроля, являются пациенты с длительным течением сахарного диабета и автономной нейропатией. Такие больные, как правило, утрачивают способность ощущать симптомы гипогликемии и в случае развития данного состояния становятся более уязвимыми для ее негативных эффектов. Поэтому жесткий гликемический контроль не компенсирует риска развития гипогликемических состояний у данной категории пациентов.
В отношении реваскуляризации авторы Рекомендаций считают, что недавно опубликованные результаты исследования FREEDOM убедительно продемонстрировали преимущества коронарного шунтирования у больных сахарным диабетом с ИБС по сравнению с PCI даже при условии применения элютинг-стентов. Таким образом, изменения в обновленных Рекомендациях касаются преимуществ полной реваскуляризации путем проведения шунтирования с применением, по возможности, артериальных шунтов по сравнению с PCI. Пациент может предпочесть выполнение процедуры PCI, однако в таких случаях больной должен быть проинформирован о различиях в показателях заболеваемости и даже смертности через несколько лет после проведения шунтирования и стентирования.
В целом, согласно Рекомендациям больные с неосложненной ИБС нуждаются, в первую очередь, в медикаментозной терапии. При тяжелом поражении коронарных сосудов или наличии у пациентов множественной сопутствующей патологии следует отдавать предпочтение проведению коронарного шунтирования, и если больной предпочитает процедуру PCI, необходимо устанавливать элютинг-стенты.
- Diamond G.A. Forrester J.S. (1979) Analysis of probability as an aid in the clinical diagnosis of coronary-artery disease. N. Engl. J. Med. 300: 1350–1358.
- Montalescot G. Sechtem U. Achenbach S. et al. (2013) 2013 ESC guidelines on the management of stable coronary artery disease. Eur. Heart J. September 1 [Epub ahead of print].
- Ryden L. Grant P.J. Anker S.D. et al. (2013) ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD: Summary. Eur. Heart J. September 1 [Epub ahead of print].