Какой прогноз при васкулите?
Начало данной статьи читайте здесь.
Существует множество типов васкулита, но, в целом, заболевание достаточно редкое. В случае развитие васкулита прогноз заболевания зависит от таких факторов:
- Типа васкулита
- Вовлеченного органа
- Насколько быстро ухудшается состояние
- Тяжести заболевания
В случае своевременной диагностики и адекватного лечения васкулиты хорошо поддаются лечению. В некоторых случаях удается добиться ремиссии. Под термином «ремиссия» подразумевают неактивное состояние заболевания, которое способно обостриться в любой момент.
Отдельные типы васкулитов хронические и нет возможности перевести последних в ремиссию. Длительное лечение медицинскими препаратами дает контроль над симптомами хронического васкулита.
В редких случаях воспаление сосудов не отвечает на лечение. В такой ситуации возникает стойкая неработоспособность, может наступить летальный исход.
Читайте далее в данной рубрике:Какие типы васкулитов существуют
симпозиум №57
Первичные системные васкулиты (часть 2): лечебные подходы и прогноз
Автор: А.И. Дядык, Н.Ф. Яровая, В.Б. Гнилицкая, М.В. Хоменко, С.Р. Зборовский, ДонНМУ им. М. Горького, кафедра внутренних болезней и общей практики — семейной медицины ФИПО
Дата проведения: с 01.01.2015 по 31.12.2015
Лечение больных с первичными системными васкулитами (СВ) представляет довольно сложную проблему, а кроме того, требует нередко междисциплинарного подхода. При наличии любых клинических проявлений, позволяющих заподозрить СВ, показана консультация ревматолога. Показаниями к госпитализации в ревматологическое отделение служат: необходимость верификации диагноза в дебюте заболевания, детальная оценка состояния жизненно важных органов при его обострениях для выбора оптимального режима патогенетической терапии и уточнения прогноза заболевания, а также развитие осложнений. Лечебная программа всегда носит строго индивидуализированный характер и определяется как типом СВ, так и особенностями его клинических проявлений.
Общие стратегические лечебные подходы при СВ включают:
1. Быстрое подавление активности СВ с помощью агрессивных режимов иммуносупрессивной терапии в дебюте заболевания (индукционная терапия), а также при его обострениях (эскалационная терапия), что позволяет значительно снизить риск тяжелых необратимых поражений органов и систем, сопровождающихся потерей зрения, неврологическими дефицитами, легочно-сердечной и почечной недостаточностью.
2. По достижении клинико-лабораторной ремиссии заболевания — обеспечение строгого соблюдения программы продолжения иммуносупрессивной терапии в дозах, достаточных для ее поддержания (т.е. поддерживающая терапия, которая проводится в течение 1–3 лет, иногда более продолжительное время).
3. Выполнение пациентами ряда немедикаментозных рекомендаций (умеренное ограничение поваренной соли, приема нестероидных противовоспалительных препаратов (НПВП), антибиотиков (АБ), пищевых несертифицированных добавок, строгое воздержание от инсоляций, поддержание комфортного режима двигательной активности, у лиц детородного возраста — эффективная контрацепция при использовании тератогенных иммуносупрессивных препаратов).
4. Мониторирование функциональных показателей внутренних органов для своевременной диагностики неуклонного прогрессирования органного поражения и проведения соответствующих мероприятий (например, терапия, замещающая почки, хирургические реконструктивные подходы).
Цели медикаментозной терапии:
1. Достижение (индукция) клинико-лабораторной ремиссии заболевания.
2. Снижение риска обострения СВ за счет адекватной поддерживающей терапии.
3. Снижение риска развития побочных эффектов используемых лекарственных препаратов.
Краеугольным камнем иммуносупрессивной терапии СВ остаются Гк и препараты цитотоксического действия (ПЦТД), из которых наиболее широко применяются циклофосфамид (Цф), метотрексат (Мт), азатиоприн (Аз), которые обеспечивают разнонаправленные иммуносупрессивные эффекты. Выбор и особенности режима иммуносупрессивной терапии определяются многочисленными факторами, включающими клинический вариант СВ (локальный или генерализованный), сроки установления диагноза и начала адекватной терапии (этап развития заболевания) и риск побочных эффектов используемых средств. В некоторых ситуациях при СВ используются экстракорпоральные методы очищения крови (плазмаферез) и внутривенное введение иммуноглобулинов.
Глюкокортикоидная терапия (ГКТ)
Соответственно решениям Консенсуса по терминологии и номенклатуре доз и режимов использования глюкокортикоидов (Гк), принятым в 2005 г. на I Европейском симпозиуме по проблемам ГКТ, низкими в преднизолоновом эквиваленте считали суточные дозы Гк ≤ 7,5 мг, средними — 7,5–30,0 мг, высокими — 30– 100 мг, очень высокими — > 100 мг и сверх- высокими (пульс-терапия) — > 250 мг при внутривенном введении (в/в).
Тактика назначения Гк при СВ показана на примере индукционной терапии СВ крупных сосудов (артериита Така- ясу — АТ и гигантоклеточного артериита — ГКА), предлагаемой экспертами EULAR (2008 г.). Так, высокая клиническая эффективность в достижении ремиссии указанных СВ продемонстрирована при раннем применении высоких дозировок Гк с начальной дозой преднизолона 1 мг/кг/сут (обычно 60 мг/сут, в тяжелых случаях заболевания — до 80 мг/сут) продолжительностью 1 мес.
После достижения клинического эффекта чрезвычайно важным является обеспечение тактики медленного снижения первоначальной дозы Гк до поддерживающих 10–15 мг/сут, алгоритм которой показан в табл. 1.
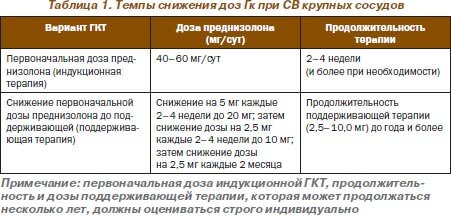
В качестве индукционной терапии возможно также использование режима пульс-терапии метилпреднизолоном (1,0 г в/в в течение трех дней), указанные сеансы могут проводиться неоднократно (1 раз в 2–3 недели), в промежутках между ними больные получают умеренные дозы Гк.
Для достижения быстрого клинического эффекта при генерализованных вариантах СВ с тяжелыми поражениями жизненно важных органов (легкие, почки, ЦНС) в качестве стандарта индукционной терапии рекомендуются сверхвысокие дозировки Гк (пульс-терапия, т.е. 1 г метилпреднизолона в/в в течение 3 дней) в комбинации с Цф, что позволило существенно увеличить 5-летнюю выживаемость больных (при некоторых СВ до 80 % и более). Первоначальная пероральная доза Цф в тяжелых случаях составляет 3–5 мг/кг м.т. в течение 3–4 дней, а затем снижается до 2 мг/кг м.т. После достижения клинической ремиссии, по мнению многих специалистов, необходимо продолжение использования Цф и поддерживающей ГКТ по меньшей мере в течение 1 года.
На рис. 1 показан один из предлагаемых подходов к лечению СВ на примере больных АНЦА-ассоциированными СВ (ААВ) — гранулематозом Вегенера (ГрВ) и микроскопическим полиартериитом (МПА).
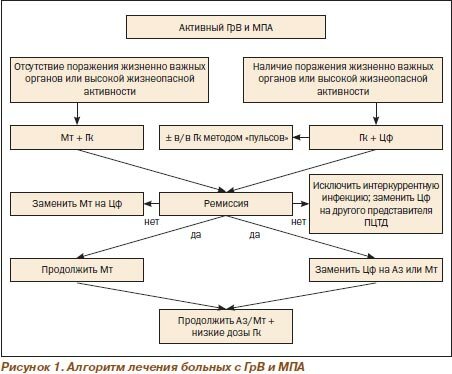
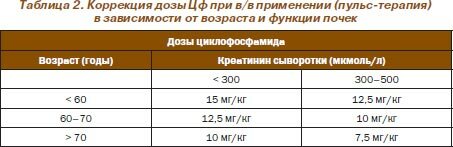
Рабочая группа EULAR предложила лечебную тактику применения Цф, включающую в/в применение препарата в дозе 15 мг/кг (максимальная — 1,2 г) каждые 2 недели (первые 3 «пульса») с последующими 3–6 «пульсами» каждые 3 недели. При пероральном применении Цф следует корригировать дозу в зависимости от возраста, снижая ее на 25 % у лиц старше 60 лет и на 50 % у лиц старше 75 лет. При использовании Цф в/в (пульс-терапия) дозировки определяются в зависимости от возраста и уровней креатинина сыворотки (табл. 2). Дозировки Аз должны также корригироваться в зависимости от состояния почечной функции, тогда как применение Мт при почечной недостаточности малоприемлемо.
В случаях ААВ, резистентных к индукционной или поддерживающей терапии, в ревматологических центрах может быть принято решение об использовании в/в иммуноглобулинов, микофенолата мофетила (ММ) или биологически активных препаратов (инфликсимаб, ритуксимаб) в дозах, приведенных в табл. 3.
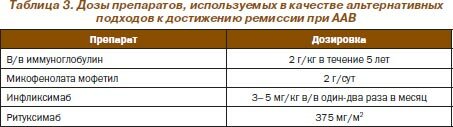
Больным с тяжелым поражением таких жизненно важных органов, как почки, легкие, ЖКТ, поджелудочная железа, головной мозг, показана пульс-терапия метилпреднизолоном и плазмаферез.
Больным с активным гепатитом В показаны противовирусная терапия и проведение плазмафереза с целью удаления ИК.
Геморрагический васкулит (ГВ), или пурпура Шенлейна — Геноха, без тяжелых поражений почек и желудочно-кишечного тракта в большинстве случаев характеризуется благоприятным течением и самопроизвольным выздоровлением, поэтому точки зрения на эффективность медикаментозной терапии с использованием Гк, ПЦТД, аминохинолиновых препаратов (АХП), нестероидных противовоспалительных препаратов (НПВП) неоднозначны. Вместе с тем, по мнению многих специалистов, при отсутствии абдоминального синдрома и поражений почек достаточно использования НПВП, оказывающих в первую очередь благоприятный эффект на суставной синдром, вместе с тем другие специалисты не рекомендуют применение НПВП в связи с риском развития абдоминального синдрома или его усугубления. Однозначно признается, что ГКТ не способна превентировать поражение почек или рецидивы ГВ в виде кожного и/или абдоминального синдромов.
Геноховский гломерулонефрит (ГГН) выявляется у взрослых больных в 45– 85 % случаев, причем тяжелые почечные поражения нередко констатируют уже при первоначальном обследовании. При этом взгляды на необходимость применения Гк и/или ПЦТД (Цф, хлорамбутил, Аз, ММ, Мт, циклоспорин) довольно противоречивы, а достаточной доказательной базы относительно их эффективности в настоящее время нет. Превалирует точка зрения об отсутствии положительного эффекта самостоятельной ГКТ, применяемой перорально или в виде «пульсов». При отсутствии тяжелых гломерулярных поражений и клиническом течении, характеризующемся минимальной протеинурией и/или гематурией различной выраженности, большинство авторов не рекомендуют проведение иммуносупрессивной терапии, а при наличии тяжелых гломерулярных поражений с нефритическим или нефротическим синдромом в связи с неблагоприятным прогнозом считают обоснованным проведение агрессивной индукционной иммуносупрессивной терапии, включающей комбинацию Гк с ПЦТД (прежде всего Цф или хлорамбуцилом) с последующей (при достижении благоприятного эффекта от индукционной терапии) поддерживающей терапией, включающей азатиоприн или микофенолатмофетил в комбинации с минимальными или умеренными дозами Гк.
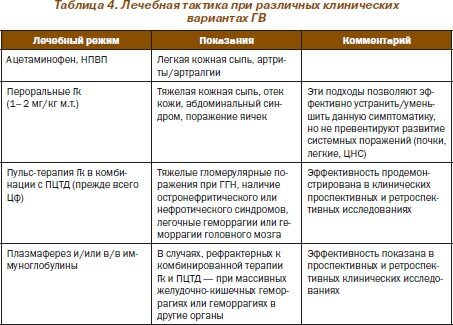
В табл. 4 мы представляем стратегические лечебные подходы при различных клинических вариантах ГВ, базирующиеся на анализе перспективных и ретроспективных клинических исследований.
Поддерживающая терапия при СВ
При локализованных вариантах СВ (без серьезных поражений внутренних органов — обычно при СВ крупных сосудов) может быть использован длительный прием (в течение нескольких лет) средних доз преднизолона (10– 15 мг/сут). Однако с целью увеличения эффективности терапии и снижения суммарной (кумулятивной) дозы Гк, а также при генерализованных вариантах СВ для поддерживающей терапии чаще предлагают использовать комбинацию Гк с ПЦТД Мт (от 7,5 до 25 мг/нед) или Аз (2 мг/кг/сут), реже — Цф (2 мг/кг м.т. ). После достижения клинической ремиссии, по мнению многих специалистов, необходимо продолжение использования указанной комбинации по меньшей мере в течение 1 года.
Использование ММ, лефлюномида и ритуксимаба для профилактики обострений СВ (обычно при ГрВ и МПА) приемлемо лишь при рефрактерности к Аз или Мт, при этом используются следующие дозировки: Лф — 20–30 мг/сут, ММ — 1–2 г/сут. Дозировки этих препаратов следует корригировать с состоянием функции почек.
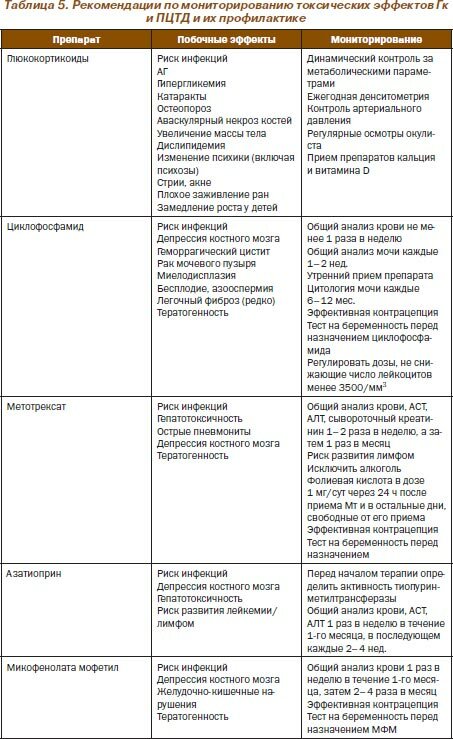
Учитывая ограниченное число исследований, ингибитор ФНО-a инфликсимаб не может быть сегодня рекомендован для поддерживающей терапии СВ в широкой клинической практике.
Мониторирование течения СВ в фазе поддерживающей терапии
Отсутствуют специфические биомаркеры, оценивающие эффективность терапии и обострение при различных СВ. Мониторирование воспалительных биомаркеров (уровни СОЭ и СРБ) должно проводиться для решения вопроса об изменении лечебного режима.
При обострениях СВ, развившихся после прекращения поддерживающей терапии, следует назначать комбинацию препаратов, аналогичную индукционной терапии. При обострениях на фоне поддерживающей терапии необходимо повышать дозировку преднизолона на 5–10 мг.
Проблемы иммуно- супрессивной терапии СВ
В крупном исследовании Национального института здоровья (НИЗ) США (158 больных ГрВ, средние сроки наблюдения ≈ 8 лет) продемонстрировано, что в описанном выше «агрессивном» режиме индукционной терапии было достигнуто существенное улучшение клинической картины у 91 % больных, а полная ремиссия — в 75 % случаев. В последующем в 50 % случаев имели место обострения заболевания с отчетливым ухудшением клинической картины, включающим развитие хронической почечной недостаточности (ХПН — 42 %), потерю слуха (35 %), косметические и функциональные назальные деформации (28 %), стеноз трахеи (13 %), нарушение зрения (8 %). Побочные эффекты Гк и Цф развились у 42 % пациентов и включали цистит (43 %), рак мочевого пузыря (2,8 %), лимфому (1,5 %), инфертильность ( > 57 % женщин), катаракты (21 %), переломы (11 %), асептический некроз (3 %). Более того, у 46 % больных имели место эпизоды тяжелой инфекции, потребовавшие госпитализации и применения интенсивной (в том числе в/в) антибактериальной терапии.
Учитывая высокую токсичность Цф, во многих ревматологических клиниках индукционная терапия Цф проводится методом «пульсов», что, по мнению ряда специалистов, позволяет снизить суммарную дозу препарата по сравнению с его пероральным использованием, а следовательно, уменьшить частоту и тяжесть побочных эффектов без снижения лечебного эффекта. В ряде исследований показано, что применение Цф методом «пульсов» по 0,7 г/м2 каждые три недели по сравнению с пероральным приемом препарата ассоциируется с существенным снижением риска развития рака мочевого пузыря, геморрагического цистита, пневмонии (прежде всего вызванной Pneumocystis carinii ), но сопряжено с увеличением частоты обострений заболевания.
Перорально применяемый Цф хорошо абсорбируется и полностью метаболизируется в печени в течение 24 часов. Множественные активные и неактивные метаболиты экскретируются преимущественно с мочой. Один из этих метаболитов (акролеин) способствует развитию геморрагического цистита, фиброза и рака мочевого пузыря. При в/в применении Цф следует рутинно проводить противорвотную терапию. Метаболиты Цф являются токсичными для эпителия мочевого пузыря и уретры и могут вызывать геморрагический цистит (непосредственное осложнение) и опухоли (отдаленное осложнение). С профилактической целью при лечении Цф следует рекомендовать обильное питье (если не противопоказано) или внутривенное введение жидкости в день инфузии Цф с целью разведения метаболитов в моче. Больным, получающим «пульс» Цф, следует назначать перорально или в/в натриевую соль 2-меркаптоэтансульфоновой кислоты, которая соединяется с токсическим метаболитом акролеином, переводя его в нетоксическое соединение, в результате чего замедляется деградация 2-гидроксиметаболитов и таким образом снижаются уровни токсических акролеиновых продуктов в моче.
Одним из частых гематологических осложнений при лечении Цф является лейкопения, в связи с чем необходим контроль лейкоцитов периферической крови и абсолютного количества нейтрофилов. При уровнях лейкоцитов менее 3500/мм3 и нейтрофилов менее 1500/мм3 необходимо снижение дозы (или отмена) Цф.
Дополнительные подходы при СВ
Для оценки течения СВ крупных сосудов (АТ, ГКА) следует проводить периодически МРТ или позитронную эмиссионную томографию крупных сосудов (особенно при наличии протодиастолического шума, обусловленного недостаточностью аортальных клапанов), так как субклиническое вовлечение ее в патологический процесс наблюдается нередко (9–18 % случаев) и может прогрессировать, формируя аневризмы и/или расслоение аорты. Возможности ультрасонографии артерий при этом ограничены. При необходимости по достижении ремиссии заболевания проводят хирургические реконструктивные мероприятия: 70 % больных с АТ нуждаются в артериальной реконструкции и шунтировании (при ангиопластике и стентировании более высокая частота рестенозирования). В связи с повышенным риском кардиоваскулярных осложнений больным с АТ и ГКА показан прием аспирина (75–150 мг/сут), если нет индивидуальных противопоказаний. При наличии факторов риска гастродуоденальных осложнений при лечении аспирином необходимо назначение ингибиторов протонового насоса с целью защиты слизистой. Нет доказательств благоприятного эффекта статинов на течение ГКА.
При ГрВ в случаях развития необратимого подглоточного стеноза требуются специальные подходы (трахеостомия, ларинготрахеопластика, микроваскулярная ларинготрахеальная реконструкция, комбинация механической дилатации с локальными инъекциями глюкокортикоидов). Специальные мероприятия требуются больным ГрВ с развитием среднего отита, синуситов, тяжелых легочных геморрагий.
У большинства больных с ГрВ в ходе наблюдения развивается вторичная инфекция периназальной области, чаще вызываемая S.аureus. Способность инфекционных агентов индуцировать обострения заболевания, а антибактериальной терапии — превентировать обострения ГрВ остается предметом дискуссий, так что для профилактики обострений ГрВ использование АБ, в частности триметоприма/котримоксазола, неприемлемо.
При тяжелом быстропрогрессирующем поражении почек (креатинин крови > 500 мкмоль/л) с целью улучшения «почечной выживаемости» дополнительно к иммуносупрессивной терапии возможно проведение плазмафереза. При развитии ТСПН показана терапия, замещающая почки (гемодиализ, перитонеальный диализ или трансплантация почки). Выживаемость почечного трансплантата у больных с ГрВ при отсутствии активности сравнима с таковой у пациентов с ТСПН, обусловленной другими заболеваниями.
Прогноз при СВ
При отсутствии лечения прогноз у больных СВ крайне неблагоприятный, летальность продолжает оставаться довольно высокой, особенно у лиц молодого и пожилого возраста, а также при вовлечении в патологический процесс жизненно важных органов (почек, сердца, легких, ЖКТ). Выживаемость пациентов во многом зависит от своевременности постановки диагноза, адекватной индукционной и поддерживающей терапии.
Высокая летальность при узелковом периартериите (УП) обусловлена церебральными или гастроинтестинальными геморрагиями, инфарктами миокарда, почечной или сердечной недостаточностью, интеркуррентными инфекциями. У подавляющего большинства больных ГВ прогноз определяется наличием ГГН и его тяжестью, причем риск развития и прогрессирования почечной недостаточности особенно высок у взрослых — от 10 до 50 % случаев. При ГВ более неблагоприятный прогноз у взрослых (особенно женщин), риск прогрессирования почечного поражения ассоциируется с персистенцией умеренной или большой протеинурии, снижением почечной функции, наличием АГ и полулуний (> 50 % клубочков) в дебюте заболевания. Неблагоприятное влияние на прогноз оказывают обострения СВ, частота которых достигает 40 %. При синдроме Чарга — Стросса на прогноз влияет также тяжесть бронхиальной астмы и своевременность/адекватность ее терапии.
Рациональное использование вышеуказанных лечебных подходов позволяет обеспечить больным СВ как увеличение продолжительности жизни, так и улучшение ее качества.
Список условных сокращений
ААВ — АНЦАассоциированные васкулиты
АГ — артериальная гипертензия
Аз — азатиоприн
АТ — артериит Такаясу
АХП — аминохинолиновые препараты
В/в — внутривенно
ГГН — Геноховский гломерулонефрит
Гк — глюкокортикоиды
ГКА — гигантоклеточный артериит
ГКТ — глюкокортикоидная терапия
ГрВ — гранулематоз Вегенера
ЖКТ — желудочнокишечный тракт
ММ — микофенолат мофетил
МПА — микроскопический полиартериит
МРТ — магнитнорезонансная томография


