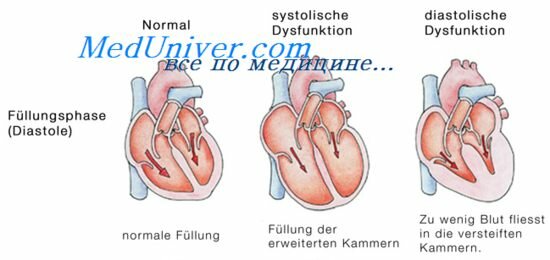
Хроническая систолическая сердечная недостаточность
Как видно из схемы, представленной на рис. 2.7, при наиболее распространенных заболеваниях, связанных с первичным повреждением или хронической перегрузкой ЛЖ (ИБС, постинфарктный кардиосклероз, АГ и др.), последовательно развиваются клинические признаки хронической левожелудочковой недостаточности, легочной артериальной гипертензии и правожелудочковой недостаточности. На определенных этапах сердечной декомпенсации начинают проявляться признаки гипоперфузии периферических органов и тканей, связанной как с гемодинамическими нарушениями, так и с гиперактивацией нейрогормональных систем. Это и составляет основу клинической картины бивентрикулярной (тотальной) СН, наиболее часто встречающейся в клинической практике. При хронической перегрузке ПЖ или первичном повреждении этого отдела сердца развивается изолированная правожелудочковая хроническая СН (например, хроническое легочное сердце).
Ниже приведено описание клинической картины хронической систолической бивентрикулярной (тотальной) СН.
Жалобы
Одышка (dyspnoe) — один из наиболее ранних симптомов хронической СН. Вначале одышка возникает только при физической нагрузке и проходит после ее прекращения. По мере прогрессирования болезни одышка начинает появляться при все меньшей нагрузке, а затем и в покое.
Одышка появляется в результате повышения КДД и давления наполнения ЛЖ и свидетельствует о возникновении или усугублении застоя крови в венозном русле малого круга кровообращения. Непосредственными причинами одышки у больных хронической СН являются:
o существенные нарушения вентиляционно-перфузионных соотношений в легких (замедление тока крови через нормально вентилируемые или даже гипервентилируемые альвеолы);
o отек интерстиция и повышение ригидности легких, что приводит к уменьшению их растяжимости;
o нарушение диффузии газов через утолщенную альвеолярно-капиллярную мембрану.
Все три причины ведут к уменьшению газообмена в легких и раздражению дыхательного центра.
Ортопноэ (orthopnoe) — это одышка, возникающая в положении больного лежа с низким изголовьем и исчезающая в вертикальном положении. Одышка появляется обычно через несколько минут пребывания больного в постели, но быстро проходит, как только он садится или занимает полусидячее положение. Нередко такие больные, ложась в постель, подкладывают под голову несколько подушек и в таком полусидячем положении проводят всю ночь.
Ортопноэ возникает в результате увеличения венозного притока крови к сердцу, наступающего в горизонтальном положении больного, и еще большего переполнения кровью малого круга кровообращения. Появление такого вида одышки, как правило, свидетельствует о значительных нарушениях гемодинамики в малом круге кровообращения и высоком давлении наполнения (или давлении “заклинивания” — см. ниже).
Непродуктивный сухой кашель у больных хронической СН нередко сопровождает одышку, появляясь либо в горизонтальном положении больного, либо после физической нагрузки. Кашель возникает вследствие длительного застоя крови в легких, набухания слизистой бронхов и раздражения соответствующих кашлевых рецепторов (“сердечный бронхит”). В отличие от кашля при бронхолегочных заболеваниях у больных с хронической СН кашель является непродуктивным и проходит после эффективного лечения сердечной недостаточности.
Сердечная астма (“пароксизмальная ночная одышка”) — это приступ интенсивной одышки, быстро переходящей в удушье. Приступ чаще всего развивается ночью, когда больной находится в постели. Больной садится, но это часто не приносит заметного облегчения: удушье постепенно нарастает, сопровождаясь сухим кашлем, возбуждением, страхом больного за свою жизнь. Быстрое ухудшение состояния больного заставляет его обратиться за медицинской помощью. После проведения неотложной терапии приступ обычно купируется, хотя в тяжелых случаях удушье продолжает прогрессировать и развивается отек легких.
Сердечная астма и отек легких относятся к проявлениям острой СН и вызываются быстрым и значительным уменьшением сократимости ЛЖ, увеличением венозного притока крови к сердцу и застоя в малом круге кровообращения. Клиническая картина сердечной астмы и отека легких подробно описана в главе 6. Запомните
Одышка, сухой непродуктивный кашель, усиливающиеся в горизонтальном положении больного с низким изголовьем (ортопноэ), а также приступы сердечной астмы и альвеолярный отек легких у больного с хронической СН относятся к типичным проявлениям левожелудочковой недостаточности и застоя крови в венозном русле малого круга кровообращения. Выраженная мышечная слабость, быстрое утомление и тяжесть в нижних конечностях, появляющиеся даже на фоне небольших физических нагрузок, также относятся к ранним проявлениям хронической СН. Эти симптомы далеко не всегда коррелируют с тяжестью одышки, выраженностью отечного синдрома и других признаков СН. Они обусловлены нарушением перфузии скелетных мышц, причем не только за счет уменьшения величины сердечного выброса, но и в результате спастического сокращения артериол, вызванного высокой активностью САС, РААС, эндотелина и уменьшением расширительного резерва сосудов.
Сердцебиение. Ощущение сердцебиений чаще всего связано с характерной для больных с СН синусовой тахикардией, возникающей в результате активации САС. Сердцебиения вначале появляются при физической нагрузке, а затем и в покое, как правило, свидетельствуя о прогрессирующем нарушении функционального состояния сердца. В других случаях, жалуясь на сердцебиение, больные имеют в виду ощущение сильных ударов сердца, связанных, например, с увеличением пульсового АД. Наконец, жалобы на сердцебиение и перебои в работе сердца могут указывать на наличие у больных разнообразных нарушений сердечного ритма, например, на появление фибрилляции предсердий или частую экстрасистолию.
Отеки на ногах — одна из наиболее характерных жалоб больных с хронической СН. На ранних стадиях недостаточности отеки локализуются в области стоп и лодыжек, появляются у больных к вечеру, а к утру могут проходить. По мере прогрессирования СН отеки распространяются на область голеней и бедер и могут сохраняться в течение всего дня, усиливаясь к вечеру.
Отеки и другие проявления отечного синдрома связаны, в первую очередь, с задержкой Nа+ и воды в организме, а также с застоем крови в венозном русле большого круга кровообращения (правожелудочковая недостаточность) и повышением гидростатического давления в капиллярном русле. Подробнее патогенез отеков описан в разделе “Осмотр”.
Никтурия — увеличение диуреза в ночное время — также весьма характерный симптом, появляющийся у больных уже на ранних стадиях развития хронической СН. Абсолютное или относительное преобладание диуреза в ночное время связано с тем, что днем, когда больной большую часть времени находится в физически активном состоянии, выполняя те или иные нагрузки, начинает сказываться недостаточная перфузия почек, что сопровождается некоторым снижением диуреза. Такая гипоперфузия почек по крайней мере частично может быть связана со своеобразным адаптационным перераспределением кровотока, направленным прежде всего на обеспечение кровоснабжения жизненно важных органов (головной мозг, сердце). Ночью, когда больной находится в горизонтальном положении, а метаболические потребности периферических органов и тканей уменьшаются, почечный кровоток возрастает, и диурез увеличивается. Следует иметь в виду, что в терминальной стадии хронической СН, когда сердечный выброс и почечный кровоток резко уменьшаются даже в покое, наблюдается значительное уменьшение суточного диуреза — олигурия.
К проявлениям хронической правожелудочковой (или бивентрикулярной) СН относятся также жалобы больных на боли или чувство тяжести в правом подреберье, связанные с увеличением печени и растяжением глиссоновой капсулы, а также на диспепсические расстройства (снижение аппетита, тошноту, рвоту, метеоризм и др.).
Осмотр
При общем осмотре больного с хронической СН прежде всего обращают внимание на некоторые объективные признаки, связанные с застоем крови в малом или большом круге кровообращения, хотя на ранних стадиях заболевания они могут отсутствовать.
Положение ортопноэ (orthopnoe) — это вынужденное сидячее или полусидячее положение в постели, как правило, с опущенными вниз ногами (рис. 2.8, см. цветную вклейку в конце книги). Такое положение характерно для больных с тяжелой левожелудочковой недостаточностью и выраженным застоем крови в малом круге кровообращения. Положение ортопноэ больные занимают не только во время приступа сердечной астмы или отека легких, но и при выраженной одышке (ортопноэ), усиливающейся в горизонтальном положении (см. выше). Рис. 2.8. Вынужденное положение больного с хронической сердечной недостаточностью, застоем в малом круге кровообращения и приступами сердечной астмы
Запомните
Хроническая правожелудочковая недостаточность проявляется рядом объективных признаков, обусловленных застоем крови в венозном русле большого круга кровообращения: цианозом, отеками, водянкой полостей (асцит, гидроторакс, гидроперикард), набуханием шейных вен, гепатомегалией, отеком мошонки и полового члена. Цианоз у больных с хронической СН обусловлен замедлением кровотока на периферии, в результате чего увеличивается экстракция кислорода тканями. Это приводит к увеличению содержания восстановленного гемоглобина выше 40–50 г/л и сопровождается периферическим цианозом — акроцианозом (рис. 2.9). Акроцианоз у больных с хронической СН часто сочетается с похолоданием кожи конечностей, что также указывает на замедление периферического кровотока. Рис. 2.9. Механизм возникновения периферического цианоза (акроцианоза) у больных с бивентрикулярной ХСН.
Вверху показан участок периферического
кровотока в норме (слева) и при
выраженном застое крови в венах
большого круга кровообращения.
Внизу – уровень восстановленного
гемоглобина и внешние признаки
цианоза, появляющегося при повышении
утилизации тканями кислорода
и повышении содержания
восстановленного гемоглобина больше
40–50 г/л
Отеки у больных с правожелудочковой или бивентрикулярной недостаточностью обусловлены рядом причин (рис. 2.10): увеличением гидростатического давления в венозном русле большого круга кровообращения, снижением онкотического давления плазмы (ОДП) в результате застоя крови в печени и нарушения синтеза белков, нарушением проницаемости сосудов, задержкой натрия и воды, вызванной активацией РААС и т.п. Однако наибольшее значение имеет повышение гидростатического давления крови.
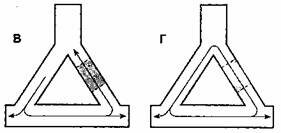
В норме (рис. 2.11, а) в венозном русле периферического кровотока гидростатичекое давление крови (темные столбики) существенно меньше онкотического (светлые столбики), что способствует поступлению воды из тканей в сосудистое русло. Наоборот, при венозном застое (рис. 2.11, б) гидростатическое давление в венозном русле может оказаться выше онкотического, что сопровождается выходом воды из сосудистого русла в ткани.
Периферические отеки у больных с хронической СН локализуются обычно в местах наибольшего гидростатического давления в венах. В течение длительного времени они располагаются на нижних конечностях, вначале в области стоп и лодыжек, а затем в области голеней. Как правило, отеки симметричны, т.е. выражены одинаково на обеих ногах. Преобладание отечности одной из конечностей, как правило, свидетельствует о местном нарушении венозного кровотока, например, при одностороннем илеофеморальном тромбозе. Отеки на ногах у больных с хронической СН обычно сочетаются с акроцианозом и похолоданием конечностей. При длительном существовании отеков появляются трофические изменения кожи — ее истончение и гиперпигментация (рис. 2.12, см. цветную вклейку).
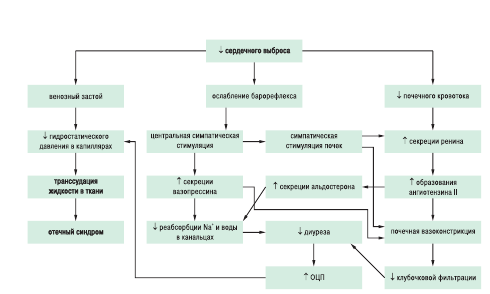
Рис. 2.10. Патогенез отеков при ХСН (по Е.Н. Амосовой в модификации). ОЦП — объем циркулирующей плазмы; ЦВД — центральное венозное давление; АДГ — антидиуретический гормон
Рис.
2.11. Роль в возникновении отеков высокого гидростатического давления и снижения онкотического давления плазмы крови: а – норма; б – повышение гидростатического давления и снижение онкотического давления при выраженной бивентрикулярной ХСН.
Темные столбики – уровень гидростатического давления в артериолярном и венозном русле периферического кровотока; светлые столбики – величина онкотического давления плазмы
Рис. 2.12. Отеки голени и стоп у больного с правожелудочковой сердечной недостаточностью (а — слева); отеки и трофические изменения кожи у больной с правожелудочковой сердечной недостаточностью (б — справа) Наконец, у тяжелых больных, длительно находящихся на постельном режиме, отеки располагаются преимущественно в области крестца, ягодиц и задней поверхности бедер.
Набухание шейных вен является важным клиническим признаком повышения центрального венозного давления (ЦВД), т.е. давления в правом предсердии (ПП), и застоя крови в венозном русле большого круга кровообращения (рис. 2.13, см. цветную вклейку). Рис. 2.13. Набухание шейных вен у больного с ХСН и повышенным центральным венозным давлением (ЦВД)
Ориентировочное представление о величине ЦВД можно составить при осмотре вен шеи. У здоровых лиц в положении лежа на спине со слегка приподнятым изголовьем (примерно под углом 45°) поверхностные вены шеи или не видны, или бывают наполненными только в пределах нижней трети шейного участка вены (рис. 2.14, а). В вертикальном положении наполнение вен уменьшается и исчезает совсем. При этом в норме уровень наполнения вен шеи на 1–3 см выше горизонтальной линии, проведенной через угол, образованный рукояткой и телом грудины (угол Людовика) и соответствующий месту прикрепления II ребра к грудине. Если учесть, что угол Людовика в любом положении пациента примерно на 5 см выше правого предсердия, то ЦВД можно измерить, определив расстояние от угла Людовика до уровня наполнения шейных вен (это расстояние измеряют строго вертикально). Прибавив к этому расстоянию 5 см, получим примерное значение ЦВД, например, 3 см + 5 см = 8 см вод. ст. При застое крови в большом круге кровообращения наполнение вен оказывается существенно выше уровня угла Людовика (более чем на 4–5 см) и сохраняется при поднимании головы и плеч и даже в вертикальном положении (рис. 2.14, б).
Рис. 2.14. Методика ориентировочного определения центрального венозного давления (ЦВД) у здорового человека (а) и пациента с бивентрикулярной ХСН (б) Абдоминально-югулярный (или гепато-югулярный) рефлюкс также является надежным показателем высокого ЦВД. Абдоминально-югулярная проба проводится путем непродолжительного (в течение 10 с) надавливания ладонью руки на переднюю брюшную стенку в околопупочной области. Исследование проводится при спокойном дыхании. Надавливание на переднюю брюшную стенку и увеличение венозного притока крови к сердцу в норме, при достаточной сократительной способности ПЖ, не сопровождаются набуханием шейных вен и увеличением ЦВД. Возможно лишь небольшое (не более 3–4 см вод. ст.) и непродолжительное (первые 5 с давления) возрастание венозного давления.
У больных с бивентрикулярной (или правожелудочковой) ХСН, снижением насосной функции ПЖ и застоем в венах большого круга кровообращения абдоминально- югулярная проба приводит к усилению набухания вен шеи и возрастанию ЦВД не менее чем на 4 см вод. ст.
Положительная абдоминально-югулярная проба косвенно свидетельствует не только об ухудшении гемодинамики правых отделов сердца, но и о возможном повышении давления наполнения ЛЖ, т.е. о выраженности бивентрикулярной ХСН.
Оценка результатов абдоминально-югулярной пробы в большинстве случаев позволяет уточнить причину периферических отеков, особенно в тех случаях, когда отсутствует значительное расширение вен шеи или другие внешние признаки правожелудочковой недостаточности. Положительные результаты пробы свидетельствуют о наличии застоя в венах большого круга кровообращения, обусловленном правожелудочковой недостаточностью. Отрицательный результат пробы исключает сердечную недостаточность как причину отеков. В этих случаях следует думать о другом генезе отеков (гипоонкотические отеки, тромбофлебит глубоких вен голеней, прием антагонистов кальция и др.). Запомните
В тяжелых случаях внешний вид больных с бивентрикулярной ХСН весьма характерен: обычно отмечается положение ортопноэ с опущенными вниз ногами, выраженные отеки нижних конечностей, акроцианоз, набухание шейных вен, заметно увеличение живота в объеме за счет асцита. Нередко лицо одутловато, кожа желтовато-бледная со значительным цианозом губ, кончика носа, ушей, рот полуоткрыт, глаза тусклые (лицо Корвизара) (рис. 2.15, см. цветную вклейку). Рис. 2.15. Лицо Корвизара у больной с бивентри-кулярной ХСН. Определяется акроцианоз, одутлова-тость лица, набухание шейных вен
В терминальной стадии хронической СН нередко развивается так называемая “сердечная кахексия”, важнейшими физикальными признаками которой являются резкое снижение массы тела, уменьшение толщины подкожно-жирового слоя, атрофия височных мышц и мышц гипотенора. Ее возникновение связывают с выраженными дистрофическими изменениями внутренних органов и скелетных мышц, обусловленными критическим снижением их перфузии и длительной гиперактивацией САС, РААС и других нейрогормональных систем. По-видимому, решающее значение имеет активация системы цитокинов, в частности фактора некроза опухолей альфа (ФНОa), которые обладают прямым повреждающим действием на периферические ткани. Повышение уровня цитокинов, в первую очередь ФНОa, ассоциируется также с иммуновоспалительными реакциями. Важными причинами развития сердечной кахексии являются также нарушения функции органов брюшной полости, вызванные застоем крови в системе воротной вены: ухудшение всасывания в кишечнике, снижение белково-синтетической функции печени, выраженная анорексия, тошнота, рвота и.т.п.
Исследование органов дыхания
Осмотр грудной клетки. Подсчет частоты дыхательных движений (ЧДД) позволяет ориентировочно оценить степень вентиляционных нарушений, обусловленных хроническим застоем крови в малом круге кровообращения. Во многих случаях одышка у больных ХСН носит характер тахипноэ, без отчетливого преобладания объективных признаков затруднения вдоха или выдоха. В тяжелых случаях, связанных со значительным переполнением легких кровью, что ведет к повышению ригидности легочной ткани, одышка может приобретать характер инспираторного диспноэ.
В случае изолированной правожелудочковой недостаточности, развившейся на фоне хронических обструктивных заболеваний легких (например, легочное сердце), одышка имеет экспираторный характер и сопровождается эмфиземой легких и другими признаками обструктивного синдрома (подробнее см. ниже).
В терминальной стадии ХСН нередко появляется апериодическое дыхание Чейна– Стокса, когда короткие периоды учащенного дыхания чередуются с периодами апноэ. Причиной появления такого типа дыхания является резкое снижение чувствительности дыхательного центра к СО2 (углекислому газу), что связано с тяжелой дыхательной недостаточностью, метаболическим и дыхательным ацидозом и нарушением перфузии головного мозга у больных ХСН.
При резком повышении порога чувствительности дыхательного центра у больных ХСН дыхательные движения “инициируются” дыхательным центром только при необычно высокой концентрации СО2 в крови, которая достигается лишь в конце 10–15-секундного периода апноэ. Несколько частых дыхательных движений приводят к снижению концентрации СО2 до уровня ниже порога чувствительности, в результате чего период апноэ повторяется.
Аускультация легких. При хронической левожелудочковой недостаточности и длительном застое крови в малом круге кровообращения в нижних отделах легких часто выслушиваются мелкопузырчатые незвучные влажные хрипы или крепитация, обычно на фоне ослабленного везикулярного или жесткого дыхания. Эти побочные дыхательные шумы выслушиваются симметрично с обеих сторон.
Крепитация нередко выслушивается при хроническом венозном интерстициальном застое крови в легких и обусловлена раскрытием на высоте максимального вдоха спавшихся альвеол. Теоретически спадение легочных альвеол во время выдоха может произойти и при отсутствии застоя крови в легких, однако объем воздуха в альвеолах, при котором это произойдет (“объем спадения альвеол”), очень мал и при обычном выдохе практически не достигается. При наличии венозного застоя крови в малом круге кровообращения и увеличении массы легочного интерстиция объем спадения альвеол увеличен и поэтому на выдохе достигается легче. Таким образом, при наличии интерстициального застоя альвеолы спадаются на выдохе уже при обычном дыхании. В результате на высоте последующего вдоха может выслушиваться крепитация.
Влажные мелкопузырчатые “застойные” хрипы в легких возникают в результате гиперпродукции жидкого бронхиального секрета. Влажные хрипы обычно выслушиваются с обеих сторон, преимущественно в нижних отделах легких.
При альвеолярном отеке легких, осложняющем течение ХСН, появление влажных хрипов связано с транссудацией в альвеолы небольшого количества плазмы крови, которая быстро достигает бронхов и, вспениваясь при дыхании, создает типичную аускультативную картину отека легких. В отличие от хронического венозного застоя, при альвеолярном отеке легких хрипы быстро распространяются на всю поверхность грудной клетки и становятся средне- и крупнопузырчатыми, что говорит о нахождении пенистого серозного секрета в крупных бронхах и трахее. В этих случаях у больного появляется клокочущее дыхание, слышимое на расстоянии.
Следует помнить, что в отдельных случаях у больных с хроническим застоем крови в малом круге кровообращения могут выслушиваться сухие хрипы при полном отсутствии влажных. Сухие хрипы в этих случаях возникают в результате выраженного отека и набухания слизистой бронхов невоспалительного характера. Они могут указывать на наличие застоя крови в легких только в том случае, если в анамнезе отсутствуют указания на сопутствующие бронхиальную астму или хронический бронхит.
Гидроторакс (транссудат в плевральной полости) нередко встречается у больных с бивентрикулярной ХСН. Обычно жидкость локализуется в правой плевральной полости, а количество транссудата не превышает 100–200 мл. При этом справа ниже угла лопатки и в аксиллярной области определяется небольшое притупление перкуторного звука и ослабление дыхания. Наблюдается также отклонение трахеи в сторону, противоположную скоплению транссудата. Побочные дыхательные шумы для гидроторакса не характерны.
Следует помнить, что плевральный выпот может быть симптомом не только правожелудочковой, но и левожелудочковой недостаточности, поскольку отток плевральной жидкости происходит как в вены большого круга кровообращения, так и в систему малого круга.
Исследование сердечно-сосудистой системы
Результаты пальпации, перкуссии и аускультации сердца у больных с хронической СН прежде всего определяются характером основного заболевания, осложнившегося развитием сердечной декомпенсации. Тем не менее можно выделить некоторые общие, хотя и неспецифические, признаки, характерные для большинства больных ХСН.
Пальпация и перкуссия сердца. Верхушечный толчок и левая граница относительной тупости сердца, как правило, смещены влево за счет расширения полости ЛЖ (рис. 2.16, а). При возникновении легочной артериальной гипертензии и вовлечении в патологический процесс правых отделов сердца пальпируются усиленный и разлитой сердечный толчок и эпигастральная пульсация, которые свидетельствуют о дилатации и гипертрофии ПЖ (рис. 2.16, б). В более редких случаях можно обнаружить смещение вправо правой границы относительной тупости и расширение абсолютной тупости сердца (рис. 2.16, в).
Следует помнить, что иногда сердечный толчок может выявляться также при значительном увеличении ЛП, поскольку оно топографически располагается позади ПЖ и при своем расширении оттесняет ПЖ кпереди.
В отличие от пульсации, обусловленной гипертрофией и дилатацией ПЖ (истинный сердечный толчок), пульсация, связанная с увеличением ЛП, определяется локально слева от грудины и не распространяется на эпигастральную область.
Аускультация сердца. Тахикардия часто выявляется у больных с ХСН. Увеличение ЧСС способствует, как известно, поддержанию более высоких значений сердечного выброса, поскольку МО = УО х ЧСС. В то же время следует помнить, что тахикардия является весьма неблагоприятным фактором, ведущим к росту внутримиокардиального напряжения и величины постнагрузки на ЛЖ. Кроме того, при тахикардии происходит укорочение диастолической паузы, что неблагоприятно сказывается на диастолическом наполнении желудочков (см. главу 1).
Рис. 2.16. Результаты пальпации и перкуссии сердца у больных с ХСН. а — смещение верхушечного толчка и левой границы сердца при дилатации ЛЖ; б — усиленный и разлитой сердечный толчок и эпигастральная пульсация при гипертрофии и дилатации ПЖ; в — смещение правой границы сердца при дилатации ПЖ При аускультации сердца у больных ХСН нередко выявляются разнообразные нарушения сердечного ритма и проводимости, в частности, фибрилляция предсердий и экстрасистолия. Сердечные аритмии не только усугубляют характерные для ХСН гемодинамические расстройства, но и существенно ухудшают прогноз больных с сердечной декомпенсацией. Диагностика нарушений сердечного ритма подробно описана в главе 3.
При ХСН важно оценить и правильно интерпретировать изменения громкости основных тонов сердца и появление дополнительных тонов. Ослабление I и II тонов наблюдается у многих больных ХСН, обычно указывая на уменьшение скорости сокращения и расслабления дилатированного ЛЖ. Однако при высоком давлении в ЛА во II межреберье слева от грудины может определяться акцент II тона на ЛА (рис. 2.17, а). Если одновременно замедляется изгнание крови из ПЖ (например, при его гипертрофии и/или снижении сократимости), на ЛА, помимо акцента II тона, определяется его расщепление за счет более позднего возникновения пульмонального компонента II тона (рис. 2.17, б).
Рис. 2.17. Изменение II тона при повышении давления в легочной артерии (а) и сочетании легочной артериальной гипертензии с замедленным изгнанием крови из ПЖ при его гипертрофии и дилатации (б) На верхушке сердца у больных ХСН с выраженной систолической дисфункцией и дилатированным желудочком нередко определяется дополнительный патологический III тон сердца и, соответственно, выслушивается трехчленный протодиастолический ритм галопа (рис. 2.18, б). Он возникает в конце фазы быстрого наполнения в результате гидравлического удара о стенку желудочка порции крови, перемещающейся под действием градиента давления из предсердия в желудочек. В норме при хорошем диастолическом тонусе сердечной мышцы и нормальном давлении в предсердии удар порции крови, поступающей из предсердия, как бы амортизируется нормально расслабляющимся миокардом желудочка (рис. 2.18, а). При любой объемной перегрузке желудочка, сопровождающейся его дилатацией, в том числе у больных ХСН, амплитуда и скорость диастолического расслабления падают и становятся существенно меньше объемной скорости кровотока из предсердия. Поэтому амортизации гидравлического удара крови о стенку дилатированного желудочка не происходит, и возникает III патологический тон сердца (рис. 2.18, б).
Рис. 2.18. Формирование патологического III тона и протодиастолического ритма галопа у больного с ХСН и объемной перегрузкой желудочка.
а — норма; б — протодиастолический ритм галопа Левожелудочковый протодиастолический ритм галопа следует выслушивать на верхушке сердца, лучше в положении больного на левом боку. При поражении ПЖ, сопровождающемся его объемной перегрузкой и дилатацией, в том числе у больных ХСН, можно выслушать правожелудочковый протодиастолический ритм галопа Он лучше определяется над мечевидным отростком или в V межреберье у левого края грудины.
Патологический IV тон и, соответственно, пресистолический ритм галопа обычно выявляется у больных с выраженной диастолической дисфункцией ЛЖ (“жесткий”, неподатливый желудочек) в момент усиленного сокращения ЛП (рис. 2.19). Поэтому любые причины, ведущие к увеличению жесткости стенки желудочка (гипертрофия, ишемия, фиброз и др.) и давления наполнения, в том числе у больных с систолической ХСН, могут вызвать появление патологического IV тона. Наоборот, при отсутствии сокращения предсердий (мерцательная аритмия) или разобщении сокращений предсердий и желудочков (АВ-блокада III степени) IV тон не выявляется.
Следует все же помнить, что для больных с систолической ХСН и объемной перегрузкой желудочка наиболее характерно появление протодиастолического ритма галопа.
Рис. 2.19. Формирование патологического IV тона у больного с ХСН при увеличении «жесткости» стенки ЛЖ (гипертрофия, ишемия, фиброз).
а — норма; б — пресистолический ритм галопа Запомните
1. Патологический III тон и, соответственно, протодиастолический ритм галопа — важнейший аускультативный признак объемной перегрузки желудочка, сопровождающейся его дилатацией. У больных с систолической формой ХСН ритм галопа — это “крик сердца о помощи” (В.П. Образцов). Он появляется при резком ухудшении сократимости и снижении амплитуды и скорости диастолического расслабления сердечной мышцы. 2. Патологический IV тон сердца и пресистолический ритм галопа менее характерны для систолической ХСН и возникает только при значительной ригидности стенки желудочка, обусловленной гипертрофией миокарда, фиброзом сердечной мышцы или выраженной ишемией, и свидетельствует о наличии сопутствующей диастолической дисфункции ЛЖ и повышении давления наполнения.
Артериальный пульс. Изменения артериального пульса у больных ХСН зависят от стадии сердечной декомпенсации, выраженности гемодинамических расстройств и наличия нарушений сердечного ритма и проводимости. В тяжелых случаях артериальный пульс частый (pulsus frequens), нередко аритмичный (pulsus irregularis), слабого наполнения и напряжения (pulsus parvus et tardus). Уменьшение величины артериального пульса и его наполнения, как правило, указывают на значительное снижение УО и скорости изгнания крови из ЛЖ.
При наличии мерцательной аритмии или частой экстрасистолии у больных ХСН важно определить дефицит пульса (pulsus deficiens). Он представляет собой разность между числом сердечных сокращений и частотой артериального пульса. Дефицит пульса чаще выявляется при тахисистолической форме мерцательной аритмии (см. главу 3) в результате того, что часть сердечных сокращений возникает после очень короткой диастолической паузы, во время которой не происходит достаточного наполнения желудочков кровью. Эти сокращения сердца происходят как бы “впустую” и не сопровождаются изгнанием крови в артериальное русло большого круга кровообращения. Поэтому число пульсовых волн оказывается значительно меньшим, чем количество сердечных сокращений. Естественно, при уменьшении сердечного выброса дефицит пульса возрастает, свидетельствуя о значительном снижении функциональных возможностей сердца.
Альтернирующий пульс (pulsus alternans) характеризуется регулярным чередованием пульсовых волн большой и малой амплитуды при правильном (чаще синусовом) ритме (рис. 2.20). Чаще всего альтернирующий пульс можно обнаружить у больных с тяжелой левожелудочковой миокардиальной недостаточностью, главным образом, у пациентов с АГ и ИБС. Альтернирующий пульс сочетается с таким же регулярным изменением величины ударного выброса и громкости тонов сердца.
Причины альтернирующего пульса у больных ХСН до конца не выяснены. Полагают, что это связано с выраженной неоднородностью мышцы ЛЖ, некоторые участки которого, например, области ишемизированного “гибернирующего” миокарда (см. главу 5), отвечают механическим сокращением не на каждый приходящий к ним электрический импульс. Это может быть связано, например, с более продолжительным рефрактерным периодом кардиомиоцитов, расположенных в данной ишемизированной зоне, или с другими причинами. Кстати, в части случаев альтернирующий пульс сочетается с такой же регулярной альтернацией желудочковых комплексов QRS на ЭКГ (электрическая альтернация).
Так или иначе, появление альтернирующего пульса у больных ХСН является весьма неблагоприятным признаком, указывающим на тяжесть гемодинамических расстройств.
Артериальное давление. В тех случаях, когда у больного ХСН до появления симптомов сердечной декомпенсации отсутствовала артериальная гипертензия (АГ), уровень АД по мере прогрессирования СН нередко снижается. В тяжелых случаях систолическое АД (САД) достигает 90–100 мм рт. ст. а пульсовое АД — около 20 мм рт. ст. что связано с резким снижением сердечного выброса. Рис. 2.20. Альтернирующий пульс (PS) и электрическая альтернация (ЭКГ)
Запомните
Если пульсовое АД не превышает 20 мм рт. ст. и имеется отчетливое снижение систолического АД, величина сердечного индекса в большинстве случаев не превышает 2,2 л/мин/м2.
У больных АГ цифры АД могут быть повышены, но в терминальной стадии ХСН, как правило, имеется отчетливая тенденция к снижению давления.
Исследование других органов
Печень. При застое в венах большого круга кровообращения практически всегда наблюдается увеличение печени (застойная гепатомегалия). Печень при пальпации увеличена, край ее закруглен. Если застой в венах большого круга развивается достаточно быстро, печень может быть болезненной при пальпации. Со временем может развиваться так называемый кардиальный цирроз печени. Край печени тогда становится заостренным, а сама печень очень плотной.
Асцит выявляется, как правило, в тяжелых случаях правожелудочковой и бивентрикулярной недостаточности, особенно при констриктивном перикардите или недостаточности трехстворчатого клапана. Его появление при систолической ХСН свидетельствует о наличии выраженной надпеченочной портальной гипертензии.
Таким образом, симптоматика ХСН весьма многообразна и позволяет прежде всего составить представление о преимущественном поражении левых или правых отделов сердца и застое крови в соответствующем круге кровообращения. Однако следует помнить, что перечисленные ниже признаки лево- и правожелудочковой недостаточности не исчерпывают всей клинической картины хронической систолической СН. Такие признаки, как тахикардия, никтурия, быстрая мышечная утомляемость, тяжесть в нижних конечностях, сердечная кахексия и другие, не могут быть объяснены только гемодинамическими расстройствами в малом или большом круге кровобращения, поскольку в их генезе решающее значение имеет активация САС, РААС, системы цитокинов и т.п. Запомните
1. Для хронической левожелудочковой недостаточности, сопровождающейся застоем крови в малом круге кровообращения, наиболее характерны следующие признаки, выявляемые при объективном исследовании и расспросе больного: одышка (тахипноэ, ортопноэ);
сухой непродуктивный кашель, возникающий преимущественно в горизонтальном положении;
удушье (сердечная астма или отек легких), т.е. проявление острой СН, возникающей на фоне ХСН;
положение ортопноэ;
влажные хрипы в легких;
дилатация ЛЖ;
акцент II тона на легочной артерии;
протодиастолический (левожелудочковый) ритм галопа;
альтернирующий пульс.
2. Для хронической правожелудочковой недостаточности, протекающей с застоем крови в большом круге кровообращения, характерны:
История болезни ибс стенокардия напряжения хсн. Способ комплексного иммуномодулирующего лечения пациентов с хр
Изобретение относится к медицине, а именно к кардиологии, и касается комплексного иммуномодулирующего лечения пациентов с хронической сердечной недостаточностью со сниженной фракцией сердечного выброса левого желудочка. Для этого в общепринятый комплекс лекарственной терапии, включащий -адреноблокаторы, ингибиторы АПФ, диуретики, кардиомагнил, дополнительно вводят рекомбинантный интерлейкин 2 (ИЛ-2) человека. ИЛ-2 вводят в дозе 500 тыс. МЕ/мл, в 200 мл физиологического раствора, содержащего для стабилизации 10 мл 5% раствора альбумина, внутривенно капельно ежедневно 1 раз в течение 10 дней; курс лечения повторяют 1 раз в 3 месяца в течение 12 месяцев. Такое комплексное лечение обеспечивает подавление хронического иммунного воспаления за счет способности ИЛ-2 в разработанном режиме введения эффективно снижать уровень эндогенных цитокинов и активировать Т- и В-лимфоциты у данной группы больных. 2 табл.
Изобретение относится к медицине и может быть использовано в кардиологии, ангиологии, кардиохирургии, реабилитологии, трансплантологии.
Известен способ лечения хронической сердечной недостаточности у больных хронической сердечной недостаточности (ХСН) на фоне ишемической болезни сердца, в котором используются -адреноблокатор, диуретик и ингибитор АПФ, титруемые до максимально переносимых доз [1].
Данный способ является наиболее близким к заявляемому по технической сущности и достигаемому клиническому результату и выбран в качестве прототипа. Предложенная терапия обеспечивает комплекс эффектов — антиатерогенный, антиангинальный и противоишемический.
Недостатком данного способа является то, что у больных с ХСН ФК II-IV по NYHA и сниженной фракцией выброса левого желудочка (ФВ ЛЖ
Задачей изобретения является повышение эффективности способа.
Поставленная задача решается путем дополнительного назначения к традиционной терапии -адреноблокатором (112-адреноблокатор нового поколения карведилол), ингибитором АПФ (энап) и диуретиком (гипотиазид) рекомбинантного человеческого интерлейкина 2 (rИЛ-2) в дозе 500 тыс. МЕ/мл, разведенного в 200 мл физиологического раствора, содержащего для стабилизации 10 мл 5% раствора альбумина, внутривенно ежедневно капельно 1 раз в течение 10 дней; курс лечения повторяют 1 раз в 3 месяца в течение 12 месяцев.
Рекомбинантный человеческого интерлейкина 2 представляет собой препарат ронколейкин® фирмы «Биотекс» Россия.
Новым в предлагаемом способе является дополнительное назначение ронколейкина® в дозе 500 тыс. МЕ/мл, разведенного в 200 мл физиологического раствора, содержащего для стабилизации 10 мл 5% раствора альбумина, внутривенно ежедневно капельно 1 раз в течение 10 дней; курс лечения повторяют 1 раз в 3 месяца в течение 12 месяцев.
Предложенный способ иммуномодулирующей терапии ХСН с использованием rИЛ-2 основан на том, что на фоне имеющейся гиперактивации провоспалительных цитокинов (ИЛ-1, ИЛ-6, ФНО), отражающей наличие хронического иммунного воспаления при атеросклерозе и приводящей к дисфункции эндотелия, развивается местная реакция на атеросклеротическое и/или ишемическое повреждение, активизирующая персистирующее воспаление, при котором усиливается, как отмечено выше, экспрессия цитокинов, иммунокомпетентных клеток, включая моноциты, макрофаги, эндотелиоциты, T-лимфоциты [8, 9]. Использование супрессивного влияния rИЛ-2 на избыточную цитокиновую активацию, содержание циркулирующих иммунных комплексов и титр антител к кардиолипину, уровень которых коррелирует с тяжестью ХСН, приводит к уменьшению тяжести тканевых повреждений и расстройств микроциркуляции. В таких условиях блокирование эндогенных провоспалительных цитокинов не только оправдано, но и может служить средством выбора для эффективной безопасной патогенетической терапии [10].
Следовательно, дополнительное назначение нового отечественного иммуномодулятора рекомбинантного ИЛ-2 к основной терапии ХСН II-IV ФК по NYHA позволяет подойти к решению следующих задач:
— обосновать новые (более эффективные и безопасные) подходы к диагностике, профилактике и лечению тяжелой, в том числе декомпенсированной, ХСН;
— обеспечить стабилизацию и обратное развитие ремоделирования ЛЖ на фоне ХСН после перенесенного Q-образующего инфаркта миокарда;
— оптимизировать современные эффективные пути медикаментозного лечения, направленного на повышение качества жизни и улучшение выживаемости пациентов с постинфарктной дисфункцией ЛЖ и хронической сердечной недостаточностью.
Отличительные признаки проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не очевидные для специалиста. Идентичной совокупности признаков в проанализированной литературе не обнаружено. Предлагаемое изобретение может быть использовано в здравоохранении.
Исходя из вышеизложенного, следует считать изобретение соответствующим условиям патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применимость».
Способ осуществляется следующим образом.
Обследовано 28 больных с ХСН III-IV ФК по NYHA и ФВ ЛЖ менее 40%: в 1 группу вошли пациенты (n=16) в возрасте 54,7±5,1 год с ХСН III ФК и ФВ ЛЖ менее 40% (в среднем 32,5±3,9%), во 2 — пациенты (n=12) в возрасте от 46 до 62 лет (57±4,2) с тяжелой ХСН IV ФК и ФВ ЛЖ
На фоне приема аспирина в дозе 75 мг/сут, 112-адреноблокатора карведилола (в дозе, начиная с 6,125 мг/сут в два приема с последующим ее увеличением до максимально переносимой (в среднем 19,6±5,4) мг/сут), иАПФ энапа и диуретика гипотиазида назначался рекомбинантный ИЛ-2 человека в дозировке 500 тыс МЕ/мл при разведении в 200 мл физиологического раствора с добавлением для стабилизации 10 мл 5% раствора альбумина, внутривенно капельно, ежедневно, 10 инъекций. В течение 12 месяцев проводили 4 курса (1 раз в 3 месяца).
Пациентам с ХСН IV ФК и низкой ФВ ЛЖ (
Критериями оценки хорошего антиишемического и гемодинамического эффектов rИЛ-2 считали: регресс симптомов ХСН, уменьшение частоты и тяжести стенокардии, снижение суточной потребности нитратов, повышение физической толерантности не менее 10%, поддержание стабильного АД, при отсутствии ухудшений метаболического состояния, а также без возникновения явных аллергических или усугубления иммунных нарушений.
Индивидуальную переносимость иммунотропного препарата rИЛ-2 оценивали по следующим показателям: отличная — при отсутствии побочных эффектов в течение всего срока наблюдения, нормализации общего состояния, улучшении иммунологических и общелабораторных показателей и параметров внутрисердечной гемодинамики; хорошая — при улучшении общего состояния, качества жизни, отчетливой клинико-лабораторной и иммунологической положительной динамики; неудовлетворительная — при возникновении побочных эффектов, потребовавших отмены препарата [11].
С целью оценки исследуемых показателей проводили забор крови из кубитальной вены натощак в стеклянную пробирку, содержащую 70-100 Ед. гепарина в количестве 7-10 мл крови, тщательно перемешивая с тем, чтобы предотвратить образование сгустков. Определение иммуноглобулинов в сыворотке крови проводили методом радиальной иммунодиффузии в геле по Манчини [12]. Определение Ауто-АТ к кардиолипину проводили с использованием иммуноферментного анализа (ИФА) на стандартных плашках по методике «БиоХимМак». Оптическую плотность определяли на спектрофотометре «Reader Pasteur LP-400», длина волны 450 нм, по результатам которой строят калибровочную кривую [12]. Исследование содержания цитокинов в сыворотке крови проводили методом твердофазного ИФА в системе бидетерминантного определения антигена с применением пероксидазы в качестве индикаторного фермента [12]. Для определения концентраций ИЛ-1, ИЛ-2, ИЛ-6, ИЛ-8, ФНО-, ИФ- использовали тест-системы производства ООО «Цитокин» (г. Санкт-Петербург) с порогом чувствительности для ИЛ-1 — 5 пг/мл, ИЛ-2, ИЛ-6, ИЛ-8 — 10 пг/мл, ФНО- — 20 пг/мл, ИФ- — 10 пг/мл, ИФ- — 10 пк/мл.
Статистический анализ полученных цифровых данных проводили с использованием пакетов статистических программ (MICROSOFT ACCESS, EXCEL for Windows; STATISTICA 6).
Изменения гуморального звена иммунитета в динамическом проспективном 12-месячном наблюдении у больных 1 и 2 групп представлены в таблице 1. Применение rИЛ-2 у больных 1 и 2 групп через 12-месячной курсовой терапии позволило снизить исходно повышенные уровни Ауто-АТ к КЛ в 1,1 и 1,5 раза соответственно, a IgA в 2,2 и 1,7 раза. К концу 12-месячной курсовой терапии содержание ЦИК у пациентов 2 группы снизилось в 1,4 раза (p
Анализ исходных значений цитокинового статуса сыворотки крови показал, что у пациентов обеих групп имелось избыточное содержание ИЛ-2, ИЛ-6, ИЛ-8, ФНО- в крови (таблица 2). В 1 группе 12-месячная терапия rИЛ-2 привела к значительному снижению уровней провоспалительных цитокинов: ИЛ-2 — на 73%, ИЛ-6 — на 38%, ИЛ-8 — на 29% и ФНО — на 50%, а во 2 группе — на ИЛ-2 — на 37,5%, ИЛ-6 — на 21,4%, ИЛ-8 — на 26% и ФНО — на 36%.
ПРИМЕР 1: Больной Н. 55 л. пенсионер, (история болезни №2657, 2005 г.) обследован в ГУ НИИ кардиологии ТНЦ СО РАМН с диагнозом: ИБС. Постинфарктный (2002, 2003 г.) кардиосклероз. Состояние после АКШ (2003 г.) Атеросклероз аорты. Недостаточность АК I ст. Относительная недостаточность МК II ст. Артериальная гипертония III стадии, II степени повышения АД, риск 4. НК I ст. III ФК по NYHA. Жалобы на одышку при подъеме при ходьбе по прямой на 400-500 м, отеки на голенях, повышение АД до 160/100 мм рт. ст. ЭКГ: Ритм синусовый правильный, тахикардия 94 в мин. Рубцовые изменения миокарда верхушечной, боковой стенки левого желудочка. ЭХО КГ: ФВ ЛЖ 45%, КДО 193 мл, ЛП 46 мл. Зоны гипокинезии. ТФН 35 Вт, КПН — одышка.
Назначено: карведилол 30 мг/сут, энап 10 мг/сут, гипотиазид 25 мг, ронколейкин 500 тыс. МЕ/мл в 200 мл физиологического раствора с добавлением для стабилизации 10 мл 5% раствора альбумина, внутривенно капельно, ежедневно №10 (4 курса за 12 мес).
Динамика иммунограммы:
Показатели исходно Через 6 мес исходно / через 6 мес Через 12 мес через 6 мес/ через 12 мес IgA г/л 2,4 2,0 -17 1,8 -10 IgM г/л 2,6 1,9 -27 1,4 -26 IgG г/л 15,5 12,5 -19 11,0 -12 ЦИК 4,17% у.е. 77 66 -14 42 -36 Ауто AT к КЛ Мед/мл 47 30 -36 18 -40 IL-1 48 33 -31 17 -49 IL-2 80 72 -10 54 -25 IL-6 32 21 -34 17 -19 TNF- 16 10 -38 8 -20
Через 12 месяцев комплексной терапии на фоне явной положительной динамики иммунограммы отмечен значительный прирост ТФН (до 125 Вт), улучшилось качество жизни, стабилизировано АД, ЧСС (68/мин), отсутствуют отеки.
ПРИМЕР 2: Больной И. 63 г. инвалид II гр. (история болезни №3088, 2004 г.) обследован с диагнозом: ИБС. Стенокардия напряжения II ФК. Постинфарктный (2002 г.) кардиосклероз. Состояние после АКШ (2003 г.). Атеросклероз аорты. Артериальная гипертония III стадии, III степени повышения АД, риск 4. НК 1 ст. II ФК по NYHA. При поступлении жалобы на одышку, сжимающие боли при ходьбе на 400-500 м (потребность в нитроглицерине до 3 т/сут), повышение АД до 190/110 мм рт. ст. ЭКГ: ритм синусовый, правильный, ЧСС 89 в мин. Рубцовые изменения миокарда нижне/боковой области ЛЖ. ЭХО: ФВ ЛЖ 52%, КДО 142 мл, ЛП 42 мм. Зоны гипокинезии. ТФН 45 Вт. КПН: ангинозные боли, одышки, ЧСС 130/мин.
Амбулаторно принимал гипотиазид 25 мг/сут, энап 20 мг/сут. В стационаре к терапии добавлен карведилол 30 мг/сут.
Динамика иммунограммы:
Показатели Исходно Через 6 мес исходно/ через 6 мес Через 12 мес через 6 мес / через 12 мес IgA г/л 2,5 2,2 -12 2,5 +13 IgM г/л 2,1 2,4 +14 3,7 +54 IgG г/л 14,5 10,8 -26 20,0 +85 ЦИК 4,17% у.е. 75 72 -4 64 -11 Ауто AT к КЛ Мед/мл 41 32 -22 23 -28 IL-1 48 46 -4 40 -13 IL-2 86 80 -7 72 -10 IL-6 36 34 -6 28 -18 TNF- 20 17 -15 14 -18
Через 12 месяцев терапии карведилолом на фоне незначительной динамики показателей иммунограммы отмечен прирост ТФН на 1 ступень (до 75 Вт), урежение ангинозных болей до 1-2 приступов в день, снижение суточной потребности в нитроглицерине до 0-1 табл./сут, АД составляет 120-140/80-90 мм рт. ст. ЧСС во время осмотра 70/мин.
В обеих группах клинический эффект терапии проявлялся регрессом симптомов ХСН, снижением тяжести ФК ХСН, уменьшением частоты и тяжести стенокардии и потребности в НТГ, улучшением физической толерантности, стабилизации АД и внутрисердечной гемодинамики, но выраженность и скорость купирования симптомов ХСН на фоне комбинированной терапии с использованием иммуномодулятора ронколейкина была достоверно и значимо выше.
Предлагаемый способ применен у 28 пациентов и позволяет повысить эффективность способа лечения хронической сердечной недостаточности за счет воздействия на основные патогенетические механизмы заболевания — снижения выраженности избыточной иммунной активации и воспаления при ХСН.
СПИСОК ЛИТЕРАТУРЫ
1. Заугольникова О.А. Малишевский М.В. Кулягина Н.В. Клевцова Т.В. Строкач В.В. Способ лечения хронической сердечной недостаточности. Патент РФ RU 2304964 C2, 27.08.2002.
2. Беленков Ю.Н. Парадоксы сердечной недостаточности: взгляд на проблему на рубеже веков. Ю.Н.Беленков, Ф.Т.Агеев, В.Ю.Мареев. Сердечная недостаточность, 2000: 1; 5-7.
3. Насонов Е.Л. Иммунопатология застойной сердечной недостаточности: роль цитокинов. Е.Л.Насонов, М.Ю.Самсонов, Ю.Н.Беленков, Д.И.Фукс. Кардиология, 1999: 3; 66-73.
4. Ольбинская Л.И. Игнатенко С.Б. Роль цитокиновой агрессии в патогенезе синдрома сердечной кахексии у больных хронической сердечной недостаточностью. Л.И. Сердечная недостаточность, 2001, Т.2, №3; 18-26.
5. Павликова, Е.П. Мерай И.А. Клиническое значение интерлейкина-6 и фактора некроза опухоли при ишемической болезни сердца. Кардиология, 2003; Т.8: 68-71.
6. Dral H. Ficher S.G. Fay W.P. Effects of amiodarone on tumor necrosis factor-alpha levels in congestive heart failure secondary to ischemic or idiopathic dilated cardiomyopathy. Am J Cardiol, 1999; 83: 388-391.
7. Gullestad L. Aukrust P. Heland T. Effect of high-versus Low dose of angiotensin converting enzyme inhibition of cytokine levels in chronic heart failure. J. Am Coll. Cardiol, 1999: Vol.34; 2061-2067.
8. Ross R. The pathogenesis of atherosclerosis: a perspective for 1990s. Nature 1993; 362: 801-809.
9. Schillinger M, Exner M, Mlekusch W et al. Acute-phase response after stent implantation in the carotid artery: association with 6-month in-stent restenosis. Radiology 2003; 227: 516-21.
10. Нагорнов B.A. Зота Е.Г. Цитокины, иммунное воспаление и атеросклероз. Успехи современной биологии, 1996; 111: 48-59.
11. Борисова A.M. Лактионова Л.В. Сетдикова Н.Х. Клиническое применение отечественного препарата полиоксидоний при вторичных иммунодефицитных состояниях взрослых. Терапевтический архив, 1998; Т. 70, №10: 52-57.
12. Хаитов P.M. Пинегин Б.В. Истамов Х.И. Экологическая иммунология. М. ВНИРО, 1995, С.218.
Таблица 1 Влияние 6-, 12-месячной курсовой терапии карведилолом и иАПФ энапом в комплексе с rИЛ-2 на показатели гуморального звена иммунитета у больных ИБС с ХСН III-IV ФК по NYHA (M±m) Показатели до лечения p через 6 мес p с группой сравнения/ с группой доноров (%) через 12 мес p с группой сравнения/ с группой доноров (%) Группа сравнения (n=88) Группа доноров (n=20) (n=16) (n=12) (n=10) груп-па 1 ХСН III ФК IgA, г/л 5,8±1,2 p1=0,05 2,4±0,2 нд -50/+20 2,2±0,1 нд -54/+10 4,8±1,5 2±0,5 IgM, г/л 1,8±0,3 нд 1,7±0,3 нд -10,5/-15 1,8±0,5 нд -5,3/-10 1,9±0,1 2±0,5 IgG, г/л 15,3±0,8 нд 14,3±0,2 нд +2,2/+30 12,8±0,3 нд -8,6/+16,4 14±1 11±3 ЦИК, у.е. 69±8,2 нд 57±8 нд -1,7/+63 57±3 нд -1,7/+63 58±9 35±15 АутоАТ к КЛ МЕ/мл 18±2,2 р1=0,01 15±5,3 р1=0,01 -10,7/- 16±2,8 р1=0,01 -4,8/- 16,8±2,3 0 (n=12) (n=10) (n=8) груп-па 2 ХСН IV ФК IgA, г/л 6,3±1,2 р1=0,05 4,2±2,5 нд -12,5/-110 3,8±1,5 нд -21/+90 4,8±1,5 2±0,5 IgM, г/л 2±0,2 нд 1,8±0,1 нд -5,3/-10 2,0±0,3 нд +5,3/0 1,9±0,1 2±0,5 IgG, г/л 18,1±0,5 нд 15,5±0,5 нд +11/+41 14,6±0,2 нд +4,3/+33 14±1 11±3 ЦИК, у.е. 78±11,2 р1=0,05 63±10 нд +8,6/+80 55±3 нд -5,2/+57 58±9 35±15 АутоАТ к КЛ МЕ/мл 24±2,3 p1=0,01 20±2,5 p1=0,01 -19/- 16±2,1 p1=0,01 -4,8/- 16,8±2,3 0 Примечание: p1 — для сравнения в группе с донорами; р2 — для сравнения в группе до и после лечения; нд — недостоверные различия; группа сравнения — группа пациентов, перенесших крупноочаговый ИМ давностью 6 месяцев и более, которые до включения исследование не имели признаков ХСН и получали базовую антиишемическую терапию без -адреноблокаторов; группа доноров — группа практически здоровых лиц.
Способ комплексного иммуномодулирующего лечения пациентов с хронической сердечной недостаточностью со сниженной фракцией выброса левого желудочка путем назначения медикаментозной терапии группой препаратов: -адреноблокаторов, ингибиторов АПФ, диуретиков, кардиомагнила, отличающийся тем, что пациентам дополнительно назначают рекомбинантный ИЛ-2 человека в дозе 500 тыс. МЕ/мл, разведенный в 200 мл физиологического раствора, содержащего для стабилизации 10 мл 5%-ного раствора альбумина, внутривенно капельно ежедневно, 1 раз в течение 10 дней; курс лечения повторяют 1 раз в 3 месяца в течение 12 месяцев.
Хроническая недостаточность сердца
Недостаточность сердца — это такое состояние, когда нарушается способность его выполнять работу, необходимую для нормального кровообращения в организме (в покое и при физических нагрузках). При этом нарушается соответствие количества крови, оттекающей от сердца и притекающей к нему из периферических сосудов. Снабжение тканей кислородом и питательными веществами резко нарушается. У детей хроническая недостаточность встречается значительно реже, чем у взрослых, что связано с меньшей частотой тяжелых заболеваний сердца и с большими компенсаторными возможностями детского организма.
Этиология хронической недостаточности сердца
Основными причинами развития недостаточности сердца являются или его поражение, или перегрузка,в ряде случаев их сочетание. Нарушение кровообращения может наступить в тяжелых случаях ревматизма, особенно при непрерывно рецидивирующем течении и выраженном пороке сердца. Кроме того, причиной могут быть врожденные пороки сердца с нарушением гемодинамики. Встречающаяся у детей стойкая гипертензия малого и большого круга кровообращения также приводит к развитию недостаточности сердца.
Патогенез и патоморфология хронической недостаточности сердца
По механизму развития различают две формы недостаточности сердца: энергетически-динамическую (обменную, Хегглин) и гемодинамическую, или застойную. Недостаточность сердца развивается при исчерпании компенсаторных возможностей и снижении сократительной способности сердечной мышцы. Это может явиться следствием нарушения обменных процессов в миокарде в результате его поражения при инфекционных заболеваниях (миокардит, токсическое поражение), интоксикациях, авитаминозах, недостаточном снабжении кровью при коронарите. Снижается сократительная способность миокарда, развивается миокардиальная (контрактильная), или обменная, форма недостаточности. Недостаточность кровообращения может развиться также в результате постоянной перегрузки миокарда из-за переполнения отделов сердца увеличенным объемом крови при недостаточности клапанов (регургитация), при повышении сопротивления оттоку крови в систоле вследствие сужения сосудов или повышения давления в них (стеноз аорты, легочного ствола, гипертензия большого или малого круга кровообращения).
При этом вначале усиливается работа миокарда, гипертрофируются его волокна (тоногенная дилатация сердца), затем по мере истощения резервов и снижения сократительной способности сердечной мышцы из-за развития дистрофических изменений наступает расширение отдельных полостей сердца (миогенная дилатация). Уменьшается скорость кровотока, снижается минутный объем сердца, ухудшается снабжение кровью, а следовательно, кислородом и питательными веществами тканей. Развивается одышка, появляются отеки, застойные изменения в органах и тканях. Такая недостаточность носит название гемодинамической. Кроме того, нарушение кровообращения может иметь в своей основе и сочетание различных форм недостаточности сердца, например, при ревматическом миокардите у ребенка с ранее сформировавшимся пороком (Ф. 3. Меерсон). Обычно нарушение обменных процессов и снижение энергетического метаболизма бывает первичным. Возможно поражение преимущественно левого или правого желудочка. За ним следует снижение сократительной функции сердечной мышцы, развивается хроническое нарушение кровообращения.
Классификация хронической недостаточности сердца
Согласно классификации Н. Д. Стражеско и В. X. Василенко, выделяют три степени хронической недостаточности кровообращения: I, IIA, ПБ и III. Лечение эффективно при I, IIА и ПБ степени. При III степени улучшение не наступает, что указывает на глубокие дистрофические изменения в миокарде.
Клиника хронической недостаточности сердца
На фоне основного заболевания (чаще ревматизма) ухудшается общее состояние больного и появляются признаки недостаточности кровообращения. При недостаточности I степени признаки нарушения кровообращения (одышка, сердцебиение, утомляемость, головная боль) появляются только после физической нагрузки.
При недостаточности II степени эти явления наблюдаются и в покое. Недостаточность кровообращения IIA степени проявляется одышкой, незначительным увеличением печени и периодически возникающей отечностью нижних конечностей. При недостаточности кровообращения ПБ степени увеличение печени более заметное, отеки стойкие, отмечается незначительное снижение диуреза.
Недостаточность кровообращения III степени характеризуется тяжелым общим состоянием, сильной одышкой, значительным увеличением печени, выраженными отеками, появлением асцита, застойными явлениями в легких, снижением диуреза. В. И. Бураковский и Б. А. Константинов (1970) модифицировали классификацию Н. Д. Стражеско и В. X. Василенко применительно к раннему возрасту: при недостаточности кровообращения I степени отмечается затруднение при кормлении; IIA — одышка и тахикардия в покое; ПБ — одышка, тахикардия, увеличение печени; III — анасарка, кахексия, гепатомегалия.
Выделяют три формы недостаточности кровообращения: острую, подострую и хроническую. Выделение таких форм связано с тем, что у детей раннего возраста классические симптомы недостаточности кровообращения часто выражены неотчетливо.
При преимущественной недостаточности левого желудочка, который не в состоянии выбросить весь объем крови в аорту, происходит застой в левом предсердии и малом круге кровообращения. Появляются одышка, приступы сердечной астмы, развивается отек легких.
Преимущественная недостаточность правого желудочка наблюдается в результате повышения давления в малом круге кровообращения при различных заболеваниях легких. Наиболее характерным является застой крови в сосудах большого круга кровообращения с увеличением печени, развитием отеков.
У детей, больных ревматизмом, обычно развивается смешанная (тотальная) недостаточность сердца (кровообращения).
Диагноз хронической недостаточности сердца
Диагноз хронической недостаточности сердца основывается на тщательном анализе данных клинического исследования. При маловыраженных явлениях недостаточности могут быть использованы функциональные пробы с нагрузкой.
Дифференциальный диагноз хронической недостаточности сердца
Дифференциальный диагноз недостаточности сердца в большинстве случаев не вызывает особых затруднений. Цианоз и одышку при поражении сердца следует дифференцировать с такими же симптомами недостаточности легких. В отличие от отеков при заболеваниях почек отеки при недостаточности сердца не сопровождаются выраженными изменениями в моче. Кроме того, они обычно появляются на нижних конечностях, тогда как первые — на лице (особенно на веках, где имеется рыхлая подкожная основа). Отечные конечности у больных с недостаточностью сердца холодны на ощупь, имеют цианотический оттенок. У больных с почечными отеками кожа бледная, но теплая. Увеличение печени может быть признаком гепатита ревматической этиологии.
Прогноз зависит от степени нарушения кровообращения и тяжести основного заболевания.
Лечение хронической недостаточности сердца
Лечение при хронической недостаточности сердца должно быть комплексным и строго индивидуализированным. Большое значение имеют рациональный режим, правильно подобранная диета. Необходимо выяснение и по возможности устранение причины недостаточности. Основную роль играет рациональная лекарственная терапия.
При явлениях хронической недостаточности сердца II и III степени показан постельный режим. Только в отдельных случаях при стабилизации клинических явлений недостаточности ПА степени можно постепенно перевести ребенка на полупостельный режим. При тяжелой недостаточности больному необходимо создать возвышенное положение в постели.
Прием пищи следует проводить чаще, но небольшими порциями. Рекомендуется увеличить количество продуктов, богатых калием (картофель, капуста, чернослив, изюм, творог, молоко). При отеках следует резко ограничить введение соли (по 2 — 4 г/сут). Питьевой режим необходимо назначать с учетом водного баланса (давать такое количество жидкости, какое организм способен выделить). Периодически можно назначать сахарно-фруктовые дни (200 г сахара в сутки) или видоизмененную диету Карреля (700 мл молока в сутки, в последующие дни постепенно добавляя белый хлеб, кашу, яйцо, картофельное пюре). П. Гегеши Кишш и Д. Сутрели рекомендуют в сутки 300 мл молока, 2 яйца, 3 яблока и 200 мл чая с лимоном.
Лекарственное лечение должно быть направлено в первую очередь на терапию основного заболевания (чаще всего ревматизма). Назначают кардиотонические средства (сердечные гликозиды), препараты, улучшающие метаболизм в миокарде, и диуретические. Значение каждой из упомянутых групп препаратов зависит от стадии недостаточности и глубины нарушения обменных процессов и сократительной функции миокарда. При выборе кардиотонических препаратов учитывается степень недостаточности кровообращения.
При недостаточности кровообращения I и 11А степени рекомендуется назначать менее активные сердечные гликозиды, например препараты горицвета, ландыша и др. Обычно применяют настой горицвета (2,0 — 100,0 по 1 десертной или столовой ложке 3 — 4раза вдень). Назначают также адонизид или настойку ландыша — по столько капель на прием, сколько лет ребенку.
При недостаточности кровообращения НА и ПБ, а также III степени необходимо назначать сердечные гликозиды, которые обладают значительным кардиостимулирующим действием. К ним относятся строфантин, коргликон, препараты наперстянки для перорального (лантозид), перорального и парентерального (изоланид, дигоксин, дигитоксин) введения, получившие наибольшее распространение в педиатрической практике. Можно применять также препараты джута — олиторизид, олеандра — нериолин, обвойника — периплоцин и др.
При назначении сердечных гликозидов следует учитывать способность препаратов кумулироваться в организме. Строфантин и коргликон относительно быстро выводятся из организма, оказывая быстрый эффект. Препараты наперстянки, наоборот, действуют более медленно, однако обладают значительно выраженными кумулятивными свойствами.
Лечение сердечными гликозидами следует начинать с определения максимальной терапевтической дозы. Строфантин детям в возрасте до двух лет назначается в дозе 0,01 мг/кг, старше двух лет — 0,007 мг/кг, что составляет 0,1 — 0,4 мл 0,05% раствора в сутки. При тяжелом состоянии строфантин следует вводить два раза в сутки. Доза коргликона детям в возрасте до двух лет — 0,013 мг/кг, детям старше двух лет — 0,01 мг/кг, т. е. от 0,2 до 0,75 мл 0,06% раствора.
Эти препараты вводят в тех случаях, когда нужен быстрый терапевтический эффект. Они показаны при острой недостаточности сердца или при нарушении предсердно-желудочковой проводимости.
Строфантин можно применять при замедленном пульсе и аритмии, так как ваготропное его действие невелико. Нередко после достижения определенного эффекта, если симптомы нарушения кровообращения остаются, переходят на препараты наперстянки.
Лечение сердечными гликозидами, и в первую очередь препаратами наперстянки, проводят в два этапа:
1) введение дозы насыщения (полной терапевтической дозы)
2) введение поддерживающей дозы. Высчитать полную терапевтическую дозу для ребенка можно исходя из полной дозы действия для взрослых.
Средняя полная терапевтическая доза для взрослых: строфантина — 0,008 — 0,01 мг/кг, изоланида, дигитоксина, дигоксина, ацетилдигитоксина (ацедоксина), целанида (изоланида) — 0,028 мг/кг.
Высчитать соответствующую дозу для ребенка можно по дозис-фактору, значение которого изменяется в зависимости от возраста: до 1 года — 1,8; от 1 года до 6 лет — 1,6; от 6 до 10 — 1,4; от 10 до 12 — 1,2; для взрослых — 1. Умножив полную терапевтическую дозу для взрослых на значение дозис-фактора и массу тела ребенка, получают полную терапевтическую дозу гликозида для больного. Эту дозу можно ввести методом быстрого, средне-быстрого и медленного насыщения (соответственно в течение 1 — 2, 3 — 5 и 5 — 7 дчей). В педиатрии применяют чаще среднебыстрый метод насыщения. В первые сутки при этом вводится 50 %, а в последующие 2 дня по 25 % полной терапевтической дозы. При введении дозы насыщения обычно наступает явный терапевтический эффект, после чего назначают поддерживающую дозу. По существу, эта доза равна количеству препарата, ежедневно выводимого (элиминирующегося) из организма. Ее легко подсчитать при учете коэффициента элиминации, равного: для строфантина — 40 %, изоланида — 20, дигоксина — 20, ацетилдигитоксина — 10, дигитоксина — 7 %. Умножив полную терапевтическую дозу на коэффициент элиминации и разделив полученную цифру на 100, получим среднюю поддерживающую дозу. Ее при необходимости назначают на протяжении длительного времени, наблюдая за состоянием больного для предупреждения передозировки. При недостаточности кровообращения ПБ и III степени сердечные гликозиды целесообразнее вводить внутривенно.
При передозировке препаратов наперстянки может развиться интоксикация, проявляющаяся потерей аппетита, тошнотой, рвотой, поносом, нарушением зрения, шумом в ушах, головокружением, головной болью, повышением артериального давления, затем брадикардией, экстрасистолией (бигеминия), желудочковой тахикардией, предсердно-желудочковой блокадой с периодами Самойлова — Венкебаха. Возможно усиление явлений недостаточности кровообращения. В таких случаях немедленно отменяют препараты наперстянки и назначают калия хлорид или калия ацетат в 5 — 10 % растворе внутрь по 1 — 2 десертные (столовые) ложки 1 — 2 раза в день, панангин. В тяжелых случаях необходимо ввести внутривенно 200 — 300 мл изотонического раствора натрия хлорида, 5 % раствор глюкозы, аскорбиновую кислоту и кокарбоксилазу. На протяжении двух-трех дней можно вводить внутримышечно или подкожно 1 — 5 мл 5 % раствора унитиола.
Назначать строфантин или его аналоги после отмены препаратов наперстянки не следует!
Параллельно с сердечными гликозидами при всех степенях недостаточности кровообращения применяют препараты, стимулирующие обменные процессы в организме, и в первую очередь — в сердечной мышце. Вводят аденозинтрифосфорную кислоту (АТФ) — 1 мл 1 % раствора внутримышечно, на курс 30 — 45 инъекций, панангин (калия и магния аспарагинат) — 1 — 3 драже в день после еды, кортикотропин — подкожно или внутримышечно, а в тяжелых случаях — внутривенно по 1 — 1,5 мл ежедневно (на курс 25 — 30 инъекций). Параллельно вводят анаболические препараты нестероидные (калия оротат — 10 — 20 мг/кг/сут, курс лечения 1 — 3 недели) или анаболические стероиды (метиландростендиол — 1 мг/кг/сут, не более 0,05 мг/кг; метандростенолон — 0,1 мг/кг детям в возрасте до двух лет, старше — 1 — 5 мг/кг/сут, в два приема; неробол — в той же дозе).
Можно назначать препараты дюрантного действия: ретаболил — 0,5 — 1 мг/кг 1 раз в 3 — 4 недели внутримышечно; нероболил — 1 — 1,5 мг/кг в месяц (1/3 — 1/4 дозы вводят через каждые 7 — 10 дней). Курс лечения 1,5 — 2 месяца.
Наряду с этим вводят витамины: аскорбиновую кислоту, кокарбоксилазу, цианокобаламин, пиридоксин, кальция пангамат, фолиевую кислоту, пентоксил.
При хронической недостаточности кровообращения с задержкой жидкости в организме (III степень) показано введение диуретических средств: дихлотиазида — гипотиазида, новурита, лазикса — фуросемида, урегита. При неэффективности, что часто связано с развивающимся альдостеронизмом, назначают антиальдостероновые препараты (верошпирон, кортикостероиды). Нередко в случаях со стойкими отеками эффективны ингибиторы карбоангидразы (диакарб). При асците, гидротораксе проводят удаление жидкости из полостей.
Профилактика хронической недостаточности кровообращения заключается в своевременном и активном лечении больных с заболеваниями, приводящими к нарушению кровообращения (ревматизм, сепсис и др.).