Ранняя реабилитация после перенесенного инсульта
В.В.Гудкова, Л.В.Стаховская, Т.Д.Кирильченко, Е.А.Ковражкина, Н.С.Чекнева, О.В.Квасова, Е.А.Петрова, Г.Е.Иванова
Кафедра фундаментальной и клинической неврологии РГМУ, ГКБ №20, ГКБ № 31, Москва
Широкая распространенность острых нарушений мозгового кровообращения, высокие показатели смертности и легальности при данном заболевании и значительный процент инвалидов среди выживших (80%) ставят инсульт на одно из первых мест в ряду медико-социальных проблем. В многоцентровых рандомизированных исследованиях доказано, что лечение больных с инсультом необходимо проводить в специализированных неврологических сосудистых отделениях. Более того, показано, что положительный эффект может быть достигнут только при наличии в сосудистом отделении реабилитационной службы [1, 2]. В мировой практике имеется хорошо разработанная система оказания помощи больным с инсультом. в которой большое место отводится реабилитации, в том числе и ранней [3,4). В нашей стране также был издан приказ №25 от 25 января 1999 г. Минздрава РФ "О мерах но улучшению медицинской помощи больным с нарушениями мозгового кровообращения", однако в нем отсутствует положение о ранней реабилитации (РР). В то же время известно, что чем раньше начаты реабилитационные мероприятия, тем они эффективнее [5, 6]. В настоящее время в Москве и Санкт-Петербурге, а затем и в других городах России созданы и доказали свою эффективность службы РР в рамках сосудистых неврологических отделений.
В организационном плане хорошо зарекомендовала себя британская модель мультидисциплинарной бригады (МДБ) |4, 7, 8], которую мы уже описывали в журнале консилиум |9|. Развитие комплексной системы РР невозможно без надлежащей материально-технической базы и специально подготовленных дополнительных штатов по типу МДБ. тем не менее простые и достаточно эффективные реабилитационные методы могут с успехом внедряться в любом сосудистом неврологическом отделении.
Хельсингборгская декларация (1995 г.), разработанная экспертами ВОЗ, для стран-членов Европейского регионального бюро, провозглашает, что "более 70% выживших пациентов должны быть независимы в повседневной жизни через 3 мес после начала заболевания". Добиться подобных результатов невозможно без развития системы РР, а также непрерывности и преемственности реабилитационных мероприятий на следующих этапах (специализированные реабилитационные стационары, центры, санатории, реабилитационная амбулаторная служба).
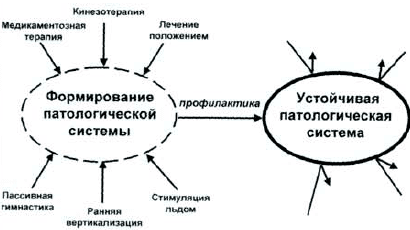
Целью РР, которая проводится в остром периоде инсульта (первые 3-4 нед заболевания), не может быть достижение независимости, провозглашенной в декларации, но она должна создать базу, позволяющую на следующих этапах лечения достичь требуемого результата. Основная цель РР это профилактика образования устойчивых патологических систем (контрактур, артралгий, патологических двигательных стереотипов и поз) или уменьшение степени выраженности их за счет активации саногенетических механизмов и разрушения патологических систем с привлечением как медикаментозных, так и не медикаментозных методов воздействия (рис. 1). Если на ранних этапах не будет проведено профилактическое лечение, то задача постстационарных реабилитационных служб значительно усложнится, а в ряде случаев может быть не выполнима.
Рис. 1. Стратегия РР — дестабилизация патологической системы.
Оптимальной организацией работы является создание МДБ. Однако до создания развернутой системы РР с командой разнопрофильных специалистов проводить РР могут специально обученные врачи и медицинские сестры из неврологического сосудистого отделения. Подобный подход определяет выбор применяемых методов восстановительной терапии эффективных, но достаточно простых, доступных как медицинскому персоналу, так и ухаживающим за пациентом лицам, что отражено на рис. 1. Наш опыт показывает, что основой лечения на ранних этапах восстановления является лечение положением и онтогенетическая кинезотерапия.
Как спонтанное восстановление после перенесенного инсульта, так и нормализация функций на фоне лечения опосредуется саногенетическими механизмами, в основе которых лежит пластичность мозга. Последняя определяется. как способность нервной ткани изменять структурно-функциональную организацию под влиянием внешних и внутренних факторов.
Процессы пластичности активируются под влиянием окружающей среды, в особенности насыщенной стимулирующими объектами, что определяет необходимость активного внедрения методов РР в восстановительный процесс. Положительную роль при этом играет двигательная мобилизация. В целом РР в большей степени направлена на двигательную сферу, это определяется не только ее воздействием на пластичность, но и тем, что: 1) двигательные расстройства наблюдаются более чем у 85% больных инсультом; 2) они в большей степени мешают самообслуживанию: 3) двигательная функция является наиболее подвижной, она быстро нарушается при снижении мозгового кровотока и также быстро может восстанавливаться: 4) неравномерное восстановление отдельных мышц приводит к развитию патологических двигательных паттернов, что определяет необходимость контроля за процессом восстановления движений; 5) на моторику можно воздействовать с периферии через интернейроны спинного мозга как методами кинезотерапии, так и сенсорными стимулами; 6) воздействие на двигательную сферу будет способствовать нормализации и других функций, так как одни и те же трансмиттеры принимают участие в передаче информации в двигательной, чувствительной, когнитивной системах.
Оснащение палат РР в неврологическом отделении не требует больших экономических затрат. Палаты должны быть просторными — для обеспечения подхода к больным со всех сторон, оснащены функциональными кроватями, специальными противопролежневыми матрацами, прикроватными функциональными креслами, функциональными прикроватными столиками, переносными биотуалетами, ширмами, приспособлениями для укладки и перекладывания больных. В отделении необходимо предусмотреть стол для кинезотерапии, кабинет и оборудование для эрготерапии (бытовая реабилитация), желательно иметь электроподъемник, параллельные брусья, ступеньки для обучения ходьбе по лестнице, "шведскую стенку" и другие приспособления для обучения больного самообслуживанию.
В фазе ранней мобилизации (3) необходима организация активизирующего ухода и контроля за витальными функциями: мочеиспусканием, дефекацией, приемом пищи. К активизирующему уходу на ранних этапах относится лечение положением (ЛП): ранняя активизация (верикализация). раннее использование прикроватного туалета (а не судна), постоянная проверка функции глотания, применение специально подобранной диеты, достаточного количества потребляемой жидкости, одевание компрессионных чулок.
ЛП — придание парализованным конечностям и телу правильного положения (корригирующие позы) в течение того времени, когда больной находится в постели или в положении сидя.
ЛП можно проводить всем больным вне зависимости от тяжести состояния с первых часов инсульта (7, 8, 10, 11). поэтому его широко применяют в блоке интенсивной терапии, куда первоначально должно поступать большинство больных с инсультом.
ЛП включает: укладку парализованных конечностей на одном уровне, в горизонтальной плоскости при положении пациента на здоровом боку, что обеспечивает равномерную гравитационную нагрузку на конечности: положение на парализованной стороне: укладку в положении противоположной позе Вернике Манна: положение на животе без подушки; положение на животе с опорой на предплечья и кисти.
Основой правильной укладки являются; симметричность расположения частей туловища и конечностей, поддержка всех сегментов тела, бережное отношение к крупным суставам, в частности к плечу паретичной руки, ограничение времени пребывания на спине. Если же больной лежит на синие, то паретичное плечо должно быть поддержано подушкой (высотой 2-3 см), под ягодицей с пораженной стороны должна находиться плоская подушка, чтобы "больная" нога не была развернута кнаружи. В настоящее время не целесообразным считается упор парстичной стопы, а также распластывание кисти руки под мешочком с песком, приводящие к нарастанию мышечного тонуса из-за механического растяжения мышц в положении дискомфорта [7].
Несмотря на свою простоту, правильное выполнение ЛП способствует:
снижению мышечной спастичности, выравниванию асимметрии мышечного тонуса, восстановлению схемы тела, нормализации глубокой чувствительности, снижению патологической активности с тонических шейных и лабиринтных рефлексов, предупреждению развития контрактур, болевого синдрома, патологических установок в конечностях и туловище. Так как положение больного меняется каждые 2-3 ч, то ЛП выполняет также функции профилактики пролежней, тромбофлебита, пневмонии.
Ранняя вертикализация больных предусматривает возвышенное положение туловища и грудной клетки уже в первые дни пребывания больного в стационаре, возвышенное положение туловища при приеме пищи. В последующие дни поднятие головного конца кровати, присаживание больного и опускание нижних конечностей, затем (при адекватном соматическом статусе) вставание с помощью медицинского персонала на 2-3-5 мин около кровати и пересаживание в прикроватное кресло при легком и средней тяжести ишемическом инсульте.
Оценка и коррекция расстройств глотания. Поперхивание при глотании жидкой или твердой пиши, которое возникает, как правило, у большого числа больных и, к сожалению, может привести к тяжелым последствиям аспирационной пневмонии, повышению артериального давления, резкой головной боли, асфиксии, потери сознания и даже к летальному исходу. С первых часов и суток больному следует поднимать и придерживать голову во время еды. Но уже на 2-3-й день показано возвышенное положение в момент приема нищи, кормление маленькими глотками, контроль за проглатыванием, исключение скопления пищи и слюны в полости рта. Активная вертикализация туловища в момент глотания и исключение поперхивания обеспечивают попадание пищи в трахею и бронхиальное дерево.
Всем пациентам с острым нарушением мозгового кровообращения необходима оценка функции глотания. В зависимости от результатов тестирования осуществляется выбор системы питания для каждого пациента. При выраженных расстройствах глотания используются зондовое и парентеральное питание или встает вопрос о гастростоме.
При затруднении глотания кормление проводят только в положении больного сидя с опорой под спину, дополнительно подбирается поза для наиболее эффективного и безопасного глотания (наклон головы вперед, поворот в пораженную сторону в момент проглатывания). Весьма важным является подбор консистенции пищи (мягкая, густое пюре, жидкое пюре, густой кисель, мусс, йогурт и пр. полужидкая пища). Исключение из рациона продуктов, часто вызывающих аспирацию, жидкость обычной консистенции, хлеб, печенье, орехи и т.п. После кормления необходимо тщательно обрабатывать полость рта для исключения возможности аспирации и сохранять вертикальное положение больного около 30 мин.
Онтогенетически обусловленная кинезотерапия. Механизмы спонтанного восстановления напоминают становление моторики ребенка в онтогенезе: сначала восстанавливается аксиальная мускулатура и проксимальные отделы конечностей, затем дистальные и тонкая моторика. По принципу использования проторенных в онтогенезе двигательных путей строится восстановительная терапия на ранних постинсультных этапах. С этой целью, в частности, используется разработанная в России методика "Баланс".
У ребенка сначала возникают двусторонние, крупные движения, напоминающие диагонали с переносом конечностей в противоположную сторону. Подобные диагонали используются в методике "Баланс". В механизмах компенсации организм стремится подстраивать свои интактные конечности под парализованные, в связи с чем работа с пациентом проводится обязательно симметрично с двух сторон (при необходимости с паретичной стороны пассивно).
Важным принципом также является постепенность нагрузки, так как аналогично онтогенетическому процессу несоответствие "зрелости нервной системы" может приводить к формированию патологических синкинезий.
Этапы онтогенетической кинезотерапии представлены в табл. 1.
Таблица 1.
Этапы онтогенетически обусловленной кинезотерапии
- Физиологические движения в осевой мускулатуре, плечевом и тазовом поясах
- Обучение переворачиванию на обе стороны, живот, перемещению на кровати
- Обучение тонкой моторике рук и ходьбе
Расстройства регуляции движений после инсульта приводит к нарушению моторного праксиса высшего автоматизма по определению Н.А.Бернштейна. Больных приходится обучать сложным, целенаправленным привычным движениям, переводя их из автоматизированных в заново обучаемые с использованием физиологических синергий. Так больному нужно объяснить, что, для того чтобы встать из положения сидя, ему нужно отодвинуть ноги под стул и переместить центр тяжести вперед. Парализованный больной не может сесть в кровати так, как это делает взрослый человек, обучение его использованию приемов ребенка значительно облегчает этот переход.
В палатах РР развивают способность к самообслуживанию: приему пищи, одеванию, умыванию, применению вспомогательных средств. Вспомогательные средства ухода не должны чрезмерно замещать собственные возможности пациента, он должен уметь ими пользоваться. Целесообразно применять устойчивую четырехопорную трость. Длина трости должна превышать уровень тазобедренного сустава, этим предотвращается перекос туловища в здоровую сторону и уменьшается спастическое напряжение мышц пораженной стороны. Следует помнить, что прежде чем приступать к тренировке ходьбы, необходимо тренировать стабильность и равновесие в положении стоя.
Медикаментозное лечение. В рамках РР больных с инсультом трудно провести грань между реабилитационными и лечебными методами. Применение лекарственных препаратов в остром периоде инсульта объясняется необходимостью коррекции системной гемодинамики, перфузии мозга, явлений отека мозга, проведения патогенетической терапии (антигипоксической, антиоксидантной, нейропротективной, нейротрофической), адекватного обеспечения двигательной системы, состояния ортостаза. Принципы медикаментозной терапии включают также лечение фоновых, сопутствующих заболеваний и активацию регенеративно-репаративных процессов мозга через механизмы пластичности. В механизмах пластичности рассматриваются как структурные изменения синапсов, дендритов, астроглии, нейронов, капилляров, так и молекулярно-генетические и биохимические процессы, сопровождающиеся выработкой биологически активных веществ, оказывающих стимулирующее, угнетающее или модулирующие воздействие на пластичность (12). К таким веществам относятся нейротрасмиттеры — ацетилхолин, адреналин, серотонин, ГАМК, глутамат, модулятор — оксид азота и др. Указанный многосторонний подход к лечению определяет целесообразность применения препаратов комбинированного действия.
К препаратам, оказывающим комбинированное действие, относится вазобрал, представляющий собой сочетание α-дигидроэргокриптина (алкалоид спорыньи) и кофеина. Дигидроэргокриптин обладает блокирующим действием в отношении α1- и α2-адренорецепторов, а также стимулирующим действием на допаминовые и серотониновые рецепторы головного мозга. Кофеин прежде всего повышает биодоступность дигидроэргокриптина, а также оказывает легкий стимулирующий эффект.
Вазобрал является вазоактивным препаратом, воздействующим в основном на микроциркуляторное русло, снижает агрегацию эритроцитов и тромбоцитов, увеличивает количество капилляров, снижает их проницаемость, улучшает венозный отток, устраняет вазоспазм, не влияя при этом на системное артериальное давление. Вазобрал оказывает действие на обменные процессы мозга: повышает утилизацию глюкозы и кислорода, увеличивает концентрацию АТФ и АДФ, воздействует на аминергические нейротрансмиттеры (норадреналин, дофамин, серотонин), которые принимают участие в двигательных, когнитивных и эмоциональных процессах.
Эффективное применение вазобрала при мигрени, синдроме Рейно, ретинопатии, в том числе и диабетической, нарушениях периферического кровообращения как артериального, так и венозного, дисциркуляторной энцефалопатии, возрастных изменениях памяти и интеллекта, паркинсонизме, кохлео-вестибулярных нарушениях, эмоциональных расстройствах, а также у больных в отдаленном периоде после инсульта.
Известно, что ишемический инсульт сопровождается расстройствами микроциркуляции, реологических свойств крови, вегетативной регуляции, венозного оттока, нейротрансмиссии, пластичности. На все эти патогенетические цепочки в той или иной степени может воздействовать вазобрал, что позволило нам применить его у больных в остром периоде ишемического инсульта.
Препарат назначали в новой для российского рынка таблетированной форме, в дозе 4 мг (1 таблетка) 2 раза в день, утром и днем (во время еды) на протяжении 3 нед (с 7-го по 28-й дни инсульта). Лечение проводили на фоне комплекса базовой медикаментозной и немедикаментозной терапии. Основную группу составили 34 больных (14 мужчин и 20 женщин) с острым полушарным ишемическим инсультом (18 с правосторонней локализацией, 16 — с левосторонней), средний возраст составил 62±2 года. В контрольную группу вошли 30 пациентов, сопоставимых по полу и возрасту, по 15 больных с право- и левосторонней локализацией инфаркта мозга, которые в комплексной терапии не получали вазобрал.
Оценку результатов проводили по клиническим шкалам: National Institutes of Health (NIH) Stroke scale. Barthel ADL index, Mini-mental state examination. На фоне проводимой терапии отмечена положительная динамика. статистически значимых различий между основной и контрольной группами не выявлено. В то же время в основной группе на фоне лечения вазобралом было отмечено достоверное уменьшение степени выраженности вегетативно-трофических расстройств на паретичных конечностях, чего не наблюдали в контрольной группе (рис. 2).
Рис. 2. Вегетативно-трофические расстройства на паретичных конечностях
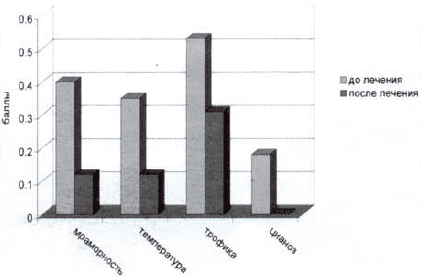
Проведенное исследование позволяет нам сделать заключение: вазобрал эффективен у больных в остром периоде ишемечиского инсульта, препарат хорошо переносится, при его применении не выявлено осложнений, в том числе и у лиц с геморрагической трансформацией инфаркта мозга (2 пациента); под воздействием вазобрала улучшаются вегетативно-трофические функции на третичных конечностях — снижается мраморность, цианоз, гипотермия.
Разнообразие препаратов комбинированного действия, которые применяются в ангионеврологии (кавинтон, винпоцетин, инстенон, стугерон, циннаризин, танакан, сермион, ницерголин, вазобрал и др.) приводят всех нас, практикующих врачей, в замешательство — какой препарат и когда лучше назначать? В целом с учетом данных литературы и собственных исследований мы определили показания для назначения вазобрала в постинсультном периоде:
- Вегетативно-трофические расстройства на парализованных конечностях
- Сопутствующие нарушения периферического кровообращения (артериальное и венозное), ретинопатия и ангиопатия при сахарном диабете, атеросклерозе, гипертонии, старении
- Кохлеовестибулярные расстройства различной этиологии
- Астенодепрессивные расстройства
- Профилактика нарастания хронической ишемии мозга после перенесенного инсульта
После выписки из стационара прием вазобрала следует продолжить еще 1,5-2 мес в дозе 4 мг 2 раза в день.
Риск повторного инсульта особенно велик в первый год после перенесенного заболевания, в связи с чем особое значение приобретает вторичная медикаментозная профилактика, которая начинается практически с острого периода. С учетом того, что после перенесенного ишемического инсульта отмечается истощение антиагрегационного потенциала сосудистой стенки, приводящее к тромбообразованию, нарастанию степени выраженности атеросклероза и прогрессированию недостаточности кровоснабжения мозга, основным направлением вторичной профилактики инсульта являются: антиагрегантная, гипотензивная терапия, улучшение церебральной гемодинамики и повышение функциональных возможностей мозга, а также адекватное лечение атеросклероза.
Учитывая, что ключевая роль в ишемических нарушениях принадлежит активации тромбоцитарно-сосудистого звена гемостаза немаловажная роль в профилактике инсультов отводится антиагрегантным средствам. В настоящее время широко используется аспирин как кишечно-растворимые формы: тромбо АСС, аспирин кардио. Новой и чрезвычайно перспективной формой аспирина с улучшенными характеристиками с точки зрения безопасности, является Кардиомагнил. В состав препарата ходит не только ацетилсалициловая кислота, но и гидроксид магния, который уменьшает ульцерогенное действие кислоты на слизистую оболочук желудка. Все указанные препараты применяются в дозе 75-100 мг (1мг/кг) ежедневно. При необходимости к лечению добавляют другие антиагреганты (дипиридамол, клопидогрель).
В исследовании PROGRESS (2001 г.) доказана эффективность использования ингибитора АПФ периндоприла для профилактики ишемических и геморрагических инсультов как у пациентов с артериальной гипертонией, так и без таковой. Препарат может быть использован в качестве монотерапии, а также при необходимости в сочетании с другими лекарственными средствами, применяемыми для лечения АГ. При наличии у пациентов атеросклероза необходимо рекомендовать диету с преимущественным использованием растительных жиров, а также применение гиполипидемических средств, в частности статинов, которые оказывают лечебное и профилактическое действие.
Таким образом, ранняя реабилитация является необходимым звеном в системе оказания стационарной помощи больным инсультом. Основными направлениями ее являются: активизирующий уход, лечение положением, онтогенетическая кинезотерапия, медикаментозное обеспечение процессов гомеостаза (включая гемодинамику и микроциркуляцию), пластичности и активной мобилизации.
ЛИТЕРАТУРА
1. Erila Т. Itmauirta М. Does an intensive-care stroke unit reduce the early case-fatality rate of ishaemic stroke? Stroke 1990:21 (Suppl. I): 153.
2. Moris AD, Grosset DG, Squire IB el. al. The experiences of an acute stroke unit: implications for multicentre acute stroke trials. J Neurol Seurosurg Psych 1993;56:352-5.
3. Юнусов ФА, Гайгер Г, Микус Э. "Организация медико-социальной реабилитации за рубежом" М. Общероссийский общественный фонд "Социальное развитие России", 2004.
4. Bapлoy Ч.П. Деннис М.С. ван Гейн Ж. и др. Инсульт. Практическое руководство для ведения больных. СПб. Политехника. 1998: 298-317,396-448
5. Кадыков АС. Реабилитация после инсульта М. МИКЛОШ, 2003.
6. Гусев ЕЛ, Гехт А.Б. Гаптов В.Б. Тихопой Е.В. Реабилитация в неврологии. Учебное пособие, М, 2000.
7. Камаева O.В. Полина Монро. Мультидисциплинарный подход в ведении и ранней реабилитации неврологических больных. Методическое пособие. Под ред. акад. РАМН проф. АА Скоромца. СПб. 2003.
8. Сорокоумов В.А. и др. Методические рекомендации по организации неврологической помощи больным с инсультам в Санкт-Петербурге. СПб. 2002.
9. Гудкова В.Л, Петрова Е.А, Митрофанова И.Н, Квасова ОВ, Кирильченко ТД, Скворцова ВЛ. Раннее восстановительное лечение бальных с церебральным инсультам. CONSILIUM MEDICUM, спец. выпуск 2003:30-3.
10. Белова АЛ, Нейрореабилитация: руководство для врачей. М.-Антидор, 2000;253-321.
11. Скворцова ВЛ. и др. Ранняя реабилитация бальных с инсультом: Методические рекомендации. № 44. М: Изд-во РУДН. 2004:40: ил.
12. Гусев ЕЛ, Камчатное ПР. Пластичность нервной системы. Журн. неврол. и психиат. 2004:3: 73-9.
HTML-код для размещения ссылки на сайте или в блоге:
Стентирование брахицефальных артерий. Методические рекомендации.
Методические рекомендации основаны на 5-летнем практическом опыте коллектива врачей ФГУ «Клиническая больница №1» УД Президента РФ при проведении стентирований брахицефальных артерий и отражают современные представления о проблеме возникновения ишемических поражений головного мозга на фоне стенозирующего атеросклероза брахицефальных артерий, а также современных методах первичной и вторичной хирургической профилактики инсультов. Сформулированы актуальные для настоящего времени показания для проведения рентгеноэндоваскулярной коррекции стенозов брахицефальных артерий, предложен алгоритм дообследования больных при их отборе на стентирование.
28 февраля 2014 г.
Краткий литературный обзор
Среди причин смертности населения одними из ведущих во всем мире остаются цереброваскулярные заболевания. В 2000 г. общая смертность россиян составила 319,8 случая на 100 тыс. населения [2, 7]. С 2001 по 2002 г. наблюдался рост смертности на 2,6%, которая составляла соответственно 330,5 и 339,1 на 100 тыс. населения [1]. В последние годы в Российской Федерации инсульт развивается примерно у 450 тысяч человек [3]. Вместе с тем, социально значимы и последствия инсульта — развитие стой¬кой инвалидности с потерей трудоспособности, сосудистая демен¬ция. Согласно литературным данным, опубликованным в журнале Circulation в 2007 году, Россия занимает первое место в мире по уровню смертности (среди мужчин 35-74 лет) как от инсультов, так и от сердечно-сосудистых заболеваний в целом. Если в Канаде, Швейцарии, Франции и Австралии показатель смертности от инсульта ниже 50 человек на 100 тысяч населения, то в России смертность в последние годы превышает 400 [27].
По данным «Доклада о состоянии здоровья населения Москвы в 2008 году» Департамента Здравоохранения Москвы, летальность госпитализированных в стационары Москвы больных с ишемическим инсультом в 2002-2008 сохраняется на стабильном уровне в 16-17%. Среди выживших в 2008 году после инсульта 27,6% пациентов стали тяжелыми инвалидами с необходимостью посторонней помощи для ухода за собой и только 14,6% работавших до инсульта возвратились к труду. На смертность от инсульта по России приходится около 20% общей смертности.
Основной вклад в заболеваемость инсультом вносит инфаркт мозга (ишемический инсульт), частота которого в 4 раза превышает частоту геморрагического ин¬сульта. Одним из наиболее значимых факторов, приводящих к развитию ишемического инсульта, является атеросклеротическое пораже¬ние артерий крупного и среднего калибра, таких, как аорта и ее ветви, приводящее к значительному сужению просвета артерии [32,33]. Разли¬чают гемодинамически незначимые стенозы – 30-50%, умеренно значимые – 50-¬69% и выраженные, либо как их часто называют «критические» или «гемодинамически значимые сте¬нозы» — более 70%. В основе указанного деления лежит снижение кровотока дистальнее места стеноза, т.е. механизм сосудисто-мозговой недостаточности, предло¬женный еще в начале 50-х годов. Таким моногене-тическим механизмом объяснить причины ишемических на¬рушений мозгового кровообращения при стенозах внутрен¬ней сонной артерии не представляется возможным. Извест¬но, что в большом количестве случаев регистрируются гемодинамически значимые стенозы, не приводящие к развитию ишемических нарушений мозгового кровообращения и даже асимптомные. Отсутствие неврологической симптоматики связано с хорошо развитой коллатеральной сетью кровоснабжения мозга и анатомо-физиологическими особенностями сосудистой системы головного мозга.
Стенозы брахицефальных артерий более 50%, сопровождающиеся острыми нарушениями мозгового кровообращения в соответствующем сосудистом бассейне, определяются как «симптомные». По литературным данным, при величине стеноза более 70-75% и имеющихся транзиторных ишемических атаках в анамнезе частота инсульта достигает 12-13% в первый год после его выявления и 30-37% в течение последующих пяти лет [13,34]. У больных, уже перенесших инсульт, риск развития повторного инсульта на протяжении первого года колеблется от 5% до 9%, а в последующие 5 лет повышается до 24-45% [29].
Понятию «асимптомный стеноз» было дано определение в 1995 году в исследовании ACAS (Asymptomatic Carotid Atherosclerosis Study): «асимптомным считается стеноз вну¬тренней сонной артерии, в зоне кровоснабжения которой не возникали какие-либо преходящие или стойкие очаговые неврологические симптомы» [14]. Нередко неврологи¬чески асимптомный стеноз обнаруживается случайно и трудно предположить, разовьется ли когда-нибудь инсульт у такого больного или поражение сосуда так и не приведет к появлению клинических признаков.
Ежегодная частота ин¬сульта для пациентов с неврологически асимптомным гемодинамически значимым стенозом составляет 2-5% [11, 19, 28, 30], причем этот показатель возрастает при увеличении степени стеноза и срока наблюдения. При невроло¬гически асимптомных стенозах внутренней сонной арте¬рии частота случаев «ТИА+инсульт» состав¬ляет 22% и возрастает до 33% у пациентов с билатеральны¬ми стенозами [20, 24]. У 50-70% больных с асимптомными поражениями сонных артерий ишемический инсульт возникает без предшествующих ТИА [15]. Можно выделить три специфических фактора инсульта, которые определяют высокий риск инсульта при «асимптомных» стeнозах внутренней, сонной артерии:
- стеноз более 70% просвета сосуда,
- прогрессирование стеноза при повторных обследованиях,
- наличие изъязвления — гетерогенная эхонегативная атеросклеротическая бляшка
Хирургические методы первичной и вторичной профилактики инсульта.
Острота представленной проблемы инициировала по¬иск наиболее эффективного метода профилактики и лечения нарушений мозгового кровообращения при атеросклеротических поражениях магистральных сосудов головы и шеи. Основными видами профилактики являются прием антиагрегантов, каротидная эндартерэктомия и стентирование артерий. Рандомизированные клинические испытания NASCET (North American Symptomatic Carotid Endarterectomy Trial, 1991) и ACAS (Asymptomatic carotid atherosclerosis study, 1995) убедительно продемонстрировали преимущества ка¬ротидной эндартерэктомии у симптомных и аисмптомных больных с выра¬женным стенозом сонных артерий (70% и более) над меди-каментозным лечением [10, 29] (табл 1.).
Таблица 1. Сравнительная оценка результатов медикаментозного и хирургического лечения стенозов ВСА в течение первого года после эндартерэктомии по данным исследования NASCET [29].
Инсульт. Современные подходы диагностики, лечения и профилактики
 Перейти
Перейтив магазин
Актуальность проблемы острых нарушений мозгового кровообращения связана как с высоким уровнем заболеваемости, так и с тем фактом, что инсульт является одной из основных причин смертности и первой причиной инвалидизации. Это определило необходимость формирования в РФ системы оказания помощи больным инсультом. Международный опыт определил на базе доказательности основные принципы ведения больных с острыми нарушениями мозгового кровообращения.
Настоящее методическое пособие написано на основе российских и международных рекомендаций диагностики, лечения, мониторинга, профилактики инсульта для врачей специализированных отделений для лечения больных инсультом, сосудистых центров с целью оптимизации работы и возможности формирования единых подходов в ведении данной категории больных.